6-氟-4-色满酮-2-甲酸的合成研究进展
徐 尧
(滁州城市职业学院,安徽 滁州 239000)
6-氟-4-色满酮-2-甲酸是6-取代-4-色满酮-2-甲酸的一种衍生物,它具有生理和药理活性,因此,对其制备的研究具有很重要的价值。6-氟-4-色满酮-2-甲酸是一种合成和开发药物的重要中间体,也可以作为一些含氟苯并吡喃类化合物的中间体,在药物合成的工艺中占据很重要的地位。
1 6-氟-4-色满酮-2-甲酸的合成方法
1.1 对氟苯酚与顺丁烯二酸酐酚酯化
酚类物质与酸酐的酯化反应所用的催化剂有碱性和酸性两类[1],对氟苯酚与顺丁烯二酸酐发生酚酯化反应时,可以先让氟苯酚和氢氧化钠作用形成钠盐,目的是增加其亲核性,再选择室温条件下,与顺丁烯二酸酐发生反应,同时,氢氧化钠还起催化作用[2]。
1.1.1 反应原理
此合成法的反应原理如图1所示。
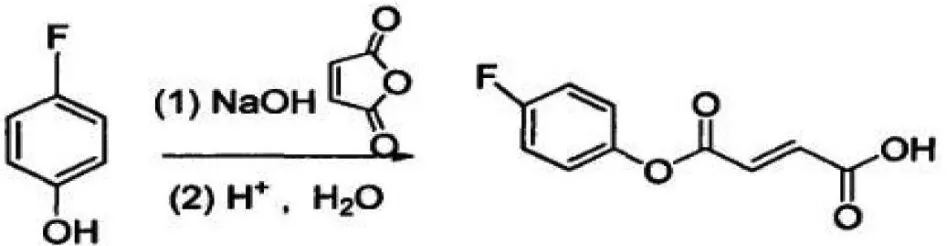
图1 对氟苯酚与顺丁烯二酸酐酚酯化
1.1.2 操作流程
(1)称量对氟苯酚2.35 g,并用1 mol/L 25 mL的氢氧化钠溶液将其溶解。
(2)称量顺丁烯二酸酐1.18 g,加入上述混合液中,搅拌使其全部溶解,再继续搅拌反应1 h。
(3)将上述反应后的液体倒入盐酸与冰的混合体系中,再过滤、水洗、干燥,可得产品1.76 g,计算产率约为70.0%。
1.2 3-(4-氟-苯基)-3-氧代-2-丁烯酸羧基酯化
在工业生产中,羧基酯化多采用无机酸作催化剂[3],酯化率较高,但存在因浓硫酸的强氧化性导致:生产设备易腐蚀、有机物易失水、碳化、反应后处理繁琐等缺点[4]。对3-(4-氟-苯基)-3-氧代-2-丁烯酸进行羧基酯化时,可以选择对甲苯磺酸作为催化剂,因为有机酸能够与有机相更好地相溶,能促进反应向着正相进行,让酯化达到更好的效果。
1.2.1 反应原理
此合成法的反应原理如图2所示。

图2 3-(4-氟-苯基)-3-氧代-2-丁烯酸的羧基酯化
1.2.2 操作流程
(1)在圆底二颈瓶中分别加入:5.88 g的3-(4-氟-苯基)-3-氧代-2-丁烯酸,0.24 g对苯二酚,7.6 g对甲苯磺酸,30 mL苯和10 mL无水乙醇。再安装一油水分离装置,用氮气做保护,在90 ℃的温度条件下,进行油浴加热,回流搅拌反应8 h。
(2)将反应液进行减压蒸馏除去苯,再加入10 mL乙酸乙酯,并用饱和碳酸氢钠溶液进行中和、洗涤3次。
(3)将洗涤之后的反应液,先用饱和氯化钠水溶液洗至中性,再用无水硫酸钠进行干燥,之后减压蒸馏除去乙酸乙酯,将得到的桔黄色油状物再经减压蒸馏,可获产物5.39 g,计算得出产率为81.0%。
1.3 3-(4-氟-苯基)-3-氧代-2-丁烯酸酯的Fries重排
酚酯在Lewis酸或者Bronsted酸催化下[5]可以发生Fries重排反应。酚酯发生酰基重排之后,可以形成邻、对位羟基芳酮,这为合成芳基酮提供了方法[6]。3-(4-氟-苯基)-3-氧代-2-丁烯酸酯的Fries重排就是在氯化铝催化的条件下反应的[7]。
1.3.1 反应原理
此合成法的反应原理如图3所示。

图3 3-(4-氟-苯基)-3-氧代-2-丁烯酸酯Fries重排
1.3.2 操作流程
(1)在100 mL烧瓶中先加入20 mL硝基苯,再迅速加入4.01 g无水氯化铝,并搅拌溶解,待温度降至室温。慢搅拌,慢滴加3.57 g的3-(4-氟-苯基)-3-氧代-2-丁烯酸酯。再缓慢将温度升至110 ℃,回流、搅拌反应6 h。
(2)对反应之后的混合液中缓缓滴加40 mL 1 mol/L盐酸水溶液,慢搅拌至固体全部溶解。用分液漏斗将反应液分层:用10 mL无水乙醚对水层萃取,再与有机层混合。将混合之后的有机层用10%氢氧化钠溶液提取数次。
(3)再进行分液,用10 mL无水乙醚萃取分液后水层。将水层中残留的乙醚蒸去后,在冰浴下用浓盐酸调整至酸性,经过滤、干燥,可得黄色固体1.92 g,计算产率为61.4%。
1.4 3-(4-氟-2-羟基苯基)-3-氧代-2-丁烯酸的环化
Michael加成反应是一个亲电的共轭体系(受体)和一个亲核碳负离子(给体)进行共轭加成的反应。Michael加成在有机合成中应用较广泛。3-(4-氟-2-羟基苯基)-3-氧代-2-丁烯酸环合反应是以碳酸氢钠溶液做催化剂,在羧基α-位碳原子发生1,4-Michael加成,环合得到产物[8]。
1.4.1 反应原理
此合成法的反应原理如图4所示。

图4 3-(4-氟-2-羟基苯基)-3-氧代-2-丁烯酸环化
1.4.2 操作流程
(1)在100 mL的圆底烧瓶中先加入2.1 g 3-(4-氟-2-羟基苯基)-3-氧代-2-丁烯酸,再加入50 mL10%的碳酸氢钠溶液将其溶解。
(2)边搅拌边加热至90 ℃,回流反应15 min,待冷却后,缓慢加入浓盐酸,将溶液的pH调节至1。溶液变浑浊,静置,等待白色晶体完全析出。
(3)将析出的白色晶体进行抽滤、水洗、风干,可制得白色固体1.8 g,计算产率为86.0%。
2 综合比较
将上所述的6-氟-4-色满酮-2-甲酸的4种合成方法:酚酯化、羧基酯化、Fries重排、Michale加成,做比较,如表1所示。

表1 6-氟-4-色满酮-2-甲酸的合成方法比较
3 结语
综合考虑反应时间、温度、催化剂等因素的影响及产率的高低,结合表1可以得出相对比较优越的工艺合成方法:Michale加成,即3-(4-氟-2-羟基苯基)-3-氧代-2-丁烯酸环合反应合成法,此方法的反应时间短、产率高,具有很明显的优势,而且反应的温度也不高,易控制。可以说,这是一条比较好的合成路线,有很好的开发前景。
[参考文献]
[1] 黄仲九,房鼎业.化学工艺学[M].北京:高等教育出版社,2001.
[2] 黄 宪,王彦广,陈振初.新编有机合成化学[M].北京:化学工业出版社,2003.
[3] 汪艳飞,黄宝华,方岩雄,等.醇酸酯化反应催化剂研究进展[J].广东化工,2007,34(7):62-66.
[4] INUI K,KURABAYASHI T,SATO S.Direct synthesis of ethyl acetate from ethanolcarried out under pressure[J].Jourmal of Catalysis,2002,2(2):207-215.
[5] OLIVEIRA A,OLIΝEIRA-CAMPOSA,RAPOSO M,et al.Fries rearrangement of dibenzofuran-2-y1 ethanoate under photochemical and Lewis-acid-catalyzed conditions[J].Tetrahedron,2004,60(29):6145-6154.
[6] 郑梅花,刘 洋,赵 瑾,等.Fries重排反应催化剂的研究进展杰[J].化工进展,2008,27(1):78-82.
[7] 王玉炉.有机合成化学[M].北京:科学出版社,2005.
[8]柏一慧.奈必洛尔全合成[D].杭州:浙江大学,2007.

