冬虫夏草内生菌Mucor luteus化学成分研究
韩雪花,李小华,王丽娜,何鑫,秦玲玲,郭大乐,邓赟
植物内生菌(Endophyte)是指在一定阶段或全部阶段生活于植物的各种组织和器官内部的真菌或细菌的统称,现一般指植物内生真菌。自Kloepper[1]第一次提出“植物内生菌”的概念开始,内生菌的研究越来越深入。内生菌除了与植物存在互利共生的关系,还能够通过产生一些与宿主植物相同或相似的化合物来对抗相同的外界环境胁迫,所以对植物内生菌的次级代谢产物进行研究不仅能够拓宽药用资源,还可以在一定程度上保护天然药用植物资源。从植物中分离内生菌,并对其次级代谢产物进行研究已经成为目前天然产物研究领域的热点内容之一[2]。
冬虫夏草为麦角菌科(Clavicipitaceae)真菌冬虫夏草菌Cordyceps sinensis(BerK.)Sacc.寄生在蝙蝠蛾科昆虫幼虫上的子座和幼虫尸体的干燥复合体。性平,味甘,归肺、肾经,具有补肾益肺,止血化痰的功效。主要含粗蛋白、粗脂肪、总糖、粗纤维,此外还含有氨基酸、脂肪酸、核苷类物质、甾醇、甘露醇、多糖等,具有增强免疫、抗肿瘤、改善肺心病患者血管功能等活性[3-4]。
本实验从新鲜冬虫夏草中分离得到一株内生菌,通过ITS测序比对鉴定为毛霉菌M. luteus,将其进行液体发酵培养后得到发酵产物,并对发酵产物的乙酸乙酯萃取部位进行化学成分研究,从中分离得到8个化合物,分别鉴定为:20-O-methyl-24-epi-cyclocitrinol(1),(15S)-15-hydroxy-24-epi-cyclocitrinol(2),(16R)-16-hydroxy-24-epicyclocitrinol(3),coniochaetones B(4),4-Hydroxybenzoic acid(5),benzoic acid(6),5,5'-diisobutoxy-2,2'-bifuran(7),bis(2-ethylhexyl)phthalate(8),化合物1-5,7-8均为首次从M. luteus中分离得到。化合物结构如图1所示:
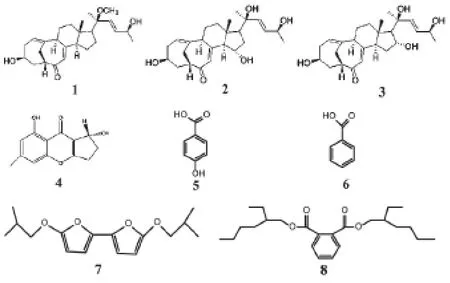
图1 化合物1-8的结构
1 仪器与材料
1.1 仪器与试剂
Finnigan-LCQDECA质谱仪(美国赛默飞世尔公司);Bruker Ascend 400核磁共振仪(TMS为内标)(德国布鲁克公司);十万分之一电子天平(瑞士奥豪斯DV-215-CD,上海顾村电光仪器厂);中压层析柱(利穗科技(苏州)有限公司);SHB-IIIS循环水式多用真空泵(上海跃进医疗器械厂);RE52CS旋转蒸发仪(上海亚荣生化仪器厂);SW-CJ-2FD型超净工作台(苏州安泰空气技术有限公司);恒温培养振荡器(上海智诚分析仪器制造有限公司);恒温恒湿培养箱(上海跃进医疗器械有限公司);优普UPT系列超纯水器(成都优普电子产品有限公司);NP7000型制备型高效液相色谱仪(江苏汉邦仪器有限公司)。柱层析硅胶(200-300目)、薄层层析硅胶板(5×10 cm,GF254)(青岛海洋化工厂); C18反相填料(日本YMC株式会社)。石油醚、丙酮、乙酸乙酯、甲醇、95%乙醇(成都科龙化工试剂厂,均为分析纯)。
冬虫夏草于2016年5月采集于甘肃省夏河县,由成都中医药大学蒋桂华教授鉴定为麦角菌科(Clavicipitaceae)真菌冬虫夏草菌Cordyceps sinensis(BerK.)Sacc.寄生在蝙蝠蛾科昆虫幼虫上的子座和幼虫尸体的干燥复合体,样品保存在成都中医药大学药学院生化制药实验室(编号DCXC-20160503-GSSXHX)。
1.2 培养基
孟加拉红固体培养基:35 g孟加拉红培养基,水1 L,煮沸溶解,pH自然。
PDA斜面培养基:土豆200 g加入自来水煮至软烂后过滤,滤液定容至1 L,滤液加入琼脂15~20 g﹒L-1,链霉素30 mg﹒L-1,葡萄糖20 g﹒L-1煮沸溶解,pH自然。
PDB液体培养基:土豆200 g加入自来水煮至软烂后过滤,滤液定容至1 L,滤液加入葡萄糖20 g﹒L-1,MgSO41.5 g﹒L-1,NaCl 2.0 g﹒L-1,K2HPO41.0 g﹒L-1,MgCl20.2 g﹒L-1,(NH4)3PO40.2 g﹒L-1煮沸溶解,pH自然。
2 实验方法
2.1 菌株的分离及鉴定
将采集的冬虫夏草的表面清洗干净,进行表面消毒,在无菌操作室的无菌操作台中用75%的乙醇消毒1 min,然后用无菌水冲洗3次,最后用无菌滤纸片吸干表面的水分,消毒完毕后在无菌条件下,用灭菌剪刀将根和茎剪成2 mm长的小段,接种于孟加拉红培养基上,待生长出菌落时挑出,在新的平板上培养纯化。
将纯化得到的菌株交于生工生物工程(上海)股份有限公司进行测序,将获得的18S rRNA基因序列提交到NCBI的GenBank基因库,BLAST比对,与数据库中的已知序列进行同源性分析,该菌株与Mucor luteus相似度为99%,故鉴定为毛霉菌M. luteus。菌种保存于成都中医药大学药学院生化制药实验室,编号为(DCXC-20160503-GSSXHX-20160512-3),ITS序列如下:。
TTTATATTGTGAAACTGCGAATGGCTCATTA AATCAGTTATGATCTACGTGACATATTCTTTACTA CTTGGATAACCGTGGTAATTCTAGAGCTAATACA TGCAAAAAAACCCTGACTTCGGAAGGGGTGCA CTTATTAGATAAAGCCAACGCGGGGTAAAACCT GTTTCCCTTGGTGATTCATAATAATTAAGCGGATC GCATGGCCTTGTGCTAGCGACGGTCCACTCGAT TTTCTGCCCTATCATGGTTGAGATTGTAAGATAG AGGCTTACAATGCCTACAACGGGTAACGGGGAATTAGGGTTCGATTCCGGAGAGGGAGCCTGAGAA ACGGCTACCACATCCAAGGAAGGCAGCAGGCGC GCAAATTACCCAATCCCGACACGGGGAGGTAGT GACAATAAATAACAATGCAGGGCCTTTAAGGTCT TGCAATTGGAATGAGTACAATTTAAATCCCTTAA CGAGGATCAATTGGAGGGCAAGTCTGGTGCCAG CAGCCGCGGTAATTCCAGCTCCAATAGCGTATAT TAAAGTTGTTGCAGTTAAAACGTCCGTAGTCAAA TTTTAGTCTTTAGGCGAAGTGGCCTGGTCTTCAT TGATCAAGCTCGTTTCTGCCGAGACTTTTTTTTT GGTTATGCTACTGTTGGCTTCGGTCGGCGGTAGT CTCTAGCCAAATGATTACCATGAGCAAATCAGAG TGTTTAAAGCAGGCTTTCAAGCTTGAATGTGTTA GCATGGAATAATGAAATATGACTTTAGTCCCTATT TCGTTGGTTCAGGAACTTAAGTAATGATGAATAG AAACGGTTGGGGGCATTTGTATTTGGTCGCTAGA GGTGAAATTCTTGGATTGACCGAAGACAAACTA CTGCGAAAGCATTTGACCCAGGACGTTTTCATTG ATCAAGGTCTAAAGTTAAGGGATCGAAGACGAT TAGATACCGTCGTAGTCTTAACCACAAACTATGC CGACTAGCGATTGGGCCTGTTTATTATGACTGGC TCAGCAGCTTAGCGAAAGTAAAGTTTTTGGGTT CTGGGGGGAGTATGGGACGCAAGGCTGAAACTT AAAGGAATTGACGGAAGGGCACCACCAGGAGT GGAGCCTGCGGCTTAATTTGACTCAACACGGGG AAACTCACCAGGTCCAGACATAGTAAGGATTGA CAGATTGAAAGCTCTTTCTAGATTCTATGGGTGG TGGTGCATGGCCGTTCTTAGTTCGTGGAGTGATT TGTCTGGTTAATTCCGATAACGAACGAGACCTTA TTCTGCTAAATAGGCAGGTCAACTTTTTAGTTGA TTAATTTATTTATAAATCTGGCTCTAGAGAG
2.2 发酵培养
将活化后的该菌株用接种针挑取适量菌丝体接种至已灭菌含80 mL培养液的250 mL或150 mL培养液的500 mL三角瓶中在25 ℃,120 rpm摇床上培养7 d,共发酵培养40 L。
2.3 提取分离
将发酵产物进行抽滤得滤液,滤液用同体积乙酸乙酯萃取三次,减压浓缩得提取物浸膏2.7 g,浸膏过硅胶(200~300目)柱层析,以石油醚-丙酮(100∶0→ 1∶1)梯度洗脱,经薄层色谱检测合并相似组分后得10个组分(Fr1~Fr10),将Fr2经HPLC制备,以甲醇-水(74∶26,v/v,流速3 mL﹒min-1)洗脱,得到化合物1(2.3 mg,Rt = 14.9 min)和组分Fr2-2,将组分Fr2-2以甲醇-水(55∶45,v/v,流速3 mL﹒min-1)洗脱,得到化合物2(6.8 mg,Rt= 27.1 min)和化合物3(7.1 mg,Rt= 30.0 min);将Fr3经HPLC制备,以甲醇-水(50∶50,v/v,流速3 mL﹒min-1)洗脱,得到化合物4(2.0 mg,Rt= 26.1 min);将Fr5经HPLC制备,以(甲醇-水,15∶75,v/v,流速3 mL﹒min-1)洗脱,得到化合物5(2.3 mg,Rt= 22.9 min);将Fr7经HPLC制备,以甲醇-水(45∶55,v/v,流速3 mL﹒min-1)洗脱,得到化合物6(12.1 mg,Rt = 26.1 min)。将Fr8经HPLC制备,以甲醇-水(70∶30,v/v,流速3 mL﹒min-1)洗脱,得到化合物7(7.2 mg,Rt = 52.5 min);将Fr9经HPLC制备以甲醇-水(85∶15,v/v,流速3 mL﹒min-1)洗脱,得到化合物8(2.4 mg,Rt= 93.6 min)。
3 实验结果
3.1 结构鉴定
化合物1 白色粉末;ESI-MSm/z415 [M+H]+。1H NMR (400 MHz, CD3OD) δ: 5.70 (1H, dd,J= 16.0,0.9 Hz, H-22), 5.59 (2H, dd,J= 13.5, 6.5 Hz, H-7, 23),5.54 (1H, d,J= 6.1 Hz, H-1), 4.30-4.23 (1H, m, H-24),3.45 (1H, m, H-3), 3.11 (3H, s, -OCH3), 2.83 (1H, dd,J= 12.1, 5.4 Hz, H-4α), 2.76 (2H, d,J=4.2 Hz, H-5, 9),2.66-2.55 (2H, m, H-18), 2.51-2.43 (1H, m, H-2β), 2.25-2.15 (3H, m, H-2α, 12β, 14), 1.82-1.73 (3H, m, H-16,17,), 1.69-1.64 (2H, m, H-4β, 11β), 1.58 (2H, ddd,J=15.7, 12.3, 4.5 Hz, H-11α, 15β), 1.49 (2H, dd,J= 12.7,4.3 Hz, H-12α, 15α), 1.31 (3H, s, H-21), 1.24 (3H, d,J= 6.4 Hz, H-25), 0.78 (3H, s, H-19);13C NMR (100 MHz, CD3OD) δ: 207.7 (C-6), 160.3 (C-8), 147.7 (C-10), 135.9 (C-22), 135.1 (C-23), 125.7 (C-7), 123.0 (C-1),81.0 (C-20), 69.1 (C-24), 65.3 (C-3), 61.9 (C-17), 57.0(C-14), 55.6 (C-9), 50.0 (23-OCH3), 47.7 (C-5), 46.7 (C-13), 42.2 (C-4), 40.7 (C-12), 36.9 (C-2), 28.9 (C-18),28.5 (C-11), 23.8 (C-25), 23.5 (C-16), 22.1 (C-21), 22.0(C-15), 15.2 (C-19)。以上数据与文献[5]中报道的波谱数据基本一致,故将该化合物鉴定为20-O-methyl-24-epi-cyclocitrinol。
化合物2 白色粉末;ESI-MS m/z 417 [M+H]+。1H NMR (400 MHz, CD3OD) δ: 5.79 (1H, d,J= 15.7 Hz, H-1), 5.66-5.57 (2H, m, H-22, 23), 5.53 (1H, s,H-7), 4.28-4.20 (2H, m, H-15α, 24), 3.25 (1H, m, H-3),2.88-2.73 (3H, m, H-4α, 5, 9), 2.66-2.55 (2H, m, H-18),2.52-2.42 (1H, m, H-2β), 2.21 (4H, dd,J= 19.9, 13.3 Hz, H-2α, 12β, 14, 16β), 1.93-1.79 (2H, m, H-11β, 17),1.74 (1H, dd,J= 15.2, 8.9 Hz, H-4β), 1.70-1.48 (3H, m,H-11α, 12α, 16α), 1.32 (3H, s, H-21), 1.22 (3H, d, J =6.3 Hz, H-25), 0.81 (3H, s, H-19);13C NMR (100 MHz,CD3OD) δ: 207.6 (C-6), 160.2 (C-8), 147.6 (C-10), 138.0(C-22), 131.8 (C-23), 125.7 (C-7), 123.1 (C-1), 75.7 (C-20), 69.5 (C-24), 69.2 (C-15), 65.3 (C-3), 63.9 (C-14),57.1 (C-17), 55.5 (C-9), 50.0 (C-5), 47.6 (C-13), 42.2(C-4), 40.6 (C-12), 36.8 (C-2), 35.1 (C-16), 29.0 (C-18),28.8 (C-21), 28.5 (C-11), 23.8 (C-25), 15.0 (C-19)。以上数据与文献[6]中报道的波谱数据基本一致,故将该化合物鉴定为(15S)-15-hydroxy-24-epi-cyclocitrinol。
化合物3白色粉末;ESI-MSm/z417 [M+H]+。1H NMR (400 MHz, CD3OD) δ: 5.79 (1H, dd,J= 15.7,1.0 Hz, H-1), 5.66-5.58 (2H, m, H-22, 23), 5.53 (1H, s,H-7), 4.24 (2H, brdd,J= 5.6 Hz, H-16α, 24), 3.25(1H,m, H-3), 2.84 (2H, dd,J= 11.9, 5.0 Hz, H-5, 9), 2.78-2.73 (1H, m, H-4α), 2.66-2.55 (1H, m, H-18α), 2.47 (2H,ddd,J= 13.3, 11.4, 6.2 Hz, H-2β, 14, ), 2.27-2.16 (2H,m, H-2α, 12β), 1.92-1.83 (1H, m, H-15β), 1.82-1.73 (1H,m, H-11β), 1.70-1.64 (1H, m, H-17), 1.64-1.49 (5H, m,H-4β, 5, 11α, 12α, 15α), 1.32 (3H, s, H-21), 1.23 (3H,d,J= 6.4 Hz, H-25), 0.82 (3H, s, H-19);13C NMR (100 MHz, CD3OD) δ: 207.6 (C-6), 160.2 (C-8), 147.6 (C-10), 137.8 (C-22), 131.9 (C-23), 125.7 (C-7), 123.1 (C-1), 75.8 (C-20), 72.8 (C-16), 71.5 (C-17), 69.0 (C-24),65.3 (C-3), 57.1 (C-14), 55.5 (C-9), 50.0 (C-5), 49.9 (C-13), 42.2 (C-4), 40.6 (C-12), 36.8 (C-2), 36.1 (C-15),29.0 (C-21), 28.9 (C-18), 28.5 (C-11), 23.8 (C-25), 15.0(C-19)。以上数据与文献[7]中报道的波谱数据基本一致,故将该化合物鉴定为(16R)-16-hydroxy-24-epicyclocitrinol。
化合物4 白色粉末;ESI-MSm/z233 [M+H]+。1H NMR (400 MHz, CDCl3) δ: 12.27 (1H ,s, 8-OH), 12.27(1H, s, 1-OH), 6.72 (1H, s, H-5), 6.63 (1H, s, H-7), 5.45(1H, d,J= 5.2 Hz, H-1), 3.11 (1H, m, H-3β), 2.83 (1H ddd,J= 18.0, 9.3, 5.0 Hz, H-3α), 2.51 (1H, td,J=13.9,8.1 Hz, H-2a), 2.36 (3H, m, 6-CH3), 2.04 (1H, m, H-2b);13C NMR (100 MHz, CDCl3) δ: 181.5(C-9), 172.1 (C-5), 161.0 (C-8), 157.9 (C-4a), 147.0 (C-6), 121.3 (C-9a), 112.8 (C-7), 109.2 (C-8a), 108.0 (C-5), 71.3 (C-1),30.1 (C-3), 29. 6 (C-2), 22.5 (C-6)。以上数据与文献[8]中报道的波谱数据基本一致,故将该化合物鉴定为coniochaetones B。
化合物5白色粉末;ESI-MSm/z: 138 [M + H]+。1H NMR (400 MHz, CDCl3) δ: 8.01 (2H, m, H-2, 6), 6.97(2H, m, H-3, 5);13C NMR (100 MHz, CDCl3) δ: 165.9(C-7), 163.3 (C-4), 133.2 (C-2, 6), 122.9 (C-1), 115.8(C-3, 5)。以上数据与文献[9]中报道的波谱数据基本一致,故将该化合物鉴定为4-Hydroxybenzoic acid。
化合物6白色粉末;ESI-MSm/z: 121 [M-H]-。1H NMR (400 MHz, CDCl3) δ: 8.17 (2H, d,J= 7.2 Hz,H-2, 6), 7.65 (1H, t,J= 7.0 Hz, H-4), 7.55 (2H, t,J= 7.1 Hz, H-3, 5);13C NMR (100 MHz, CDCl3) δ: 173.6 (C-7),134.2 (C-4), 131.0 (C-2, 6), 128.7 (C-1), 127.5 (C-3, 5)。以上数据与文献[10]中报道的波谱数据基本一致,故将该化合物鉴定为benzoic acid。
化合物7无色油状;ESI-MSm/z279 [M+H]+。1H NMR (400 MHz, CDCl3) δ: 7.71 (2H ,dd,J= 5.7, 3.3 Hz, H-3, 3'), 7.52 (2H, dd,J= 5.7, 3.3 Hz, H-4, 4'), 4.31(2H, t,J= 6.7 Hz, H-6, 6'), 1.72 (2H ,dt,J= 14.6, 6.8 Hz, H-7, 7'), 1.44 (2H, d,J= 14.7, 7.4 Hz, H-8, 8'), 0.96(6H t,J= 7.4 Hz, H-9, 9');13C NMR (100 MHz, CDCl3)δ: 167.9 (C-5, 5'), 132.5 (C-2, 2'), 131.0 (C-4, 4'), 129.0(C-3, 3'), 65.7 (C-6, 6'), 30.7 (C-7, 7'), 19.3 (C-8, 8'),13.9 (C-9, 9')。以上数据与文献[11]中报道的波谱数据基本一致,故将该化合物鉴定为5,5'-diisobutoxy-2,2'-bifuran。
化合物8黄色油状;ESI-MSm/z389 [M-H]-。1H NMR (400 MHz, CDCl3) δ: 7.71 (2H, m, H-3'', 6''),7.53 (2H, dd,J= 4.7, 2.4 Hz, H-4'', 5''), 4.21 (4H, dd,J= 13.6, 8.7 Hz, H-1, 1'), 1.72 (2H, m, H-2, 2'), 1.45-1.25 (16H, m, H-3, 3', 4, 4', 5, 5', 7, 7'), 0.96-0.86 (12H,m ,H-6, 6', 8, 8');13C NMR (100 MHz, CDCl3) δ: 167.9(2×C=O), 132.6 (C-1'', 2''), 131.0 (C-3'', 6''),129.0 (C-4'',5''), 68.3 (C-1, 1'), 38.9 (C-2, 2'), 30.5 (C-3, 3'), 29.1 (C-4,4'), 23.9 (C-7, 7'), 23.1 (C-5, 5'), 14.2 (C-8, 8'), 11.1 (C-6, 6')。以上数据与文献[12]中报道的波谱数据基本一致,故将该化合物鉴定为bis(2-ethylhexyl)phthalate。
4 结论与讨论
本次实验从新鲜冬虫夏草药材中分离得到一株内生菌,通过ITS测序比对鉴定为毛霉菌M. luteus,毛霉菌又名黑霉、长毛霉,是接合菌亚门接合菌纲毛霉目毛霉科真菌中的一个大属,存在于禾草、土壤、粪便等环境中,在高温、高湿度以及通风不良的条件下生长良好。将其进行液体发酵后得到次级代谢产物,从中共分离鉴定了8个化合物,其中1~5,7~8共计7个化合物为首次从M. luteus中分离得到。经查阅相关文献报道,从化合物1具有抑制人细胞癌的作用[5],化合物8能够通过影响与激素相关基因蛋白的表达从而引起内分泌紊乱并干扰大鼠性激素的合成,从而使其生殖功能产生障碍[13]。此外,毛霉菌的次级代谢产物1-Hydroxy-4-methyl-2,4,6-dodecatrienoic acid还具有细胞毒活性[14]、吲哚二萜类化合物采用MTT和SRB方法使用阿霉素用作阳性对照,发现对HL-60(人白血病)和A549(人肺腺癌)细胞有细胞毒活性[15]。

