糖尿病性勃起功能障碍与性激素水平相关性研究
陈 诚
(四川省遂宁市中心医院内分泌代谢内科,四川 遂宁 62900)
糖尿病性勃起功能障碍(DED)为男性糖尿病患者发生率较高的一种慢性并发症,研究称勃起功能障碍(ED)发生率为35%~70%,且随着病程与年龄增长其发生率也相应提升,相较于非糖尿病患者,DED发生高出三倍,且发生时间早10年左右[1]。目前临床多认为多种因素密切关联于糖尿病患者ED发生,且大量基础研究已经证实其作用,但临床对DED中性激素的作用存在争议[2]。笔者选取我院收治的85例男性糖尿病患者为研究对象,探讨DED与性激素水平间存在的关联性。现报告如下。
1 资料与方法
1.1一般资料:选取我院2016年7月~2017年7月收治的男性糖尿病患者85例为研究对象,均与2型糖尿病诊断标准相符,年龄29~76岁,平均(45.9±8.4)岁。其中合并性勃起功能障碍(ED)患者45例,未合并ED者40例。所有对象均已婚,无严重心脑血管疾病史、肝肾功能不全或肾上腺、性腺及甲状腺功能异常,无生殖器解剖畸形、外伤疾病史、手术史,无脊髓及大脑病变,无长期摄取会诱发勃起功能障碍的用药史,12个月内无抗性激素或性激素类药物应用史。
1.2一般方法:采用调查表对患者勃起功能障碍程度予以了解,并用国际勃起功能指数-5(IIEF-5)评估,按照如下标准判断DED:以往无勃起功能障碍现象,确诊为糖尿病后勃起功能指数≤21分,无神经损伤如脊髓等、泌尿生殖道病变、抗高血压药物诱发的ED。常规检测两组FPG、2hPG及HbA1c,并应用免疫化学法发光法定量测量两组LH、FSH、E2及T指标水平。
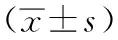
2 结果
两组性激素水平及血糖水平比较:见表1。
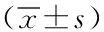

组别例数FPG(mmHg)2hPG(mmHg)HbA1c(%)FSH(μIU/ml)T(ng/ml)E2(pg/ml)LH(μIU/ml)ED组4510.4±2.715.0±3.711.8±2.17.0±1.34.1±0.718.7±3.45.6±1.4非ED组4010.5±2.912.9±3.19.8±1.58.7±1.95.6±1.016.7±2.65.2±1.1t值0.0450.7613.5180.6242.8160.3380.061P值>0.05>0.05<0.05>0.05<0.05>0.05>0.05
3 讨论
男性性功能障碍多表现为感觉障碍、性欲异常、异常勃起或射精异常及ED等,以ED最重要,即阴茎无法获取持续勃起或维持足够勃起以实现满意的性生活的疾病,临床发生率较高。当前临床多应用IIEF评估ED,研究称其特异性为88%、敏感性为98%,为临床诊断ED及评估疗效的最佳量化指标[3]。糖尿病患者中ED发生率高,且病程与年龄增长后发病率也逐渐提升。本组ED发生率为52.9%,与文献报道相近[4],说明对于男性糖尿病患者而言ED为主要并发症,对患者生活质量影响较大,因此一定要高度重视。
研究表明,相较于健康男性,2型糖尿病中老年(40~69岁)男性患者血清游离睾酮水平下降,迟发性性腺功能减退症也有更高的发生风险;2型糖尿病男性与同年龄健康组比较血清总睾酮、游离睾酮及生物有效性睾酮均降低,且多数表现为迟发性性腺功能减退症。另有研究调查,2型糖尿病男性患者,与非ED的2型糖尿病患者比较ED的2型糖尿病患者有更低的游离睾酮与生物有效性睾酮水平。本组结果表明ED组HbA1c水平高于非ED组,T水平低于非ED组,两组比较,差异有统计学意义(P<0.05);其他指标如FPG、2 hPG、FSH、E2及LH比较差异无统计学意义(P>0.05),说明睾酮、HbA1c为DED独立危险因素,与临床证实的病程、年龄等因素类似。睾酮水平降低可能通过以下机制诱发ED:正常阴茎勃起主要对阴茎解剖结构的完整性产生依赖,睾酮可通过增生或凋亡细胞对阴茎海绵体组织结构正常性予以维持,降低睾酮水平可增加海绵体细胞组织凋亡风险,破坏阴茎组织结构后诱发ED;阴茎组织中睾酮依赖区占比为60%~70%,睾酮水平降低后会抑制阴茎中该区睾酮NOS活性,减少合成NO量,降低血管舒张功能后诱发ED;此外,睾酮水平降低也会降低性欲,诱发勃起功能障碍。由此可知,DED密切关联于睾酮水平降低。
[1] 周 华,孙志兴,项子良,等.二地鳖甲煎联合他达拉非治疗糖尿病性勃起功能障碍35例[J].南京中医药大学学报,2015,(5):491.
[2] 杨丕坚,吕以培,李舒敏,等.糖尿病性勃起功能障碍与血管内皮功能的相关性[J].中国老年学杂志,2012,32(22):5072.
[3] 林向楠,石 磊,高振利,等.糖尿病性勃起功能障碍中血管因素发病机制的研究[J].中国男科学杂志,2016,30(10):66.
[4] 李进兵,吕立国,覃 勇,等.糖尿病性勃起功能障碍患者阴茎血管形态及血流动力学改变[J].中国老年学杂志,2012,32(12):2468.

