双动全髋关节置换治疗移位性股骨颈骨折的疗效分析
陈 辉
股骨颈骨折在全身骨折中占较大比例,而老年人因为骨质疏松等易造成骨折,并且很多会发生骨折移位,即移位性股骨颈骨折、股骨头坏死,病死率高达76%[1]。因此,发生这种情况一般均采取手术治疗,如人工股骨头置换术、内固定治疗以及全髋关节置换术[2]。采用内固定治疗虽然创伤较小,但是手术失败率较高,与关节置换手术比较功能改善不明显且并发症发生率高[3]。全髋关节置换术是最优选择,尤其是在髋臼磨损方面效果明显,但术后脱位却是一大问题[4-7]。鉴于此,本文主要对双动全髋关节置换(爱康APP生物系列半髋关节置换)治疗移位性股骨颈骨折的疗效进行分析,为临床治疗提供参考。
临床资料
1 一般资料
2015年2月—2017年2月就诊的移位性股骨颈骨折的老年患者36例作为研究对象,按随机数字表法分为试验组和对照组(各18例)。两组男女比例、平均年龄、骨折分型和受伤原因比较差异无统计学意义(P>0.05),见表1。所有研究对象入院后均被告知两种手术方案的优点与风险,经医院伦理委员会审核通过,并签署知情同意书。
纳入标准:经术前X线及计算机体层摄影等检查确诊股骨颈骨折、GardenⅢ型或Ⅳ型;单侧受伤且同侧无手术史;患者受伤前身体一般状况良好;能够配合服从试验安排,定期随访。排除标准:多发骨折、病理性骨折、陈旧性骨折,合并有严重的血管、神经损伤者;同侧髋部或股骨既往有手术史;无法定期随访。

表1 两组患者基本资料比较
2 治疗方法
试验组采取双动(dual articulation,DAC)全髋关节置换治疗:患者椎管内麻醉及静脉复合麻醉后侧卧位,后侧切口直至臀大肌,切断外旋肌群,将关节囊切开后切出股骨颈,测量股骨头直径;用小号髋臼锉将清理过的髋臼和四周软组织垂直打磨直至看到髋臼底部,以外展45°、前倾15°方向以小于股骨头直径2cm打磨到软骨下骨,取规格符合的髋臼杯将其固定匹配。通过屈髋、屈膝动作使髋关节方向转变之后露出股骨近端,用髓腔锉慢慢逐步挫磨股骨髓腔,使假体在股骨侧以10°~15°前倾固定,通过压头器将股骨头压入内衬里,实现髋关节复位,之后进行髋关节弯曲等动作检查是否出现脱位。如果没有出现活动出血则清洗伤口放置常规引流,缝合切口。使用生物型假体(爱康生物半髋APP系列)。
对照组采取传统全髋关节置换治疗:按照传统方法对患者进行常规手术臼杯安装、置换髋关节等并进行固定检查无松动之后清洗缝合伤口。
围手术期处理:手术前30min和手术后3d内常规抗生素预防感染,术后锻炼下肢肌肉及收缩功能。使用低分子肝素钠常规预防血栓。整个恢复过程中第1天观察引流管是否出现异常,如果没有异常第2天撤除。手术后2~5d练习辅助下地行走,半个月后完全负重行走,确保手术1个月后不需要任何辅助器具即可行走。
3 研究指标
观察两组患者手术时间、术中出血量、术后下床时间及围手术期并发症发生情况并记录。所有患者均进行电话随访、门诊复查,随访时间为12~26个月(平均17.5个月),由同一医师进行评价。
4 质量控制
功能学评价:采用Harris评分[6]评估术前,术后1、3、6、9及12个月时髋关节功能,满分为100分,90~100分为优,80~89分为良,70~79分为中,<70分为差。采用欧洲生活质量EQ-5D评分[7]评定患者术后12个月的健康生活质量。影像学评价:复查时行X线检查判断有无假体松动、下沉等并发症。
5 统计学分析
结 果
1 两组患者围手术期治疗情况分析
通过对患者围手术期治疗情况进行分析,结果显示,试验组的手术时间、术中出血和下床时间低于对照组,两组比较差异有统计学意义(P<0.01)。见表2。
表2 两组患者围手术期治疗情况比较
2 两组患者髋关节功能恢复情况分析
通过对患者髋关节功能恢复情况进行分析,结果显示,术后两组患者髋关节功能恢复情况均较好;术后1、3、6、9和12个月,试验组的Harris评分高于对照组,两组比较差异有统计学意义(P<0.05)。见表3。
3 两组患者健康生活质量分析
通过对两组患者健康生活质量进行比较分析,结果显示,试验组术后12个月时健康生活质量优于对照组,两组比较差异有统计学意义(P<0.05)。见表4。
表3 两组患者术前及术后Harris评分比较
与对照组Harris评分比较:+χ2=9.395,P=0.011
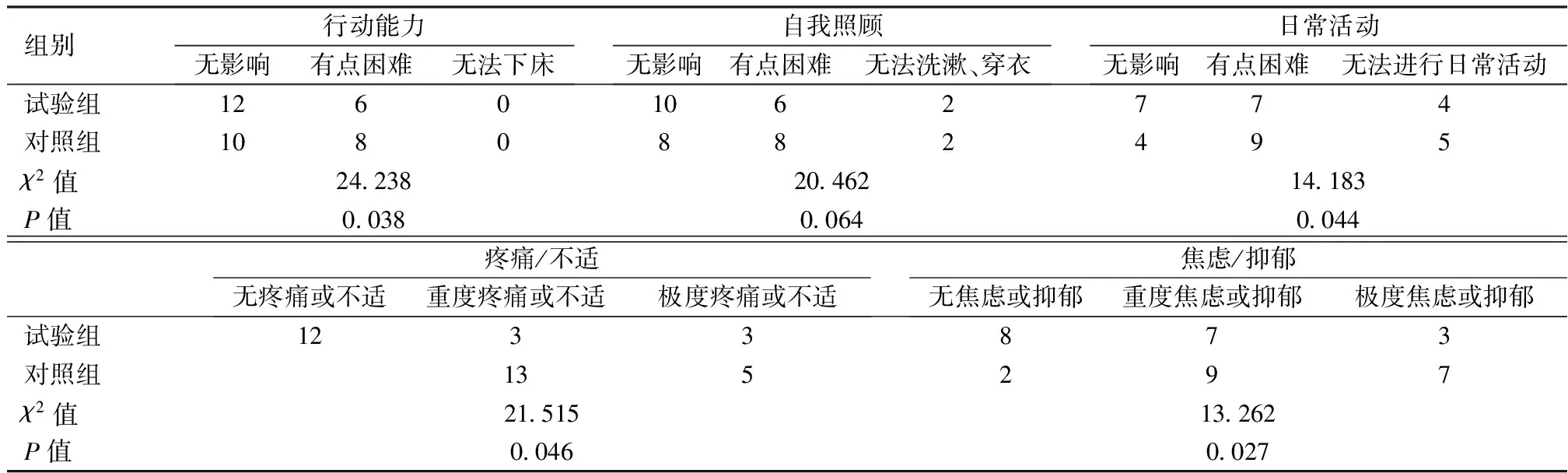
表4 两组患者术后12个月时健康生活质量比较(n)
讨 论
随着老年人群所占比重的增加,老年股骨颈骨折的发病率逐年提升。Schilcher等[8]指出发生股骨颈骨折的原因是因为力量方向的改变,轴向应力增大转换为角应力导致剪切而形成骨折。而老年人因为肌肉比较松弛,加上存在骨质疏松,因而容易发生骨折[9]。目前,关于双动全髋关节置换与传统全髋关节治疗的疗效报道并不一致,本研究比较了两种方法治疗老年移位性股骨颈骨折的临床效果,以期为临床决策提供参考。
随着现代医学的快速发展,临床研究人员一致认为如果患者无手术禁忌应该尽早采取手术治疗,能够更快地减轻疼痛,恢复活动能力。采用何种手术进行治疗要根据患者年龄以及发生骨折位移的严重程度,可采用的方法有内固定以及置换关节。临床上优先采取的是人工关节置换手术,因为内固定手术的患者卧床时间较长,体内的血供还未得到改善,容易造成患者病情加重致死。采用人工髋关节置换手术的患者能够更早地下床活动,并得到良好的髋关节锻炼,但是由于多数老年患者髋部肌肉功能松弛,采用传统的置换关节手术后会有10%出现脱位的情况。在上世纪七十年代末有研究人员提出DAC的概念,如双动人工股骨头,区别之处是在股骨头假体和金属臼杯之间的内衬材质是高分子聚乙烯,这使得假体和臼杯自成关节,能够降低脱位的发生概率。
股骨颈部四周没有肌肉,所以该处受力的大小和髋关节差不多,合力的走线没有和股骨颈受力平行,当出现交叉的时候,延伸外展向下在股骨颈上形成张压力,且压力大于张力,内侧缘压力最大,股骨颈中轴力度最小,因为合力斜向作用与股骨颈,所以很容易变成剪力,这种力的大小是由合力和股骨颈轴线形成的角度一起形成的。
Nebergall等[10]认为采用传统的轴向固定方式不符合人体生物力学,下针的地方外侧股骨皮薄,且又要经过Ward氏三角区,这个地方是最脆弱的,所以作用不大。同时Nebergall等[10]的研究亦显示,通过对合力和扭转力各种角度的计算得到从力干角方向下手,也就是股骨下侧呈23°的位置,这种进针角度比较合理。D’Apuzzo等[11]认为进行股骨颈骨折内不固定的要求必须能够抵抗得了骨折线上的剪力,平衡弯力,轴心上的应力能够抵抗。
通过对比双动全髋关节置换和以往的全髋关节置换在手术之后发生脱位或松动的概率数据发现,前者发生的概率明显要低于后者,原因和置换的关节构造有关。前者的关节构造是置换的股骨头假体和臼杯之间有一个内衬,这个由聚乙烯组成的内衬让假体跟臼杯之间能够无拘束地大直径活动,能降低脱位的概率。Homma等[12]通过对法国MOUSSA地区119例患者的跟踪发现,在第一次手术时采用双动全髋关节置换手术的患者能够更好地缓解疼痛,手术后恢复髋关节活动速度快,脱位率低。进行双动全髋关节置换手术不仅能够控制脱位率下降,还能够降低关节磨损率,这种材质的内衬磨损每年平均0.082mm,而传统的磨损率是0.096~0.200mm,同时内衬提供了假体更多的活动空间,旋转角度可以超过220°,屈伸度达到186°,要远远超过传统的髋关节假体[13]。
本文研究结果显示,试验组的手术时间低于对照组[(65.1±13.2)minvs. (76.5±18.4)min],术中出血量低于对照组[(339.2±14.6)minvs. (440.1±23.8)min],下床时间低于对照组比为[(3.1±1.5)dvs. (4.6±2.4)d],两组比较差异有统计学意义(P<0.01)。术后,两组患者髋关节功能恢复情况都较好;术后1个月,试验组的Harris评分高于对照组[(49.9±10.1)分vs. (38.4±5.3)分],术后3个月,试验组的Harris评分高于对照组[(79.3±13.5)分vs. (68.9±8.7)分],术后6个月,试验组的Harris评分高于对照组[(89.6±11.8)分vs. (82.4±5.1)分],术后9个月,试验组的Harris评分高于对照组[(92.5±9.6)分vs. (84.6±6.3)分],术后12个月,试验组的Harris评分高于对照组[(94.7±5.3)分vs. (87.2±3.5)分],两组比较差异有统计学意义(P<0.05)。试验组术后12个月时健康生活质量优于对照组,两组比较差异有统计学意义(P<0.05)。这表明双动全髋关节置换在治疗老年移位性股骨颈骨折的效果优于传统全髋关节置换治疗,且在降低脱位、延长使用寿命方面具有更大的优势。
综上所述,与传统全髋关节置换治疗相比,双动全髋关节置换治疗移位性股骨颈骨折,能显著改善患者术后恢复情况,并更好提高患者的健康生活质量,值得临床上推广应用。
[1] Dimitriou D,Liow MH,Tsai T Y,et al.Early outcomes of revision surgery for taper corrosion of dual taper total hip arthroplasty in 187 patients[J].J Arthroplasty,2016,31(7):1549-1554.
[2] Kwon YM,Antoci V,Leone WA,et al.Utility of serum inflammatory and synovial fluid counts in the diagnosis of infection in taper corrosion of dual taper modular stems[J].J Arthroplasty,2016,31(9):1997-2003.
[3] D’Apuzzo M R,Koch C N,Esposito C I,et al.Assessment of damage on a dual mobility acetabular system[J].J Arthroplasty,2016,31(8):1828-1835.
[4] Plummer DR,Christy JM,Sporer SM,et al.Dual-mobility articulations for patients at high risk for dislocation[J].J Arthroplasty,2016,31(9):131-132.
[5] Tarity TD,Koch CN,Burket JC,et al.Fretting and corrosion at the backside of modular cobalt chromium acetabular inserts: a retrieval analysis[J].J Arthroplasty,2016,24(6):327-334.
[6] Xie J,Hu Q,Qiang H,et al.Comparison of intravenous versus topical tranexamic acid in primary total hip and knee arthroplasty: an updated meta-analysis[J].Thromb Res,2017,35(3)153:28-36.
[7] Kwon YM,Tsai TY,Leone WA,et al.Sensitivity and specificity of metal ion levels in predicting “pseudotumors” due to taper corrosion in patients with dual taper modular total hip arthroplasty[J].J Arthroplasty,2016,42(11):1435-1442.
[8] Schilcher J,Ivarsson I,Perlbach R,et al.No difference in periprosthetic bone loss and fixation between a standard-length stem and a shorter version in cementless total hip arthroplasty: a randomized controlled trial[J].J Arthroplasty,2016,7(2):269-274.
[9] Xia Z,Ricciardi BF,Liu Z,et al.Nano-analyses of wear particles from metal-on-metal and non-metal-on-metal dual modular neck hip arthroplasty[J].Nanomedicine,2016,11(5):582-586.
[10] Nebergall AK,Freiberg AA,Greene ME,et al.Analysis of dual mobility liner rim damage using retrieved components and cadaver models[J].J Arthroplasty,2015,31(7):1595-1602.
[11] D’Apuzzo MR,Koch CN,Esposito CI,et al.Assessment of damage on a dual mobility acetabular system[J].J Arthroplasty,2016,31(8):1828-1835.
[12] Homma Y,Baba T,Kobayashi H,et al.Benefit and risk in short term after total hip arthroplasty by direct anterior approach combined with dual mobility cup[J].Eur J Orthopc Surg Traumato,2016,26(6):1-6.
[13] Plummer DR,Christy JM,Sporer SM,et al.Dual-mobility articulations for patients at high risk for dislocation[J].J Arthroplasty,2016,31(9):131-137.

