棉花GhFAD2-1基因5’UTR内含子的克隆与序列分析
孙 亮,文 凤,刘 峰,张新宇,孙 杰
(石河子大学农学院,新疆石河子 832000)
0 引 言
【研究意义】在棉籽中,Δ12-油酸去饱和酶基因GhFAD2-1是控制油酸向亚油酸转化的关键酶基因,对棉籽中多不饱和脂肪酸的含量与比例起着重要的调控作用[1]。GhFAD2-1上游序列所包含的调控元件等是对其组织特异性、作用强弱和时空表达进行精确调控的关键。对GhFAD2-1上游序列相关转录调控元件及调控作用的识别成为理解其表达机制的必要步骤。研究克隆并分析棉花GhFAD2-1上游5'UTR内含子序列,对研究GhFAD2-1时空表达特性及调控的分子机制具有重要的意义。【前人研究进展】包括陆地棉(G.hirsutum)、海岛棉(G.barbadense)、雷蒙德氏棉(G.raimondii)以及鲁宾逊氏棉(G.robinsonii)等棉属的FAD2-1基因的上游序列都含有一个位于5'非翻译区(5'UTR)的内含子[2];GhFAD2-1的启动子序列则位于该5'UTR内含子的上游,由于GhFAD2-1的上游区域含有内含子,所以增加了其表达调控的复杂性。一直以来对其调控序列研究的不够深入。基因编码区的上游序列在很大程度决定着目的基因表达的时间、空间和强度。内含子是基因组中的一种重要元件,其对转录及转录后水平的基因表达水平起着重要的调控作用[3-4]。从目前已有的研究结果中,尚不能准确判定GhFAD2-1基因转录起始位点,5'UTR区内含子的剪切位点,其具体碱基序列及片段长度等。【本研究切入点】农业生产栽培的棉花主要是四倍体的陆地棉(G.hirsutum),其基因组AADD数据及相关基因编码序列等已经公布在棉花基因组数据库(http://www.cottongen.org)、NCBI等中,为研究进行序列比对分析奠定基础。【拟解决的关键问题】研究基于陆地棉GhFAD2-1基因编码区序列,设计特异性引物,通过进行5' RACE 扩增,获得完整的GhFAD2-1非翻译区(5'UTR)全长序列。通过结合5'-RACE获得GhFAD2-1基因的5'-端核苷酸序列与基因组扩增GhFAD2-1序列进行比较,获得GhFAD2-1基因5'-端UTR区域内的内含子序列,并对其进行作用原件分析,为进一步研究GhFAD2-1基因的表达与调控奠定基础。
1 材料与方法
1.1 +材 料
棉花(Gossypiumhirsutum)品种新陆早33号、大肠杆菌菌株E.coliDH5α等均为实验室保存。克隆载体pMD18-T、ExTaqDNA聚合酶、Clontech SMART RACE cDNA Amplification Kit、限制性内切酶、DNA Marker等购自大连宝生物公司。DNA凝胶回收试剂盒、Plant RNA快速提取试剂盒(离心柱型)等购自天根生化有限公司;其他试剂均为国产和进口分析纯。
1.2 方 法
1.2.1 5'-RACE获得GhFAD2-1基因的5'-端
取新陆早33号花后15 d的棉花种子,去除外层软壳后,将棉仁在研钵中用液氮冷激后快速研磨,将粉末快速装入RNase-free的离心管中,保证样品不溶解,并让液氮挥发,采用高纯总RNA快速提取试剂盒提取总RNA。
根据GenBank中已报道的棉花GhFAD2-1基因编码区的序列信息,利用Primer Premier 6设计特异性扩增引物FAD2-1-R: 5'-GGATGCAACCTTGGAGAACC-3';引物由上海生工公司合成。参照Clontech SMART RACE cDNA Amplification Kit说明,合成获得5'-RACE-Ready cDNA。以5'-RACE-Ready cDNA为模板,以已设计的特异性引物FAD2-1-R和5'-RACE Kit 中提供的UPM引物组成配对引物,进行PCR反应。PCR产物于1%的琼脂糖凝胶中,3 V/cm电泳45 min后,在紫外凝胶成像系统中观测目的条带。获得清晰的预期目标条带,进行胶回收。胶回收操作步骤参照天根生物公司胶回收试剂盒说明书。参照Takara公司pMD18-T Vector试剂盒说明将回收目的片段连接到pMD18-T Vector上。转化大肠杆菌DH5α,筛选抗Amp菌落,同时进行菌落PCR鉴定。挑选6个PCR阳性克隆送华大基因公司测序。
1.2.2GhFAD2-1基因的5'-端UTR内含子克隆与序列分析
以5'-RACE获得GhFAD2-1基因的5'-端核苷酸序列为基础:以转录起点处设计PCR特异性扩增上游引物;以翻译起始点处设计PCR特异性扩增下游引物。应用植物基因组提取试剂盒提取新陆早33号叶片基因组DNA。以新陆早33号基因组DNA为模板,进行PCR反应;PCR 产物于1%的琼脂糖凝胶中,3 V/cm 电泳45 min 后,在紫外凝胶成像系统中观测目的条带。胶回收、PCR鉴定等方法同上。挑选6个PCR阳性克隆送华大基因公司测序。
对比分析5'-RACE获得GhFAD2-1基因的5'-端核苷酸序列与上述基因组扩增的特异序列,鉴定出GhFAD2-1基因的5'-端UTR区域内的内含子序列,并对其进行生物信息学分析。顺式作用元件采用http://www.dna.affrc.go.jp/PLACE/以及http://bioinformatics.psb.ugent.be/webtools/plantcare/html/在线分析。
2 结果与分析
2.1 GhFAD2-1基因5端序列的克隆
应用高纯总RNA快速提取试剂盒(离心柱型)提取获得高质量的总RNA(图1);采用Clontech SMART RACE cDNA Amplification Kit将总RNA转录成cDNA。以反转录的cDNA为模板进行PCR扩增,在350 bp左右出现目标条带(图2)。取PCR阳性克隆进行测序。测序结果表明,cDNA扩增出两条序列,片段大小为362 bp。与GhFAD2-1基因编码区序列(GenBank: HQ259410)有285 bp 的重叠片段,表明GhFAD2-1基因5'端非翻译区(5'-untranslated region, 5'-UTR)长77 bp,转录的起点碱基为T(图3)。图1~3
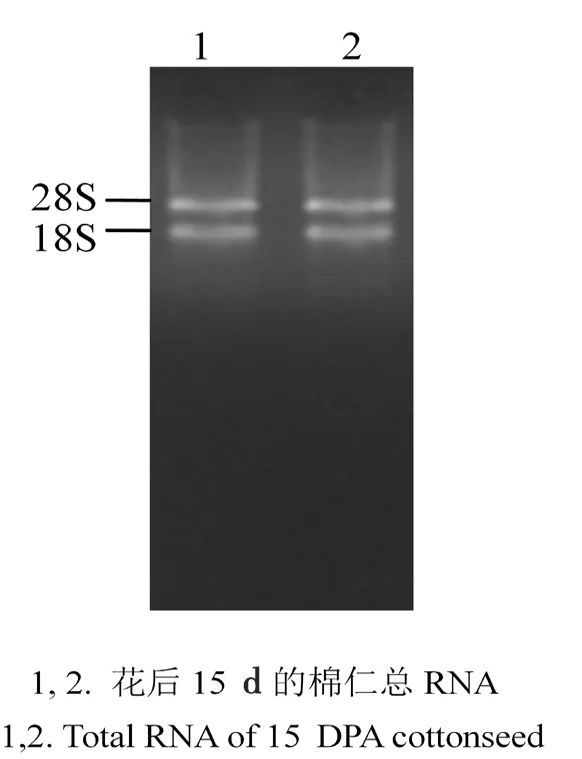
图1 新陆早33号提取的总RNA检测
Fig.1 The detection of total RNA of xinluzao33
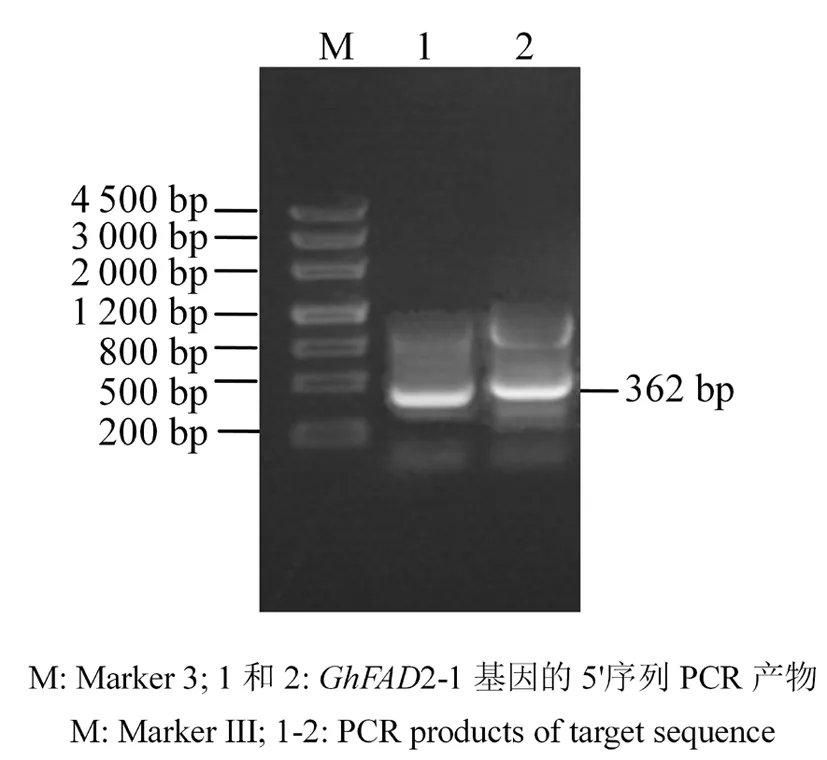
图2 5'-RACE扩增目标序列
Fig.2 5'-RACE technique of target sequence

图3 5'-RACE获得GhFAD2-1基因的5'-端序列
Fig.3 The 5'- end sequence of GhFAD2-1 was obtained by 5'-RACE technique
2.2GhFAD2-1基因5'UTR内含子克隆及序列
以新陆早33号基因组DNA为模板,以5'-RACE获得GhFAD2-1基因的5'-端核苷酸序列的转录起点为基础设计的特异性上游引物FAD2-1-5F: 5'-TCGCCCAAAACCAACACGCCT-3';以翻译起始点处设计特异性扩增下游引物FAD2-1-5R: 5'-CATCCTACCACCGGCACC-3'。PCR扩增产物电泳显示约在1 200 bp左右出现特异性条带(图4)。采用T-A克隆方法将PCR产物与pMD18-T连接、转化;6个PCR阳性克隆测序表明,所克隆获得的片段分成了两类:有4个克隆序列完全一致,片段全长为1 209 bp;另外2个克隆序列完全一致,片段全长为1 201 bp;两者有174个碱基差异(图5)。由于棉花是异源四倍体(AADD基因组);研究表明,扩增获得的高度同源的片段可能分别来源于A或D基因组。进一步对比棉花基因组数据库(http://www.cottongen.org)中的GhFAD2-1基因组的序列进行分析;结果表明,片段全长为1 201 bp与棉花基因组数据库中Gh_A13G1850(GhFAD2-1)的序列相吻合,表明该序列来源于A基因组。片段全长为1 209 bp与棉花基因组数据库中Gh_A13G1850(GhFAD2-1)的序列存在较多的碱基差异,推测其可能来源于D基因组。将其于棉花基因组数据库中Gh_D13G2238(GhFAD2-1)的序列进行对比分析;研究表明,两者的序列与较好的一致性,表明所克隆的1 209 bp序列来源于D基因组。值得注意的是,通过1 209 bp序列与基因组数据库中GhFAD2-1(Gh_D13G2238)的5'序列对比分析表明,棉花基因组数据库中Gh_D13G2238(GhFAD2-1)基因的上游出现冗余重复信息(位于起始密码子上游-1 880 bp~-693 bp),该序列全长1 187 bp;综合GhFAD2-1的5'RACE与基因组扩增研究结果,可以判定棉花基因组数据库中Gh_D13G2238(GhFAD2-1)基因上游的序列在基因组测序时或基因组组装过程中,出现了错误。当将棉花基因组数据库中Gh_D13G2238(GhFAD2-1)基因的上游的错误重复冗余1 187 bp序列删除后,其序列就与所克隆获得的片段全长为1 209 bp的序列完全一致。
结合5'-RACE获得GhFAD2-1基因的5'-端核苷酸序列与基因组扩增获得序列,进一步分析比较。研究表明,位于A基因组的GhFAD2-1基因5'-端UTR区域内的内含子序列全长1 103 bp;位于D基因组的GhFAD2-1基因5'-端UTR区域内的内含子序列全长1 111 bp(图5)。A和D基因组的GhFAD2-1基因5'-端UTR区域内的内含子的剪切位点相同,5'-端UTR内含子两个剪切位点分别AA-GG、CA-GC。这表明,该内含子剪切位点不具有GT-AG规则,并且序列中富含AT,其剪切位点可能为一新的剪切方式。
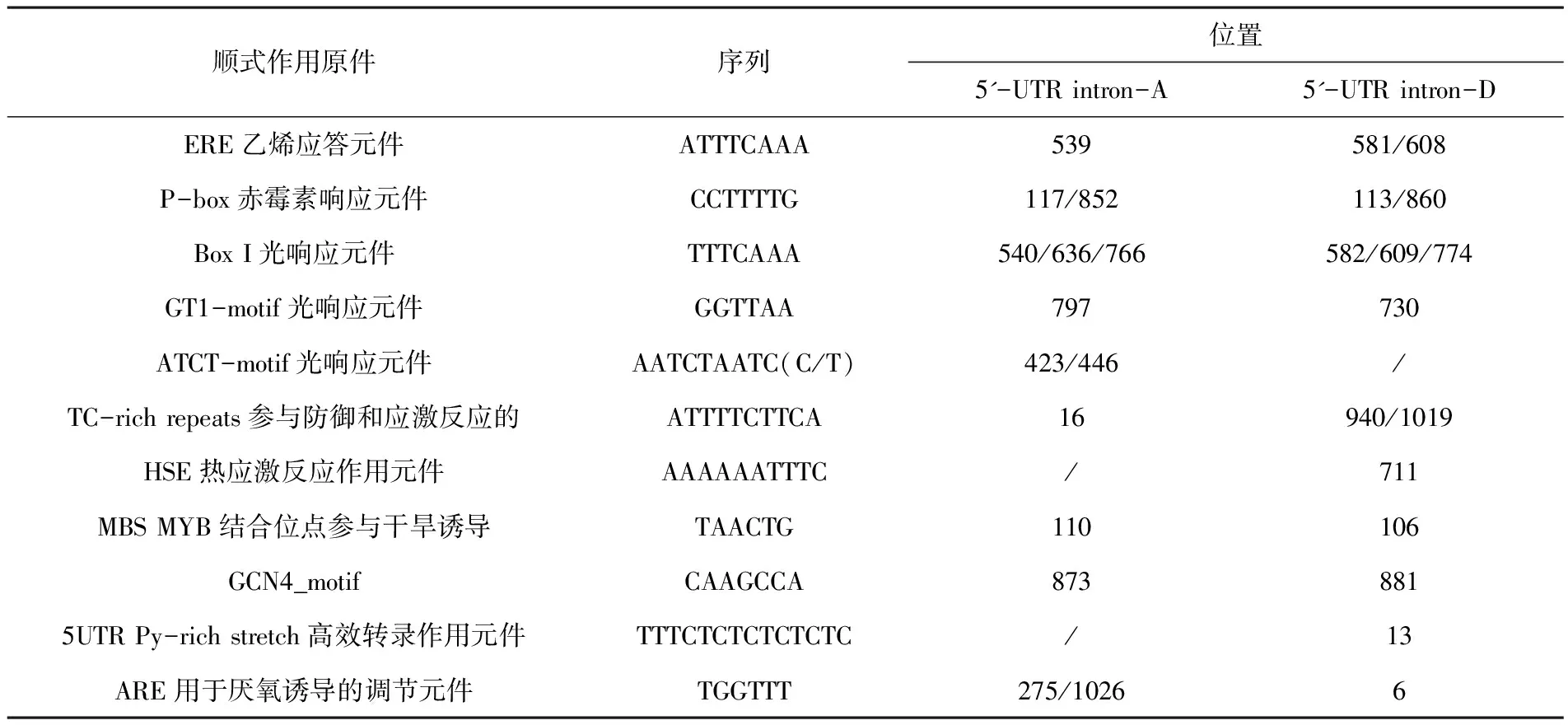
使用PlantCARE 在线分析克隆到的GhFAD2-1 5'-端UTR内含子序列的顺式作用元件,结果表明,在A基因组和D基因组序列中都具有与激素相关的作用原件:乙烯应答元件ERE(ATTTCAAA)和赤霉素响应元件P-box(CCTTTTG),以及胁迫等相关的作用元件,如干旱诱导元件MBS(TAACTG)、防御和应激反应元件TC-rich repeats(ATTTTCTTCA)等。GhFAD2-1 5'-端UTR内含子序列还含有与光响应相关的作用元件Box I(TTTCAAA)、GT1-motif(GGTTAA)、ATCT-motif(AATCTAATCC)等。在A基因组和D基因组序列中都还具有种子特异的表达元件GCN4_motif(CAAGCCA),这也与GhFAD2-1在种子优势表达这一组织特异性表达相一致。此外,在D基因组中,GhFAD2-1 5'-端UTR内含子序列还包含高效转录作用元件5UTR Py-rich stretch(TTTCTCTCTCTCTC)。GhFAD2-1 5'-端UTR内含子序列包含的主要顺式作用元件及其在内含子序列上的位置。图4,图5,表1
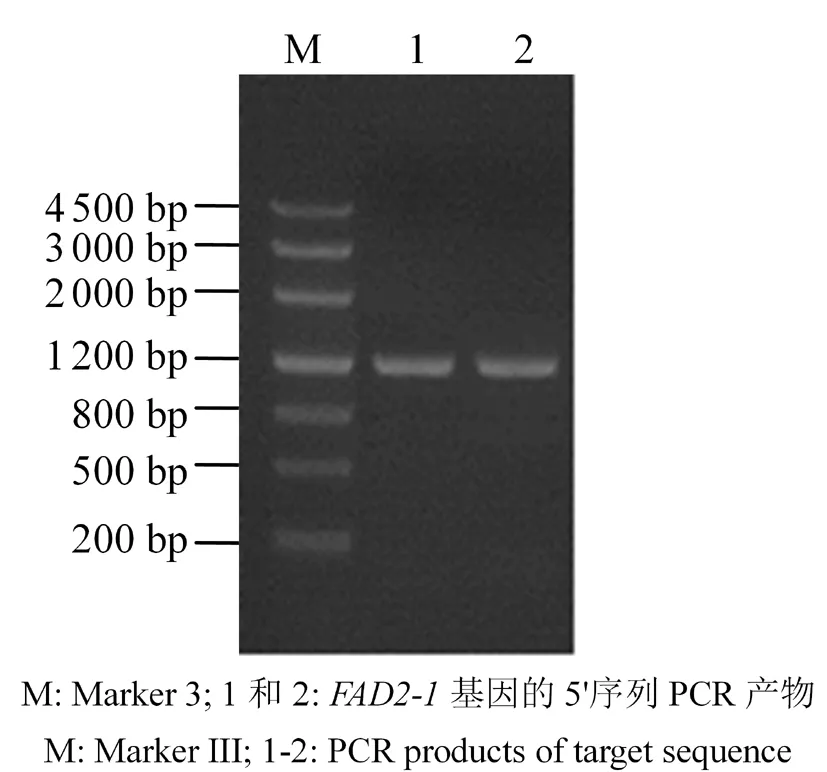
图4 PCR扩增目标序列
Fig.4 PCR amplification of target sequence

注:5'UTR_intron_A: 棉花D基因组GhFAD2-1基因5'-UTR及内含子; 5'UTR_intron_D: 棉花D基因组GhFAD2-1基因5'-UTR及内含子红色字体为碱基差异;加粗字体为起始密码子;下划线为基因组PCR扩增相对应的引物序列;aaGG、CAgc分别为5'-端UTR内含子两个剪切位点
Note: 5'UTR_intron_A: 5'- terminal UTR and intron sequence of GhFAD2-1from a A-genome cotton; 5'UTR_intron_D: 5'- terminal UTR and intron sequence of GhFAD2-1from a D-genome cotton; Red fonts represents base differences; The bold font represents the start codon; The underline is the sequence corresponding to the primers; The aaGG and CAgc are two 5'- terminal UTR intron splice site, respectively
图5 GhFAD2-1基因5'-端UTR及内含子
Fig.5 5'-UTR and intron sequence of GhFAD2-1
表1 GhFAD2-1 5'UTR内含子区顺式调控元件
Table 1 The cis regulatory elements of GhFAD2-1 5'UTR intron
顺式作用原件序列位置5'-UTRintron-A5'-UTRintron-DERE乙烯应答元件ATTTCAAA539581/608P-box赤霉素响应元件CCTTTTG117/852113/860BoxI光响应元件TTTCAAA540/636/766582/609/774GT1-motif光响应元件GGTTAA797730ATCT-motif光响应元件AATCTAATC(C/T)423/446/TC-richrepeats参与防御和应激反应的ATTTTCTTCA16940/1019HSE热应激反应作用元件AAAAAATTTC/711MBSMYB结合位点参与干旱诱导TAACTG110106GCN4_motifCAAGCCA8738815UTRPy-richstretch高效转录作用元件TTTCTCTCTCTCTC/13ARE用于厌氧诱导的调节元件TGGTTT275/10266
3 讨 论
研究基于陆地棉GhFAD2-1基因编码区序列,通过进行5' RACE 扩增,结合基因组PCR扩增序列进行比较,分别克隆获得了A、D基因组的GhFAD2-1基因5'UTR内含子序列。通过序列比对分析,发现了D基因组GhFAD2-1基因基因的上游出现冗余重复信息(位于起始密码子上游-1 880 bp~-693 bp),该序列全长1 187 bp,可能是由于基因组测序或组装过程中导致的错误冗余信息。克隆获得的内含子序列富含AT,对棉花GhFAD2-1基因5'UTR内含子区顺式调控元件进行分析,发现其包括一些典型的与光响应相关的作用元件如Box I(TTTCAAA)、GT1-motif(GGTTAA)等;以及与激素(乙烯、赤霉素)和胁迫因素相关的应答元件等。这也与相关研究认为棉花等植物的FAD2基因的转录水平受到多种激素和非生物胁迫等因素的影响相一致[4-7]。
内含子是基因组中的一种重要元件,在许多植物中都已证实内含子的存在可以显著增强基因的转录效率,如在单子叶植物中能够提高基因表达量的内含子有来自玉米的Adh1、Sh1、Bz1、Hsp82、Actin、Ubi1和GapA1基因等[8-10]和来自水稻的SalT、Act1、OsTubA1和OsCDPK2基因等[11-12];在双子叶植物中可以提高表达量的内含子有来自矮牵牛的RbcS基因[13]和马铃薯的ST-LS1基因等[14]。内含子介导的增强效应一般在2~10倍左右,有的甚至可提高基因表达100倍以上[11]。尤其是当内含子位于转录本5'UTR时,可以显著增强基因的转录效率[15]。同时,不同内含子对同一基因表达增强的程度不同,玉米Shl基因的内含子1可以使报告基因表达水平增强40倍,而玉米Adhl基因的内含子1使报告基因的表达水平仅提高4倍。Adhl基因的内含子2和6均能不同程度的增强报告基因的表达水平,但内含子9却不能[16]。对于研究获得的棉花GhFAD2-1的5'UTR内含子是否发挥转录增强子的功能,其对所调控基因的转录程度的影响如何,仍有待于进一步研究。此外,D基因组5'UTR内含子序列中,具有高效转录作用元件5UTR Py-rich stretch,对于棉花GhFAD2-1在棉籽中是否是D亚组表达量高于A亚组表达量,也有待于进一步分析。对棉花GhFAD2-1基因的上游的调控序列的克隆研究,有助于进一步在分子水平上研究GhFAD2-1基因功能及其表达调控规律,进而为植物的遗传改良奠定了基础。
4 结 论
研究利用5'RACE技术,克隆获得棉花Δ12-油酸去饱和酶基因GhFAD2-1的5'UTR序列:GhFAD2-1成熟mRNA的5' UTR为77 bp;通过进一步分析棉花基因组序列,进而再利用PCR技术克隆获得GhFAD2-1的5'UTR内含子序列:在棉花的A、D基因组中,GhFAD2-1的5' UTR中各含有一个全长分别为1 103 bp、1 111 bp的内含子序列;其转录的起点碱基为T;5' UTR内含子两个剪切位点分别AA-GG、CA-GC。作用元件分析表明,内含子包括一些典型的与光响应相关的作用元件,以及与激素和胁迫因素相关的应答元件等。该研究的结果为进一步在分子水平上研究GhFAD2-1功能及其表达调控规律,进而为植物的遗传改良奠定了基础。
)
[1] Shanklin, J., & Cahoon, E. B. (1998). Desaturation and related modifications of fatty acids1.AnnualReviewofPlantPhysiology&PlantMolecularBiology, 49(49): 611-641.
[2] Liu, Q., Brubaker, C. L., Green, A. G., Marshall, D. R., Sharp, P. J., & Singh, S. P. (2001). Evolution of the fad2-1 fatty acid desaturase 5' utr intron and the molecular systematics of gossypium (malvaceae).AmericanJournalofBotany, 88(1): 92-102.
[3] 牛俊奇,吴朝兴,杨丽涛,等. 甘蔗SoNIN1基因结构及其内含子信息分析[J]. 生物技术通报,2014,(12):147-152.
Niu Jun-qi, Wu Chao-xing, Yang Li-tao, et al. (2014). Analysis of Genomic Structure and Introns of SoNIN1 Gene from Sugarcane [J].BiotechnologyBulletin, (12):147-152. (in Chinese)
[4] 李秀兰,姜曰水. 高等植物细胞器Ⅱ类内含子剪接的研究进展[J]. 植物生理学报,2017,53(8):1 365-1 371.
LI Xiu-Lan, JIANG Yue-Shui. (2017). Research progress of group II intron splicing in higher plant organelles [J].PlantPhysiologyJournal, 53(8):1,365-1,371. (in Chinese)
[5] Zhang, J., Liu, H., Sun, J., Li, B., Zhu, Q., & Chen, S., et al. (2012). Arabidopsis fatty acid desaturase fad2 is required for salt tolerance during seed germination and early seedling growth.PlosOne, 7(1): e30355.
[6] Matteucci, M., D'Angeli, S., Errico, S., Lamanna, R., Perrotta, G., & Altamura, M. M. (2011). Cold affects the transcription of fatty acid desaturases and oil quality in the fruit of olea europaea l. genotypes with different cold hardiness.JournalofExperimentalBotany, 62(10): 3,403-3,402.
[7] Kargiotidou, A., Deli, D., Galanopoulou, D., Tsaftaris, A., & Farmaki, T. (2008). Low temperature and light regulate delta 12 fatty acid desaturases (fad2) at a transcriptional level in cotton (gossypium hirsutum).JournalofExperimentalBotany, 59(8): 2,043-2,056.
[8] Donath, M., Mendel, R., Cerff, R., & Martin, W. (1995). Intron-dependent transient expression of the maize gapa1, gene.PlantMolecularBiology,28(4): 667-676.
[9] Callis, J., Fromm, M., & Walbot, V. (1987). Introns increase gene expression in cultured maize cells.Genes&Development, 1(10): 1,183-1,200.
[10] Maas, C., Laufs, J., Grant, S., Korfhage, C., & Werr, W. (1991). The combination of a novel stimulatory element in the first exon of the maize shrunken-1 gene with the following intron 1 enhances reporter gene expression up to 1,000-fold.PlantMolecularBiology, 16(2): 199-207.
[11] Morello, L., Bardini, M., Cricrì, M., Sala, F., & Breviario, D. (2006). Functional analysis of dna sequences controlling the expression of the rice oscdpk2, gene.Planta, 223(3): 479-491.
[12] Jeon JongSeong, Lee SiChul, Jung KiHong, Jun SungHoon, Kim ChanHong, & An GynHeung. (2000). Tissue-preferential expression of a rice α-tubulin gene, ostuba1, mediated by the first intron.PlantPhysiology, 123(3): 1,005-1,014.
[13] Dean, C., Favreau, M., Bond-Nutter, D., Bedbrook, J., & Dunsmuir, P. (1989). Sequences downstream of translation start regulate quantitative expression of two petunia rbcs genes.PlantCell, 1(2): 201-208.
[14] Leon, P., & Walbot, V. (1991). Transient gene expression in protoplasts of phaseolus vulgaris isolated from a cell suspension culture.PlantPhysiology, 95(3): 968-972.
[15] Bourdon, V., Harvey, A., & Lonsdale, D. M. (2001). Introns and their positions affect the translational activity of mrna in plant cells.EmboReports, 2(5): 394-398.
[16] Vasil, V., Clancy, M., Ferl, R. J., Vasil, I. K., & Hannah, L. C. (1989). Increased gene expression by the first intron of maize shrunken-1 locus in grass species.PlantPhysiology, 91(4): 1,575-1,579.

