外源病毒检验用抗鸡传染性支气管炎病毒特异性血清的制备与检定
毛娅卿,吴 涛,王 嘉,王 哲,孔冬妮,李 岭,李慧姣,蒋桃珍,李俊平
(中国兽医药品监察所,北京 100081)
鸡传染性支气管炎(Infectious bronchitis,IB)是一种由传染性支气管炎病毒(IBV)引起的鸡的常见急性、高度传染性,并具有重大经济意义的病毒病。目前国内外主要靠疫苗接种来防治该病[1-2]。根据现行《中华人民共和国兽药典》(简称《中国兽药典》)三部的规定[3],IBV活疫苗成品或制作疫苗的毒种须用抗 IBV 特异性血清进行中和试验,以检验外源病毒。鉴于当前兽用生物制品生产企业检验所使用抗IBV特异性血清难以满足实际需求,本研究优化了免疫条件,利用 IBV活疫苗进行基础免疫,再用灭活苗进行加强免疫,制备了抗 IBV特异性血清,并对其纯净性、中和效价及特异性进行了鉴定。
1 材料
1.1 毒种
IBV H120 株、M41株,鸡传染性法氏囊病病毒(Infectious bursal disease virus,IBDV)B87株,鸡新城疫病毒(Newcastle disease virus,NDV)La Sota株,鸡传染性喉气管炎病毒(Infectious laryngotracheitis disease virus,ILTV),鸡痘病毒(Avian pox virus,APV),禽呼肠孤病毒(Avian reo virus,ReoV)S1133株:由中国兽医药品监察所鉴定、保管和供应。
1.2 试验动物
SPF鸡胚和鸡:由北京梅里亚维通实验动物技术有限公司提供。
1.3 试剂和试剂盒
NDV红细胞凝集抑制试验抗原、鸡马立克氏病病毒(Marek's disease virus,MDV)琼脂凝胶扩散试验抗原、减蛋综合征病毒(Egg drop syndrome virus,EDSV)红细胞凝集抑制试验抗原、APV琼脂凝胶扩散试验抗原:中国兽医药品监察所制备、提供;禽流感病毒(Avian influenza virus,AIV)H5、H9 亚型红细胞凝集抑制试验抗原:购自哈尔滨维科生物技术开发公司;ILTV 抗 体 检测 试 剂 盒:购 自 Biocheck 公 司;鸡传染性贫血病 毒(Chicken infectious anemia virus,CIAV),IBV,ReoV,禽网状内皮组织增生症病毒(Avian reticuloendotheliosis virus,REV),禽脑脊髓炎病毒(Avian encephalomyelitis virus,AEV),禽白血病病毒(Avian leukosis virus,ALV,A、B亚群)等抗体检测试剂盒:购自 IDEXX 公司。
2 方法
2.1 抗原制备
IBV H120株、M41株繁殖及灭活抗原乳剂的制备,均参照《中华人民共和国兽用生物制品规程》(2000年版简称《中国兽用生物制品规程》)[4]。
2.2 免疫程序
取SPF鸡300只(3~4周龄),以IBV H120株活疫苗进行基础免疫,再用IBV M41株油乳剂灭活疫苗加强免疫2~3次。
2.3 血清采集与分离
最后一次免疫21 d后,将所有鸡进行心脏采血并分离血清。
2.4 半成品检验与分装
将收集的血清,按现行《中国兽药典》进行无菌检验。将血清混合后分装入瓶(2 mL/瓶),参照《中国兽用生物制品规程》(2000年版)要求进行冷冻、真空干燥。
2.5 无菌检验与中和效价测定
外源病毒检验和剩余水分测定按现行《中国兽药典》三部进行。将抗IBV特异性血清用灭菌生理盐水恢复至2 mL后,进行200、400、800、1 600倍稀释,分别与等体积的IBV H120株病毒液(100 EID50/0.1 mL)混合,室温(18~25 ℃)作用1 h;经尿囊腔接种 SPF鸡胚(10~11日龄),每个稀释度接种鸡胚5枚(0.2 mL/胚);设病毒对照,鸡胚5枚,病毒液接种0.1 mL/胚;置37 ℃孵育6 d;每日照蛋,记录鸡胚死亡情况,按Reed-Muench法计算中和效价。
2.6 特异性检验
2.6.1 交叉中和试验 将NDV LaSota 株、IBV H120株、ILTV、APV、IBDV B87株、ReoV S1133等毒种做10倍系列稀释,分装于2列试管中。一组取适宜稀释度加入等量的抗IBV特异性血清;另一组加入等量的阴性血清,室温作用1 h后,经尿囊腔(绒毛尿囊膜)接种SPF 鸡胚(9~11日龄),置37 ℃孵育,计算中和指数。
2.6.2 抗体检测 将抗IBV特异性血清,按照表1中列出的检验方法,对 IBDV、APV、ILTV、NDV、Reo V、REV、CIAV、EDSV、MDV、AEV、AIV(H5、H9亚型)和ALV(A、B 亚群)进行抗体检测。
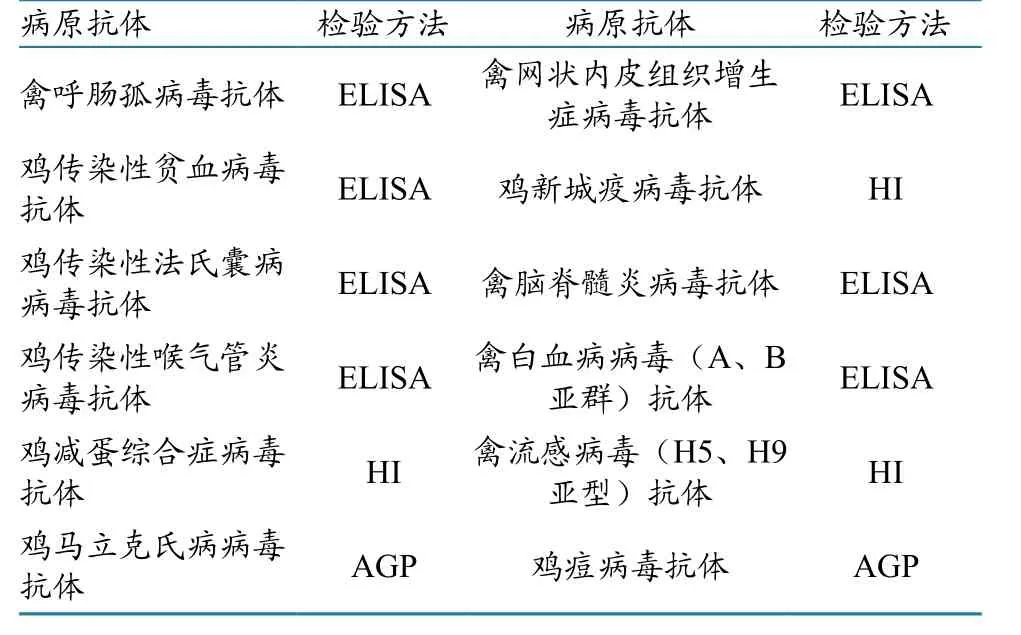
表1 病原抗体及其检验方法
2.7 中和试验和外源病毒检验
按照现行《中国兽药典》三部要求,将本研究制备的抗IBV特异性血清,分别与IBV种毒、活疫苗进行中和试验和外源病毒检验。
2.7.1 IBV H120株种毒中和试验 将制备的抗IBV特异性血清,用灭菌生理盐水分别进行10、20、40倍稀释,然后与等量(104.5EID50/0.1 mL 10羽份)的IBV H120株病毒液混合,室温作用1 h;经尿囊腔接种SPF鸡胚(10~11日龄),接种5枚(0.2 mL/胚),同时设病毒对照;37 ℃培养6 d,每日照蛋,记录鸡胚死亡情况。
2.7.2 IBV活疫苗(H120株)外源病毒检验 按照现行《中国兽药典》三部要求,将3批疫苗样品分别稀释至10羽份/0.1 mL,然后与等体积的抗IBV特异性血清混合,37 ℃中和1 h;接种SPF鸡胚(10日龄),进行外源病毒检验。
3 结果与分析
3.1 无菌检验与外源病毒检验
随机选取5瓶冻干的抗 IBV 特异性血清进行无菌检验,未发现菌生长。随机选取3瓶冻干的抗IBV特异性血清中进行外源病毒检验,未发现外源病毒污染。
3.2 剩余水分与中和效价测定
随机选取4瓶冻干的抗IBV特异性血清中进行剩余水分测定,发现含量分别为2.0%、2.3%、2.2%、2.1%。用IBV H120株进行基础免疫,再用IBV M41株油乳剂灭活疫苗加强免疫,制备抗 IBV特异性血清8 000 mL,发现中和效价为1∶800(表2)。

表2 抗IBV 特异性血清中和效价测定
3.3 特异性
3.3.1 交叉中和试验 将抗IBV特异性血清与IBV H120株进行中和试验,发现中和指数为106.3, 与 IBDV B87株、ILTV、NDV La Sota株、ReoV S1133株、APV的中和指数均不大于 10(表3)。

表3 抗 NDV 特异性血清交叉中和
3.3.2 抗体检测 经 AGP、ELISA、HI方法检测,本研究制备的抗IBV 特异性血清不含APV、IBDV、NDV、ILTV、REV、ReoV、CIAV、EDSV、MDV、AEV、AIV(H5、H9亚 型) 和ALV(A、B亚群)抗体,表明本血清具有良好的特异性。
3.4 中和试验与和外源病毒检验
3.4.1 IBV H120株种毒中和试验 试验制备的抗IBV特异性血清20倍稀释后可完全中和104.5EID50病毒。
3.4.2 IBV活疫苗(H120株)外源病毒检验 结果均为阴性,表明2 mL抗IBV特异性血清能够完全中和每批次各10羽份的疫苗样品。
4 讨论
IBV为非细胞适应性病毒,因此在外源病毒检验的鸡胚检查法中,只需将IBV活疫苗或毒种稀释成10羽份/0.1 mL(含104.5EID50),然后与等量抗血清中和即可。这就要求抗血清应具有良好的特异性和较高的效价。本实验室借助多年积累的经验[5~9],通过优化免疫方法,制备了 8 000 mL抗血清。对该血清进行无菌检验、外源病毒检验和剩余水分测定,发现结果均符合现行《中国兽药典》三部规定。为保证抗血清的单特异性,疫苗选用的是中国兽医微生物菌种保藏管理中心保存的 IBV H120、M41株毒种制备的试验用疫苗,并按照《中国兽用生物制品规程》(2000年)进行鉴定。
本研究在首免前,对试验用SPF鸡进行了血清抗体筛查,确保了无外源病毒感染。试验用SPF鸡专门饲养在隔离器中,接受严格管控,以降低微生物感染风险;建立了完善的卫生防疫和消毒机制,以确保整个实验过程无外界病原微生物污染;使用活疫苗进行基础免疫,再用灭活疫苗加强免疫,提高了抗血清的中和效价。
本研究采用2种试验方法,对IBV抗血清进行了特异性检验,涵盖了13种禽源病毒抗体,确保了试验结果的准确性。
5 结论
本研究通过优化免疫制备的8 000 mL抗IBV特异性抗血清,经鉴定证实纯净,无细菌、支原体或其他外源病毒污染,剩余水分测定结果符合《中国兽药典》三部规定。
制备的IBV抗血清特异性检验结果表明:本抗血清与IBV H120株的中和指数为106.3,与IBDV B87株、NDV La Sota株、ILTV、APV和 ReoV S1133 株的中和指数均不大于10;经HI、AGP、ELISA 方法检测,IBDV抗体等13种禽源病毒抗体均为阴性;血清中和效价为1∶800,20倍稀释后能等量中和10羽份/0.1 mL(含104.5EID50)的IBV疫苗或种毒。
检测结果表明,本研究制备的IBV抗血清具有良好的特异性,可以用于IBV活疫苗或种毒的外源病毒检验。
[1] 殷 震,刘景华.动物病毒学[M]. 2版. 北京:科学出版社,1997.
[2] SAIF Y M. 禽病学[M]. 12版. 北京:中国农业出版社,2012.
[3] 中国兽药典委员会. 中华人民共和国兽药典(2015年版):三部[M]. 北京:中国农业出版社,2011.
[4] 农业部兽用生物制品规程委员会. 中华人民共和国兽用生物制品规程(2000年)[M].北京:科学出版社,2000.
[5] 章振华,李 林,姜北宇,等. 鸡传染性法氏囊病高免血清的制备与检验[J]. 安徽农业科学,2012,40(11):6529-6530.
[6] 李俊平,杨承槐,李启红,等. 鸡抗REV 血清的制备与检定[J]. 中国兽药杂志,2011,45(9):15-18.
[7] 李翠,王在时,关孚时,等. 鸡新城疫高免血清的制备[J]. 中国兽药杂志,2008,42(2):30- 31.
[8] 孙 淼,李 岭,李启红,等. 外源病毒检验用抗鸡传染性法氏囊病病毒特异性血清的制备与检定[J]. 中国兽药杂志,2015,49(9):11-14.
[9] 薛青红,李 润,印春生,等. 犬细小病毒特异性抗血清的制备及应用研究 [J]. 中国兽药杂志,2014,48(10):11-13 .

