进展期胃癌TP酶活性与XELOX新辅助化疗效果研究
胡浔科,余亚萍
(景德镇第二人民医院普外科,江西 景德镇 333000)
胃癌(gastric cancer,GC)是一种消化道恶性肿瘤,在我国临床上有较高发生率,且近几年表现为递增趋势[1]。我国经济水平逐渐提高,人口老龄化现象越来越严重,在经济条件较差的农村和城市,胃癌的发生率逐渐上升,对人们的生命安全造成巨大的威胁。大部分胃癌患者在就诊时已表现为终末期,无法彻底清除原发病灶,术后普遍有肿瘤细胞残余,或者肿瘤细胞转移性较高;根据资料显示,术后五年生存率大约保持在35%[2]。除手术治疗以外,新辅助化疗在临床上又较高使用率,且疗效甚佳;因其可有效降低胃癌细胞水平,缓解胃癌组织内渗出现象,缩小胃癌原病发灶,降低临床分期[3]。因此,新辅助化疗在胃癌治疗过程中逐渐广泛使用,有效改善患者的生存期和生存质量。本院研究了进展期胃癌TP酶活性与XELOX新辅助化疗效果,现报道如下。
1 资料与方法
1.1 临床资料 将本院2014年7月~2017年5月期间收治的进展期胃癌患者进行归纳总结,从中随机抽取106例进行临床研究,根据数字法将其分为对照组和研究组,各53例。对照组中男31例,女22例;年龄31~78岁,平均年龄(52.1±5.7)岁;根据病理分期情况分类,其中18例患者为Ⅲ期,其余35例患者均为Ⅳ期。研究组中男30例,女23例;年龄32~81岁,平均年龄(53.5±5.2)岁;根据病理分期情况分类,其中19例患者为Ⅲ期,其余34例患者均为Ⅳ期。两组患者的性别、年龄和病理分期等基本情况比较差异无统计学意义,具有可比性。纳入标准:①经增强CT检查,均判断为中晚期(Ⅲ期或Ⅳ期)胃癌;②预计生存期在3个月以上;③均知晓本次研究详情,并签好知情协议书。
1.2 方法 研究组通过XELOX(Oxaliplatin+Xeloda)新辅助化疗;其中Xeloda(卡培他滨)使用剂量为1 000 mg/m2,使用规格为2次/d,使用方式为饭后30 min口服;连续服用两周,休息1周。第1天给予患者Oxaliplatin(奥沙利铂),使用剂量为130 mg/m2,给予方式为静脉滴注,连续治疗21 d为1个疗程。在化疗前实施化疗不适反应预防措施,若患者出现呕吐反应,则通过静脉推注方式常规给予患者2.5 mg的盐酸帕洛诺司琼或者8 mg的昂丹司琼注射液进行止吐;若患者出现过敏反应,则静脉推注10 mg的地塞米松。对患者进行定期复查,复查内容包括血常规、血生化和心电图等;手术选择在化疗结束后第4周。对照组则直接实施手术治疗。
1.3 观察标准 在完成3个疗程XELOX化疗方案后,观察比较两组患者的TP酶浓度水平和临床疗效。临床疗效主要分为肿瘤彻底缓解(CR)、肿瘤局部缓解(PR)、肿瘤无改善化(SD)和肿瘤进展(PD)四项,其中CR:胃肿瘤原发病灶、肝脏转移病灶在影像学上较新辅助化疗前,彻底消失或减小50%以上;PR:胃肿瘤原发病灶、肝脏转移病灶在影像学上较新辅助化疗前,减小程度在50%以下;SD:胃肿瘤原发病灶、肝脏转移病灶在影像学上较新辅助化疗前,无改善或增大25%以下;PD:胃肿瘤原发病灶、肝脏转移病灶在影像学上较新辅助化疗前,至少增大25%或者增加新病灶;CR+PR代表肿瘤有效缓解。
1.4 统计学方法 本研究数据均用SPSS 16.0统计软件处理,计量资料采用“x±s”表示,组间比较采用t检验;计数资料用例数(n)表示,计数资料组间率(%)的比较采用χ2检验。P<0.05为差异有统计学意义。
2 结果
2.1 观察比较两组患者的TP酶浓度水平 研究组患者的TP浓度均数为(458.41±9.08)ng/ml,对照组患者的TP浓度均数为(179.32±7.34)ng/ml;可见,研究组患者的TP浓度均数明显高于对照组,组间数据比较差异有统计学意义(P<0.05)。
2.2 观察比较两组患者的临床疗效 研究组患者的有效率明显优于对照组,组间数据比较差异有统计学意义(P<0.05),见表1。
3 讨论
新辅助治疗可减少胃癌术后复发情况,提高了胃癌根治术比率,提高了晚期胃癌患者术后生存质量;同时分将其为新辅助化疗(neoadjuvant chemotherapy,NC)、辅助放疗(neoadjuvant radiotherapy)以及新辅助放化疗(neoadjuvant chemoradiotherapy)[4]。新辅助化疗还可称为术前化疗,在进展期恶性肿瘤术前实施局部或全身化疗,有效降低进展期恶性肿瘤分期分级,为后期根治术治疗提供有利条件,并降低恶性肿瘤细胞转移率和扩散率[5]。新辅助化疗概念最早在1982年便有所记载,为中晚期恶性肿瘤患者找到实施根治术的途径,临床效果突出,逐渐引起外科医师的关注[6]。针对晚期胃癌患者而言,术前化疗为患者提供了新型治疗方案,通过术前化疗有效减小了癌症原发病灶,降低了癌症分期;同时调整了患者精神上和心理上的不适反应。
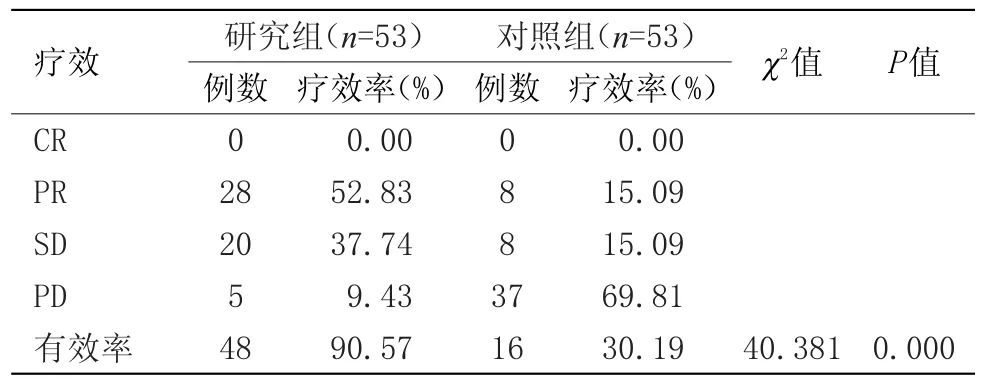
表1 两组患者的有效率对比分析(n)
有大量临床研究证明,新辅助化疗的作用主要表现在以下几个方面:①利用癌症组织内部淋巴管和毛细血管的作用,化疗药物浓度在病灶内迅速达到高峰,从而发挥消灭癌细胞作用[7]。②术前化疗可有效减少临床和亚临床转移病灶,从而防止术中癌细胞扩散。③可有效减少癌细胞数目,降低病灶临床病理分期,从而彻底切除癌症原发病灶,起到改善患者生存质量的作用[8]。④利用TP来评估癌细胞对化疗药物的敏感度,从而为术后化疗药物的选择做铺垫。⑤减少局部肿瘤组织肿瘤细胞,在术前准备途程中,促进化疗药物消灭癌细胞;同时抑制癌细胞活性,达到最佳限制癌细胞状态[9]。本研究表明:研究组患者的TP浓度均数和有效率均明显高于对照组,组间数据比较差异有统计学意义(P<0.05)。
综上所述,进展期胃癌患者的TP酶活性与XELOX新辅助化疗效果存在密切联系,同时XELOX新辅助化疗的临床效果甚佳。
[1] 韩刚,王以东,曹羽,等.进展期胃癌术后三维适形放疗联合XELOX方案化疗的疗效观察[J].实用癌症杂志,2013,28(2):168-170.
[2] 尹继磊,刘峥,李海燕,等.进展期胃癌术后三维适形放疗联合同期XELOX化疗临床观察[J].河北医药,2013,35(14):2108-2110.
[3] 吕文瑜,陈绍水.SOX方案与XELOX方案治疗进展期胃癌的临床对比研究[J].癌症进展,2017,15(3):304-307.
[4] 靖昌庆,李乐平,王金申,等.XELOX和FOLFOX4新辅助化疗方案对不能手术切除的局部进展期胃癌的疗效比较[J].中华消化外科杂志,2010,9(6):430-433.
[5] 刘峥,尹继磊,张振军,等.进展期胃癌术后三维适形放疗联合同期XELOX化疗临床观察[J].河北医药,2011,33(6):860-861.
[6] 张建宇,何立,许新华,等.XELOX方案一线治疗进展期胃癌临床观察[J].山东医药,2012,52(43):58-60.
[7] 李明辉,刘红波,冯运章,等.康莱特腹腔热灌注联合 XELOX方案化疗治疗进展期胃癌的疗效观察[J].现代肿瘤医学,2017,25(2):266-269.
[8] 陈力,张玉新,左艳娇,等.SOX和 XELOX在进展期胃癌新辅助化疗中的临床疗效比较[J].实用肿瘤学杂志,2017,31(1):23-30.
[9] 樊志明,贺鸿桂,黄超红,等.FOLFOX4和XELOX治疗进展期胃癌的临床疗效比较[J].实用癌症杂志,2013,28(4):396-398.

