固体酸催化混合胺的CO2解吸性能分析
曹一凡,史焕聪,崔立峰
(上海理工大学 环境与建筑学院,上海 200093)
碳排放过量导致的温室效应和厄尔尼诺现象已严重影响了人类的生产生活,碳捕获与封存技术(CCS)是解决这一难题的有效途径[1]。胺基溶液CO2解吸作为一项操作简便的CCS技术,已成功应用于燃煤工厂中。然而,过高热负荷带来的巨大能耗和过长反应时间导致的设备冗杂等问题都严重阻碍了工业发展[1-2]。
可使用的胺基溶液中,乙醇胺(MEA)溶液因成本低廉且易与CO2反应的特点而倍受青睐。工业中使用MEA或 MEA/N−甲基二乙醇胺混合液(MEA/MDEA)作为吸收剂。解吸过程的热负荷可分为反应热、汽化热和显热[2]。改变吸收剂组分能降低反应热;控制解吸温度能削弱汽化热;而显热却很难改变[3]。
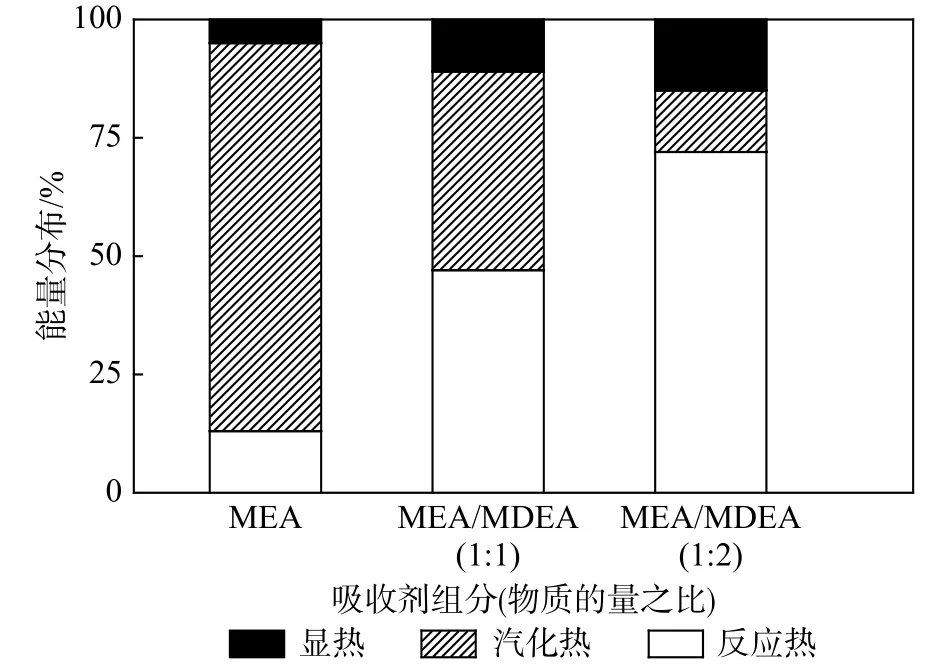
图1 MEA与MEA/MDEA的热负荷分布Fig.1 Heat duty distribution of MEA and MEA/MDEA
基于能量分配理论,评价3个重要指标:能量占比、能源效率和反应时间[3]。能量占比指各组分能量占总能量的比例;能源效率是有效能量(本试验指反应热)的能量占比[4-6]。图1为MEA及MEA/MDEA的相对能量分布。MEA的热负荷中有13%是反应热,82%是汽化热,其余为显热,能源效率仅为 13%。MEA/MDEA(1∶1,物质的量之比)相比于MEA,能源效率上升了 50%,MEA/MDEA(1∶2,物质的量之比)上升了75%。因此MEA解吸过程中混合三级胺是提高能源效率、减少热负荷的有效方法。
缩短反应时间是提高能源效率的另一大重要因素,最有效的方法是使用特性催化剂。研究发现,固体酸能够有效催化解吸碱性胺基溶液,同时不污染溶液,极大地降低了溶液的循环使用成本[7]。本文选择γ−Al2O3和HZSM−5两种固体酸作为催化剂,其中γ−Al2O3是路易斯酸,HZSM−5是质子酸。
以MEA为主体的混合胺解吸过程分两步:氨基甲酸酯的分解和去质子化反应,见式(1)和式(2)。DEAB是一种自由能较低的三级胺,其反应机理与MDEA相近,添加DEAB同样能降低热负荷[8]。式(3a)和式(3b)分别为 DEAB和 MDEA 的化学反应方程式。
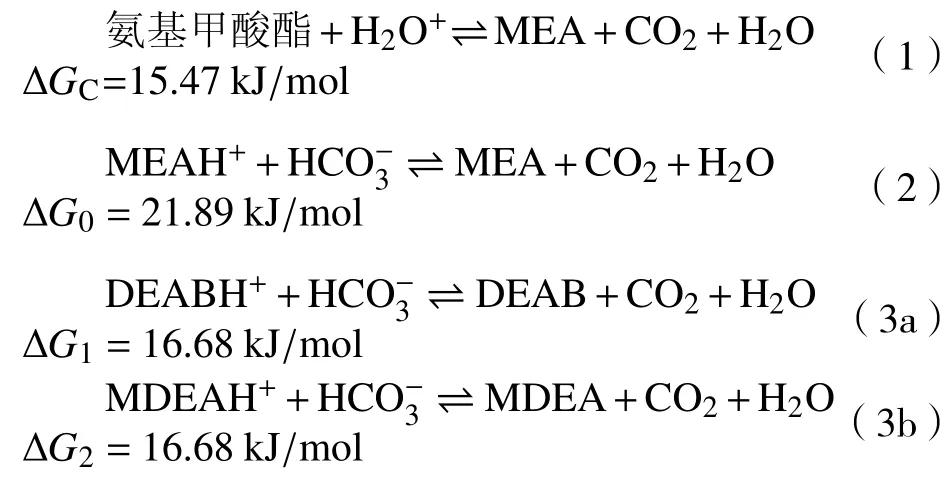
式中:ΔGC,ΔG0,ΔG1,ΔG2为标准化学反应自由能。
两种三级胺的理论反应自由能均明显小于MEA。综上考虑,在胺基溶液的解吸过程中,添加MDEA和 DEAB与 MEA混合,并使用 γ−Al2O3和HZSM−5作为催化剂,探讨不同配比条件对CO2解吸速率和体系热负荷的影响,旨在为胺基溶液CO2解吸提供一定的基础数据及理论依据。
1 试 验
1.1 试验原料与设备
试验原料为:CO2气体(纯度 99.9%),盐酸(HCl),MEA,MDEA 和 DEAB(分析纯),催化剂 γ−Al2O3和HZSM−5。
1.2 试验设备和方法
主要试验设备如图2所示。量取2 L负载率为0.50~0.52(无量纲,可写作 mol CO2/mol amine)的混合液于三颈烧瓶内,精确称量25.0 g粒径为3.0~4.0 mm的催化剂颗粒,包裹成球状并浸没于溶液内,上接冷凝管和温度计,下置磁力搅拌加热套。加热套程序升温,磁转子匀速搅拌且不碰撞催化剂球。
当溶液温度稳定在85 ℃后,记录时间变化,并在 120,240,360和 540 min时刻取 2 mL样品进行CO2负载率检测(Chittick仪器,AOAC 法[9])。通过绘制负载率与反应时间的变化曲线,分析混合胺溶液热解速率。溶液加热120 min以后,记录电能表数值,所消耗的能量是胺再生的热负荷。这样的低温操作(低于100 ℃)可以保证反应热的能量占比优势,提升反应热的能源效率。

图2 胺再生过程简易循环装置Fig.2 Simplified recirculation apparatus for amine regeneration process
1.3 试验指标
对胺基溶液解吸性能的评价指标包括CO2负载率、胺再生速率和相对热负荷占比,各个指标的含义如下。
(1) CO2负载率α
CO2负载率指胺基溶液中单位物质的量的醇胺所含CO2的物质的量,其表达式为:

式中:α为CO2负载率;为CO2体积测量读数;VHCl为滴定时消耗的HCl体积;C0为胺基溶液初始浓度;ζ为体积校正系数。
(2) 胺再生速率r
胺再生速率指单位时间内单位体积的胺基溶液CO2解吸的量,其表达式为:

(3) 相对热负荷占比η
相对热负荷占比指单位物质的量的CO2所消耗的热量占对照试验的百分比,其表达式为:

式中:η为相对热负荷占比;Q为解吸过程消耗的热能;Q0为对照试验消耗的热能。
2 结果与分析
试验以 5 M(mol/L)MEA,5 M MEA/1.25 M MDEA和 5 M MEA/1.25 M DEAB为吸收剂,以γ−Al2O3和HZSM−5为催化剂。解吸过程中的CO2负载率随时间的变化趋势如图3所示。由方程式推导计算,CO2负载率与时间的函数关系为类一级模型[10]。使用专业绘图软件拟合试验数据,拟合常数R2均高于0.978,在2.5%系统误差范围内。

图3 MEA, MEA/MDEA和MEA/DEAB的CO2负载率的变化Fig.3 Changes of CO2 loading ratio of MEA,MEA/MDEA and MEA/DEAB
图3 中,曲线的斜率代表反应速率,CO2负载率随加热时间的推移呈下降趋势,各曲线以不同速率分开,分别呈规律性变化。同一吸收剂,使用HZSM−5比使用 γ−Al2O3反应速率更快。在 5 M MEA/1.25 M DEAB中,前120 min的平均速率:无催化剂<γ−Al2O3<HZSM−5。同一催化剂,添加DEAB的反应速率更快,而添加MDEA的反应速率却更慢。以使用HZSM−5为例,平均反应速率:MEA/MDEA<MEA<MEA/DEAB。表1列出了各项试验条件下的平均反应速率数值。
两种催化剂不仅对MEA单一溶液起催化解吸作用,添加三级胺溶液后依旧适用。同时,三级胺的加入能够提高反应速率,加快反应进程,缩短反应时间。根据图3中曲线走势可分为2个阶段:0~120 min为快速阶段,走势陡峭,醇胺分子与CO2及H2O的反应非常激烈,该阶段平均还原52.3%的醇胺分子;随着反应时间的延长,斜率越来越小,曲线逐渐趋于平缓,这一阶段为慢速阶段。快速阶段有助于探究CO2解吸速率,慢速阶段有助于分析热负荷的降低。
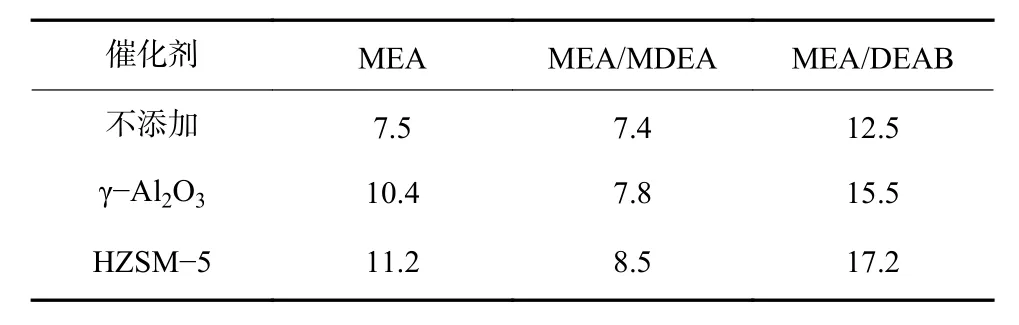
表1 前 120 min 胺再生速率(10-3 mol/mol·h-1)Tab.1 Regeneration rate of amine in the first 120 minutes(10-3 mol/mol·h-1)
快速阶段与慢速阶段的醇胺分子的还原比例相近,慢速阶段所用时间是快速阶段的2倍。受类一级反应模型影响,反应物与反应时间的变化为指数关系,随着反应物的消耗,CO2的生成速率越来越慢[11-12]。本试验条件保证常温常压,反应速率逐渐减小,最终趋于动态平衡,各条曲线达到平衡的时间不一,这与添加剂和催化剂的化学属性密切相关。
慢速阶段下(120~540 min)测得的热负荷数值,以5 M MEA作为空白对照,其他各组与之对比,结果见表2,数值以百分数表示。由表2可知,添加DEAB的热负荷占比最低,仅为基准的51.4%,使用催化剂后可降低至40.1%和38.2%;添加MDEA的各组试验效果均不如DEAB。根据式(3a)和式(3b),MDEA的化学反应自由能(16.68 kJ/mol)与DEAB(16.68 kJ/mol)相同,添加量相同时,两种三级胺对热负荷的降低效果应一致,但实际却有出入,MEA/MDEA(73.5%)高于 MEA/DEAB(51.4%)。但这并不矛盾,由式(2)、式(3a)和式(3b)可知,胺基溶液催化解吸的反应物主要是,在MEA/MDEA体系中,的体积分数占比为MDEA的65%~68%;而MEA/DEAB体系中,却可达到80%,多出的10%~12%的使得MEA/DEAB体系的热负荷消耗的更少[7-10,13-14]。综合图3、表1和表2及上述分析,5 M MEA/1.25 M DEAB+HZSM−5组合对总体热负荷在能源效率上表现最优,可达到61.8%,即可节约61.8%的能量输入。
这一组合表现优良,不仅受DEAB的影响,还有HZSM−5的催化作用。γ−Al2O3是一种两性氧化物,与两性阴离子的作用相似,既可提供质子又可接收质子,反应过程相当于为醇胺分子还原增加了一条途径[7]。HZSM−5只是单纯的质子供体,缺少接受质子的机制,使得反应仅能从单一方向进行,故而反应速率更快。
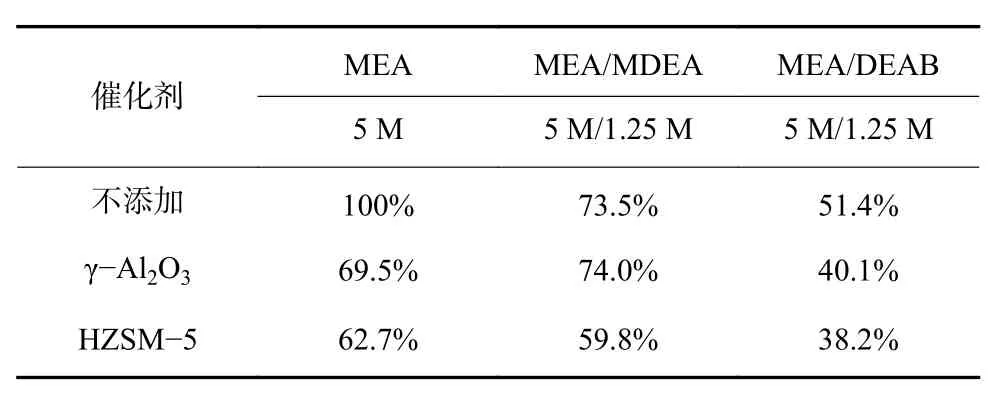
表2 120~540 min相对热负荷占比汇总Tab.2 Summary of relative heat duties during the period of 120-540 min
通过改进吸收剂和使用特性催化剂,胺基溶液CO2催化解吸的整体热负荷大大降低。工业CCS中,5 M MEA的热负荷数值为0.37~0.51,若应用最优条件(5 M MEA/1.25 M DEAB+HZSM−5)可将热负荷降低至0.15~0.20,反应速率可提高2.3倍,设备尺寸减小,工业成本大幅度降低。
本试验使用非均相催化剂,在实际工业应用中凸显了低运行温度下的高再生速率和低热负荷优势。并且,在实际胺基溶液吸收−解吸过程中,非均相催化剂也优于均相催化剂,因为固相催化剂易于从液相中分离,同时更换方便。
3 结 论
本文以碳捕获与封存技术为背景,采用工业应用较为成熟的化学溶液吸收法,并在混合三级胺降低溶液热负荷的理论基础上,进行相关试验,对非均相催化过程做出直观的解释,从而证实固体酸催化剂能够催化混合胺溶液CO2解吸这一理论的可行性。
通过对比2种固体酸在MEA与2种混合溶液的催化效果,发现γ−Al2O3与HZSM−5均为有效催化剂。其中,HZSM−5的催化效果比γ−Al2O3更强一 些 ,最 快 速 率 为 17.2×10−3mol/mol·h−1。 另 外 ,MDEA和DEAB的添加均可提高能源效率,降低热负荷。其中,DEAB的效果最佳,热负荷最大可减少61.8%。试验结果证明,5 M MEA/1.25 M DEAB+HZSM−5的配比在加快反应速率和降低热负荷两方面同时达到最优。根据两性氧化物特质和非均相反应分析,证明该配比条件确实是胺基溶液CO2解吸的优选之项。

