胰十二指肠切除术后早期液体平衡与胰瘘相关
刘 薇 张 进 赵 松 李文雄 郑 悦
(首都医科大学附属北京朝阳医院外科ICU,北京 100027)
胰十二指肠切除术(pancreaticoduodenectomy,PD)是治疗壶腹周围恶性肿瘤和某些良性疾病的主要手术方式。由于手术创伤大、时间长,PD术后合并症较为多见,其中术后胰瘘(postoperative pancreatic fistula,POPF)是PD最常见的合并症之一,可致腹腔内感染和致命性大出血,从而延长住院时间,增加病死率。性别(男性)、体质量指数(body mass index,BMI)(>25 kg·m-2)、胰管直径(≤3 mm)、柔软的胰腺质地、术中大量输液等术前术中因素被认为与PD术后POPF的发生率相关[1-4],但术后液体管理对POPF的影响尚不明确。本研究旨在探讨对PD术后住重症加强治疗病房(intensive care unit, ICU)的患者进行早期液体管理对POPF的影响。
1 资料与方法
1.1 一般资料
经首都医科大学附属北京朝阳医院伦理委员会批准(批准文号:2016—科73),回顾性收集2014年1月至2016年12月期间首都医科大学附属北京朝阳医院外科ICU(surgical ICU,SICU)连续收治的PD术后患者的临床资料。纳入标准:①行PD手术者;②术后入住SICU;③年龄≥18岁。排除标准:①消化道重建方式采用非Child法和/或胰肠吻合方式采取非胰管空肠黏膜吻合的患者;②术前诊断休克的患者;③急诊手术患者;④慢性肾功能不全和/或肾病患者。最终入选病例237例,其中男性129例,女性108例,年龄:31~83岁。POPF的诊断与分级采用国际胰腺外科学组(International Study Group on Pancreatic Surgery,ISGPS) 2016年更新的定义和分级系统[5],引流液淀粉酶浓度大于血清淀粉酶正常值上限的3倍且发生了与术后胰瘘直接相关的临床状态及预后改变可诊断为POPF,POPF分级详见表1。
1.2 研究方法
回顾性收集和记录患者术前、术中和术后的临床资料。1)术前资料:包括性别、年龄、合并症(糖尿病、高血压等)、入院时的BMI等基础疾病状况,原发病性质为良性或恶性疾病、病变部位为胰腺或非胰腺疾病(依据术后病理诊断)、入院时和术前血清白蛋白(albumin, Alb)和总胆红素浓度、术前是否存在胆管炎、是否行胆道引流[包括经皮肝穿胆道引流(percutaneous transhepatic cholangial drainage,PTCD)和内镜下乳头括约肌切开术(endoscopic sphincterotomy, EST)],ASA分级(American Society of Anesthesiologists Physical Status Classification,ASA class)等术前疾病状况;2)术中资料:包括手术时间、术中液体平衡、术中是否使用血管活性药物、出血量以及是否行血管切除重建等术中情况;3)术后资料:包括术后24 h液体平衡量(FB 24 h)和48 h累积液体平衡量(FB 48 h),术后当天(Day 0 Alb)、第1天(Day 1 Alb)和第2天(Day 2 Alb)的白蛋白浓度,术后当天红细胞压积(hematocrit, Day 0 Hct),术后12 h内动脉血乳酸最高值[lactic acid, Lac12 h(max)]等。随访患者是否发生POPF以及发生的时间,研究终点为PD术后28d内患者的POPF发生率,并据此将患者分为胰瘘组(POPF)和非胰瘘组(Non-POPF)。分析影响POPF发生的危险因素以及术后液体平衡对POPF发生率的影响。
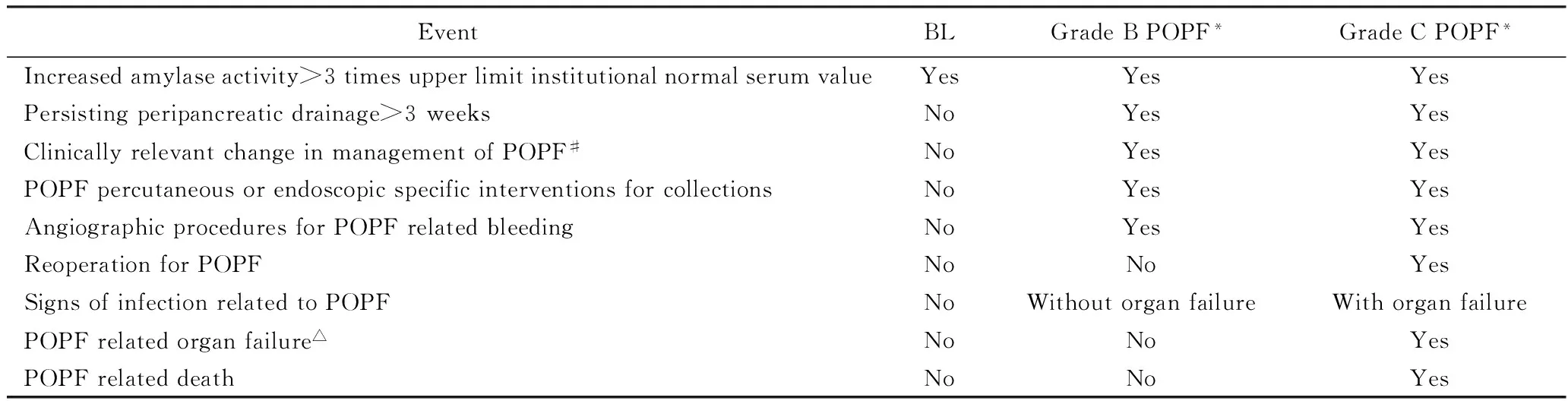
表1 国际胰腺外科学组(ISGPS)2016年更新POPF分级临床评定表[5]Tab.1 The Revised 2016 ISGPS Classification and Grading of POPF[5]
*: A clinically relevant POPF is defined as a drain output of any measurable volume of fluid with amylase level greater than 3 times the upper Institutional normal serum amylase level, associated with a clinically relevant development/condition related directly to the POPF;#: Suggests prolongation of hospital or ICU stay, includes use of therapeutic agents specifically employed for fistula management or its consequences(of these: somatostatin analogues, TPN/TEN, blood product transfusion or other medications).△: Postoperative organ failure is defined as the need for re-intubation, hemodialysis, and/or inotropic agent>24 hours for respiratory, renal, or cardiac insufficiency, respectively.ISGPS: International Study Group on Pancreatic Surgery;POPF: postoperative pancreatic fistula;BL: biochemical leak;ICU:intensive care unit;TPN:total parenteral nutrition;TEN:total enteral nutrition.
1.3 统计学方法

2 结果
2.1 患者术前基线资料
237例患者中,术后28d内发生POPF者共30例(12.7%),其中B级POPF 24例(10.1%),C级POPF 6例(2.5%),死亡3例(1.3%),死亡均发生在C级POPF患者,C级POPF患者病死率为50%。患者术前基线资料见表2。性别、是否患有糖尿病、原发病是否为胰腺疾病、入院和术前白蛋白浓度、术前是否行胆道引流在POPF组和Non-POPF组之间差异有统计学意义(P<0.05)。
2.2 患者术中和术后资料
患者术中及术后临床资料见表3。FB 48 h在两组之间差异有统计学意义(P<0.05)。
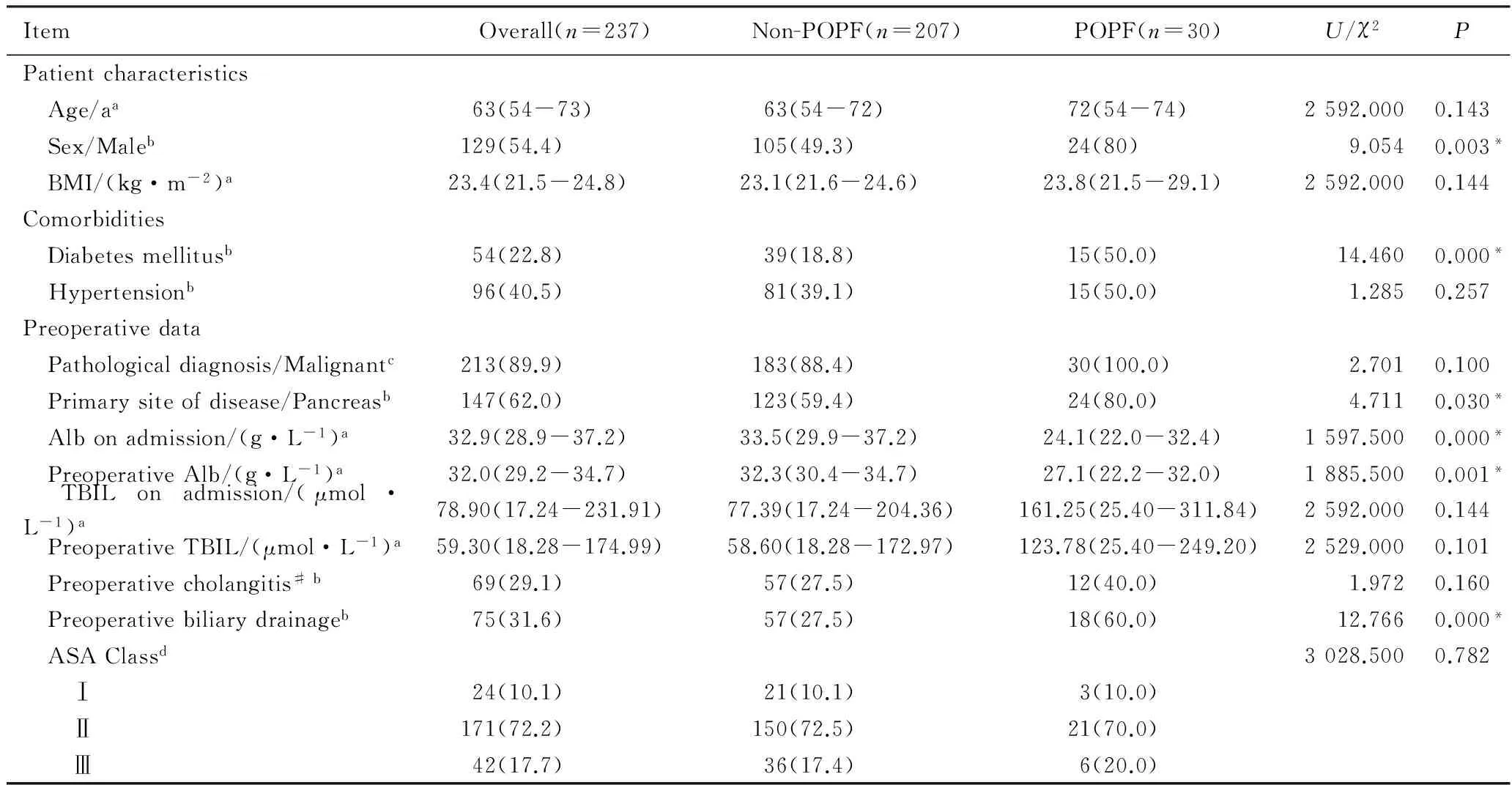
表2 患者术前基线资料Tab.2 Baseline characteristics of patients
a: Value expressed as median(IQR),Pby Mann-WhitneyUtest;b: Value expressed as number(percentage),Pby Chi-square test;c: Value expressed as number(percentage),Pby Chi-square test with continuity correction;d: Value expressed as number(percentage),Pby Mann-WhitneyUtest.*P<0.05; #: Cholangitis was diagnosed based on the following criteria:①presence of fever with upper quadrant pain;② radiological(sonographic or computed tomographic) or endoscopic evidence of biliary tract obstruction due to stones or stricture from benign or malignant origin; and③ laboratory findings of hyperbilirubinemia and an elevated serum alkaline phosphatase level;POPF: postoperative pancreatic fistula;BMI:body mass index;Alb: albumin;TBIL: total bilirubin;ASA:American Society of Anesthesiologists;IQR: interquartile range.
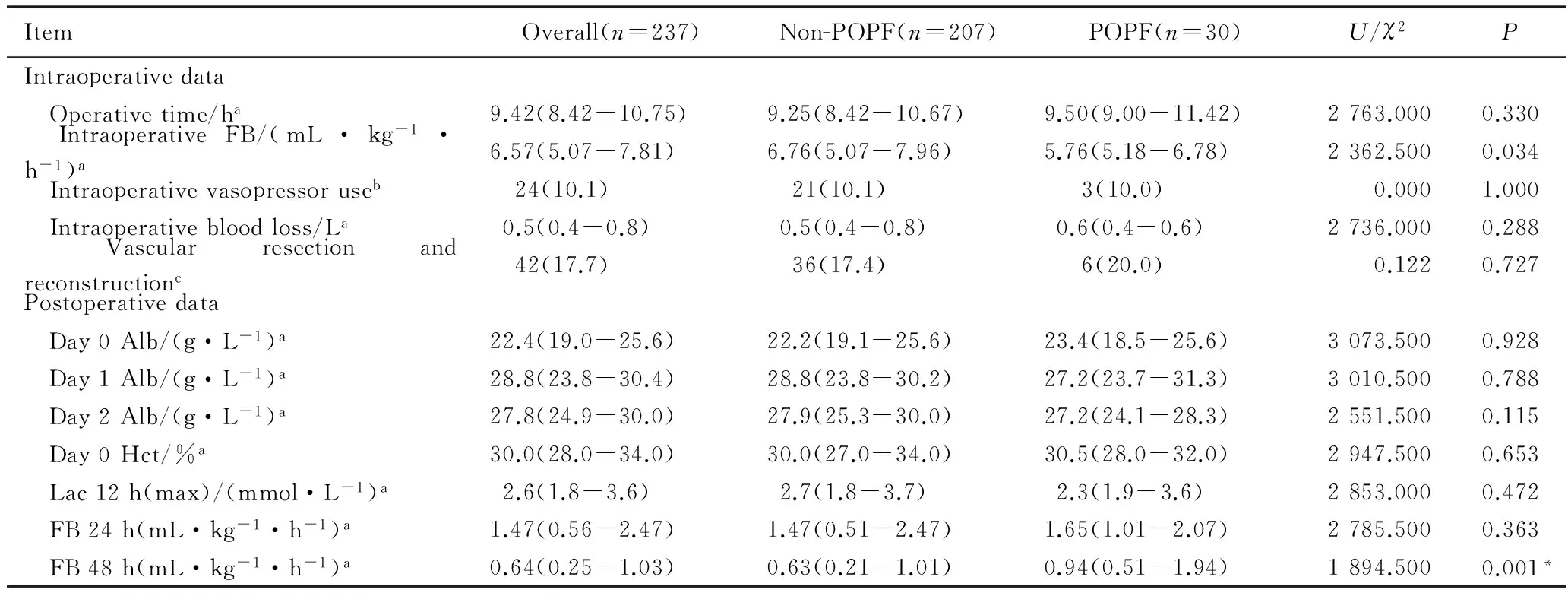
表3 患者术中及术后资料Tab.3 Intraoperative and postoperative data
a: Value expressed as median(IQR),Pby Mann-Whitney U test;b: Value expressed as number(percentage),Pby Chi-square test with continuity correction;c: Value expressed as number(percentage),Pby Chi-square test;*P<0.05;POPF: postoperative pancreatic fistula;FB: fluid balance;Alb: albumin;Day0Alb: albumin at immediately postoperation;Day1Alb: albumin at postoperative day 1;Day2Alb: albumin at postoperative day 2;Hct: hematocrit;Day0Hct: hematocrit at immediately postoperation;Lac: Lactate;Lac12h(max): Maximal value of postoperative Lactate within 12h;FB24h: cumulative fluid balance postoprative 24h;FB48h: cumulative fluid balance postoprative 48 h;IQR: interquartile range.
2.3 POPF相关因素的Logistic回归分析
多因素Logistic回归分析模型显示,患者性别(男性)、高BMI、患有糖尿病、入院时低白蛋白浓度、术前高胆红素浓度以及FB 48 h是POPF的独立危险因素,详见表4。
2.4 FB 48 h对POPF及C级POPF发生率的影响
根据FB 48 h将患者分为4组:液体负平衡组(FB 48 h≤0 mL·kg-1·h-1)、少量液体正平衡组(0 mL·kg-1·h-1
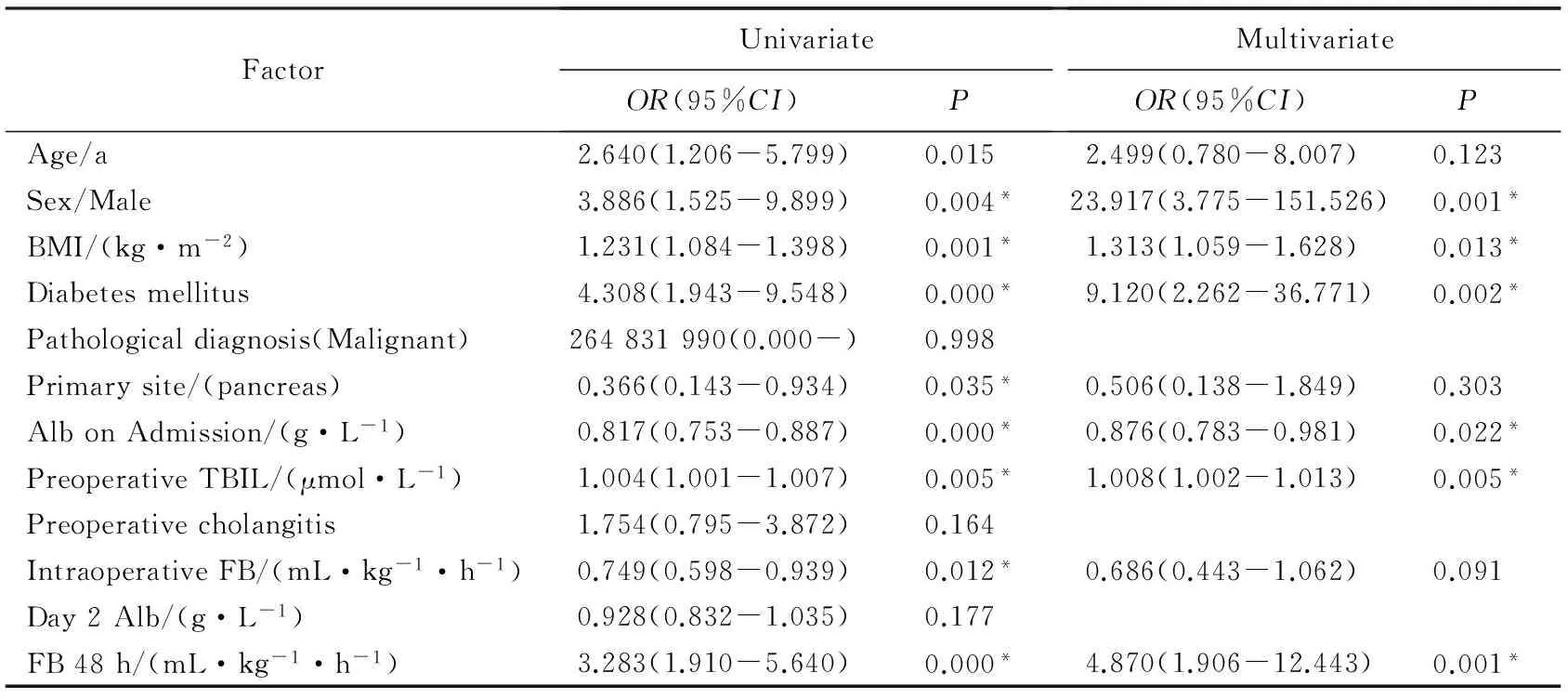
表4 PD术后POPF相关因素的Logistic回归分析Tab.4 Logistic regression analysis: risk factors associated with POPF following PD
*P<0.05;PD: pancreaticoduodenectomy;POPF: postoperative pancreatic fistula;BMI:body mass index;Alb: albumin;TBIL: total bilirubin;FB: fluid balance;Day2Alb: albumin at postoperative day 2;FB48h: cumulative fluid balance postoperative 48 h.

表5 FB 48 h对POPF及C级POPF发生率的影响Tab.5 Impact of FB 48 h on the incidence of POPF and Grade C POPF
*P<0.05;a: value expressed as number(percentage),Pby likelihood ratio Chi-square test;FB: fluid balance;FB48h: cumulative fluid balance postoperative 48h;POPF: postoperative pancreatic fistula.
3 讨论
2005年的POPF定义和分级系统[6]中的A级POPF,因其与无胰瘘患者不存在明显的临床治疗及预后差异[7-8],在2016年国际胰腺外科组(ISGPS)更新的POPF定义和分级系统中被更名为生化漏(biochemical leak,BL)[5],不再被诊断为POPF。2016年的一项国际多中心研究[9]中,纳入与不纳入2005年定义和分级系统中A级胰瘘的POPF发生率分别为19.2%和11.1%,在本研究中,POPF发生率为12.7%,与之相当。
多个研究[10-11]显示,围术期液体管理可以影响术后患者的结局。围术期低血容量状态可产生严重的后果,导致单一或多个器官功能障碍,甚至是死亡[12]。值得注意的是,液体过负荷同样有害,可导致术后合并症的发生率显著增加[10]。对于PD,没有文献定义术中、术后给予多少液体是恰当的。本研究结果显示,PD术前和术中影响POPF发生率的独立危险因素包括性别(男性)、高BMI、罹患糖尿病、入院时低白蛋白浓度、术前高胆红素浓度;而术后影响POPF发生率的独立危险因素只有FB 48 h。进一步研究显示,FB 48 h达负平衡能显著降低POPF发生率;与中等量和少量液体正平衡相比,大量液体正平衡(FB 48 h>1 mL·kg-1·h-1)虽不显著增加POPF发生率,但显著增加了C级POPF的发生率。
既往的研究[13]显示,C级POPF相关病死率高达25%(0%~100%)。在PD术后早期,应尽量避免大量液体正平衡(FB 48 h>1 mL·kg-1·h-1)以降低C级POPF的发生率。造成术后早期液体大量正平衡的原因可能有如下两种情况:①术中容量相对不足:麻醉药物有可能通过减慢心率等作用掩盖某些提示容量不足的征象,麻醉医师亦有可能将血压下降等容量不足的征象误判为麻醉药物的不良反应,从而造成术中隐匿性容量不足,这种情况下,术中和术后早期胰肠吻合口可能已经遭受到因灌注不足而导致的愈合障碍,而对于循环系统则需要更多的液体正平衡来弥补术中的容量不足,这也可以解释胰瘘组术中液体平衡显著低于非胰瘘组而术后早期液体平衡显著高于非胰瘘组的临床现象。有文献[14]推荐腹腔内手术术中应给予10 mL·kg-1·h-1~15 mL·kg-1·h-1的液体输注,但这一推荐缺乏可靠的研究证据。②术后容量过负荷:术后患者在ICU中的液体管理通常以维持血流动力学稳定、保障组织器官灌注为目标,有可能导致不必要的容量过负荷。无论何种原因导致的液体正平衡过多,都有可能对胰肠吻合口愈合造成影响。有研究[15]显示,过多的液体输注降低组织氧合并导致水肿,这种效应与吻合口愈合不良密切相关。
PD手术时间长、创伤大,全身炎性反应通常较其他腹腔脏器手术更为严重,可导致全身毛细血管通透性增高(毛细血管漏),血管内液体强制性转移至第三间隙,因此在术后早期往往不得不给患者补液,恰当的液体正平衡有利于维持有效循环血容量及恰当的组织灌注,同时保障胰肠吻合口的血流供应[16-17]。尽管笔者的研究结果提示FB 48 h达负平衡能显著降低POPF发生率,但对于术后全身炎性反应较重的患者,FB 48 h难以达到负平衡;ICU医师应在保障有效血容量和良好器官组织灌注的前提下,尽量减少PD术后早期的液体正平衡量以降低C级POPF发生率。
本研究存在一些局限性:由于该研究是回顾性的,无法获得有关胰腺组织结构、胰肠吻合细节的客观资料,而这些因素可能是POPF的重要原因之一。但研究中提供的数据均来自于首都医科大学附属北京朝阳医院肝胆外科、麻醉科和外科ICU的临床信息管理系统,数据的真实性使研究结果具有一定的可信度。
总之,PD术后早期液体正平衡量是POPF的独立危险因素,FB 48 h超过1 mL·kg-1·h-1时,C级POPF发生率显著增高。临床尚需要一些大型前瞻性研究以评价PD术后早期液体管理对POPF的影响。
[1] Hu B Y, Wan T, Zhang W Z, et al. Risk factors for postoperative pancreatic fistula: analysis of 539 successive cases of pancreaticoduodenectomy[J]. World J Gastroenterol, 2016, 22(34):7797-7805.
[2] Yu L, Huang Q, Xie F, et al. Risk factors of postoperative complications of pancreatoduodenectomy[J]. Hepatogastroenterology, 2014, 61(135):2091-2095.
[3] Bruns H, Kortendieck V, Raab H R, et al. Intraoperative fluid excess is a risk factor for pancreatic fistula after partial pancreaticoduodenectomy[J]. HPB Surg, 2016:2016, 1601340.
[4] Wang S, Wang X, Dai H, et al. The effect of Intraoperative fluid volume administration on pancreatic fistulas after pancreaticoduodenectomy[J]. J Invest Surg, 2014, 27(2):88-94.
[5] Bassi C, Marchegiani G, Dervenis C, et al. The 2016 update of the international study group(ISGPS) definition and grading of postoperative pancreatic fistula: 11 Years After[J]. Surgery, 2017, 161(3):584-591.
[6] Bassi C, Dervenis C, Butturini G, et al. Postoperative pancreatic fistula: an international study group(ISGPF) definition[J]. Surgery, 2005, 138(1):8-13.
[7] Pratt W B, Maithel S K, Vanounou T, et al. Clinical and economic validation of the international study group of pancreatic fistula(ISGPF) classification scheme[J]. Ann Surg, 2007, 245(3):443-451.
[8] Kim W S, Choi D W, Choi S H, et al. Clinical validation of the ISGPF classification and the risk factors of pancreatic fistula formation following duct-to-mucosa pancreaticojejunostomy by one surgeon at a single center[J]. J Gastrointest Surg, 2011, 15(12):2187-2192.
[9] McMillan M T, Soi S, Asbun H J, et al. Risk-adjusted outcomes of clinically relevant pancreatic fistula following pancreatoduodenectomy: a model for performance evaluation[J]. Ann Surg, 2016, 264(2):344-352.
[10] Bundgaard-Nielsen M, Secher N H, Kehlet H. ‘Liberal’vs‘restrictive’ perioperative fluid therapy—a critical assessment of the evidence[J]. Acta Anaesthesiol Scand, 2009, 53(7):843-851.
[11] Chappell D, Jacob M, Hofmann-Kiefer K, et al. A rational approach to perioperative fluid management[J]. Anesthesiology, 2008, 109(4):723-740.
[12] de Aguilar-Nascimento J E, Diniz B N, do Carmo A V, et al. Clinical benefits after the implementation of a protocol of restricted perioperative intravenous crystalloid fluids in major abdominal operations[J]. World J Surg, 2009, 33(5):925-930.
[13] Pedrazzoli S. Pancreatoduodenectomy(PD) and postoperative pancreatic fistula(POPF): A systematic review and analysis of the POPF-related mortalityrate in 60,739 patients retrieved from the English literature published between 1990 and 2015[J]. Medicine(Baltimore), 2017, 96(19):e6858.
[14] Nisanevich V, Felsenstein I, Almogy G, et al. Effect of intraoperative fluid management on outcome after intraabdominal surgery[J]. Anesthesiology, 2005, 103(1):25-32.
[15] Jonsson K, Jensen J A, Goodson W H 3rd, et al. Tissue oxygenation, anemia, and perfusion in relation to wound healing in surgical patients[J]. Ann Surg, 1991, 214(5):605-613.
[16] 李洁. 弹簧圈在胰十二指肠切除术后出血治疗中的临床应用[J].首都医科大学学报,2015,36(3):483-487.
[17] 李可,杨艳.胰十二指肠切除术后胰瘘的防治进展[J].中国煤炭工业医学杂志,2015,18(12):2155-2160.

