高效液相色谱-三重四极杆/复合线性离子阱质谱法测定血液中唑吡坦和扎莱普隆的含量
时巧翠,朱 斌
(浙江警察学院 刑事科学技术系,杭州310053)
样品前处理是法庭科学中毒物分析的关键步骤,直接影响毒物的检出率[4]。传统的样品前处理方法如固相萃取、液液萃取等,存在操作繁琐费时、提取率低、需要使用大量对人体和环境有毒害作用的有机溶剂等问题[5-6]。介质液液萃取(SLE)是1997年由Johnson提出的一种新型的样品前处理技术[7]。与传统萃取技术相比,SLE具有操作简便,能大大缩短样品提取时间,回收率高,基质干扰小,可以应用于以96孔板结构为代表的高通量体系等特点。SLE已被广泛应用于环境分析,食品安全等方面[8-10],但在法庭科学中的应用鲜有报道[11]。
目前,测定血液中唑吡坦和扎莱普隆的方法主要有气相色谱法[12]、液相色谱法[13]、气相色谱-质谱法[14]及液相色谱-质谱法[15]等。但这些方法均存在灵敏度较低,分析时间略长等缺点。本工作建立了介质液液萃取-高效液相色谱-三重四极杆/复合线性离子阱质谱(SLE-HPLC QTRAP-MS/MS)测定血液中唑吡坦和扎莱普隆含量的方法。
1 试验部分
1.1 仪器与试剂
Biotage ISOLUTE SLE 1mL 介质液液萃取柱;Shimazu LC 20A/AB Sciex Qtrap 6500型高效液相色谱-质谱联用仪。
唑吡坦标准储备溶液:1.000g·L-1,使用时用甲醇稀释至所需质量浓度。
扎莱普隆标准储备溶液:1.000g·L-1。
缓冲溶液:pH 7的缓冲溶液以饱和氯化钠溶液代替;用0.2mol·L-1氨水和0.2mol·L-1氯化铵溶液按比例配制成pH 9的缓冲溶液;0.2mol·L-1乙酸铵溶液作为pH 10的标准缓冲溶液;用0.2mol·L-1氢氧化钠溶液和0.2mol·L-1氯化钾溶液按比例配制成pH 12和pH 13的缓冲溶液。
乙醚、乙酸乙酯、二氯甲烷、三氯甲烷均为分析纯;甲酸、乙酸铵、乙腈均为色谱纯。
1.2 仪器工作条件
1)色谱条件 Kinetex C18色谱柱(50mm×3.0mm,2.6μm),柱温40℃;进样量5μL;流量0.5mL·min-1;流动相 A为含5mmol·L-1乙酸铵的0.1%(体积分数,下同)甲酸溶液,B为乙腈。梯度洗脱程序:0.0~4.0min时,B为10%;4.0~4.1min时,B由10%升至90%,保持2min;6.0~6.1min时,B由90%降至10%,保持3min。
2)质谱条件 电喷雾离子(ESI)源,正离子模式;多反应监测(MRM)模式;辅助加热气温度500℃;离子化电压5 500V;气帘气压力275.8kPa;碰撞气为氮气,压力选择 Medium;喷雾气压力344.7kPa;辅助加热气压力344.7kPa。主要质谱参数见表1,其中“*”为定量离子。
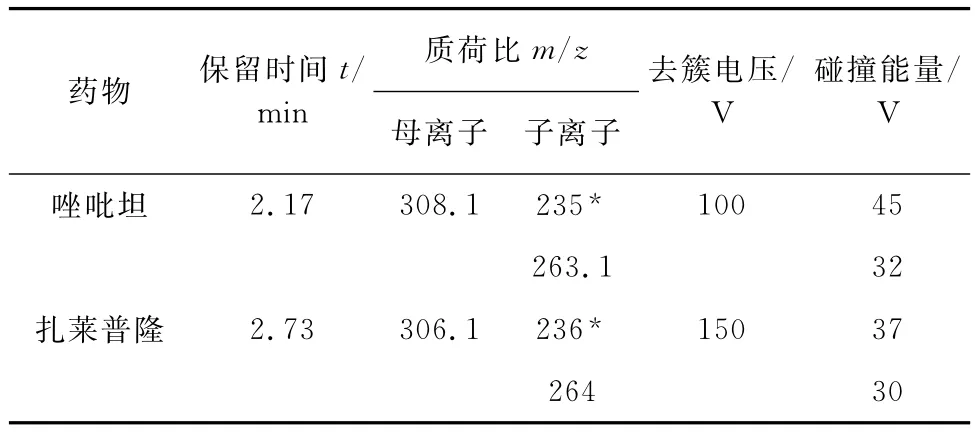
表1 质谱参数Tab.1 MS parameters
1.3 试验方法
移取含有唑吡坦与扎莱普隆的血液0.50mL,加入pH 10的缓冲溶液0.3mL。混匀后将样品加入介质液液萃取柱中,施加压力,使样品全部均匀分散在填料上后,静置2min。用二氯甲烷8mL洗脱,控制其流量在1mL·min-1左右,最后施加压力将柱中残余的二氯甲烷挤出。洗脱液用氮气吹干后,用初始流动相溶解并定容至0.50mL,在仪器工作条件下进行测定。
2 结果与讨论
2.1 色谱行为
唑吡坦和扎莱普隆的总离子流色谱图见图1。

图1 唑吡坦和扎莱普隆的总离子流色谱图Fig.1 TIC chromatogram of zolpidem and zaleplon
2.2 SLE萃取条件的选择
以空白血液为基质,分别配制含有1.0μg·L-1唑吡坦与10μg·L-1扎莱普隆的标准溶液,按仪器工作条件进行测定。
2.2.1 萃取剂
选用pH 10的缓冲溶液、平衡时间2min、溶剂使用量6mL,试验分别考察了乙酸乙酯、三氯甲烷、乙醚、二氯甲烷等萃取剂的萃取效果。结果表明:二氯甲烷作为萃取剂时,效果较好,这可能是因为唑吡坦与扎莱普隆在二氯甲烷中有较好的溶解度。试验选择二氯甲烷为萃取剂。
2.2.2 萃取剂用量
选用pH 10的缓冲溶液、平衡时间2min,试验考察了二氯甲烷用量分别为4,6,8,10mL时唑吡坦与扎莱普隆的回收率。结果表明:随着二氯甲烷用量的增加,唑吡坦和扎莱普隆的回收率也逐渐提高,但当二氯甲烷的用量为8,10mL时,两种药物回收率趋于稳定。试验选择二氯甲烷的用量为8mL。
2.2.3 缓冲溶液酸度
固定平衡时间2min、萃取剂二氯甲烷6mL,试验考察了缓冲溶液pH 分别为7,9,10,12,13时唑吡坦和扎莱普隆的萃取回收率。结果表明:随着缓冲溶液pH的增大,唑吡坦和扎莱普隆的回收率也逐渐提高。但当缓冲溶液的pH由10增大至13时,两种药物的回收率相差很小。考虑到碱性太强,血液容易凝固而堵塞SLE萃取柱,试验选择pH为10的缓冲溶液。
2.2.4 平衡时间
在缓冲溶液pH为10、萃取剂二氯甲烷6mL的条件下,样品均匀分散在介质液液萃取柱填料上以后,试验考察了静置时间分别为2,5,8,10min时唑吡坦和扎莱普隆的萃取回收率。结果表明:平衡时间对目标物回收率的影响较小。试验选择平衡时间为2min。
2.3 色谱条件的选择
试验分别比较了0.1%甲酸-甲醇、0.1%甲酸-乙腈、0.1%甲醇-乙腈和水-乙腈4种流动相体系对分析结果的影响。结果表明:流动相选用0.1%甲酸-乙腈体系时峰形更好,分离效果更优,因此流动相选择0.1%甲酸-乙腈体系进行梯度洗脱。添加不同体积分数的甲酸(0.1‰,0.5‰,1‰)、乙酸(0.1‰,0.2‰,0.5‰),不同浓度的乙酸铵(0.5,1,5mmol·L-1),结 果 发 现 在 流 动 相 中 加 入5mmol·L-1乙酸铵不仅可以改善待测化合物的峰形,同时还可以增加待测物质的响应值。试验选择在0.1%甲酸的流动相中加入了5mmol·L-1乙酸铵,以提高方法的灵敏度。优化的色谱条件见1.2节。
2.4 质谱条件的选择
试验采用ESI正离子模式作为其离子化方式。取质量浓度均为0.100g·L-1的吡唑坦、扎莱普隆标准溶液,采用微量蠕动泵连续进样,一级质谱全扫描,确定准分子离子。结果显示唑吡坦与扎莱普隆均在正离子模式下获得准分子离子峰。唑吡坦与扎莱普隆的准分子离子峰分别为m/z308.1,306.1。以唑吡坦与扎莱普隆的准分子离子峰为母离子进行二级质谱扫描,选丰度最高的两个特征碎片离子作为定性定量离子,并优化相应离子对的去簇电压、碰撞能量、碰撞室出口电压和入口电压。主要质谱参数见表1。
2.5 标准曲线和检出限
以空白血液为基质,分别配制唑吡坦的质量浓度为 0.10,0.20,0.50,1.00,2.00,5.00,10.00μg·L-1,扎莱普隆的质量浓度为 1.00,2.00,5.00,10.00,20.00,50.00,100.0μg·L-1的标准混合溶液系列,按仪器工作条件进行测定。以药物的质量浓度为横坐标,对应的峰面积为纵坐标绘制标准曲线,唑吡坦和扎莱普隆的线性范围、线性回归方程和相关系数见表2。
按3倍信噪比计算方法的检出限(3S/N),其结果见表2。

表2 线性参数及检出限Tab.2 Linearity parameters and detection limits
2.6 精密度和回收试验
取空白血液,在线性范围内分别加入质量浓度为0.20,2.00,10.00μg·L-1的唑吡坦和2.00,10.00,25.00μg·L-1的扎莱普隆,按试验方法平行测定6次,其加标回收率和测定值的相对标准偏差(RSD)见表3。
由表3可知:两种目标化合物的加标回收率在85.0%~103%之间,RSD在3.5%~8.5%之间。
2.7 样品分析
案例1:某女46岁,长期受失眠困扰。一天其被发现在家中自杀身亡。抽取该女子心脏内血液按照试验方法进行检测分析,结果在其血液中检出唑吡坦的质量浓度为1.26mg·L-1,其多反应监测色谱图见图2(a)。

表3 精密度和回收试验结果(n=6)Tab.3 Results of tests for precision and recovery(n=6)
案例2:某女38岁,因与其丈夫吵架而吞服大量Sonata自杀身亡。抽取其心脏内血液按照试验方法进行测定,结果在其血液中检出扎莱普隆的质量浓度为46.7μg·L-1,其多反应监测色谱图见图2(b)。

图2 样品的多反应监测色谱图Fig.2 MRM chromatograms of samples
本工作建立了高效液相色谱-三重四极杆/复合线性离子阱质谱结合介质液液萃取技术测定血液中的唑吡坦和扎莱普隆的分析方法,优化了介质液液萃取试验条件及高效液相色谱-串联质谱法的仪器条件,对血液中的这两种药物进行了定性与定量分析。方法具有较高的灵敏度、回收率和精密度,能有效测定血液中唑吡坦与扎莱普隆的含量,可满足侦查、诉讼及医疗急救的检测要求。
[1] SANGER D J,MOREL E,PERRAULT G.Comparison of the pharmacological profiles of the hypnotic drugs,zaleplon and zolpidem[J].European Journal of Pharmacology,1996,313(1/2):35-42.
[2] GIROUD C,AUGSBURGER M,MENETREY A,et al.Determination of zaleplon and zolpidem by liquid chromatography-turbo-ionspray mass spectrometry:application to forensic cases[J].Journal of Chromatography B,2003,789(1):131-138.
[3] 张蕾萍,于忠山,何毅,等.法庭鉴定中的新型催眠药[J].刑事技术,2008(5):37-40.
[4] OSEMWENGIE L I,STEINBERG S.On-site solidphase extraction and laboratory analysis of ultra-trace synthetic musks in municipal sewage effluent using gas chromatography-mass spectrometry in the full-scan mode[J].Journal of Chromatography A,2001,932(1/2):107-118.
[5] BESTER K.Analysis of musk fragrances in environmental samples[J].Journal of Chromatography A,2009,1216(3):470-480.
[6] PIETROGRANDE M C,BASAGLIA G,DONDI F.Signal processing to evaluate parameters affecting SPE for multi-residue analysis of personal care products[J].Journal of Separation Science,2009,32(9):1249-1261.
[7] HARA K,KASHIMURA S,HIEDA Y,et al.Simple extractive derivatization of methamphetamine and its metabolites in biological materials with Extrelut columns for their GC-MS determination[J].Journal of Analytical Toxicology,1997,21(1):54-58.
[8] LIU H T,HUANG L P,CHEN Y X.Simultaneous determination of polycyclic musks in blood and urine by solid supported liquid-liquid extraction and gas chromatography-tandem mass spectrometry[J].Journal of Chromatography B,2015,992:96-102.
[9] RAMES B,MANJUL N,RAMAKRISHNA S,et al.Direct injection HILIC-MS/MS analysis of darunavir in rat plasma applying supported liquid extraction[J].Journal of Pharmaceutical Analysis,2015,5(1):43-50.
[10] ALBERO B,SNCHEZ-BRUNETE C, MIGUEL E,et al.Determination of selected pharmaceutical compounds in biosolids by supported liquid extraction and gas chromatography-tandem mass spectrometry[J].Journal of Chromatography A,2014,1336:52-58.
[11] ROSITANO J,HARPAS P,KOSTAKIS C,et al.Supported liquid extraction(SLE)for the analysis of methylamphetamine, methylenedioxymethylamphetamine and delta-9-tetrahydrocannabinol in oral fluid and blood of drivers[J].Forensic Science International,2016,265:125-130.
[12] DEBRUYNE D,LACOTTE J, HURAULT DE LIGNY B,et al.Determination of zolpidem and zopiclone in serum by capillary column gas chromatography[J].Journal of Pharmaceutical Sciences,1991,80(1):71-74.
[13] METWALLY F H, ABDELKAWY M, ABDEL-WAHAB N S.Application of spectrophotometric,densitometric and HPLC techniques as stability indicating methods for determination of zaleplon in pharmaceutical preparations[J].Spectrochimica Acta Part A,2007,68(5):1220-1230.
[14] KELLER T,SCHNEIDER A,TUTSCH-BAUER E.GC/MS determination of zolpidem in postmortem specimens in a voluntary intoxication[J].Forensic Science International,1999,106(2):103-108.
[15] HORSTKOTTER C,SCHEPMANN D,BLASCHKE G.Separation and identification of zaleplon metabolites in human urine using capillary electrophoresis with laser-induced fluorescence detection and liquid chromatography-mass spectrometry[J].Journal of Chromatography A,2003,1014(1/2):71-81.

