胸腔镜纵隔肿瘤切除术27例临床分析
王永歧
纵隔肿瘤是胸外科的常见肿瘤,以手术切除治疗为主要方法。传统以剖胸手术切除肿瘤,随着微创外科技术的飞速发展、手术器械日新月异的创新,更多的胸部疾病可以通过胸腔镜进行诊断和治疗,胸腔镜手术已逐渐应用于纵隔肿瘤手术中[1]。腔镜手术使胸部手术范围及视野更宽阔、更容易、患者术后恢复更快,充分体现了微创发展的趋势,并指引了胸外科手术的发展方向。本文回顾分析 27例施行胸腔镜纵隔肿瘤手术切除的临床资料,探讨其在纵隔肿瘤诊断及治疗中的价值。
1 资料与方法
1.1 一般资料:回顾分析2008年2月-2016年8月我院胸外科手术的62例纵隔肿瘤患者,男性34例,女性28例;年龄17~78岁,中位年龄 48.7岁。23例患者常规检查时发现纵隔肿瘤,平素无临床症状。39例患者因声音嘶哑、咳嗽、吞咽不适、不同程度胸痛、乏力等症状就诊发现纵隔肿瘤,其中位于上纵隔19例,中纵隔26例,后纵隔肿瘤17例。肿瘤大小在1.5~6.8 cm,平均2.9 cm。所有患者均无明显胸腔镜手术禁忌证。患者术前均行胸部CT或MRI等相关检查。所有患者术前均未行穿刺活检或纵隔镜检查。3例肌无力患者术前予以抗胆碱酯酶药物口服控制症状后手术。术后病检恶性肿瘤11例,良性肿瘤 51例。肿瘤类型有:淋巴瘤15例,胸腺瘤15例,畸胎瘤8例,神经纤维肿瘤11例,支气管囊肿10例,纵隔型肺癌3例。2组患者性别、年龄、肿瘤大小、病理类型等差异无统计学意义(P>0.05)。
1.2 手术方法:腔镜组27例,麻醉方式为静脉复合麻醉。根据胸部CT提示肿瘤所在部位不同,选择相应左侧或右侧手术入路。通常依据肿瘤所在纵隔的位置选择合适的手术体位,前纵隔肿瘤通常为半侧卧位后倾15~30°,中纵隔肿瘤取侧卧位。后纵隔肿瘤侧卧位后前倾15°。本组14例患者取健侧卧位,12例取抬高患侧30°卧位。观察孔通常选择肿瘤所在位置第4~6肋间腋后线或腋前线,操作孔选择2个,位于第4~7肋间腋后线或腋中线。一般3个操作孔呈三角形,切口长度1.5~2 cm。经观察孔置入 30°胸腔镜探查,明确肿瘤所在具体部位,以及其周围相邻脏器、神经、血管等决定2~3个操作孔的位置。在手术中根据需要操作孔与胸腔镜孔可以交替使用,可以选择一个2.0~3.5 cm操作孔取标本,必要时还可延长切口至4~6 cm协助切除肿瘤。可利用血管钳、吸引器等钝性分离肿瘤将其完整剥除,对于实性肿瘤,可利用电钩切开肿瘤表面包裹的纵隔胸膜,自肿瘤包膜外用钝性结合锐性小心剥除。对于囊性肿瘤较小时应完整摘除,如巨大囊肿影响手术操作时,可利用穿刺器吸出大部分囊液后再行剥离。术中要把囊肿壁及其蒂部完整切除,对少量粘连致密无法切除的残存囊壁,为避免术后复发可用电刀或双极电凝烧灼破坏。由于肿瘤蒂部的滋养血管血运丰富,术中需仔细分离电凝、使用钛夹夹闭或腔镜下结扎或缝扎。术中严格实施无瘤原则,肿瘤切除后放入标本袋中取出,或放入标本袋内剪成小块后再取出,可以避免肿瘤种植。对于胸腺瘤合并重症肌无力时,切除范围要扩大,包括整个胸腺、胸腺瘤和纵隔内脂肪组织。手术结束时生理盐水仔细冲洗胸腔,查术区无活动性出血,退出胸腔镜,观察孔放置胸腔闭式引流管。切除组织常规送病检。
对照组患者35例,行传统开胸纵隔肿瘤切除术,亦根据术前胸部CT决定手术入路及术中体位。全麻后气管插管,切口选择在肋间后外侧进胸,长15~20 cm。可使用肋骨牵开器将肋骨牵开充分暴露胸腔,直视下找到纵隔肿瘤进行手术。
1.3 观察指标:观察分析2组患者平均手术时间、术中出血量、术后引流管放置的时间、住院时间、使用镇痛药物时间和术后并发症等情况,并进行统计学分析。

2 结果
2.1 2组手术常用指标比较:2组患者均顺利完成手术后治愈出院。腔镜组27例患者成功完成胸腔镜下纵隔肿瘤切除。2例因瘤体太大,延长4~8 cm辅助小切口完成手术。2例因术前合并重症肌无力术中行胸腺切除术。腔镜组手术时间与对照组比较无明显差异(P>0.05),而腔镜组术后胸管引流时间、术后镇痛药物使用时间、术后住院时间均比对照组短,差异有统计学意义(P<0.05),见表1。
表1 2组患者术中、术后观察指标的比较
2.2 2组患者术后并发症发生率比较:腔镜组1例术后肌无力症状无明显缓解,调整溴比斯的用量并定期复查,至今未发现复发;1 例术后早期出现轻微声音嘶哑后自行缓解。对照组2例术后声音嘶哑、4例术后出现发热、肺部感染,2例切口液化,1例肺不张,4例胸膜腔粘连。2组患者并发症发生率比较差异有统计学意义(χ2= 4.12,P<0.05),见表2。
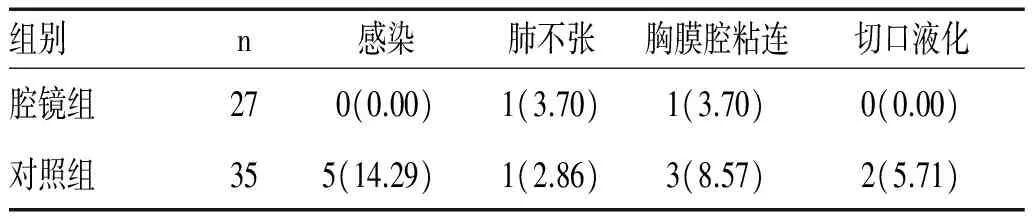
表2 2组患者并发症发生率的比较[n(%)]
3 讨论
纵隔肿瘤是胸外科常见疾病,肿瘤来源可为原发性或转移性[2]。由于成像技术敏感性的提高以及胸部CT及MRI的普及应用,更多无症状的纵隔肿瘤患者在早期即获得诊断[3]。患者均正规胸部摆位行CT扫描平扫加增强,扫描范围自胸廓入口至膈面的胸部,扫描层厚1 mm,层间距10 mm,进行连续扫描。当上纵隔肿瘤与颈部相连时,扫描应包括颈部。使用局部薄层扫描可发现隐蔽部位的较小肿瘤,CT密度分辨率高,能根据病变区的CT值确定病变是囊性、实性还是脂肪,其中是否有微小钙化、脂肪沉着、坏死及出血等改变,对显示肿瘤的位置、形态、来源、包膜完整性、与周围脏器组织相邻关系以及病变发展状况有很好的诊断价值。部分患者无临床症状,只有当纵隔内的重要组织被肿瘤压迫或侵犯时会出现相应的临床表现。纵隔肿瘤的治疗首选手术,同时根据病检术后需进行必要的化疗和放疗。
传统开胸手术路径多为外侧或胸骨正中行纵隔肿瘤切除,术中创伤大需断开胸骨、肋骨,损伤软组织、肌肉和神经,手术切口长、术中出血量多、术后患者因切口剧烈疼痛,不能有效咳嗽排痰从而影响肺功能的恢复,同时存在术后恢复慢,并发症多,延长住院时间等弊端[4]。随着胸外科微创技术的发展及手术器械的不断更新,胸腔镜被广泛应用于胸外科手术中,其微创性弥补了开胸手术的不足,逐渐成为胸外科医生的优先选择[5],同时逐步应用于纵隔肿瘤的诊断与治疗中。经胸壁穿刺套管或经微小切口完成纵隔手术,其优势在于切口美观创伤小、恢复快、术后疼痛明显减少、对肺功能影响小、术后并发症少等[6]。
在本研究中,27例患者行胸腔镜下纵隔肿瘤切除术,与传统的纵隔开胸手术比较更具有优势,手术中出血量明显减少,住院时间缩短,术后患者疼痛明显减轻,同时手术并发症大大减少,相比较差异有统计学意义(P<0.05)。杨列等[7]临床研究认为,胸腔镜下纵隔肿瘤切除,其肿瘤清除率与开胸手术无明显差异,但术后并发症发生率显著低于开胸手术,这与本研究结果相似。
本研究显示,胸腔镜尤其适合无症状、肿瘤体积小、与周围组织界线清的纵隔肿瘤。对于直径> 10 cm的纵隔肿瘤,特别是实性肿瘤,常常与周围脏器、血管等粘连界限不清分离困难,为避免术中损伤,宜选择安全的常规开胸手术。对于中纵隔囊肿均可经胸腔镜手术切除。当与周围组织有粘连,为避免损伤可保留少量囊壁,同时为避免术后复发,残留囊壁行电灼或化学方法破坏。后纵隔手术视野较宽阔,便于胸腔镜手术。当肿瘤直径> 5 cm,必要时辅助小切口行肿物切除 。在本研究中3例神经源性肿瘤均在胸腔镜下完成手术,当后纵隔神经源性肿瘤术前确诊呈哑铃形并经椎间孔向椎管内生长时应行开胸手术。
本资料在手术中,除了对纵隔解剖十分熟悉外,还要正确使用重要手术切割止血器械、高频电钩和超声刀。超声刀在微创外科中非常实用,使手术操作精细、术野清晰、热效应低而降低周围组织损伤。在超声刀使用中,对具有完整包膜的纵隔肿瘤可以使用电凝钩或者超声刀进行包膜的剥离。超声刀能量距离传播<0.5 mm,切割精确,因此可以在重要大血管和脏器旁操作,并尽可能地避免热效应损伤神经[8]。在距离神经较近的区域操作时,超声刀每完成20 s左右操作后,可以将超声刀头放入常温生理盐水中冷却处理1~2次,能对神经起到保护作用。同时注意超声刀头的方向,功能杆朝向肿瘤,无功能杆朝向后方,尤其当膈肌颤动时更要小心膈神经的热损伤。
对于纵隔肿瘤的诊断和治疗,胸腔镜是一种安全有效的选择,尤其对于纵隔良性肿瘤较传统的开胸手术更具有明显优势,精细的手术解剖分离操作,创伤小,恢复迅速,术后疼痛减轻,建议在临床上推广应用。
[1] 殷勇.胸腔镜和传统开胸手术治疗纵隔肿瘤的临床疗效比较[J].中国肿瘤临床与康复,2014,21(10) :1164-1166.
[2] Bernard C,Frih H,Pasquet F,et al.Thymoma associated with autoimmune diseases:85 cases and literature review[J].Autoimmun Rev,2016,15(1):82-92.
[3] 赵凯华,孙万兴.64排螺旋CT在纵膈型肺癌诊断中的应用[J].中国药物与临床,2013,13(17):893-894.
[4] Jiao W,Qiu T.The minimally invasive thoracic surgery for lung cancer:a voice from China[J].Indian J Cancer,2015,51(Suppl 2):2.
[5] Reichert M,Steiner D,Kerber S,et al.A standardized tech-nique of systematic mediastinal lymph node dissection by vid-eo - assisted thoracoscopic surgery (VATS ) leads to a highrate of nodal upstaging in early-stage non-small cell lungcancer[J].Surg Endosc,2015,14(7):1104-1108.
[6] Khan S,Khan S,Chawla T,et al.Harmonic scalpel versus electro-cautery dissection in modified radical mastectomy:a randomizedcontrolled trial[J].Ann Surg Oncol,2014,21(3):808-814.
[7] 杨列,姜建青,郑轶峰,等.全胸腔镜下胸腔内巨大包块切除的临床疗效分析[J].西南军医,2012,14 (5):697-699.
[8] Motus IY,Bazhenov AV,Massard G.Surgery for huge medi-astinal tumors[J].Asian Cardiovasc Thorac Ann,2015,23(7):846-850.

