壳聚糖颗粒吸附纳米氧化石墨烯的研究
王梓川,汤韩挺,薛 超,张国庆,杨 帅,张大伟
(东北林业大学 材料科学与工程学院,黑龙江 哈尔滨 150040)
前 言
石墨烯及其衍生物已经被广泛应用于材料学、能源、生物医学[2]等领域,由于氧化石墨烯纳米材料的大量生产,在生产和应用中会产生大量的废弃物,研究表明这些废弃物会进入到空气、水体、土壤中,造成生物体毒性,破坏生态环境[1~4]。而壳聚糖是一种碱性多糖并且自然资源丰富,壳聚糖分子链结构上具有大量的游离—NH2和—OH活性基团[5~9],是一种拥有良好吸附效果的螯合型吸附剂[10],作为一种天然高分子材料,壳聚糖可生物降解,对环境不会产生二次污染造成破坏[11]。利用壳聚糖颗粒吸附氧化石墨烯,能作为一种回收氧化石墨烯的环保新方法。
本文研究了壳聚糖的粒径、脱乙酰度、pH值、温度等因素对吸附氧化石墨烯的影响,并且对壳聚糖吸附氧化石墨烯后的形貌、官能团进行了研究。
1 实验部分
1.1 实验材料及仪器
壳聚糖(脱乙酰度分别为81%、85%、91%、95%,浙江金壳药业有限公司);氧化石墨烯水溶液(自制,固含量为0.05%,实验室自制);HJ-6A数显恒温磁力加热搅拌器(金坛市白塔新宝仪器厂);NaOH(分析纯,天津市大陆化学试剂厂);HCl(分析纯,宜兴市辉煌化学试剂厂);Na2CO3(分析纯,沈阳市新西试剂厂);冰醋酸(优级纯,天津市科密欧化学试剂有限公司);蒸馏水(哈尔滨文景蒸馏水厂);分析天平(FA2204B,北京华运安特科技有限责任公司);扫描电子显微镜(QUANTA 200型,FEI公司);红外光谱仪(ALPHA型,德国布鲁克公司)。
1.2 不同粒径壳聚糖的制备
将不同脱乙酰度的壳聚糖用100目、200目、300目和500目筛子分离,从而得到不同目数的壳聚糖,用其吸附分散于水中的氧化石墨烯纳米层片。
1.3 壳聚糖吸附氧化石墨烯层片
取一定质量的不同脱乙酰度壳聚糖,分别倒入匀速搅拌中的氧化石墨烯溶液中,定时观察氧化石墨烯溶液的颜色。观察间隔为1次/5min,如果氧化石墨烯溶液颜色有明显变浅变澄清的趋势时,将观察间隔缩短为1次/5s。
1.4 pH值对吸附的影响
取锥形瓶在其中加入50mL的氧化石墨烯溶液,然后用HCI、NaOH将溶液pH值调整到2~9,当pH值超过12后破坏氧化石墨烯溶液的稳定性,溶液体系易发生沉降,为此将pH值设定为9以下。然后置于搅拌器中匀速搅拌,再在溶液中分别加入粒度为500目、脱乙酰度85%的壳聚糖2g,观察上层溶液完全澄清的时间。
1.5 温度对吸附的影响
取8个锥形瓶,在其中分别加入50mL的氧化石墨烯溶液,置于搅拌器上搅拌,在搅拌的同时将锥形瓶内的溶液分别加热至20~90℃,每隔10℃取一个测试点。每个锥形瓶中再分别加入粒度为500目、脱乙酰度85.85%的壳聚糖2g,记录吸附完成时间。
1.6 红外光谱与扫描电镜表征
使用红外光谱分析了吸附前后壳聚糖化学结构的变化,使用扫描电子显微镜观测了吸附前后壳聚糖表面形貌的变化。为保持测试试样的物理和化学性质不发生变化,使用冷冻干燥机,将吸附后的壳聚糖冷冻干燥,然后再进行测试分析。
2 结果讨论
2.1 脱乙酰度、粒径对吸附的影响
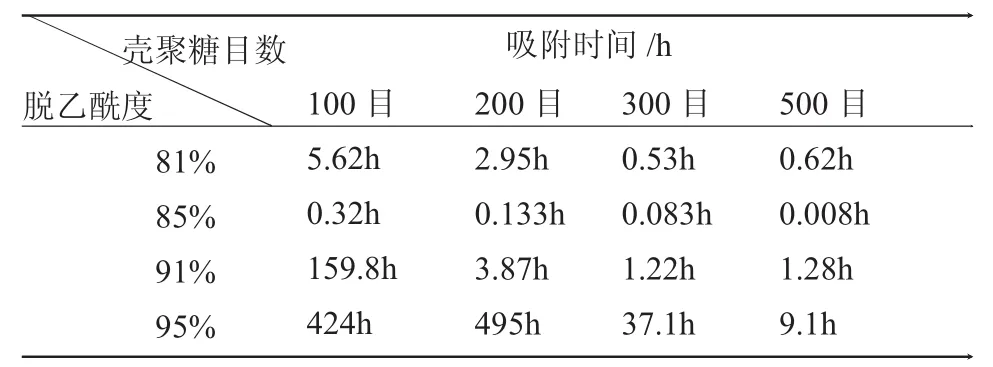
表1 不同粒径、不同脱乙酰度壳聚糖吸附氧化石墨烯时间Table 1 The adsorption time of graphene oxide by chitosan with different particle sizes and degrees of deacetylation
研究了壳聚糖的脱乙酰度和粒径对吸附速率的影响,结果如表1所示。
从表1中可以发现,随着壳聚糖过筛目数的增加,即其颗粒直径的下降,吸附速率迅速增加,以吸附速率最快、脱乙酰度85%的壳聚糖为例,粒径从100目增加500目时,吸附时间由0.32h(19.2min),减少到0.008h(0.48min)。从中可以发现,增加了吸附剂的比表面积可以极大地提高其吸附能力,加快氧化石墨烯的沉降速度。从表1中还可以发现,并不是脱乙酰度最高的壳聚糖吸附速率最快,而是脱乙酰度为85%的吸附速率最快。壳聚糖的吸附能力来源于其分子主链上的氨基,脱乙酰度越高,分子主链上的氨基数量越多,而大量的氨基相互间容易形成氢键,从而影响了其吸附性能的发挥,脱乙酰度越高的壳聚糖其吸附速率越慢。而脱乙酰度过低,如脱乙酰度81%时,分子链上有大量的N-乙酰氨基,影响了壳聚糖分子的吸附性能。因为壳聚糖依靠分子主链上的氨基吸水后电离产生带有正电荷的铵离子去吸附带有负电荷的氧化石墨烯,如果氨基数量太少会导致体系中能电离出铵离子的数量不足,进而影响吸附速率。
2.2 pH值对吸附速率的影响

图1 pH值对吸附时间影响曲线Fig.1 The effect of pH value on the adsorption time
pH值对吸附氧化石墨烯的影响如图1所示。经pH计测量,超声制得的氧化石墨烯溶液的pH值为4.4,此pH值下脱乙酰度为85%、粒径为500目的壳聚糖吸附时间为29s。当将pH值调到2~3时,壳聚糖在氧化石墨烯的溶液中迅速溶胀甚至溶解,在H+的作用下,壳聚糖分子上的氨基迅速转变为带正电荷的铵根离子,破坏氧化石墨烯的双电层结构,使其发生絮凝沉淀。这种方式虽然能迅速将氧化石墨烯从水中分离,但很难再把壳聚糖与氧化石墨烯分离,为氧化石墨烯的收集带来困难。当pH值增加后可以发现,吸附时间迅速增加,当pH值增加到7时,吸附时间延长到43s,而pH值超过9时,壳聚糖已经不能把氧化石墨烯从溶液中吸附出来。这充分说明,壳聚糖吸附氧化石墨烯是依靠其氨基电离产生的带正电荷的铵根离子破坏氧化石墨烯的双电层结构,从而将其从溶液中吸附在壳聚糖粒子的表面。碱性条件下,氨基的电离受到抑制,因此与氧化石墨烯官能团之间的静电吸附效应下降,吸附速率降低、时间延长。
2.3 温度对吸附的影响
随着温度升高,壳聚糖分子上的氨基电离速度加快,氧化石墨烯在溶液中无规则热运动速率也相应提高,对于一般的吸附而言,往往是升高温度,吸附速率加快,但解吸附速率升高的更多,往往导致吸附速率并没有实质的提升。为清晰显示氧化石墨烯在壳聚糖表面的吸附,选择粒径比较大(100目)、脱乙酰度85%的壳聚糖吸附氧化石墨烯。实验结果如图2所示。
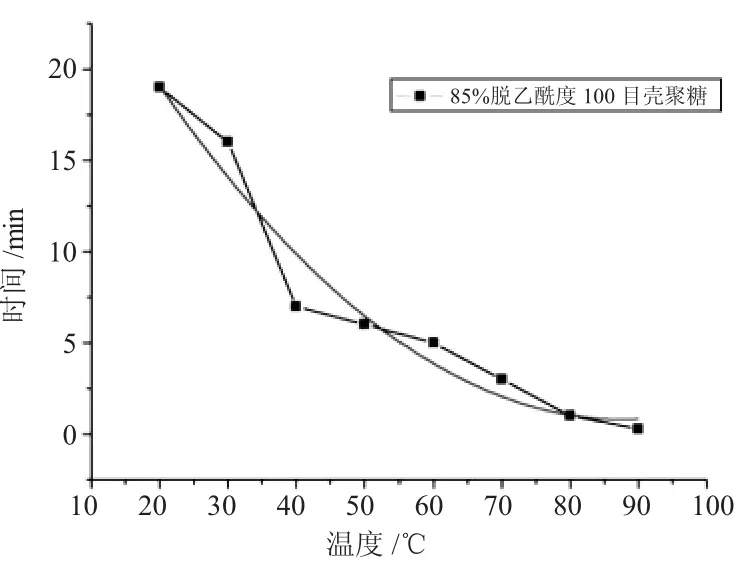
图2 温度对壳聚糖吸附氧化石墨烯时间的影响Fig.2 The effect of temperature on the adsorption time
从图2中可以发现,随着温度升高,壳聚糖对氧化石墨烯的吸附时间迅速缩短,从20℃时的19min左右,缩短到90℃时的几分钟,特别在30~40℃之间吸附速率升高特别明显。分析是由于温度的升高使得分子热运动加快,增加了氧化石墨烯与壳聚糖的接触概率,同时温度的升高使得氧化石墨烯表面的双电层结构破坏,聚沉加速,吸附速率增快。
2.4 壳聚糖质量对吸附的影响
在量筒中加入50mL的氧化石墨烯水溶液,分别加入0.1~2.0g脱乙酰度85%、粒径500目的壳聚糖颗粒,步长为0.1g。测试过程中,每隔30s搅拌一次,直至搅拌后上层清液呈无色透明为止。再对测得的壳聚糖质量进行细分,以0.01g为步长,测得吸附完全时,壳聚糖的最小用量,依据公式(1)计算单位质量壳聚糖对氧化石墨烯的吸附量。

式(1)中为单位质量壳聚糖吸附氧化石墨烯的质量,g/g;V为氧化石墨烯溶液体积,mL;ρ为氧化石墨烯密度,g/mL;S为氧化石墨烯固含量,g/g;M为壳聚糖颗粒质量,g。
研究发现,步长0.1g时加入壳聚糖量0.7g可完全吸附,据此判断吸附完全时壳聚糖的最少用量在0.6~0.7g。为进一步精细实验,以0.01g为步长,发现加入0.65g壳聚糖可将氧化石墨烯吸附完全,测得吸附完全最小壳聚糖量M为0.65g。以此按照公式(1)计算得为1.39g/g。
2.5 吸附对壳聚糖形态的影响
采用扫面电子显微镜观测了壳聚糖、氧化石墨烯及吸附了氧化石墨烯的壳聚糖的表面形貌,结果如图3所示。

图3 吸附前后壳聚糖及氧化石墨烯的SEM图(a)壳聚糖(b)氧化石墨烯(c)吸附GO的壳聚糖Fig.3 The SEM images of chitosan,graphene oxide and chitosan(after adsorption)(a)CS,(b)GO and(c)CS after adsorption
从图3可以看出,吸附前壳聚糖表面存在大量微小凸起,吸附前的氧化石墨烯呈现类似于纸张的层片状结构,而吸附后的壳聚糖出现大量的褶皱,而原有的表面凸起消失,图3(c)中吸附后壳聚糖颗粒表面的褶皱与图3(b)氧化石墨烯表面褶皱形状相似,从中可以发现,氧化石墨烯被壳聚糖颗粒吸附后,氧化石墨烯是以平铺的方式包覆在壳聚糖表面。
2.6 吸附前后壳聚糖官能团变化

图4 吸附氧化石墨烯前后壳聚糖的红外光谱图Fig.4 The FT-IR spectra of chitosan before and after the adsorption(a)CS and(b)CS after adsorption
借助红外光谱,分析了吸附氧化石墨烯前后壳聚糖表面官能团的变化,结果如图4所示。从图4中可以发现,壳聚糖吸附氧化石墨烯前后无新的官能团特征峰出现,说明并无化学反应产生,但是壳聚糖吸附氧化石墨烯后原有官能团吸收峰伸缩振动频率向低波数方向移动,并且吸收峰强度增强,证明壳聚糖和氧化石墨烯之间产生了强烈的氢键作用[12-13],宏观上产生吸附现象。
3结 论
氧化石墨烯的羧基等基团电离后带负电荷,形成双电子结构,受到表面氨基、羟基电离后携带正电荷的壳聚糖作用而双电子层结构破坏,氧化石墨烯中的阴离子与壳聚糖中的阳离子产生静电作用。同时,壳聚糖所携带的氨基、羟基与氧化石墨烯所携带的羧基之间产生强烈的氢键作用。壳聚糖与氧化石墨烯之间依靠静电作用和氢键作用相结合。壳聚糖比表面积的增大有助于增加壳聚糖与氧化石墨烯的接触概率,温度升高分子热运动加剧,使得壳聚糖与氧化石墨烯接触概率增大,同时温度升高破坏氧化石墨烯的双电层结构,导致吸附速率加快。而pH值在酸性条件下尤其在3~5之间,有助于壳聚糖官能团的电离,加剧与氧化石墨烯作用,pH值低于2时壳聚糖开始溶融形成凝胶,降低了与氧化石墨烯的接触,而碱性条件下壳聚糖官能团活性被抑制,不能大量电离,从而吸附速率大幅下降。
[1] SANCHEZ V C,JACKHAK A,HURT R H,et al.Biological interactions of graphene-family nanomaterials:An interdisciplinary review[J].Chemical Research in Toxicology,2012,25(1):15~34.
[2] YANG K,FENG L Z,HONG H,et al.Preparation and functionalization of graphene nanocomposites for biomedical applications[J].Small,2013,8(12):1492~1503.
[3] ZHAO J,WANG Z Y,WHITE J C,et al.Graphene in the aquatic environment:Adsorption,dispersion,toxicity and transformation [J].Environmental Science&Technology,2014,48(17):9995~10009.
[4] 李婷,张智超,沈丹,等.石墨烯和氧化石墨烯的生物体毒性研究进展[J].南京大学学报(自然科学),2016,52(2):235~243.
[5] 胡惠媛,朱虹.壳聚糖及其衍生物对重金属离子的吸附[J].化学进展,2012,24(11):2212~2223.
[6] MUZZARELLI R A A.Chitin[M].Oxford:Pergamon Press,1977.
[7] YAO R S.Use of surfactants in enzymatic hydrolysis of rice straw and lactic acid production from rice straw by simutaneous saccharification and fermentation [J].Bioresources,2007,2(3):389~398.
[8] 刘倩,杨炳超,霍杰,等.质子化交联壳聚糖对氨基黑10B的吸附[J].材料科学与工程学报,2012,30(6):928~932.
[9] 石光,袁彦超,陈炳稔,等.交联壳聚糖的结构及其对不同金属离子的吸附性能[J].应用化学,2005,22(2):195~199.
[10] DIXON B G,DEANS J R.Uptake of Pb2+and Cu2+by novel biopolymers[J].Water Research,1992,26(4):469~472.
[11] 车小琼,孙庆申,赵凯.甲壳素和壳聚糖作为天然生物高分子材料的研究进展[J].高分子通报,2008,(2):45~49.
[12]袁余洲.影响红外光谱峰位变化的因素之一——氢键形成的新因素[J].玉林师专学报(自然科学),1997,18(3):45~48.
[13] CHRISSAFIS K,PARASKEVEOPOULOS K M,PAVLIDOU E.Thermal degradation mechanism of HDPE nanocomposites containing fumed silica nanoparticles[J].Thermochim Acta,2008,485(1):65~71.

