多级孔ZIF-67的合成及对染料分子甲基橙的吸附性能研究
韩文华 刘诗新 单振楠 陈金喜
(南京诺卫检测技术有限公司,江苏 南京 210007;*东南大学化学化工学院,江苏 南京 211189)
多级孔金属有机骨架(MOFs)材料是一类同时具有微孔和介孔或大孔的多孔结构的新型材料,该材料结构不但能够有效克服传质阻力,加速分子扩散,同时较小的微孔提供高比表面积、高孔隙率,从而达到催化、吸附等应用要求,因而多级孔MOF在气体吸附与分离[1~4]、催化[5~7]、传感器[8~10]、质子传导[9~11]和药物传递[12~14]等领域具有良好的工业应用前景。基于MOFs材料的吸附剂[15~17]在液相吸附/去除水[18, 19]或液体燃料[20, 21]等方面表现出良好的性能,目前已被广泛应用于去除一些有害的有机化合物如染料,苯类和双酚-A[22~26]。因此,将ZIF材料的较高稳定性与多级孔MOF独特的孔结构相结合所制备的吸附剂在吸附领域有良好的应用前景。
本文采用简单快速的微波合成法成功制备多级孔ZIF-67,通过XRD、SEM、TEM以及氮气吸附曲线等手段对其进行表征,并不断调节膨胀剂TMB与活性剂F123的摩尔比研究所合成的ZIF-67对染料分子甲基橙(MO)的吸附性能变化规律。
1实验部分
1.1 试剂与仪器
四水乙酸钴(分析纯,国药集团化学试剂有限公司);2-甲基咪唑(分析纯,Aladdin生化科技股份有限公司);P123(分析纯,Sigma-Aldrich贸易有限公司);1,3,5-三甲基苯(TMB)(分析纯,Sigma-Aldrich贸易有限公司),甲基橙(分析纯,Aladdin生化科技股份有限公司)。微波快速反应系统(WF-4000,上海屹尧仪器科技发展有限公司);X射线粉末衍射仪(Ultima IV,Rigaku公司);扫描电子显微镜(S-4800,Hitachi);透射电子显微镜(JEM-2100,日本电子株式会社);吸附分析仪(Surfer,Thermo Fisher Scientific);紫外-可见分光光度计(UV-2600,岛津有限公司)。
1.2 实验过程
1.2.1ZIF-67的制备
称取一定量P123溶解在20.0 mL去离子水中,搅拌30 min后,将TMB加入上述溶液中,充分混合后依次加入Co(OAc)2·4H2O 0.249 g (1 mmol)和2-甲基咪唑0.492 g (6 mmol),搅拌后将溶液转入60 mL的聚四氟乙烯反应釜中,采用微波反应容器加热,在120 ℃下反应30 min,自然冷却至室温后,用去离子水和乙醇分别洗涤3次,于60 ℃烘箱中干燥12 h得到紫色粉末状产物。
为探究膨胀剂TMB与活性剂P123的不同摩尔比对甲基橙吸附性能的影响,分别制备TMB/P123的摩尔比为0、2、10时的多级孔ZIF-67。
1.2.2ZIF-67对染料分子甲基橙吸附性能测试
样品在90 ℃下真空处理12 h后将15mg ZIF-67样品加入到15 mL,24 mg·L-1的MO水溶液中,超声分散后室温避光搅拌6 h。最后,将所剩的染料溶液离心分离,取上清液,利用紫外可见光分光光度计(UV-vis)在波长为463 nm处进行吸附测试,研究分析含有不同TMB/P123摩尔比的多级孔ZIF-67对染料分子甲基橙的吸附性能,并计算样品对染料分子的吸附量以及吸附率。
2结果与讨论
2.1 ZIF-67的结构表征
2.1.1XRD分析
图1是不同TMB/P123摩尔比时所得产物的PXRD图。从图中可以看出所合成的ZIF-67样品均与ZIF-67单晶模拟图谱的衍射峰相吻合。然而随着TMB膨胀剂的量逐渐增加,7.4°(对应于0 1 1晶面)处的峰强度在逐渐降低,12.7°(对应于1 1 2晶面)对应的峰强度在逐渐增大,说明在ZIF-67晶体生长过程中,TMB量的增大不利于0 1 1晶面的生长,而有利于1 1 2晶面的生长。
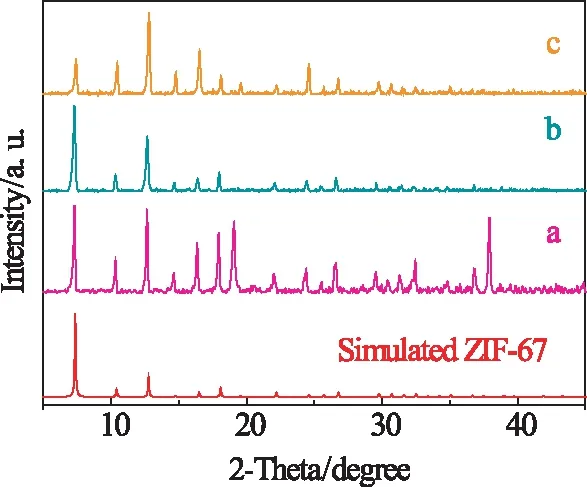
图1 微波反应下不同TMB/P123物质的量比得到产物的PXRD图,(a) 0, (b) 2, (c) 10Fig 1 PXRD patterns of ZIF-67 samplesprepared by microwave irradiation with differentTMB/P123 molar ratios:(a) 0, (b) 2, (c) 10
2.1.2SEM分析
图2是不同TMB/P123摩尔比条件下得到产物的SEM图。由图中可以看出,当无TMB添加时,粒子尺寸约为50~60 nm,粒子之间具有团聚现象。当添加少量TMB即TMB/P123物质的量比为2时,得到的样品形貌较为均一,粒子尺寸约为80~100 nm。当TMB/P123物质的量比进一步增加为10时,粒子尺寸变化不明显,可以看到粒子间堆积形成的介孔。说明TMB的添加对形成更加明显的介孔或大孔结构起到了重要的作用。
2.1.3TEM分析
图3是不同TMB/P123物质的量比条件下得到的产物的TEM图。从图中可以进一步看出随着TMB的添加,形成了平均直径约为100 nm的ZIF-67球状纳米晶。在这些泡沫状粒子间堆积形成不规则的介孔结果,进一步说明TMB是一个合适的胶束膨胀剂。
2.1.4氮气吸附分析
图4是不同TMB/P123物质的量比得到的多级孔ZIF-67在77 K时氮气吸附图,插图是其对应的孔径分布曲线。由图可以看出,当TMB/P123物质的量比为2时,在相对压强(P/P0<0.01)较低时产物对N2的吸附量迅速上升,属于Type-I型吸附,表明得到的产物具有微孔材料的气体吸附特征。而在相对压强较高(P/P0>0.8)时观察到伴有二次吸附的滞后回线,这是由颗粒之间相互堆积产生的介孔所引起的。然而,没有TMB时只能看到微小的滞后回线。当进一步增加TMB的量使TMB/P123物质的量比等于10时,相对压强较低区域对N2的吸附量增加缓慢表明产物的微孔含量有所降低,而且产物对N2的吸附量也明显降低。从插图中可以看出,无TMB添加时,介孔孔径约为17 nm,随着TMB/P123物质的量比的增加,介孔的孔径尺寸也在增加。当TMB/P123物质的量比等于2时,孔径分布由双峰变成了三峰,具有最大孔径的大孔尺寸达到80 nm左右,而当TMB/P123物质的量比为10时,大孔孔径增加到了110 nm左右,增大了的孔径和更加宽泛的孔径分布进一步说明了TMB对形成多级孔结构的重要作用。

图2 微波反应下不同TMB/P123物质的量比得到产物的SEM图,(a) 0, (b) 2, (c)10Fig 2 SEM patterns of ZIF-67 samples prepared by microwave irradiation withdifferent TMB/P123 molar ratios: (a) 0, (b) 2, (c) 10

图3 微波反应下不同TMB/P123物质的量比得到产物的TEM图,(a) 0, (b) 2, (c) 10Fig 3 TEM patterns of ZIF-67 samples prepared by microwave irradiation withdifferent TMB/P123 molar ratios: (a) 0, (b) 2, (c) 10
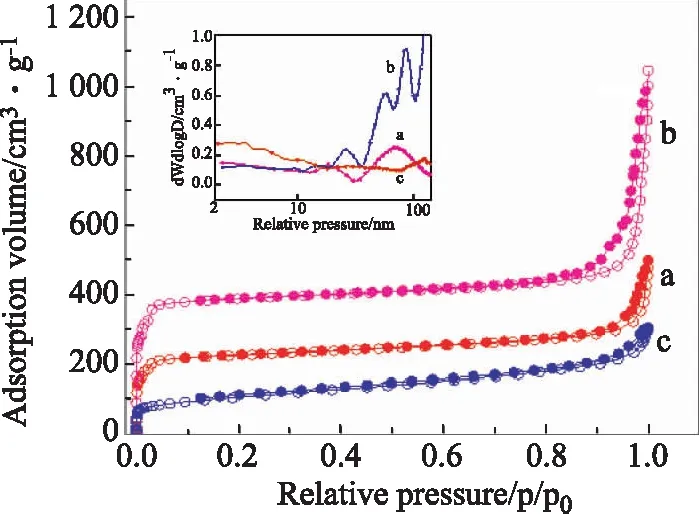
图4 77 K下不同TMB/P123物质的量比得到的多级孔ZIF-67氮气吸附图
2.2 ZIF-67吸附甲基橙性能研究
图5是不同TMB/P123物质的量比合成的多级孔ZIF-67对甲基橙的吸附测得的紫外吸收峰。从图中可以看出,随着TMB量的增加,在463 nm处的最大吸光度值呈现持续下降的趋势,说明多级孔ZIF-67对甲基橙有一定的吸附作用并且TMB能够更好地促进多级孔ZIF-67对甲基橙的吸附。这可能是因为一方面甲基橙分子较小,更容易进入多级孔ZIF-67孔道,另一方面,TMB含量的增加使ZIF-67的孔径大小和孔径分布发生改变,促进了对染料分子甲基橙的吸附。当TMB/P123物质的量比为10时,通过式(1)(2)可计算得合成的多级孔ZIF-67对甲基橙的吸附量q达14.3 mg·g-1,吸附率η约为60%。
(1)
(2)
式中,q:吸附量(mg·g-1),C0:初始浓度(mg·L-1),Ce:吸附后溶液浓度(mg·L-1),V:反应溶液体积(L),m:吸附剂的用量(g)。
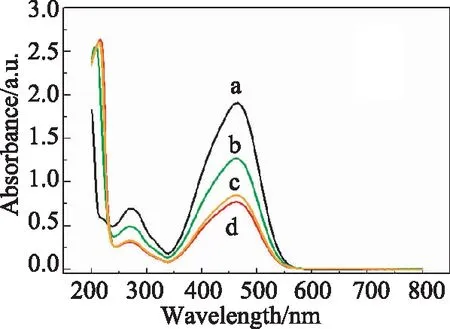
图5 微波条件下不同TMB/P123物质的量比合成的多级孔ZIF-67对甲基橙的吸附测得的紫外吸收峰a: 24 mg·L-1甲基橙溶液;b-d:TMB/P123物质的量比分别为 0、2和10Fig 5 The UV absorption peaks of the adsorptionof methyl orange by hierarchical ZIF-67 synthesizedunder microwaveconditions with different TMB/ P123 molar ratios. a: methyl orange solution of24 mg·L-1; b-d: the molar ratios ofTMB/P123 of 0, 2 and 10
3结 论
采用微波法合成多级孔ZIF-67,方法简单、快速,所得到的ZIF-67形貌规整、尺寸均一,在应用到吸附染料分子甲基橙的实验中表现出良好的吸附性能。TMB的添加有效增大了多级孔ZIF-67的介孔孔径,降低了大分子的扩散传输阻力,从而提高对染料分子的吸附性能,使其吸附率高达60%左右。当TMB/P123物质的量比为10时,多级孔ZIF-67对甲基橙的吸附量可达14.3 mg·g-1。因此,通过此方法制备的多级孔ZIF-67为染料吸附提供了新的可能,具有良好的工业应用前景。
[1] Inagaki F, Matsumoto C, Iwata T., et al. CO2-Selective Absorbents in Air: Reverse Lipid Bilayer Structure Forming Neutral Carbamic Acid in Water without Hydration[J]. J Am Chem Soc, 2017, 139(13): 4 639~4 642.
[2] Jian Y, Yin H M, Chang F Y., et al. Facile synthesis of highly permeable CAU-1 tubular membranes for separation of CO2/N2mixtures[J]. J. Membrane Sci., 2017, 522: 140~150.
[3] Leea S J, Yoona T U, Kim A R., et al. Adsorptive separation of xenon/krypton mixtures using a zirconium-based metal-organic framework with high hydrothermal and radioactive stabilities[J]. J Hazard Mater, 2016, 320:153~520.
[4] Wee L H H, Meledina M, Turner S., et al. 1D-2D-3D Transformation Synthesis of Hierarchical Metal-Organic Framework Adsorbent for Multicomponent Alkane Separation[J]. J Am Chem Soc, 2017, 139: 819~828.
[5] Gascon J, Corma A, Kapteijn F, Xamena F. Metal Organic Framework Catalysis: Quo vadis[J]. ACS Catal, 2014, 4(2): 361~378.
[6] Tao Z, Wang T, Wang X J, Zheng J, Li X. MOF-Derived Noble Metal Free Catalysts for Electrochemical Water Splitting[J]. ACS Appl Mater Interfaces, 2016, 8(51): 35 390~35 397
[7] Yang D, Odoh, S O, Borycz J., et al. Tuning Zr-6 Metal-Organic Framework (MOF) Nodes as Catalyst Supports: Site Densities and Electron-Donor Properties Influence Molecular Iridium Complexes as Ethylene Conversion Catalysts[J]. ACS Catal, 2016, 6(1): 235~247.
[8] Qi A W, Chen Y. Charge-transfer-based terbium MOF nanoparticles as fluorescent pH sensor for extreme acidity[J]. Biosens Bioelectron, 2016, 87: 236~241.
[9] Du P Y, Liao S Y, Gu W, Liu X. A multifunctional chemical sensor based on a three-dimensional lanthanide metal-organic framework[J]. J Solid State Chem, 2016, 244: 31~34.
[10] Campbell M G, Sheberla D, Liu S F. Cu3(hexaiminotriphenylene)2: An Electrically Conductive 2D Metal-Organic Framework for Chemiresistive Sensing[J]. Angew Chem Int Ed, 2015, 54(14): 4 349~4 352.
[11] Dong X Y, Wang R, Wang J Z., et al. Highly selective Fe3+sensing and proton conduction in a water-stable sulfonate-carboxylate Tb-organic-framework[J]. J Mater Chem A, 2015, 3(2): 641~647.
[12] Li C, Sun M, Xu L., et al. The first heteropoly blue-embedded metal-organic framework: crystal structure, magnetic property and proton conductivity[J]. CrystEngComm, 2016, 18(4): 596~600.
[13] Fujie K, Kitagawa H. Ionic liquid transported into metal-organic frameworks[J]. Coord Chem Rev, 2016, 307: 382~390.
[14] Orellana T C, Baxter E F, Tian T., et al. Amorphous metal-organic frameworks for drug delivery[J]. Chem Commun, 2015, 51(73): 13 878~13 881.
[15] Zheng H, Zhang Y, Liu L., et al. One-pot Synthesis of Metal-Organic Frameworks with Encapsulated Target Molecules and Their Applications for Controlled Drug Delivery.[J]. J Am Chem Soc, 2015, 138(3):962.
[16] Bag P P, Wang D, Chen Z., et al. Outstanding drug loading capacity by water stable microporous MOF: a potential drug carrier[J]. Chem Commun, 2016, 52(18): 3 669~3 672.
[17] Jhung S H, Khan N A, Hasan Z. Analogous porous metal-organic frameworks: synthesis, stability and application in adsorption[J]. 2012, CrystEngComm, 14(21): 7 099~7 109.
[18] Khan N A, Hasan Z, Jhung S H. Adsorptive removal of hazardous materials using metal-organic frameworks (MOFs): a review[J]. J Hazard Mater, 2013, 244: 444~456.
[19] Khan N A, Hasan Z, Jhung S H. Adsorption and removal of sulfur or nitrogen-containing compounds with metal-organic frameworks(MOFs)[J]. Adv Porous Mater, 2013, 1(1): 91~102.
[20] Hasan Z, Choi E J, Jhung S H. Adsorption of naproxen and clofibric acid over a metal-organic framework MIL-101 functionalized with acidic and basic groups[J]. Chem Eng J, 2013, 219: 537~544.
[21] Haque E, Jun J W, Jhung S H. Adsorptive removal of methyl orange and methy-lene blue from aqueous solution with a metal-organic framework material, iron terephthalate (MOF-235)[J]. J Hazard Mater, 2011, 185(1): 507~511.
[22] Khan N A, Hasan Z, Jhung S H. Ionic liquids supported on metal-organic frameworks: remarkable adsorbents for adsorptive desulfurization[J]. Chem Eur J, 2014, 20(2): 376~380.
[23] Ahmed I, Khan N A, Jhung S H. Graphite oxide/metal-organic framework(MIL-101): remarkable performance in the adsorptive denitrogenation of model fuels[J]. Inorg Chem, 2013, 52(24): 14 155~14 161.
[24] Jung B K, Jun J W, Hasan Z, Jhung S H. Adsorptive removal of p-arsanilic acid from water using mesoporous zeolitic imidazolate framework-8[J]. Chem Eng J, 2015, 267: 9~15.
[25] Bhattacharjee S, Chen C, Ahn W S. Chromium terephthalate metal-organic framework MIL-101: synthesis, functionalization and applications for adsorption and catalysis[J]. RSC Adv, 2014, 4(94): 52 500~52 525.
[26] Zhou M, Wu Y, Qiao J., et al. The removal of bisphenol A from aqueous solutions by MIL-53 (Al) and mesostructured MIL-53(Al)[J]. J Colloid Inter Sci, 2013, 405: 157~163.

