t-PA负向调控p75NRT改变血管外膜自主神经重构参与动脉粥样硬化*
张劲松,杜荣增,王中群,李光宇,张新茹,张梓桑
(江苏大学附属江滨医院心内科, 江苏镇江 212001)
论著·基础研究
t-PA负向调控p75NRT改变血管外膜自主神经重构参与动脉粥样硬化*
张劲松,杜荣增△,王中群,李光宇,张新茹,张梓桑
(江苏大学附属江滨医院心内科, 江苏镇江 212001)
目的研究组织型纤溶酶原激活物(t-PA)对p75NTR、炎性反应、免疫调节、氧化应激的作用,以及对内膜增生的影响。方法对糖尿病兔给予颈动脉外膜剥除建立动物模型,然后进行血管损伤处理,同时给予t-PA控释微球后,免疫荧光染色分别观察对照组和处理组神经重构的变化情况,同时检测给予t-PA控释微球对乙酰胆碱和去甲肾上腺素释放的影响。RT-PCR检测t-PA释控微球对局部血管组织的炎症、免疫反应和氧化应激的影响。采用交感神经元与平滑肌细胞共培养,之后给予乙二醛进行处理作为动脉粥样硬化细胞模型,以t-PA处理组作为干预组,观察t-PA对胆碱能神经元数目,与平滑肌细胞之间的突触连接数目、乙酰胆碱分泌的影响。RT-PCR检测t-PA-MMP-p75NTR-NF-κB信号通路的改变。结果给予t-PA控释微球能明显增加胆碱能神经元数目和神经纤维(P<0.05)而不影响去甲肾上腺素能神经元数目和神经纤维(P>0.05),并且导致乙酰胆碱释放增多(P<0.05),最终抑制内膜增生(P<0.05)。离体交感神经元与平滑肌细胞共培养,之后给予乙二醛处理作为动脉粥样硬化细胞模型中t-PA促进胆碱能神经元增殖、增加乙酰胆碱的分泌和促进胆碱能神经纤维的数目增多(P<0.05)。RT-PCR检测发现t-PA能够激活MMPs,抑制p75NTR-NF-κB信号通路(P<0.05)。结论t-PA激活MMPs反馈抑制p75NTR-NF-κB信号通路增加血管外膜自主神经重构延缓动脉粥样硬化疾病的发生发展。
自主神经重构;纤溶酶原激活剂;p75NTR;动脉粥样硬化;血管外膜
血管外膜自主神经重构障碍可导致血管的结构、功能及机体的炎性反应和代谢状态紊乱,参与动脉粥样硬化疾病的发生发展[1-3]。血管外膜自主神经主要由分布在动脉内膜/外膜交界区域的胆碱能神经纤维,和位于动脉外膜区域的去甲肾上腺素能神经纤维构成[4-5]。组织型纤溶酶原激活物(tissue plasminogen activator,t-PA)是除了尿激酶以外主要已知的可有效降解动脉壁细胞外基质的神经系统产物。p75NTR作为神经元的负向调控受体即凋亡相关受体,其对中枢胆碱能神经元具有选择性抑制作用,基因敲除p75NTR可增加中枢神经系统的胆碱能神经元数目、调节细胞大小并抑制细胞的凋亡,其表现类似神经重构,但在外周神经中是否同样存在类似作用还缺乏研究。在乳腺转移肿瘤细胞中,p75NTR负向调节基质金属蛋白酶(MMPs)和组织金属蛋白酶抑制剂11(TIMP11),这一调控通路提示神经营养因子系统与血管外膜的局部纤溶系统可能存在某种相关性,如t-PA可能通过激活MMP反馈抑制p75NTR,随后有下游的核因子κB(NF-κB)和JNK介导信号传导,进而影响神经细胞轴突的延伸及外周神经的神经重构等,有必要进行深入研究。本实验主要研究t-PA通过激活MMP反馈抑制p75NTR,促进局部胆碱能神经纤维再生,抑制局部血管神经重构,使局部血管的交感/副交感神经比例倾向于副交感,使过多的胆碱能神经纤维末梢释放的乙酰胆碱等物质发挥抗炎、免疫调节、抗氧化应激作用,最终抑制内膜增生。本实验不但有利于进一步阐明动脉粥样硬化新的调控机制,丰富动脉粥样硬化发生发展的新理论,而且将会为研制消退动脉粥样硬化斑块的新型药物打下基础。
1 材料与方法
1.1主要材料 t-PA购自美国R&D公司;雌性新西兰兔购自济南金丰实验动物有限公司;高糖、高脂饲料(10%猪油、37%白蔗糖混合53%基础饲料)由扬州大学比较医学中心提供;苏木素购自中国医药集团上海化学试剂公司;伊红购自上海试剂三厂;重组人神经生长因子(nerve growth factor,NGF)购自美国R&D公司;兔乙酰胆碱和去甲肾上腺素ELISA试剂盒购自上海泸鼎生物科技有限公司;胆碱转移酶和酪氨酸羟化酶一抗购自上海硕博生物有限公司; 反转录PCR(RT-PCR)试剂盒购自碧云天生物科技有限公司;引物由上海生工生物科技有限公司合成;荧光倒置光学显微镜(日本Olympus公司);体视显微镜(中国江南仪器有限公司);显微手术器械(上海手术器械厂);病理包埋机(中国派斯杰公司);病理石蜡切片机(德国Leica公司);-80 ℃低温冰箱(日本Sanyo公司);RT-PCR仪(美国ABI公司)。
1.2糖尿病兔颈动脉外膜剥除血管损伤模型的建立 60只6个月体质量均在3.5 kg左右的雌性新西兰兔给予高糖、高脂饲料单笼喂养诱发糖尿病,通过代谢指标(血糖、血脂、糖化血红蛋白等)筛选出成功建立模型的42只糖尿病兔。暴露兔的颈动脉,采用胶原酶结合物理方法剥除外膜制成血管损伤动物模型备用,在手术后放置t-PA控释微球在剥离外膜血管与未剥离的交界处做为处理组,对照组在相同位置放入介质微球,在洁净环境下继续高脂喂养14 d后处死动物并取材。
1.3免疫荧光染色和苏木精-伊红(HE)染色 戊巴比妥钠腹腔注射(50 mg/kg)麻醉后,4%多聚甲醛灌注新西兰兔,在显微镜下分离血管放入4%多聚甲醛固定, 4 ℃保存。取下的标本石蜡包埋前测量动脉瘤的颈宽、瘤高。之后10%多聚甲醛固定,梯度乙醇脱水,常规石蜡包埋切片,HE染色和光镜检查。另一部分标本进行荧光染色,OTC包埋动脉样品常规5 μm切片,切片脱蜡,水化,3%甲醇-过氧化氢孵育10 min,PBS 洗 10 min×3次,0.1 mol/L枸橼酸缓冲液(pH为6.0)抗原修复98 ℃持续20 min,自然冷却至室温, PBS常规漂洗,用Triton-X100 BSA封闭37 ℃ 2 h,加一抗分别使用胆碱转移酶(choline acetyltransferase,ChAT)抗体标记胆碱能神经纤维、络氨酸羟化酶(tyrosine hydroxylase,TH)抗体标记去甲肾上腺素能神经纤维,4 ℃过夜,第2天PBS常规漂洗,荧光二抗37 ℃孵育2 h,PBS常规漂洗甘油封片。显微镜观察拍照。HE染色图片和免疫荧光图片采用莱卡RX250/QWN进行图像采集,内膜的增生以新生内膜与中膜的比例(I/M)评价新生内膜厚度。IPP软件用于细胞数目的统计。
1.4交感神经元与平滑肌细胞共培养 平滑肌细胞和交感神经元的分离:取新西兰兔血管组织,充分剪碎后用0.25%的胰酶消化的方法获得单细胞悬液,在含有15%胎牛血清的DMEM培养液中差速贴壁1 h,取上清离心,以去除成纤维细胞。收集未贴壁细胞,其中主要为平滑肌细胞。找到交感神经干(兔子的迷走神经和交感神经是分开行走的,不像反刍动物在颈部是迷走神经、交感神经干向前行走的),然后顺交感干向前至颅底腹侧,找到颈前神经节,用眼科剪准确地夹住颈前神经节的前端,取出颈前神经节,用注射器和小滤器过滤到一个15 mL无菌的离心管中,加上分离神经节组织。置培养箱中用0.25%的胰酶消化液消化18 min,然后加10 mL含10%胎牛血清的DMEM培养液于组织中作用1~2 min,终止消化。离心后,吸除上清中的细胞碎片,将沉淀用含5% FBS的DMEM重悬,然后将分离的新生兔平滑肌(浓度为1.0×106个mL)与分离的平滑肌细胞细胞(浓度为2×105个mL)混合,加入预先包被的12孔板中,加2 mL含胎牛血清的培养基,50 ng/mL NGF,5% CO2、37 ℃培养箱中,进行共培养,第2天换液1次[6-7]。
1.5ELISA检测乙酰胆碱和去甲肾上腺素 根据乙酰胆碱和去甲肾上腺素ELISA试剂盒说明书,检测剥离外膜段血管内膜的乙酰胆碱和去甲肾上腺素的水平。
1.6RT-PCR 分别随机抽取8只处理组新西兰兔,用Trizol沉淀法提取总 RNA,按照反转录试剂盒的操作步骤进行反转录反应。所得 cDNA用于后续NF-κB、MMP-2、MMP-9、p75NTR的实时荧光定量 PCR反应。将GAPDH作为内参基因。同时将 PCR产物进行测序以及做熔解曲线,以保证以上 PCR反应产物良好的特异性。计算△Ct值用来比较给药前后mRNA的表达变化。每个PCR反应都设置3个复孔。引物序列如下,NF-κB正向引物:5′-GGT GCC TTT TGC GAG CAG TAT C-3′;反向引物:5′-CGT ATG GAC CAG AAT GTG ACG G-3′。MMP-2正向引物:5′-CTG GCT GTG CAA TAC CTG AA-3′;反向引物:5′-CAG GGT CCA TAG CTC ATC GT-3′。MMP-9正向引物:5′-ATC TTC CTG GGC AAG CAG TA-3′;反向引物:5′-CTG GCA CCG ATG AAT GAT CT-3′。p75NTR正向引物:5′-AGG CAC CAC CGA CAA CCT C-3′;反向引物:5′-CAC AAG GCC CAC AAC CAC A-3′。GAAPDH正向引物:5′-ACC ACC ATG GAG AAG GCT GG-3′;反向引物:5′-CTC AGT GTA GCC CAG GAT GC-3′。
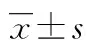
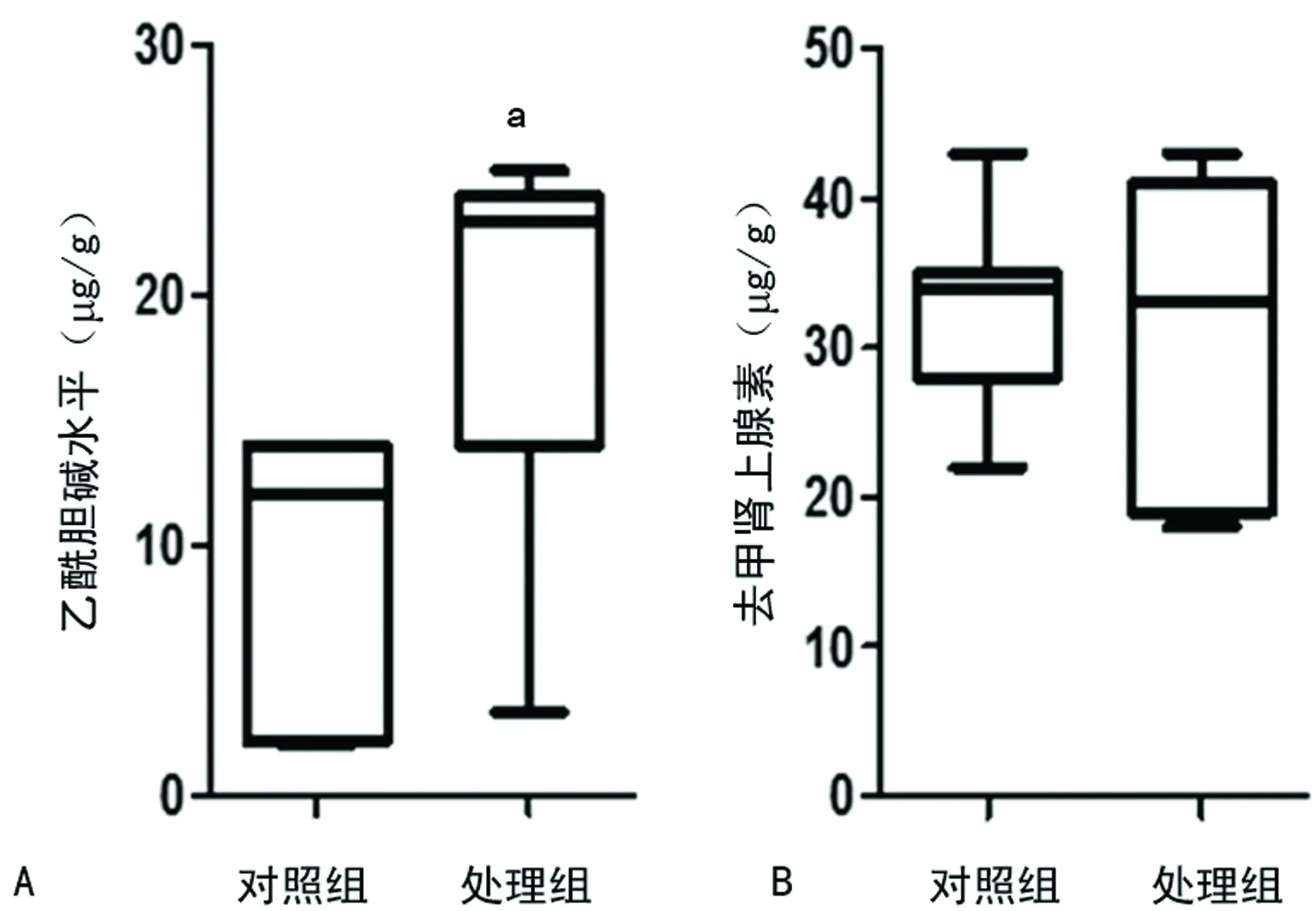
2 结 果
2.1t-PA控释微球后明显增加胆碱能神经元数目而不影响去甲肾上腺素能神经元 糖尿病兔颈动脉外膜剥除血管损伤模型建立后给予t-PA控释微球,笔者通过对临近剥离外膜的一段仍完整的血管进行免疫荧光检测胆碱能神经元数目和去甲肾上腺素能神经元。结果发现处理组胆碱能神经元的数目较对照组明显增加(P<0.05),但去甲肾上腺素能神经元未受影响(P>0.05),见图1。
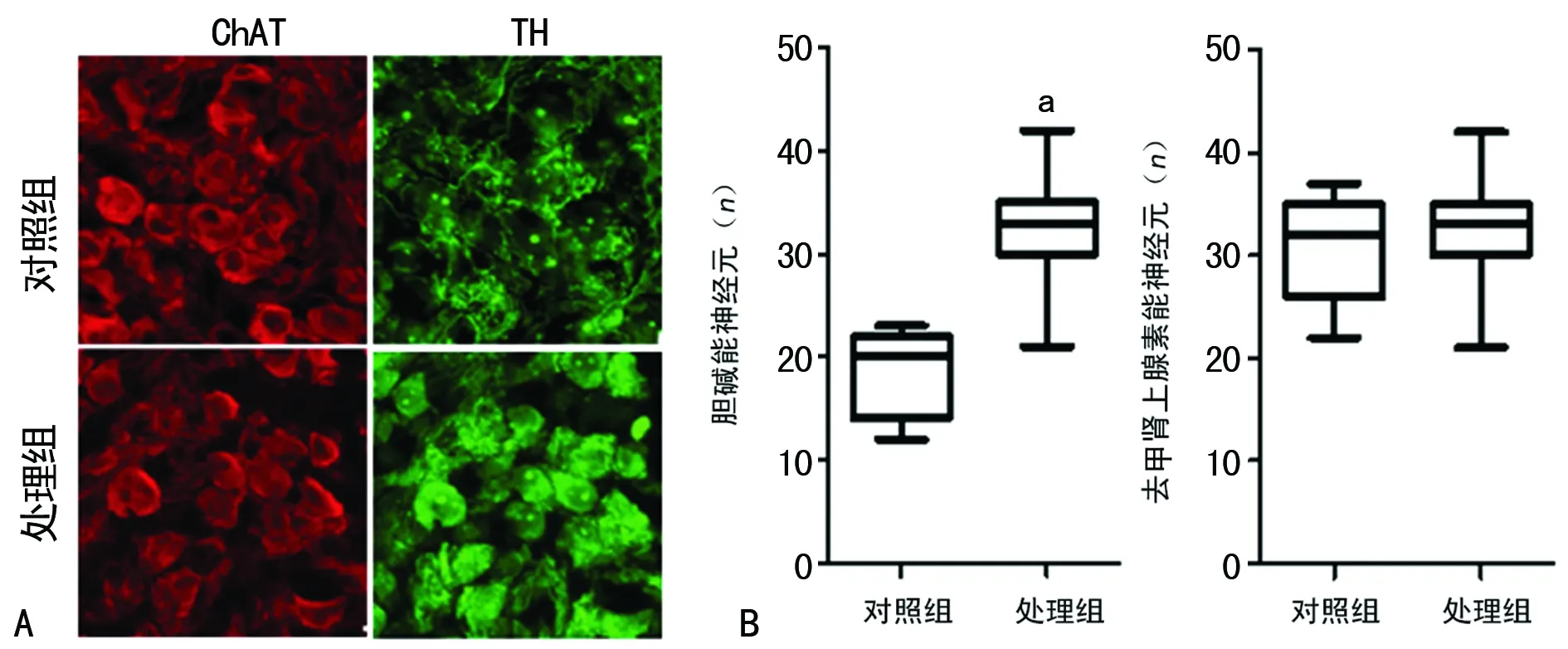
2.2t-PA控释微球后明显增加胆碱能神经纤维而不影响去甲肾上腺素能神经纤维 通过观察剥除血管外膜段的单纯内膜胆碱能神经纤维和外膜及内膜处去甲肾上腺素能神经纤维的变化情况,笔者发现与神经元数目结果一致,处理组胆碱能神经纤维较对照组明显增加(P<0.05);而去甲肾上腺素能神经纤维未受影响(P>0.05),见图2。
A:免疫荧光图;B:荧光定量分析图;a:P<0.05,与对照组比较
图1 t-PA对动脉粥样硬化模型兔交感神经中胆碱能神经元及去甲肾上腺素能神经元的影响
A:组织免疫荧光图;B:荧光定量分析图;a:P<0.05,对照组比较
图2 t-PA控释微球对胆碱能神经纤维及去甲
肾上腺素能神经纤维的影响
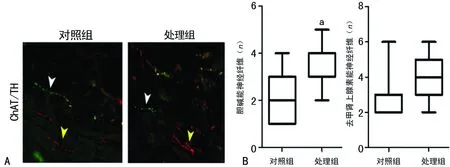
A:乙酰胆碱;B:去甲肾上腺素;a:P<0.05,与对照组比较
图3两组大鼠乙酰胆碱和去甲肾上腺素水平比较
2.3t-PA控释微球后明显增加胆碱能神经纤维末梢释放的乙酰胆碱而不影响去甲肾上腺素水平不变 通过ELISA检测剥除血管外膜段的单纯内膜乙酰胆碱、去甲肾上腺素水平发现处理组胆碱能神经纤维末梢释放的乙酰胆碱较对照组明显增加(P<0.05),去甲肾上腺素水平不变,见图3。
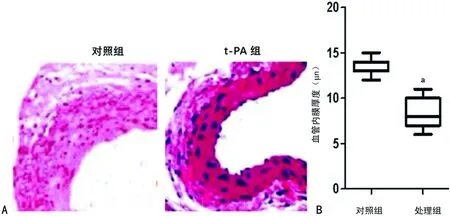
A:HE染色图;B:HE染色分析图;a:P<0.05,与对照组比较
图4 t-PA控释微球对血管内膜的影响
2.4t-PA控释微球后明显降低血管内膜的增生 HE染色发现t-PA控释微球明显降低血管内膜的增生(P<0.05),见图4。
2.5离体t-PA促进胆碱能神经元突触形成,增加乙酰胆碱的分泌和促进胆碱能神经纤维的数目 笔者通过VAChT染色检测胆碱能神经元突触形成、胆碱能神经纤维的数目发现,在离体细胞中t-PA促进胆碱能神经元突触形成,增加乙酰胆碱的分泌和促进胆碱能神经纤维的数目增加(均P<0.05),见图5。
2.6t-PA能够激活MMPs反馈抑制p75NTR-NF-κB信号通路 为了进一步探讨t-PA影响胆碱能神经元的机制,笔者用RT-PCR检测MMP-2,MMP-9,p75NTR和NF-κB的表达的情况。发现在离体培养的交感神经元中t-PA能够增加MMP-2和MMP-9的表达,抑制p75NTR的表达(均P<0.05),抑制NF-κB的表达见图6。
A:胆碱能神经元突触;B:乙醇胆碱;C:胆碱能神经纤维;a:P<0.05,与对照组比较
图5两组大鼠胆碱能神经元突触、乙醇胆碱、胆碱能神经纤维比较
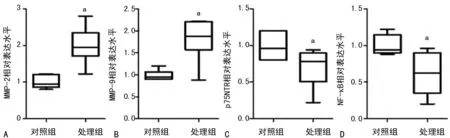
A:MMP-2;B:MMP-9;C:p75NTR;D:NF-κB;a:P<0.05,与对照组比较
图6两组大鼠MMP-2、MMP-9、p75NTR、NF-κB水平比较
3 讨 论
血管外膜自主神经重构障碍可导致血管的结构、功能及机体的炎性反应和代谢紊乱,参与动脉粥样硬化疾病的发生发展[1-3]。目前的基础研究表明,除血管内膜损伤可导致动脉粥样硬化病变之外,外膜病变也可导致动脉粥样硬化而且其起病时间还早于内膜病变。研究提示若早期对外膜实施一定的干预措施可能延缓或中止AS病变的进程,因此近年来动脉粥样硬化疾病的基础研究重点已由血管内膜和中层转向外膜[8]。血管周围分布有大量的神经纤维,这些神经纤维除了含有传统的神经递质去甲肾上腺素和乙酰胆碱之外,还含有神经营养因子(如BDNF、NGF、NT-3和CDNF等)及t-PA等。神经末梢中的t-PA与外膜其他细胞分泌的PAI-1构成局部纤溶系统,t-PA是除了尿激酶以外已知主要的可有效降解动脉壁细胞外基质的神经系统产物。在移植的静脉血管周围通过控释给予t-PA(血管周围放置微球,控释t-PA)在细胞外基质产生趋化性梯度能够引导血管平滑肌细胞从血管腔中迁移出来,Okdama等[9]的研究发现术后7 d t-PA处理组的血管平滑肌细胞大多分布于血管外周,其内膜/中层比值明显降低,并抑制新生内膜的增生。但t-PA抑制新生内膜增生和防止术后再狭窄的作用,目前仍有争论。Kodama等[10]通过反转录病毒载体将t-PA和一氧化氮合酶(eNOS)基因分别转染平滑肌细胞,再将细胞种植至聚四氟乙烯编织的移植物中,随后将血管移植物置入兔的主动脉内,在术后30 d和100 d后分别检查移植物内的血栓形成和内膜增生情况,发现经过基因工程修饰的表达t-PA的血管平滑肌(SMC)尽管有助于抑制移植物腔内血栓的形成,但却导致内膜显著增生,而仅有在种植细胞内表达eNOS才可抑制新生内膜的增生。本研究发现给予t-PA控释微球后明显增加胆碱能神经纤维而不影响去甲肾上腺素能神经纤维,乙酰胆碱释放增多,炎性反应被抑制,最终抑制内膜增生。离体交感神经元与平滑肌细胞共培养,之后给予乙二醛处理体外培养的交感神经元作为动脉粥样硬化细胞模型中,t-PA促进胆碱能神经元增殖、增加乙酰胆碱的分泌和促进胆碱能神经纤维的数目,而不影响去甲肾上腺素能神经元。
神经营养因子家族中主要有BDNF、NGF、络氨酸激酶受体(tyrosine kinase receptor,Trk)和p75NTR,在动脉粥样硬化病变中BDNF和p75NTR高表达,而NGF低表达,且其表达程度与病变的严重程度显著相关。 NGF、BDNF、正向调控的Trk及负向调控的p75NTR构成局部神经营养因子系统。p75NTR作为神经元的负向调控受体即凋亡相关受体,其对中枢胆碱能神经元具有选择性抑制作用,基因敲除p75NTR可增加中枢神经系统的胆碱能神经元数目、细胞大小并抑制细胞的凋亡,其表现类似神经重构,但在外周神经中是否同样存在还缺乏研究[11]。t-PA可能通过激活MMPs反馈抑制p75NTR,随后有下游的NF-κB和JNK介导信号传导, 在乳腺转移肿瘤细胞中,p75NTR负向调节MMP和TIMP11,这一调控通路提示神经营养因子系统与血管外膜的局部纤溶系统可能存在某种相关性[12-13]。本研究结果表明t-PA能够增加MMP-2和MMP-9的表达,抑制p75NTR的表达,抑制NF-κB的表达。综上所述t-PA通过激活MMPs反馈抑制p57NTR,促进局部胆碱能神经纤维再生,抑制局部血管神经重构,使局部血管的交感/副交感神经比例倾向于副交感,使过多的胆碱能神经纤维末梢释放的乙酰胆碱等物质发挥抗炎、免疫调节、抗氧化应激作用,最终抑制内膜增生,延缓动脉粥样硬化疾病的发生发展。
[1]Toda N,Nakanishi S,Tanabe S.Aldosterone affects blood flow and vascular tone regulated by endothelium-derived NO:therapeutic implications[J].Br J Pharmacol,2013,168(3):519-533.
[2]Philips JC,Marchand M,Scheen AJ.Haemodynamic changes during a squat test,pulsatile stress and indices of cardiovascular autonomic neuropathy in patients with long-duration type 1 diabetes[J].Diabetes Metab,2012,38(1):54-62.
[3]陈玮,梁春,刘星,等.血管外膜损伤致动脉粥样硬化斑块形成对兔局部交感神经功能的影响[J].第二军医大学学报,2010,31(6):585-589.
[4]Huang WC,Newby GB,Lewis AL,et al.Periadventitial human stem cell treatment reduces vein graft intimal thickening in pig vein-into-artery interposition grafts[J].J Surg Res,2013,183(1):33-39.
[5]Bloor J,Shukla N,Smith FC,et al.Folic acid administration reduces neointimal thickening,augments neo-vasa vasorum formation and reduces oxidative stress in saphenous vein grafts from pigs used as a model of diabetes[J].Diabetologia,2010,53(5):980-988.
[6]王静,郭志峰,郭立国,等.神经生长因子诱导后的交感神经元样PC12细胞与新生大鼠心肌细胞共培养的实验研究[J].生物医学工程研究,2008,27(3):205-209.
[7]陈文东.孕酮对原代培养仔兔交感节后神经元活性和Ca2+的影响[D].咸阳:西北农林科技大学,2014.
[8]Tepe G,Schmitmeier S,Speck U,et al.Advances on drug-coated balloons[J].J Cardiovasc Surg (Torino),2010,51(1):125-143.
[9]Ohnaka M,Marui A,Yamahara K,et al.Effect of microRNA-145 to prevent vein graft disease in rabbits by regulation of smooth muscle cell phenotype[J].J Thorac Cardiovasc Surg,2014,148(2):676-682.
[10]Kodama A,Itoh T,Komori K.Possible roles of 5-HT in vein graft failure due to intimal hyperplasia 5-HT,nitric oxide and vein graft[J].Surg Today,2014,44(2):213-218.
[11]Nyakas C,Granic I,Halmy LG,et al.The basal forebrain cholinergic system in aging and dementia.Rescuing cholinergic neurons from neurotoxic amyloid-beta42 with memantine[J].Behav Brain Res,2011,221(2):594-603.
[12]Strongin AY.Proteolytic and non-proteolytic roles of membrane type-1 matrix metalloproteinase in malignancy[J].Biochim Biophys Acta,2010,1803(1):133-141.
[13]Hafer-Macko CE,Ivey FM,Sorkin JD,et al.Microvascular tissue plasminogen activator is reduced in diabetic neuropathy[J].Neurology,2007,69(3):268-274.
t-PAnegativelyregulatingp75NRTforinvolvinginatherosclerosisbychangingreconstructionofvascularoutermembraneautonomicnerve*
ZhangJingsong,DuRongzeng△,WangZhongqun,LiGuangyu,ZhangXinru,ZhangZisang
(DepartmentofCardiology,AffiliatedJiangbinHospitalofJiangsuUniversity,Zhenjiang,Jiangsu212001,China)
ObjectiveTo study the effect of tissue plasminogen activator (t-PA) on p57NTR,inflammatory reaction,immune regulation and oxidative stress and its effect on intimal hyperplasia.MethodsThe vascular injury treatment was performed in the diabetic rabbit model with carotid arterial adventitia stripping,meanwhile t-PA controlled release microspheres were given,the nerve distribution in the local blood vessels was observed by immunohistochemical staining.The change of nerve remodeling in the control group and treatment group was observed,meanwhile the effect of giving t-PA controlled release microspheres on the release of acetylcholine and norepinephrine was detected.RT-PCR was used to detect local vascular tissue inflammation,immune effects and oxidative stress.The sympathetic neurons and smooth muscle cell co-culture was adopted,then giving glyoxal treatment as the atherosclerosis cell model.With the t-PA treatment group as the intervention group,the effect of t-PA on the number of cholinergic neuron,and synaptic connections between the smooth muscle cells and acetylcholine secretion was observed.The change of t-PA-MMP-p75NTR and NF-kappa B signaling pathway were detected by RT-PCR.ResultsThe vascular injury treatment was performed in the diabetic rabbit model with carotid arterial adventitia stripping,meanwhile t-PA controlled release microspheres were given,the nerve distribution in the local blood vessels was observed by immunohistochemical staining.The change of nerve remodeling in the control group and treatment group was observed,meanwhile the effect of giving t-PA controlled release microspheres on the release of acetylcholine and norepinephrine was detected.RT-PCR was used to detect local vascular tissue inflammation,immune effects and oxidative stress.The sympathetic neurons and smooth muscle cell co-culture was adopted,then giving glyoxal treatment as the atherosclerosis cell model.With the t-PA treatment group as the intervention group,the effect of t-PA on the number of cholinergic neuron,and synaptic connections between the smooth muscle cells and acetylcholine secretion was observed.The change of t-PA-MMP-p75NTR and NF-kappa B signaling pathway were detected by RT-PCR.Conclusiont-PA activates MMPs and feedback inhibits p75NTR-NF-kappa B signaling pathway to increase vascular adventitia autonomic nerve reconstruction and delay the occurrence and development of atherosclerosis disease.
] autonomic nerve reconstruction;plasminogen activators;p75NTR;atherosclerosis;vascular adventitia
10.3969/j.issn.1671-8348.2017.36.006
2015年江苏省镇江市课题(SH2015036)。
张劲松(1976-),硕士,主治医师,主要从事动脉粥样硬化研究。△
,E-mail:dubingchen001@foxmai1.com。
R541.4
A
1671-8348(2017)36-5055-04
2017-08-20
2017-09-28)

