二联与多西他赛三联疗法对低分化胃癌的治疗观察
闫 旭
二联与多西他赛三联疗法对低分化胃癌的治疗观察
闫 旭
目的对比二联与多西他赛三联疗法对低分化胃癌的治疗效果与安全性。方法择取80例低分化胃癌患者作为研究对象,根据患者对治疗的意愿分为2组,即二联组(30例)与三联组(50例)。二联组采用二联方案(奥沙利铂+替吉奥胶囊)治疗,三联组采用三联方案(多西他赛+顺铂+氟尿嘧啶)治疗。观察2组近期临床疗效、治疗前后外周血T淋巴细胞水平及治疗期间药物的毒副作用。结果三联组总有效率(32/50,64.00%)高于二联组(12/30,40.00%)(P<0.05)。治疗后三联组CD4+水平高于二联组(P<0.05)。三联组神经毒性(20/50,40.00%)、粒细胞减少(23/50,46.00%)、手足综合征(10/50,20.00%)的发生率高于二联组(5/30,16.67%)、(7/30,23.33%)、(2/30,6.67%)(P<0.05)。结论多西他赛+顺铂+氟尿嘧啶三联疗法对低分化胃癌的治疗效果优于奥沙利铂+替吉奥胶囊二联疗法,但三联疗法的不良反应发生率高于二联疗法,临床工作中应结合患者的病情进行灵活选择。
多西他赛;二联疗法;三联疗法;低分化胃癌
胃癌是消化系统常见的恶性肿瘤,临床根据肿瘤的恶性程度将其分为高分化胃癌、低分化胃癌及未分化胃癌,其中低分化胃癌具有较高的恶性度,且预后较差[1]。目前,低分化胃癌尚未有统一的治疗方案,临床多以二联与三联化疗方案治疗,但由于不同药物收效不同,这使得治疗的疗效与安全性参差不齐[2]。为了进一步完善低分化胃癌的临床治疗方案,并对其疗效及安全性进行分析,现将结果报告如下。
1 资料与方法
1.1 临床资料
择取2015年1月至2016年1月我院肿瘤科住院治疗的低分化胃癌患者80例作为研究对象。纳入标准:①经病理学证实为低分化胃癌,至少有1个可测量病灶;②预计生存期>3个月;③患者及其家属对研究内容知情,同意配合研究;④经医学伦理委员会批准。排除标准:①严重脏器功能障碍;②有化疗治疗史或存在化疗禁忌证;③凝血功能异常;④严重高血压,且经药物治疗无法有效控制血压水平。根据患者对治疗的意愿将其分为2组,即二联组(30例)与三联组(50例)。二联组:男性15例,女性15例;年龄45~76岁,平均(63.5±8.2)岁;原发病灶部位:胃底5例,胃窦5例,食管胃交界5例,胃腺癌15例。三联组:男性25例,女性25例;年龄45~75岁,平均(63.8±7.4)岁;原发病灶部位:胃底8例,胃窦8例,食管胃交界8例,胃腺癌26例。2组临床资料对比,差异无统计学意义(P>0.05)。
1.2 方法
2组治疗前1 d均注射地塞米松8 mg进行预处理,化疗期间定期监测血尿常规及肝肾功能,并适当给予5-HT3受体拮抗剂止吐。
1.2.1 二联组 采用二联方案(奥沙利铂+替吉奥胶囊):奥沙利铂,静脉给药2 h,130 mg/m2,1次/天;替吉奥胶囊,餐后口服,60 mg/m2,2次/天。1个疗程为21 d,持续治疗4个疗程。
1.2.2 三联组 采用三联方案(多西他赛+顺铂+氟尿嘧啶),且均以静脉方式给药:第1天,多西他赛,75 mg/m2,1次/天;第1~5天,顺铂,20 mg/m2,1次/天;第1~5天,氟尿嘧啶,500 mg/m2,1次/天。1个疗程为21 d,持续治疗4个疗程。
1.3 观察指标
2组患者均完成4个疗程的治疗。⑴参照实体瘤疗效标准(RECIST)[3]评估2组近期疗效,完全缓解(CR):持续4周以上病灶消失,无新病灶,肿瘤标志物正常;部分缓解(PR):持续4周以上病灶减少>30%;稳定(SD):病灶增大<20%或缩小≤30%;进展(PD):病灶增大≥20%。总有效率=(CR+PR)/总例数(二联30例,三联50例)×100%。⑵以ELASA法检验2组治疗前后免疫指标的变化,即外周血淋巴细胞CD8+、CD4+及CD3+水平。⑶参照美国国立癌症研究所于2006年制定的不良事件毒性评估标准(CTC3.0版)[4]对比2组患者用药期间的不良反应。
1.4 统计学处理
采用SPSS17.0软件处理,计数资料采用χ2检验,计量资料用t检验,P<0.05为差异有统计学意义。
2 结果
2.1 近期疗效对比
三联组总有效率(32/50,64.00%)高于二联组(12/30,40.00%),差异有统计学意义(χ2=4.364,P=0.023)。见表1。
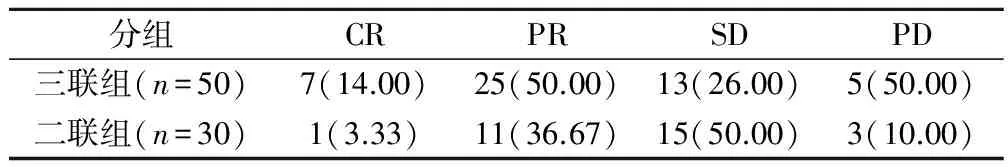
表1 近期疗效对比(例,%)
2.2 外周血T淋巴细胞变化
治疗前:2组CD8+、CD4+、CD3+差异无统计学意义(P>0.05);治疗后:三联组CD4+较二联组更高(P<0.05),在CD8+、CD3+比较无明显差异(P>0.05)。见表2。

表2 外周血T淋巴细胞变化
2.3 治疗期间的不良反应对比
2组治疗期间的不良反应对比,三联组神经毒性(20/50,40.00%)、粒细胞减少(23/50,46.00%)、手足综合征(10/50,20.00%)的发生率高于二联组(5/30,16.67%)、(7/30,23.33%)、(2/30,6.67%)(P<0.05)。见表3。

表3 不良反应对比(例,%)
3 讨论
胃癌是临床常见的消化系统恶性肿瘤,早期发病时无明显的症状表现,仅部分患者可见与溃疡病相似的临床症状,所以晚期患者相对较多。低分化胃癌具有较高的恶性程度,手术治疗往往无法取得较佳的临床疗效,现主要联合化学药物治疗。然而,目前缺少统一的胃癌治疗金标准,因此低分化胃癌的临床疗效参差不齐[5]。
多项研究指出,联合化疗治疗方案的临床疗效显著优于单一用药,且不良反应更低[6-7]。有学者对比了三药与两药方案在胃癌患者中的应用效果,结果发现以多西他赛为基础的三联用药疗效显著优于二联用药[8]。本文研究结果与此结果相符,2组近期疗效对比,三联组总有效率(32/50,64.00%)高于二联组(12/30,40.00%)(P<0.05)。结果可见,相较于二联疗法(奥沙利铂+替吉奥胶囊),多西他赛三联疗法(多西他赛+顺铂+氟尿嘧啶)治疗低分化胃癌的疗效更佳。
从免疫功能来看,治疗后三联组的CD4+水平较二联组更高(P<0.05)。CD4+属于辅助型T淋巴细胞,其检测水平对免疫功能判断具有十分重要的作用。本文研究结果中,三联组治疗后CD4+水平明显提高,且高于二联组,这也进一步说明三联疗法可以在一定程度上提高机体的免疫功能[9]。然而,药物毒副作用是三联疗法中争议较多的地方,许多资料对三联疗法的安全性存在质疑[10-11]。本文研究发现,虽然三联组患者均耐受了4个疗程的治疗,但三联组神经毒性(20/50,40.00%)、粒细胞减少(23/50,46.00%)、手足综合征(10/50,20.00%)的发生率高于二联组(5/30,16.67%)、(7/30,23.33%)、(2/30,6.67%)(P<0.05)。可见,相较于二联疗法,三联疗法在神经毒性、粒细胞减少及手足综合征方面的毒副作用较高,这与部分研究结果相符[12-13]。
总之,多西他赛+顺铂+氟尿嘧啶三联疗法对低分化胃癌的治疗效果优于奥沙利铂+替吉奥胶囊二联疗法,且可以从一定程度上提高免疫功能。然而,三联疗法的不良反应发生率高于二联疗法,2种治疗方案均存在利弊,临床工作中应结合患者的病情状况灵活选择,以便保证医疗质量。
[1] 乐 薇,项晓军,张 凌,等.改良FOLFIRI方案二线治疗老年晚期胃癌患者的临床观察〔J〕.实用肿瘤杂志,2013,28(2):200-203.
[2] 张孟国,张 孟.多西他赛联合顺铂替加氟治疗晚期胃癌的临床观察〔J〕.安徽医学,2013,34(5):593-595.
[3] 孙 燕,石远凯.临床肿瘤内科手册(第5版)〔M〕.北京:人民卫生出版社,2007:152-153.
[4] Li J,Qin S,Xu J,et al.Apatinib for chemotherapy-refractory advanced metastatic gastric cancer:results from a randomized,placebo-controlled,parallel-arm,phase Ⅱ trial〔J〕.J Clin Oncol,2013,31(26):3219-3225.
[5] Hallam MJ,Butt DA,Pacifico MD,et al.Exploiting the perforator concept to minimise donor site morbidity in harvesting the radial forearm free flap〔J〕.Br J Oral MaxillofacSurg,2013,51(1):79-80.
[6] 岳 顺,张大红,周磊磊.雷替曲塞联合多西他赛治疗晚期胃癌的临床疗效〔J〕.肿瘤防治研究,2014,41(2):160-162.
[7] 董金垚,杜志杰,肖帅帅,等.多种化疗药物对胃癌细胞杀伤效应的研究〔J〕.中国普通外科杂志,2014,23(4):488-493.
[8] 陈 浮,王 璐.多西他赛为主的两药与三药方案对低分化胃癌的疗效研究〔J〕.实用癌症杂志,2015,30(3):401-404.
[9] 毛志远,郭晓川,张婷婷,等.多西他赛为主与奥沙利铂为主一线治疗晚期Lauren分型胃癌的疗效对比〔J〕.肿瘤防治研究,2014,41(6):635-640.
[10] 郑 鸿,祝子华,张 宁,等.改良DOC联合DDP和5-FU一线治疗晚期胃癌及胃食管结合部癌的临床观察〔J〕.实用肿瘤杂志,2014,29(4):364-368.
[11] 吴稚冰,吴 侃,李夏东,等.DF方案联合顺铂腹腔热灌注化疗治疗晚期胃癌的临床研究〔J〕.科技导报,2014,32(30):55-58.
[12] 王 允.多西他赛联合奥沙利铂和替吉奥一线治疗晚期胃癌的疗效观察〔J〕.实用癌症杂志,2016,31(6):1000-1002.
[13] 周 然,王 峰,曹 蕾,等.紫杉醇联合卡培他滨一线治疗晚期胃癌后卡培他滨维持治疗的疗效和安全性〔J〕.世界华人消化杂志,2014,22(17):2456-2462.
CombinedTherapyandDocetaxelTripleTherapyintheTreatmentofPoorlyDifferentiatedGastricCarcinoma
YANXu.
HanzhongPeople'sHospital,Hanzhong,723000
ObjectiveTo compare the efficacy and safety of combined therapy and docetaxel triple therapy for poorly differentiated gastric cancer.Methods80 cases of poorly differentiated gastric cancer patients were selected and divided into 2 groups,namely combined group (30 cases) and triple therapy group (50 cases).Second plenary with combined regimen (oxaliplatin + s-1) treatment,the triple group with triple regimen (docetaxel+cisplatin+fluorouracil) treatment.Clinical curative effect,peripheral blood T lymphocyte level before and after treatment and the side effects of drugs during the treatment period of the 2 groups were observed.ResultsTotal efficiency of triple therapy group(32/50,64.00%) was higher than that of combined group (12/30,40.00%) (P<0.05). CD4+of triple group after treatment was higher than that of combined group(P<0.05). Neurotoxicity(20/50,40.00%),neutropenia(23/50,46.00%),hand foot syndrome (10/50,20.00%) of triple group was higher than that of combined group (5/30,16.67%),(7/30,23.33%),(2/30,6.67%) (P<0.05).ConclusionDocetaxel + cisplatin + fluorouracil triple therapy of poorly differentiated gastric cancer is better than that of oxaliplatin combined with S-1 capsule combined therapy,but the adverse reaction of the triple therapy is higher than combined group,clinical choice should be flexible according to the condition of patients.
Docetaxel;Combined group;Triple therapy;Poorly differentiated gastric cancer
(ThePracticalJournalofCancer,2017,32:2017~2019)
723000 陕西省汉中市人民医院
10.3969/j.issn.1001-5930.2017.12.032
R735.2
A
1001-5930(2017)12-2017-03
2016-10-09
2017-04-20)
(编辑:甘艳)

