阿帕替尼联合化疗在Ⅳ期胃癌中的临床疗效观察
唐友明,田洪刚
(江油市人民医院肿瘤科,四川 绵阳 621700)
·药物与临床·
阿帕替尼联合化疗在Ⅳ期胃癌中的临床疗效观察
唐友明,田洪刚
(江油市人民医院肿瘤科,四川 绵阳 621700)
目的观察阿帕替尼与化疗同步治疗Ⅳ期胃癌的疗效及毒副反应。方法 选取2015年6月~2017年4月我院收治的入组晚期胃癌48例。随机分为单纯化疗组、低剂量阿帕替尼(500mg qd)加化疗组及高剂量阿帕替尼(750 mg qd)加化疗组,各16例。阿帕替尼使用56天后评价疗效。结果 单纯化疗组有效率为43.75%,低剂量阿帕替尼加化疗组为68.75%(P<0.05),高剂量阿帕替尼加化疗组为75.00%(P<0.05),毒副反应分为血液学毒性及非血液学毒性,前者包括白细胞及血小板等的减少,后者包括手足综合征、蛋白尿、高血压及末梢神经炎。结论 阿帕替尼联合化疗能提高近期有效率,而且毒副反应可以耐受。
阿帕替尼;化疗;胃癌
胃癌是发病率较高的肿瘤之一,50%左右的的患者就诊时属于晚期,晚期胃癌的主要治疗方法仍为化疗[1-2],其5年生存率约为30%左右[3-4]。近年来抗血管生成治疗已成为治疗恶性肿瘤的重要研究领域之一[5-6]。相关研究提示,抗血管生成药物与化疗药物联合应用可提高疗效[7-11]。阿帕替尼是江苏恒瑞医药股份有限公司生产的1.1类新药,可强效阻断肿瘤血管生成,国家食品药品监督管理总局(CFDA)于2014年批准阿帕替尼用于晚期胃癌的治疗。目前阿帕替尼主要用于胃癌的二、三线治疗,为了进一步观察阿帕替尼与化疗是否有协同作用,现将阿帕替尼与化疗药联合用于治疗Ⅳ期胃癌,观察其近期疗效及不良反应。
1 资料与方法
1.1 一般资料
选取2015年6月~2017年4月我院收治的入组晚期胃癌48例。其中,男27例,女21例,年龄在35岁到75岁之间。入组病例均由组织病理学证实为晚期胃腺癌,均无法手术或存在复发转移。其他入组标准包括:KPS评分≥70分,预计生存时间至少为12周,以及最少存在1个可测量病灶,血常规、肝肾功能、心电等均为正常,无消化道大出血、穿孔、梗阻、2级及以上高血压等高危因素。其中,低分化腺癌、中高分化腺癌、黏液腺癌、印戒细胞癌分别为32例、3例、4例和9例。最常见的转移部分依次为淋巴结、肝、肺。7例为原发病灶不能手术切除,其余均为胃癌术后发生复发转移。按入院时间顺序随机分到单纯化疗组、低剂量阿帕替尼(500 mg qd)加化疗组(以下简称低剂量组)及高剂量阿帕替尼(750 mg qd)加化疗组(以下简称高剂量组),各16例。三组患者的年龄、性别、临床分期及身体状况(KPS评分)等没有统计学差异。
1.2 治疗方法
化疗:FOLFOX4方案(奥沙利铂85 mg/m2iv,2小时,d1;5-氟尿嘧啶(5-FU)400 mg/m2iv,d1-2;氟尿嘧啶600 mg/m2iv;亚叶酸钙200 mg/m2iv d1)。
低剂量阿帕替尼加化疗组:FOLFOX4方案加用阿帕替尼500 mg qd,连续服用56天;高剂量阿帕替尼加化疗组:FOLFOX4方案加用阿帕替尼750 mg qd,连续服用56天;化疗组:FOLFOX4方案。
1.3 疗效评价
参考世界卫生组织(WHO)实体瘤疗效评价标准将治疗效果分为完全缓解(CR)、部分缓解(PR)、稳定(SD)和进展(PD)。每两个周期评价一次治疗效果。
1.4 不良反应
按照WHO对抗肿瘤药物的不良反应(AE)评价标准,将AE分为5个级别(0-IV度),级别越高表示AE越严重。治疗期间,有关不良反应的检测项目为常规检查(血常规,肝肾功能等)。
1.5 统计学方法
本研究中统计部分使用SPSS 18.0,当P<0.05表示差异有统计学意义。
2 结 果
2.1 近期疗效
在阿帕替尼治疗2个月后评价疗效,计算总有效率(RR=CR+PR)。单纯化疗组RR=43.75%,低剂量阿帕替尼加化疗组RR=68.75%(P=0.024),高剂量阿帕替尼加化疗组RR=75.00%(P=0.016),加用阿帕替尼组与单用化疗组之间对比有统计学意义(P=0.016),高、低剂量阿帕替尼组之间无明显统计学差异(P=0.062),详见表1。
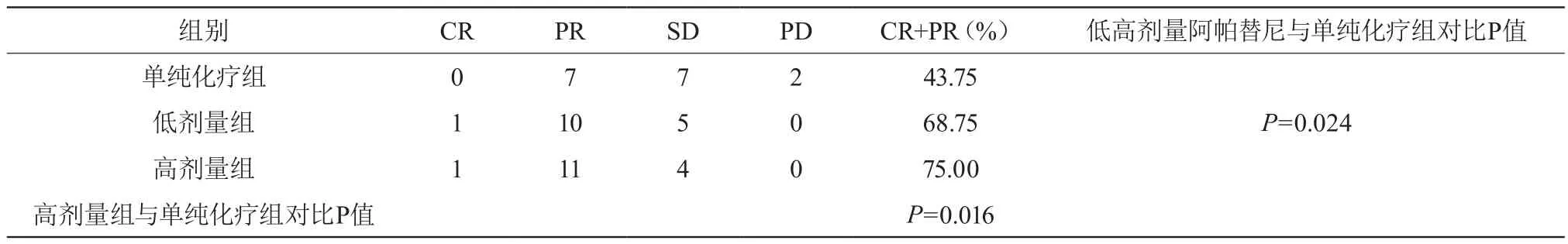
表1 三组患者近期疗效比较(n)
2.2 毒副反应
主要表现为白细胞减少、血小板减少、高血压、蛋白尿、手足综合征及末梢神经炎等。但多为I-Ⅱ度。高剂量组阿帕替尼加化疗组和另两组相比,仅高血压和手足综合征上存在统计学差异(P<0.05),详见表2。
3 讨 论
肿瘤的生长、转移均依赖于血管生成,当肿瘤血管体积在l~2 mm3以上时,肿瘤易发生转移[12-13]。目前的研究热点为如何选择最优的抗血管生成药物的用法用量及用药时机,从而有效地抑制肿瘤血管生成及转移[14]。甲磺酸阿帕替尼片通过阻断VEGF/VEGFR-2的信号通路,从而发挥抗肿瘤的疗效。相关临床研究[15-17]表明,在胃癌三线及三线以上的治疗中,阿帕替尼是有效且安全的。本研究资料回顾分析显示,治疗开始2月后评价疗效,三组总有效率(CR+PR)分别为单纯化疗组43.75%,低剂量阿帕替尼加化疗组为68.75%(P=0.024).,高剂量阿帕替尼加化疗组为75.00%(P=0.016),加用阿帕替尼组与单用化疗组对比有统计学意义,但阿帕替尼组之间无明显统计学差异(P=0.062)。目前此类报道尚少。同时,三种方案的毒副反应多为I-Ⅱ度。高剂量组阿帕替尼加化疗组和另外两组相比,高血压和手足综合征的毒副作用存在统计学差异(P<0.05),表明低剂量阿帕替尼联合化疗用于晚期胃癌较为合适。
目前,贝伐单抗是国内使用的抗血管生成药物之一。与阿帕替尼相比,贝伐单抗价格较为昂贵,据相关资料统计[18],使用贝伐单抗进行化疗,花费约10万美元/年。随着阿帕替尼纳入医保,其成为性价比最高的抗血管生成药物之一。
综上所述,阿帕替尼在晚期胃癌的临床研究及药物经济学研究均表明,阿帕替尼在晚期胃癌中值得进一步推广使用。
[1]Chen HD,Zhou J,Wen F ,et a1.Cost-effectiveness analysis of apatinib treatment for chemotherapy-refractory advanced gastric cancer[J].J Cancer Res Clin Oncol,2017 Feb;143(2):361-368.
[2]de Mello RA,de Oliveira J,Antoniou G.Angiogenesis and apatinib:a new hope for patients with advanced gastric cancer?[J].Future Oncol.2017 Feb;13(4):295-298.
[3]中国肿瘤登记中心.2015年中国肿瘤登记年报[EB/OL].2015[2015-08-10.]
[4]Goel A,Aggarwal BB.Curcuminthe golden spice from Indian saffron,is a chemosensitizer and radiosensitizer for tumors and chemoprotector and radioprotector for normal organs[J].Nutr Cancer.2010;62(7):919-30.
[5]Gaur S,Oo TH,Aish LS,et al.Gastric relapse of solitary bone plasmacytoma[J].Am J Clin Oncol.2005 Jun;28(3):325-6.
[6]Feng R,Zhang X,Yang S.Research status quo and progression in targeted therapy for advanced gastric cancer.Chinese Journal of Gastrointestinal Surgery.[J]2016 Oct 25;19(10):1191-1196.
[7]Zhu XR,Zhu ML,Wang Q,et a1.A case report of targeted therapy with apatinib in a patient with advanced gastric cancer and high serum level of alpha-fetoprotein[J].Medicine (Baltimore).2016 Sep;95(37):e4610.
[8]Ji G,Hong L,Yang P.Successful treatment of angiosarcoma of the scalp with apatinib:a case report[J].Onco Targets Ther.2016 Aug 11;9:4989-92.
[9]Brower V.Apatinib in treatment of refractory gastric cancer[J].Lancet Oncol.2016 Apr;17(4):e137.
[10]Ilson DH.Targeting the Vascular Endothelial Growth Factor Pathway in Gastric Cancer:A Hit or a Miss?[J].J Clin Oncol.2016 May 1;34(13):1431-2.
[11]Mahipal A,Choi M,Kim R.Second-Line Treatment of Advanced Gastric Cancer:Where Do We Stand?[J].J Natl Compr Canc Netw.2015 Oct;13(10):1281-91.
[12]Liu L,Yu H,Huang L,et a1.Progression-free survival as a surrogate endpoint for overall survival in patients with third-line or later-line chemotherapy for advanced gastric cancer[J].Onco Targets Ther.2015,22(8):921-8.
[13]Schulte N,Ebert MP,H?rtel N.Gastric Cancer:New Drugs-New Strategies[J].Gastrointest Tumors.2014 May;1(4):180-94.
[14]Zhang H.Apatinib for molecular targeted therapy in tumor[J].Drug Des Devel Ther.2015 Nov 13;9:6075-081
[15]Lankhorst S,Kappers MH,van Esch JH,et al. Hypertension during vascular endothelial growth factor inhibition:focus on nitricoxide,endothelin-1,and oxidative stress[J].Antioxid RedoxSignal,2014,20(1):135-45.
[16]Bakris GL,Black HR,et al.Initial assessment,surveillance,and management of blood pressure in patients receiving vascular endothelial growth factor signaling pathway inhibitors[J].J Natl Cancer Inst,2010,102(9):596-604.
[17]Ivanyi P,Winkler T,Ganser A,et al. Novel therapies in advanced renal cell carcinoma:Management of adverse events from sorafenib and sunitinib[J].Dtsch Arztebl Int,2008,105(13):232-37.
[18]Larochelle P,Kollmannsberger C,Feldman R,et al.Hypertension management in patients with renal cell cancer treated with anti-angiogenic agents[J].Curr Oncol,2012,19(4):202-08.
R735.2
B
ISSN.2095-8242.2017.065.12810.03
本文编辑:王雨辰

