参麦注射液联合化疗治疗中晚期肺癌疗效观察
吴柏平, 唐 青
(江苏省阜宁县人民医院, 江苏 阜宁, 224400)
参麦注射液联合化疗治疗中晚期肺癌疗效观察
吴柏平, 唐 青
(江苏省阜宁县人民医院, 江苏 阜宁, 224400)
中晚期肺癌; 参麦注射液; 化疗; 疗效; 安全性
肺癌[1]分为小细胞肺癌(SCLC)和非小细胞肺癌(NSCLC), 其中NSCLC占75%~80%[2], 临床上对于中晚期肺癌患者多采用药物化疗、放疗等方式治疗,而药物化疗往往作为首选之一。肺癌在中医基本理论中属于“肺积”,“咳嗽”,“痰液”,“咯血”等范畴,中成药能有效提高患者的免疫力,减轻化疗药物对骨髓的抑制作用,对放化疗有增敏减毒等功效[3-4]。本研究观察参麦注射液联合化疗治疗中晚期肺癌的临床疗效和安全性,为临床用药提供参考。
1 资料与方法
1.1 一般资料
筛选本院2010年1月-2016年6月化疗的晚期非小细胞肺癌患者60例,随机分为对照组和治疗组各30例。其中对照组男20例,女10例; 年龄(56.1±7.2)岁; 病理分型: 鳞癌19例,腺癌9例,鳞腺癌2例。治疗组男21例,女9例; 年龄(56.2±7.1)岁;病理分型: 鳞癌18例,腺癌9例,鳞腺癌3例。2组患者的年龄、性别、病理分型等一般资料比较,差异无统计学意义(P>0.05), 具有可比性。纳入标准: ① 所选病例均符合《美国国家综合癌症网非小细胞肺癌治疗指南》[5]; ② 符合NSCLC的病理学或细胞学诊断标准[6]; ③ 依据美国AD Anderson医学中心和国立癌症研究所指定的肺癌TNM分期标准(第6版)[7], 为Ⅲ~Ⅳ期的患者并且不宜进行手术的治疗者; ④ 检测发现患者至少存在一个病灶具有可测量性; ⑤ KPS评分≥70分且预计生存期≥3个月; ⑥ 患者无其他严重器质性病变或造血功能异常等; ⑦ 至少完成2个周期的化疗。排除标准: 不符合上述纳入标准的患者; 同时合并有其他严重感染性疾病的患者; 不能配合治疗,依从性较差,无自知能力者; 近3个月内曾使用过免疫增强剂或相关药物; 化疗治疗不能完成的患者。
1.2 化疗方法
对照组患者给予常规剂量化疗,主要方案包括NP方案(顺铂80~100 mg/m2+长春瑞滨25 mg/m2, 第1、8 天静脉滴注,每21天重复1次,共2周期); GP方案(顺铂80~100 mg/m2+吉西他滨1 000 mg/m2, 第1、8天静脉滴注,每21天重复1次,共2周期)。治疗组在对照组的基础上给予参麦注射液50 mL+250 mL生理盐水静脉滴注, 1次/d, 连续治疗4周。
1.3 评价指标
① 2个周期结束后对患者病情进行评估,评价标准参照世界卫生组织(WHO)实体瘤疗效评价标准[8]。② 参照《中药新药临床研究指导原则》[9]对患者干咳、胸闷、痰中带血、乏力、气短、发热等6项主要临床症状改善情况进行评分,按照症状改善程度分为显著改善、部分改善、无改善,每周观察并记录1次。③ 参照WHO抗肿瘤药物的不良反应分级标准,评价化疗药物的毒性反应程度,观察其白细胞、血红蛋白、血小板、转氨酶比值(AST/ALT)、尿素氮、恶心呕吐等临床指标并按标准分为0、Ⅰ、Ⅱ、Ⅲ、Ⅳ级。每周记录1次,并计算此临床发生率。④ 生活质量(QOL)评价参照Karnofsky, 体力状况(KPS)评分标准[10]。
2 结 果
2.1 2组近期疗效比较
2组患者均按常规完成2个周期的化疗治疗,没有1例放弃治疗亦无死亡病例。对照组PR 8例, SD 11例, PD 11例; 治疗组分别为14例、11例、5例。治疗组总有效率、稳定率分别为46.67%、80.00%, 明显高于对照组的26.67%、63.33%。
2.2 2组症状改善情况比较
治疗组干咳、胸闷、痰中带血、乏力、气短、发热等6项症状缓解率比较。见表1。
2.3 2组不良反应比较
2组患者均未发生化疗导致死亡的毒副反应,对照组中发生白细胞减少,血红蛋白减少,血小板减少,恶心呕吐的发生率显著高于治疗组(P<0.05); 脱发、尿素氮、AST/ALT升高的发生率与治疗组相比,差异无统计学意义(P>0.05), 见表2。
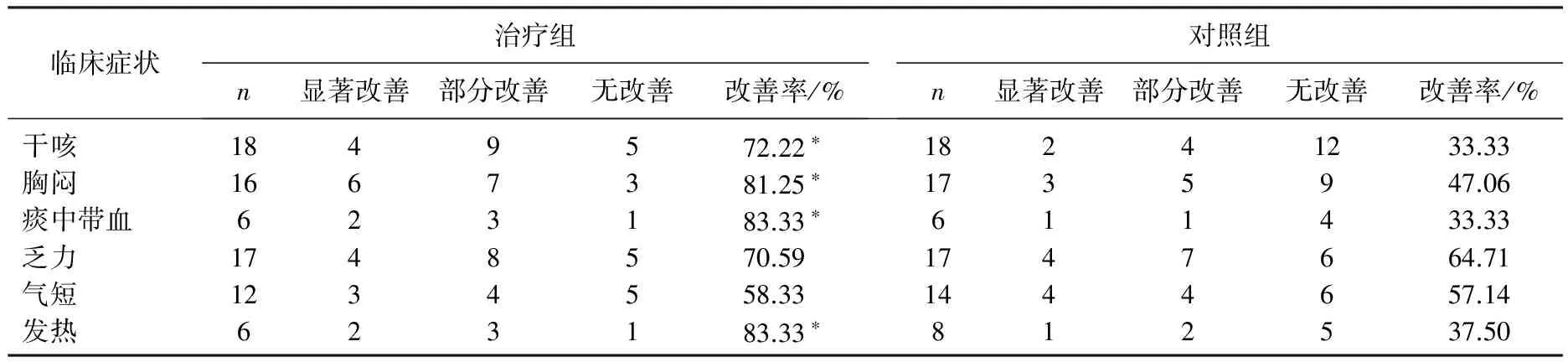
表1 2组患者治疗2周期后6项主要临床症状改善情况比较
与对照组比较, *P<0.05。
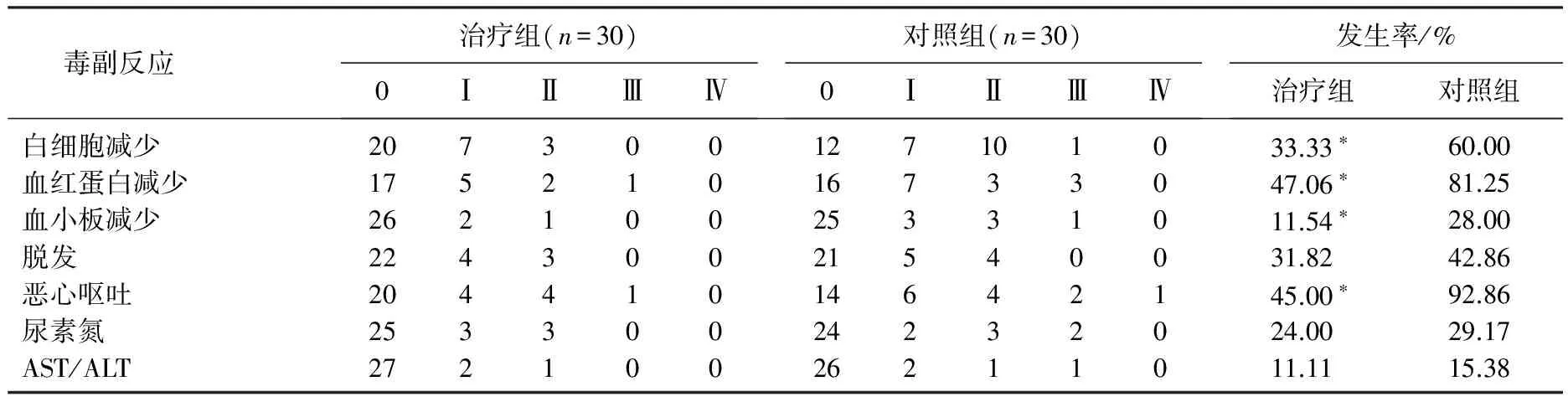
表2 2组不良反应比较[n(%)]
与对照组比较, *P<0.05。
2.4 2组远期疗效比较
治疗组QOL稳定28例,局部控制24例,无进展生存23例,总生存率83.33%; 对照组分别为23例、18例、16例、总生存率56.67%。治疗组QOL稳定率、局部控制率、无进展生存率、总生存率均显著高于对照组(P<0.05)。
3 讨 论
目前,非小细胞肺癌治疗手段主要有手术治疗、放化疗治疗、生物免疫治疗等方法。对于不易手术的患者,临床常采用铂类药物为基础进行化疗,其方案是治疗中晚期NSCLC患者标准的化疗方案[11], 目前第3代含铂类化疗药物,因临床疗效欠佳并且药物副作用较多,为了增强疗效,减少药物副作用常采用中药制剂联合化疗。
参麦注射液是一种复合中药制剂,组方为红参和麦冬。该组方中红参含有大量的人参皂苷,其成分可以干扰肿瘤细胞的生长周期,抑制和杀灭癌细胞,从而使肿瘤病灶缩小或消失。同时红参具有大补元气之功效,可提高机体的适应性; 保护机体的造血功能,提高脑、体力活动能力,增强人体免疫力。同时,可以减轻化疗药物引起的不良反应等,从而多种途径达到治疗肿瘤的效果[12]。该组方中麦冬具有养阴生津,润肺清心,泻热生津,化痰止呕,肺燥干咳,虚劳咳嗽,心烦失眠等功效。近期药理研究表明,麦冬有镇静、催眠,抗疲劳,清除自由基,升高白细胞的作用,还能提高机体免疫功能,具有良好的抗肿瘤作用。
[1] 石远凯. 临床肿瘤内科手册[M]. 5版. 北京: 人民卫生出版社, 2007: 9-13.
[2] Jemal A. Bray F. Center MM, et al. Global cancer. Statistics[J]. CA cancer J Clin, 2011, 61(2): 69-90.
[3] 席青, 王建清, 常小红, 等. 艾迪注射液在肺癌治疗中的研究进展[J]. 中国医药导报, 2014, 11(4): 163-165.
[4] 曹礼慧. 中药注射剂辅助治疗非小细胞肺癌的循证研究[D]. 广州: 暨南大学, 2014.
[5] 石远凯, 牛奕. 美国国家综合癌症网非小细胞肺癌治疗指南2007年第一版结束[J]. 中华肿瘤杂志, 2007, 29(10): 799-800.
[6] 刘涛. GP方案联合恩度在治疗晚期非小细胞肺癌的临床疗效研究[J]. 中国实用医药, 2015, 30(2): 43-44.
[7] 牛晓敏, 廖美琳. 国际肺癌研究会推荐的肺癌TNM新分期简介[J]. 肿瘤, 2008, 28(3): 198-202.
[8] 于世英, 胡国涛. 肿瘤临床诊疗指南[M]. 北京: 中国科学出版社, 2005: 412-413.
[9] 郑筱萸. 中药新药临床研究指导原则(试行)[S]. 北京: 中国医药科技出版社, 2002.
[10] 楚何莹, 白勇, 杨睿, 等. 恩度联合顺铂对老年晚期非小细胞肺癌患者血清MMP-2和VEGF水平的影响[J]. 肿瘤基础与临床, 2014, 27(4): 300-301.
[11] 田锦玲, 张欢欢. 艾迪注射液联合奥沙利铂、多西紫杉醇方案治疗非小细胞肺癌47例[J]. 中国药业, 2014(15): 83-84.
[12] 高华, 郑业, 刘自建, 等. 参麦联合化疗对肺癌的疗效观察[J]. 中国社区医师, 2012, 14(29): 178-179.
R 734.2
A
1672-2353(2017)21-162-02
10.7619/jcmp.201721064
2017-06-11

