羟考酮联合舒芬太尼用于剖宫产术后静脉镇痛的随机对照研究
聂晶晶,黄绍强,刘宇琦
复旦大学附属妇产科医院麻醉科,上海 200011
·短篇论著·
羟考酮联合舒芬太尼用于剖宫产术后静脉镇痛的随机对照研究
聂晶晶,黄绍强,刘宇琦*
复旦大学附属妇产科医院麻醉科,上海 200011
目的探讨羟考酮联合舒芬太尼用于剖宫产术后静脉镇痛的临床疗效。方法选择60例行择期剖宫产术的单胎初产妇,按随机数字表法分为羟考酮联合舒芬太尼组(OS组)和舒芬太尼组(SF组)。所有患者均采用腰硬联合阻滞,术后采用患者静脉自控镇痛(PCIA)。镇痛泵配方:OS组为羟考酮50 mg+舒芬太尼50 μg+雷莫司琼0.3 mg,SF组为舒芬太尼100 μg+雷莫司琼0.3 mg。药液均用0.9%氯化钠溶液配至100 mL,持续剂量1 mL/h,冲击剂量 2 mL,锁定时间为10 min。于术后6 h、12 h和24 h记录随访活动时切口疼痛评分(NRS-M)、静息时切口疼痛评分(NRS-R)、宫缩痛评分(NRS-U)、镇痛泵药物消耗量、患者满意度评分及不良反应的发生情况。结果OS组患者在各时点的NRS-M、NRS-R、NRS-U均低于SF组,按压次数及镇痛药的消耗量也低于SF组(P<0.05)。SF组术后恶心发生率高于OS组(P<0.05),呕吐、皮肤瘙痒、呼吸抑制、眩晕发生率两组差异无统计学意义。结论剖宫产术后采用羟考酮联合舒芬太尼行PCIA效果优于单独使用舒芬太尼,且不增加不良反应。
剖宫产术;患者自控镇痛;羟考酮;舒芬太尼
剖宫产术后常规使用大剂量催产素,可促进子宫恢复和减少产后出血,但伴随较强的宫缩痛[1]。因此,切口痛之外,宫缩痛也是术后疼痛之一。尽管目前采用了多模式镇痛,但剖宫产术后疼痛依然控制不佳。
舒芬太尼是特异性μ受体激动剂,易诱发恶心呕吐、眩晕、呼吸抑制等不良反应[2]。盐酸羟考酮是由阿片生物碱蒂巴因衍生物制成的半合成阿片类药物,镇痛作用可能与μ、κ受体有关[3-5],能够显著减少内脏疼痛[6]。羟考酮已被广泛用于治疗术后疼痛、慢性疼痛及严重的恶性疼痛[7]。然而通过静脉滴注的方式用于剖宫产术后镇痛的效果并不明确。因此,本研究拟探讨羟考酮联合舒芬太尼用于剖宫产术后静脉自控镇痛(PCIA)的效果。
1 资料与方法
1.1 一般资料 选择2015年1月至2015年5月于复旦大学附属妇产科医院就诊的60例初产产妇,在腰硬联合麻醉下择期行子宫下段横切口剖宫产手术。入组标准:美国麻醉医师协会(ASA)评分Ⅰ或Ⅱ级。60例孕周≥37周,单胎,年龄20~45岁,身高155~175 cm,体质量60~90 kg,手术时间约1 h。排除标准:有严重内科并发症,包括子痫前期、妊娠合并糖尿病、妊娠合并贫血、妊娠合并心脏病;术前48 h内服用或近期正在服用阿片类药物、非甾体类抗炎药物;术中改变麻醉方式者,术中麻醉平面不足需要硬膜外加局麻药患者;不能配合使用数字疼痛评分法(NRS)评分的患者。本研究获得医院伦理委员会审核批准,患者知情同意并签署知情同意书。
1.2 随机分组 60例产妇按随机数字表法分为2组:羟考酮联合舒芬太尼组(OS组)和舒芬太尼组(SF组)。镇痛泵配方OS组为羟考酮50 mg+舒芬太尼50 μg+雷莫司琼 0.3 mg;SF组为舒芬太尼100 μg+雷莫司琼0.3 mg。每组药物使用0.9%氯化钠溶液稀释至100 mL。采用患者自控静脉镇痛(PCIA):持续剂量1 mL/h,冲击剂量2 mL,锁定时间10 min。本研究由计算机产生2套各30例随机用药编号,编码形成后采用文件形式予以确定,密封后由配制药物者保存。通过计算机随机选取试验药物编号,根据编号配制试验药物,均为无色透明液体,手术结束时交与麻醉操作者接术后镇痛泵,配制药物者不参与任何其他操作及数据收集。数据分析完毕后揭盲。
1.3 麻醉方法 所有患者入室后左倾15°仰卧位,开放静脉后以20 mL/min的速度滴注羟乙基淀粉130/0.4氯化钠注射液(万汶)500 mL,使用S/5 麻醉监护仪(GE, Finland)监测心电图、无创血压、脉搏血氧饱和度。左侧或右侧卧位L2~3行腰硬联合麻醉,26号穿刺针斜面朝头端,使用等比重罗哌卡因13~15 mg,用脑脊液稀释至2.5 mL,注射至蛛网膜下腔,15~30 s注射结束。蛛网膜下腔阻滞成功后留置硬膜外导管,患者恢复左侧15°平卧位。温度感觉阻滞平面达T4后开始行剖宫产手术。若发生低血压[平均动脉压低于基础值的20%或低于60 mmHg(1 mmHg=0.133 kPa)],静脉滴注去氧肾上腺素50 μg;若出现心动过缓(心率<50次/min)静脉给予阿托品0.5 mg。胎儿娩出后给予缩宫素20 U静脉缓慢滴注。手术结束前15 min静脉注射氟比洛芬酯50 mg+雷莫司琼0.3 mg。手术结束后拔除硬膜外导管。静脉连接患者自控镇痛泵(AM330, ACE Medical, Gyeonggi-Do, Korea)。若患者术后镇痛不足(NRS>5分),告知患者按压镇痛泵,不再给予额外镇痛药。术后常规使用缩宫素20 U静脉缓慢滴注。
1.4 术后随访 由不参与任何操作的研究者记录术后6 h、12 h和24 h随访活动时切口疼痛评分(NRS-M)、静息时切口疼痛评分(NRS-R)、宫缩痛评分(NRS-U)。NRS评分:“0”代表不痛,“5”代表中等疼痛,“10”代表无法忍受的疼痛。能明确定位来源于腹壁切口的刀割样或烧灼样疼痛为切口痛;下腹部定位不明确的,阵发性隐痛、胀痛或绞痛为宫缩痛。同时记录各时间点自控镇痛按压的次数、镇痛药物的消耗量,以及头晕、嗜睡、呼吸抑制、恶心呕吐、皮肤瘙痒等不良反应。术后24 h记录患者满意度评分,满意度分为4级:非常满意、满意、一般、不满意。满意度以非常满意及满意患者所占比例计算。

2 结 果
2.1 一般资料的比较 SF组有1例患者因数据丢失退出研究,OS组2例患者拒绝进行疼痛评分。最终对SF组29例、OS组28例患者数据进行分析。结果(表1)表明:两组患者基线资料身高、体质量、年龄、体质指数(BMI)、孕周、手术时间比较差异均无统计学意义。
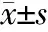
表1 两组患者基线资料的比较
BMI:体质指数
2.2 术后NRS评分的比较 结果(表2、表3)表明:术后6、12、24 h,OS组NRS-R、NRS-M、NRS-U评分明显低于SF组(P<0.05)。
2.3 两组患者PCIA使用情况的比较 结果(表4)表明:术后6、12、24 h时,OS组PCIA单次注射次数和PCIA药物的总消耗量明显少于SF组(P<0.05)。
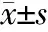
表2 两组患者切口疼痛评分(NRS)的比较
NRS-R :静息时切口疼痛评分;NRS-M:活动时切口疼痛评分.*P<0.05与SF组相比
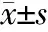
表3 两组患者宫缩疼痛NRS评分的比较
*P<0.05与SF组相比
2.4 两组患者不良反应发生率的比较 SF组有5例患者术后0~6 h发生恶心,OS组无患者发生恶心。两组患者0~6 h恶心发生率差异有统计学意义 (P<0.05)。术后两组均无患者发生呕吐、皮肤瘙痒或呼吸抑制,OS组1例发生眩晕,SF组无患者发生眩晕,差异无统计学意义(表 5)。两组患者满意等级分布情况见表6,两组差异有统计学意义(P=0.038)。OS组满意度为96.5%,明显高于SF组(78.6%),差异有统计学意义(P<0.05)。
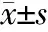
表4 两组患者PCIA使用情况的比较
*P<0.05与SF组相比

表5 两组患者不良反应发生率的比较 n(%)

表6 两组患者镇痛满意度的比较 n(%)
3 讨 论
近年来,关于羟考酮在术后镇痛的研究主要涉及腹腔镜胆囊切除术、脊柱手术等[8-9],目前尚缺乏羟考酮联合舒芬太尼用于剖宫产术后静脉镇痛的研究。研究表明,羟考酮与吗啡的效价比是1∶1[10],舒芬太尼与吗啡的效价比是1 000∶1[11]。因此,本研究采用1∶1 000为羟考酮与舒芬太尼的效价比,即1 mg注射用羟考酮等效于1 μg舒芬太尼针剂。
本研究表明,OS组子宫收缩NRS评分低于SF组,说明羟考酮能较好地缓解子宫收缩引起的疼痛。主要原因是羟考酮具有κ受体激动作用[12],在缓解内脏疼痛方面相比舒芬太尼更为有效。无论患者处于休息或下床活动状态,OS组患者切口疼痛的NRS评分低于SF组。结果说明羟考酮联合舒芬太尼对切口痛的缓解效果也好于单独使用舒芬太尼。这可能由于OS组患者宫缩疼痛缓解后,舒适度提高,从而使得患者的切口痛评分也较低。
本研究中,OS组6、12、24 h PCIA镇痛药物累计消耗药量较SF组少,说明OS组镇痛效果优于SF组。Kalso等[13]认为相比较于吗啡,羟考酮能快速和持续较长时间地缓解疼痛。因此,羟考酮长效持续镇痛能减少PCIA中阿片类药物的消耗。
有研究[14]比较了腹腔镜下胆囊切除术后采用羟考酮或芬太尼的镇痛作用后发现,尽管累积PCIA剂量在羟考酮组低于芬太尼组,但术后羟考酮组恶心的发生率高于芬太尼组,这与本研究的结果不一致。本研究中,SF组5例患者发生恶心,而OS组未发生恶心、呕吐,推测由于μ激动效果会引发恶心等胃肠道反应,而羟考酮的μ受体亲和力弱于舒芬太尼[8],所以OS组的恶心呕吐发生率较低。
阿片类药物在哺乳患者中的应用仍存在争议。Baka等[15]发现,剖宫产术后接受PCIA镇痛的患者进行母乳喂养时,母乳中吗啡的浓度非常小,因此对新生儿较为安全。另外由于羟考酮清除率为0.7~0.8 L/min,消除半衰期为2~3 h[8],因此乳汁分泌时,羟考酮的血液浓度已很小,乳汁浓度则更小,故而安全性较高。
本研究也有一定的局限性。首先,本研究中并未单独使用羟考酮作为术后镇痛药物而是复合舒芬太尼,主要是考虑到实际临床应用中一般较少单独使用羟考酮作为术后静脉自控镇痛。其原因包括羟考酮费用昂贵及κ受体的镇静作用,患者易发生眩晕、嗜睡等不良反应。其次,本研究为单中心研究,且研究对象仅为择期剖宫产的单胎初产产妇,结论推广到一般人群尚需进一步研究。此外,本研究中,无论患者处于休息或下床活动状态,OS组患者切口疼痛的NRS评分均低于SF组,这可能表明舒芬太尼与羟考酮的效价比定为1 000∶1不准确,需要进一步的研究。
综上所述,羟考酮联合舒芬太尼用于剖宫产术后患者自控镇痛的效果确切,优于舒芬太尼单独使用,且不增加不良反应。
[ 1 ] ADENIJI A O, ATANDA O O. Randomized comparison of effectiveness of unimodal opioid analgesia with multimodal analgesia in post-cesarean section pain management[J]. J Pain Res, 2013,6(5):419-424.
[ 2 ] GADSDEN J, HART S, SANTOS A C. Postcesarean delivery analgesia[J]. Anesth Analg, 2005, 101(5Suppl):S62-S69.
[ 3 ] PECKHAM E M, TRAYNOR J R. Comparison of the antinociceptive response to morphine and morphine-like compounds in male and female Sprague Dawley rats[J]. J Pharmacol Exp Ther, 2006,316(3):1195-1201.
[ 4 ] NARITA M, NAKAMURA A, OZAKI M, et al. Comparative pharmacological profiles of morphine and oxycodone under a neuropathic pain-like state in mice: evidence for less sensitivity to morphine[J]. Neuropsychopharmacology, 2008,33(5):1097-1112.
[ 5 ] KALSO E. How different is oxycodone from morphine?[J] Pain, 2007,132(3):227-228.
[ 6 ] DE SCHEPPER H U, CREMONINI F, PARK M I, et al. Opioids and the gut: pharmacology and current clinical experience[J]. Neurogastroenterol Motil, 2004,16(4):383-394.
[ 7 ] KOKKI H, KOKKI M, SJOVALL S. Oxycodone for the treatment of postoperative pain[J]. Expert Opin Pharmacother, 2012,13(7):1045-1058.
[ 8 ] LENZ H, SANDVIK L, QVIGSTAD E, et al. A comparison of intravenous oxycodone and intravenous morphine in subject-controlled postoperative analgesia after laparoscopic hysterectomy[J]. Anesth Analg,2009,109(4):1279-1283.
[ 9 ] KOCH S, AHLBURG P, SPANGSBERG N, et al. Oxycodonevsfentanyl in the treatment of early post-operative pain after laparoscopic cholecystectomy: a randomized double-blind study[J]. Acta Anaesthesiol Scand,2008,52(6):845-850.
[10] MCNIEOL E, HOROWICZ-MEHLER N, FISK R A, et a1. Management of opioid side effects in cancer-related and chronic noncancer pain: a systematic review[J]. J Pain,2003,4(5):231-256.
[11] FREYE E, LEVY J V. Opioids in medicine: a comprehensive review on the mode of action and the use of analgesics in different clinical pain states[M]. Germany:Springer Verlag,2008.
[12] NIELSEN C K, ROSS F B, LOTFIPOUR S, et al. Oxycodone and morphine have distinctly different pharmacological profiles: radioligand binding and behavioural studies in two rat models of neuropathic pain[J]. Pain,2007,132(3):289-300.
[13] KALSO E, PÖYHIR, ONNELA P, et al. Intravenous morphine and oxycodone for pain after abdominal surgery[J]. Acta Anaesthesiol Scand,1991,35(7):642-646.
[14] HWANG B Y, KWON J Y, KIM E, et al. Oxycodonevsfentanyl patient-controlled analgesia after laparoscopic cholecystectomy[J]. Int J Med Sci,2014,11(7):658-662.
[15] BAKA N E, BAYOUMEU F, BOUTROY M J, et al.Colostrum morphine concentrations during posteesarean intravenous patientcontrolled analgesia[J].Anesth Analg,2002,94(1):184-187.
Effectobservationofpatient-controlledintravenousanalgesiausingoxycodonecombinedwithsufentanilaftercesareansection:arandomizedcontrolledtrial
NIE Jing-jing, HUANG Shao-qiang, LIU Yu-qi*
Department of Anesthesiology, Obstetrics and Gynecology Hospital, Fudan University, Shanghai 200011, China
Objective: To explore the effect of patient-controlled intravenous analgesia (PCIA) using oxycodone combined with sufentanil on cesarean section patients.MethodsSixty elective cesarean section patients were randomly divided into two groups: SF group (sufentanil 100 μg and ramosetron 0.3 mg), OS group (sufentanil 50 μg, oxycodone 50 mg, and ramosetron 0.3 mg). All patients were
combined spinal-epidural anesthesia, and applied with PCIA after surgery. Making 0.9% sodium chloride solution to 100 mL, continuous dosage 1 mL/h, pulse dosage 2 mL, the time was 10 min. Numerical pain scores of somatalgia at rest(NRS-R) or movment(NRS-M), numerical pain scores of uterine contraction(NRS-U) , patient-controlled intravenous analgesia doses, and side effects were assessed at 6 h,12 h and 24 h after the operation.ResultsAt the time points of 6,12 and 24 h after surgery, the scores of NRS-M, NRS-R, and NRS-U in OS group were lower than those in SF group. Times of bolus and accumulated drugs consumption in OS group were less than those in SF group (P<0.05).The incidence of nausea in SF group was higher than that in OS group (P<0.05). There was no significant difference in the incidences of vomiting, dizziness, pruritus or respiratory depression between the two groups.ConclusionsOxycodone combination with sufentanil in patient-controlled intravenous analgesia may be more effective and without increasing side effects compared with sufentanil alone after cesarean section.
cesarean section; patient controlled analgesia,; oxycodone; sufentanil
2016-12-11接受日期2017-09-22
聂晶晶,主治医师.E-mail: jingjingjingnie@sina.com
*通信作者(Corresponding author). Tel:021-63455050-8479, E-mail: yukianesth@126.com
10.12025/j.issn.1008-6358.2017.20161146
R 614
A
[本文编辑] 叶 婷, 贾泽军

