[Bmim]BF4/EA-(NH4)2SO4-H2O双水相体系萃取黄连中盐酸小檗碱
赵晓军,田 刚, 李鑫垚, 娄文涛, 郭鹏鹏, 侯延民
(平顶山学院 化学与环境工程学院,河南 平顶山 467000)
[Bmim]BF4/EA-(NH4)2SO4-H2O双水相体系萃取黄连中盐酸小檗碱
赵晓军,田 刚, 李鑫垚, 娄文涛, 郭鹏鹏, 侯延民*
(平顶山学院 化学与环境工程学院,河南 平顶山 467000)
研究了亲水性离子液体1-丁基-3-甲基咪唑四氟硼酸盐/乙酸乙酯 ([Bmim]BF4/EA)-硫酸铵-水双水相体系萃取(ATPS)黄连中盐酸小檗碱,考察了双水相体系中有机溶剂种类、分相盐种类及质量分数、体系温度及pH值对盐酸小檗碱萃取率的影响,得到最佳条件为:[Bmim]BF4:EA(2.5 mL:2.5 mL)5 mL,硫酸铵溶液质量分数36.7%,温度60 ℃,pH值5.5,在此条件下萃取率可达78.89 %。此工艺对黄连中有效成分的提取、分离、纯化具有一定的应用价值,同时对建立离子液体双水相溶剂浮选体系提取天然产物中活性成分具有一定的指导意义。
离子液体;乙酸乙酯;双水相萃取;黄连;盐酸小檗碱
黄连,多年生草本植物,是我国传统名贵药材之一,与蒲公英、大蒜、博落回是优良的天然植物源性抗炎药物[1]。黄连中主要成分为小檗碱,结构式如图1,为季铵型生物碱,强碱性生物碱[2],医学上常用盐酸盐,溶于热水和热乙醇,而难溶于氯仿、乙醚等溶剂。黄连作为传统中药材,具有泻火解毒,清热燥湿等功效,具有良好的抗菌[3]、抗病毒[4],降血糖[5],治疗心血管疾病[6]等医用价值。随着研究的深入,临床应用越来越多,高效的提取方法就显的更加重要,传统工艺有酸式提取法[7],石灰乳法提取[8],乙醇回流提取法[9]等传统方法,新的提取技术有二氧化碳超临界流体萃取法[10],微波-索氏联合提取工艺[11],超声波提取[12],酶浸提法[13],液膜法等[14-16]。这些提取工艺有一定的局限性,如耗电量大、消耗溶剂量大、耗时长、操作烦琐、提取率低等。而离子液体双水相体系作为一种新型的、绿色的、温和的、高效的体系,具有双水相体系和离子液体二者的优点,具有体系易于放大、分相时间短、无毒、熔点低、蒸气压小、电化学窗口大、不挥发、液程宽、溶解性强和可设计调节、萃取过程中不易乳化和易回收等优点[16]。Gutowski等[18]于2003年首次提出了离子液体双水相的概念,多年的研究发现,这一体系在很多领域具有很好的应用前景[19-32],作者在本文中利用 [Bmim]BF4/EA- (NH4)2SO4-H2O双水相体系萃取黄连中盐酸小檗碱,探讨了形成这一体系的条件,并进行了萃取的单因素探索,得出了最佳萃取条件,优化了提取工艺, 拟为其工业化应用打下基础。
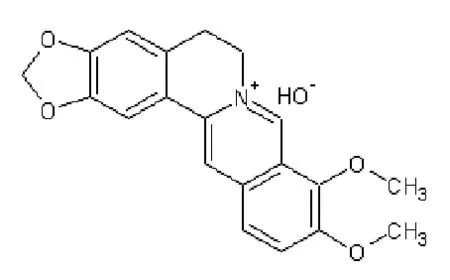
图1 小檗碱结构
1 实验部分
1.1 仪器和试剂
TU-1901双光束紫外可见分光光度计(北京普析通用仪器有限公司),KQ3200E超声波清洗器(昆山市超声仪器有限公司),HH-S型智能恒温水浴锅(巩义市予华仪器有限责任公司),ZN-04AL小型粉碎机(北京兴时利和科技发展有限公司),SHZ-D(Ⅲ)循环水真空泵(郑州市国瑞仪器有限公司),DZR-6020真空干燥箱(上海一恒科学仪器有限公司),CP224C电子天平(奥豪斯仪器(上海)有限公司),SHZ-A水浴恒温振荡摇床(上海龙跃仪器设备有限公司)。
1-丁基-3-甲基咪唑四氟硼酸盐(>99%,中科院兰州化学物理研究所),黄连(益众医药有限公司),盐酸小檗碱标准品(HPLC≥98%,国药集团化学试剂有限公司),乙酸乙酯(天津市凯通化学试剂有限公司),硫酸铵(天津市北精细化工有限公司),无水乙醇(天津市大茂化学试剂厂),丙酮(郑州派尼化学试剂厂),正丙醇(郑州派尼化学试剂厂),异丙醇(津市光复科技发展有限公司),磷酸二氢钠(天津市福晨化工试剂厂),氯化钠(郑州派尼化学试剂厂),浓盐酸(上海建信化工有限公司),氢氧化钠(郑州派尼化学试剂厂),以上试剂未注明均为分析纯,蒸馏水为二次蒸馏水。
1.2 实验方法
1.2.1 标准曲线的绘制
准确称取11.0000 mg盐酸小檗碱标准品于100 mL容量瓶中,用[Bmim]BF4定容,配制浓度为110 μg/mL的储备液,再用移液管吸取25 mL配置好的储备液于250 mL容量瓶中,[Bmim]BF4定容,再分别吸取2 ,4 ,6 ,8 ,11 ,13 ,15 ,17 ,19 ,22 ,25 mL于25 mL容量瓶,[Bmim]BF4定容,得浓度为0.88 ,1.76 ,2.64,3.52,4.84 ,5.72,6.60 ,7.48 ,8.36 ,9.68 ,11 μg/mL的一系列标准品溶液,在最大吸收波长下测定吸光度,以质量浓度为横坐标,吸光度为纵坐标作图。
1.2.2 黄连粗提液的制备和含量的测定
准确称取1.0000 g的黄连粗品(先经60 ℃真空干燥8 h,粉碎后过60目筛)于250 mL烧杯中,加入50 mL无水乙醇,保鲜膜覆盖,60 ℃水浴温浸15 min后超声处理30 min,冷却至室温,抽滤,滤液用盐酸调节pH值2,滤液转移到1000 mL容量瓶中,蒸馏水定容,得黄连粗提液,4 ℃冷藏备用。准确移取0.5 mL粗提液到25 mL容量瓶中,[Bmim]BF4定容并测定其吸光度,由标准曲线测得粗提液中盐酸小檗碱的含量。
1.2.3 双水相体系中有机相、分相盐的选择
在室温条件下,分别考察无水乙醇、丙酮、异丙醇、正丙醇、无水乙醇与正丙醇的混合物(1:1)、[Bmim]BF4与EA的混合物(1:1)六种有机溶剂与三种分相盐(NH4)2SO4、NaCL、NaH2PO4的分相能力,浊点滴定法[33]绘制双水相体系相图。
1.2.4 无机盐质量分数的选择
固定水相及有机相的体积不变,只改变水相中无机盐的质量分数,确定分相时分相盐的质量分数。
1.2.5 双水相萃取
准确移取2.50 mL黄连粗提液,于100 mL比色管中,加入50 mL一定质量分数的无机盐溶液,再加入5 mL有机溶剂,滴加盐酸或氢氧化钠来调节溶液的pH值,摇床上控制某一温度萃取30 min,萃取后静置,待相界面清晰后测量上下相体积,取上相1 mL于25 mL容量瓶中,[Bmim]BF4定容,在最大吸收波长处处测定其吸光度。
根据回归直线方程计算出对应的浓度,计算盐酸小檗碱萃取率,计算公式如下:
相比R=V上:V下
萃取率Y =[M1/M2]× 100 %
V上——表示上相体积;
V下——表示下相体积
M1——表示上相所含盐酸小檗碱的质量。
M2——表示黄连粗提液中盐酸小檗碱的含量。
1.2.6 温度的影响
改变双水相萃取时的温度,按照1.2.5的双水相萃取过程进行实验,其它条件不变。
1.2.7 pH值的影响
改变双水相萃取时的pH值,按照1.2.5的双水相萃取过程进行实验,其它条件不变。
2 结果与讨论
2.1 标准曲线的绘制
盐酸小檗碱在238 nm,261 nm,350.5 nm处有三个吸收峰,[Bmim]BF4与EA的混合液体在350.5nm的吸光度相对较小,因此该实验将检测波长定为350.5 nm,以[Bmim]BF4:EA(1:1)的混合物为参比,在350.5 nm处测定吸光度值,以盐酸小檗碱质量浓度为横坐标,吸光度为纵坐标作图,如图3所示,得线性回归方程y = 0.0446x + 0.0047,R2=0.9948,即盐酸小檗碱的标准曲线方程,结果显示盐酸小檗碱质量浓度在0.88 μg/mL~11 μg/mL内线性关系良好。
2.2 双水相体系的确定

表1 不同体系的分相能力(50 mL饱和盐水溶液)
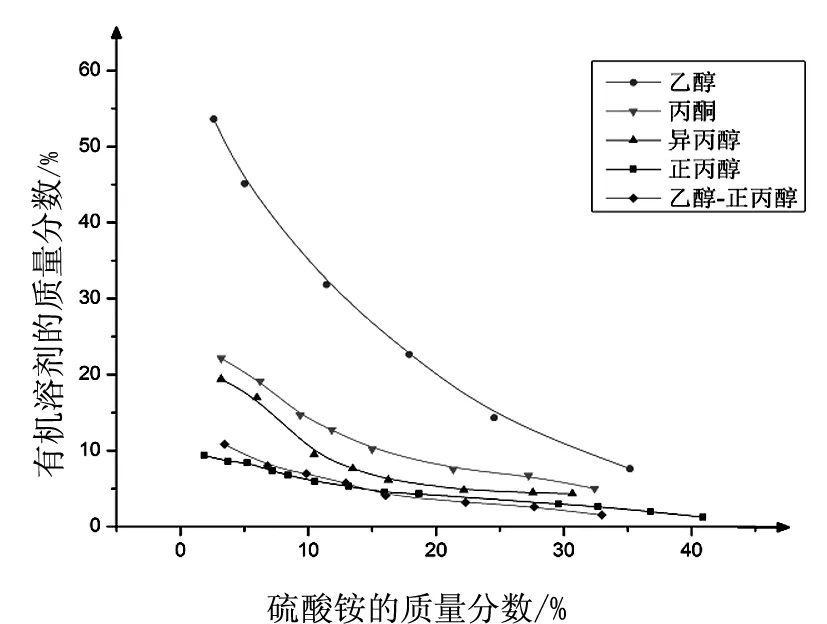
图2 不同的有机溶剂与硫酸铵的相图
Fig.2 the Phase diagram of different organic solvents and (NH4)2SO4
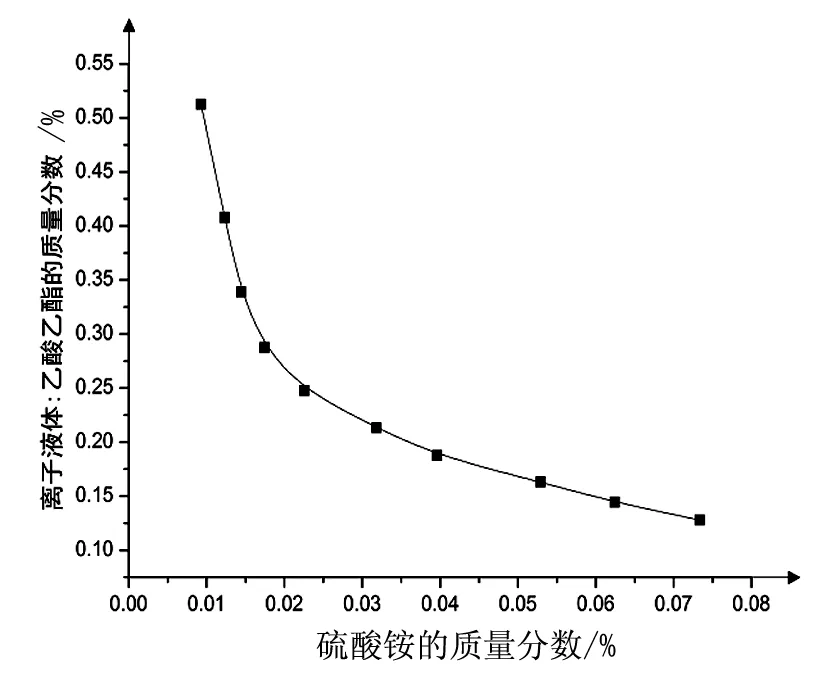
图3 离子液体/乙酸乙酯-硫酸铵-水的相图
在分相盐的选择中,考察了(NH4)2SO4、NaCl、NaH2PO4三种较常用的无机盐,如表1所示,分相最好的是[Bmim]BF4:EA(1:1)与(NH4)2SO4形成的体系,在使用较少的的有机相时,就能形成稳定的双水相体系,而且相界面清晰。因此我们选择[Bmim]BF4:EA(1:1)- (NH4)2SO4-水双水相体系。
图2、3是室温下由浊点法绘制的不同有机溶剂与(NH4)2SO4水溶液的相图,由图2、3可知,有机溶剂分相能力为:[Bmim]BF4:EA(1:1)>正丙醇>乙醇:正丙醇(1:1)>异丙醇>丙酮>乙醇,[Bmim]BF4/EA-(NH4)2SO4-H2O体系表现出比较宽的分相范围,且分相效果最好,且该有机相密度比水小,这一特性可以用于双水相溶剂浮选体系,因此选用[Bmim]BF4:EA(1:1)作为有机相。
2.3 分相盐的质量分数的确定
50 mL水中加入一定质量的(NH4)2SO4,溶解后加入5 mL[Bmim]BF4:EA(1:1),观察分相情况,如表2所示。

表2 同硫酸铵质量分数下的分相情况
由表2可知,硫酸铵浓度过低时,体系不分相,过高时分相明显但是下相会析出盐,不适合盐酸小檗碱的萃取。当硫酸铵质量分数36.7 %时,体系最稳定,因此,确定最佳硫酸铵质量分数为36.7 %。
2.4 萃取体系温度的确定
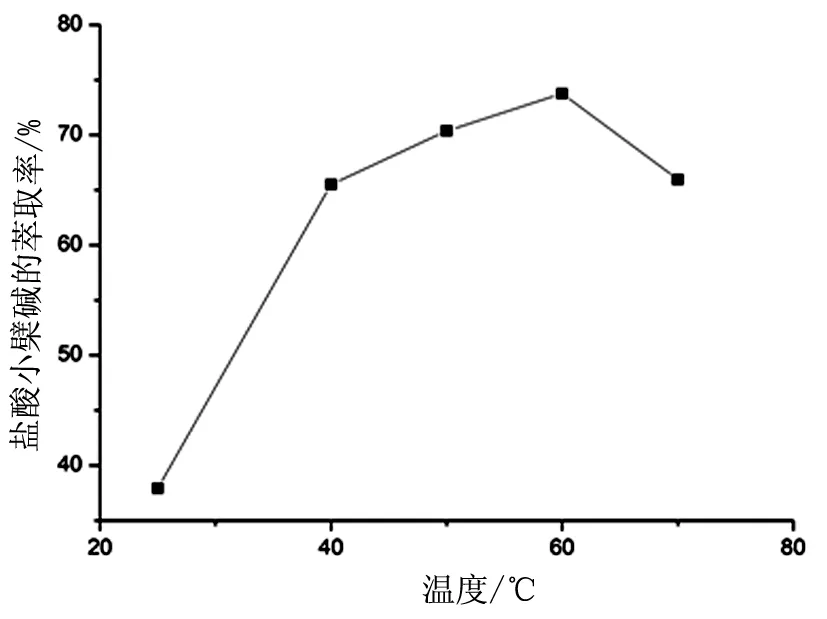
图4 温度对萃取盐酸小檗碱的影响
图4是温度对盐酸小檗碱萃取率的影响,由图4可知,在温度小于60 ℃时,盐酸小檗碱的萃取率随着温度的增加逐渐增加,在温度大于60 ℃时,盐酸小檗碱的萃取率呈下降趋势,这是因为硫酸铵的溶解度随温度的变化所致,体系中盐的质量分数下降致使盐酸小檗碱随着有机相进入水相造成的,另外温度过高盐酸小檗碱的结构也变得不稳定,确定最佳萃取温度为60 ℃。
2.5 萃取体系pH值的确定
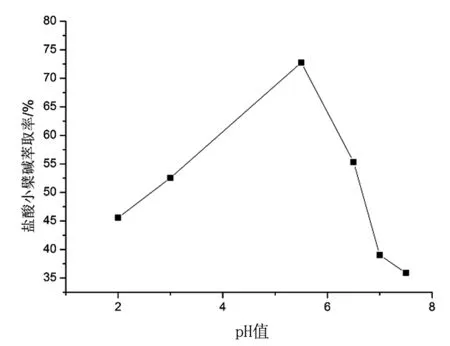
图5 pH值对萃取盐酸小檗碱的影响
图5是pH值对盐酸小檗碱萃取率的影响关系图,由图5可知,随着双水相体系pH值的变大,盐酸小檗碱的萃取率先变大后变小,在pH值约为5.5时,萃取率达到最大,pH值大于5.5时,萃取率迅速下降;这可能是因为小檗碱的盐酸盐在强酸性条件下能够稳定存在,随着pH值的增大,盐酸盐生成易溶于水的游离小檗碱,重新回到水相中,使有机相中盐酸小檗碱的含量下降造成的,因此确定体系最佳pH值为5.5。
3 结论
采用离子液体双水相体系萃取盐酸小檗碱,通过试验及分析对此工艺进行优化,得出最优提取条件为盐质量分数为36.7 %,pH值5.5,温度60 ℃,在此条件下萃取率可达78.89 %。离子液体双水相体系萃取盐酸小檗碱比传统的提取方法在操作方面更为方便,时间更短,提取率更高,因此其具有较好的发展前景。
[1] 李建建,张明军,柳亦松,等.天然植物源性抗炎药物研究概况[J].中兽医医药杂志,2016,16(02):24-26.
[2] 徐怀德.天然产物提取工艺学[M].北京:中国轻工业出版社,2011:305.
[3] 孙 艳,李 娜,陆 颖,等.大蒜素与盐酸小檗碱联用体外抗菌试验[J].中成药,2015,37(12):2589-2595.
[4] 隗 丽,朱美玲,董月柳,等.盐酸小檗碱在黄连水煎液中的生物药剂学分类系统属性研究[J].中国中药杂志,2016,41(7):1192-1197.
[5] 谭学莹,赵林双,胡静波.黄连素的降糖机制及临床应用新进展[J].中国糖尿病杂志,2015,23(12):1131-1133.
[6] 杨 硕,佟 倩.黄连素在心血管疾病中的研究进展[J].中国老年学杂志2016,36(3):1526-1527.
[7] 吕 俊,张鸿雁,蒋文强,等.HPLC法分析优选黄连提取方法[J].山东医药工业,2003,22(4):2-4.
[8] 尹蓉莉,杨军宣,李化.黄柏中盐酸小檗碱提取实验方法的改进[J].基层中药杂志,2000,14(6):27-28.
[9] 武 佳,谭桂莲,杨 红.黄连中盐酸小粟碱提取工艺探究[J].时珍国医国药,2007,18(2):437-438.
[10] 程泓波,刘为为,张少华,等.超临界CO2微乳法制备盐酸小檗碱脂质体工艺的考察与优化[J].安徽医药,2015,19(01):18-22.
[11] 郭锦棠,李雄勇,杨俊红,等.微波-索氏联合工艺提取盐酸小檗碱[J].化工进展,2003,22(12):1338-1341.
[12] 岑志芳,李海燕.不同频率超声提取对川黄柏中盐酸小檗碱提出率的影响[J].时珍国医国药,2005,16(05):374-375.
[13] 梁柏林,周民杰.酶法提取小檗碱工艺研究[J].应用化工,2006,35(5):373-374,378.
[14] 吕宏凌,王保国.液膜分离技术在生化产品提取中的应用进展[J].化工进展,2004,23(7):696-700.
[15] 王大杰,郑 毅,江红梅,等.用液膜法从黄连中提取黄连素的研究[J].成都大学学报(自然科学版),2006,25(4):260-262,266.
[16] 汤 洪,刘利军.液膜法从川黄连中提取黄连素的研究[J].宁夏大学学报(自然科学版),1990,11(1):260-262,266.
[17] 张锁江,吕兴梅.离子液体-从基础研究到工业应用[M].北京:科学出版社,2006:265.
[18] Gutowski KE,Broker GA,Willauer HD,et al.Controlling the aqueous miscibility of ionic liquids: aqueous biphasic systems of water-miscible ionic liquids and water-structuring salts for recycle, metathesis, and separations [J]. J Am Chem Sci,2003,125( 22):6632-6633.
[19] 陈 继,邓岳锋 ,张冬丽. 一种水溶液中离子液体富集工艺:CN,1973943A[P].2006-11-03.
[20] 宋溪明,刘术军,张国林,等. 一种新型离子液体-无机盐-水双水相体系: CN,101016176A[P].2007-08-15.
[21] Soto A,Arce A, Khoshkbarchi M K. Partitioning of antibiotics in a two-liquid phase system formed by water and a room temperature ionic liquid. [J]. Sep Purif Tech, 2005, 44( 3) :242-246.
[22] 刘庆芬,胡雪生,王玉红,等.离子液体双水相萃取分离青霉素[J].科学通报,2005,50(8):756-759.
[23] Liu Q F, Yu J, Li W L, et al. Partitioning behavior of penicillin G in aqueous two phase system formed by ionic liquids and phosphate[J].Sep Sci Technol,2006,41( 12):2849-2858.
[24] Jiang YY, Xia H S, Guo C, et al.[J]. Ind Eng Chem Res, 2007, 46( 19) :6303-6312.
[25] 张建敏,张锁江,陈玉焕,等. 离子液体双水相中抗生素类药物制备分离一体化的新方法:CN,1587240A[P].2005-03-02.
[26] 邓凡政,郭东方.离子液体双水相体系萃取分离牛血清白蛋白[J].分析化学,2006,34(10):1451-1453.
[27] Ruiz-Angel M J, PinoV, Carda-Broch S, et al. Solvent systems for countercurrent chromatography: an aqueous two phase liquid system based on a room temperature ionic liquid[J]. J Chromatogr A, 2007,1151( 1) : 65-73.
[28] Du Z, Yu Y L, Wang J H, et al. Extraction of proteins from biological fluids by use of an Ionic liquid/aqueous two-phase system [J]..Chem Eur J, 2007, 13( 7) : 2130-2137.
[29] 邓凡政,郭东方.离子液体双水相萃取分离苋菜红的研究[J].分析实验室,2007,27(6):15-17.
[30] HE Chiyang, LI Shehong, LIU Huwei, et al. Extraction of testosterone and epitestosterone in human urine using aqueous two-phase systems of ionic liquid and salt[J]. J Chromatogr A, 2005,1082(1):143-149.
[31] Li S H, He CY, Liu H W, et al. Ionic liquid-based aqueous two-phase system,a sample pretreatment procedure prior to highperformance iquid chromatography of opium alkaloids[J].Chromatogr B, 2005, 826( 1~2) :58-62.
[32] 邓凡政,郭东方.芦丁在离子液体双水相中分配性能[J].应用化学,2007,24(7):838-840.
[33] Lu Y, Hao T F, Zhou Y, et al. Aqueous two-phase systems of polyoxyethylene lauryl ether and potassium gluconate/potassium oxalate/potassium citrate at different temperature-experimental results and modeling of (liquid + liquid) equilibrium data [J]. The Journal of Chemical Thermodynamics, 2014, 71(4): 137-147.
ExtractionBerberineHydrochloridefromCoptisbyBmimBF4/EA-(NH4)2SO4-H2OAqueousTwo-PhaseSystem
ZhaoXiaojun,TianGang,LiXinyao,LouWentao,GuoPengpeng,HouYanmin*
(College of Chemistry and environmental Engineering,Pingdingshan University,Pingdingshan 467000,China)
Berberine hydrochloride was extracted from coptis by [Bmim]BF4/EA- (NH4)2SO4-H2O aqueous two-phase system.It were investigated that the type of the solvent and salt,salt concentration,the ATPS of temperature and pH ,which In order to improve extraction rate, Finally, the optimal conditions were obtained: [Bmim]BF4:EA(2.5 mL:2.5 mL)5 mL ,(NH4)2SO4concentration of 38.27 %, temperature 60 ℃, pH 5.5, in this optimal conditions, the extraction rate was 78.89 %. This technology was certain application value for the extraction, separation and purification effective components of coptis. At the same time, it has certain guiding significance for the establishment of ionic liquid aqueous two-phase solvent flotation system.
ionic liquid; ethylacetate; aqueous two-phase extraction; coptis, berberine hydrochloride
2017-08-30
2014年度河南省教育厅科学技术研究重点项目(14B150050)
赵晓军(1979—),学士,讲师,主要研究方向:双水相溶剂浮选;通讯作者:侯延民(1968—),博士,教授,硕士生导师,主要研究方向:双水相溶剂浮选。
R284.2
A
1008-021X(2017)18-0014-04
(本文文献格式赵晓军,田刚,李鑫垚,等.[Bmim]BF4/EA-(NH4)2SO4-H2O双水相体系萃取黄连中盐酸小檗碱[J].山东化工,2017,46(18):14-17.)

