LiH合成反应器的CFD模拟与过程强化
蒋 涛,王丽军
1.中国核电工程有限公司郑州分公司,河南 郑州 450000;2.浙江大学化学工程与生物工程学院,浙江 杭州 310027
LiH合成反应器的CFD模拟与过程强化
蒋 涛1,王丽军2
1.中国核电工程有限公司郑州分公司,河南 郑州 450000;2.浙江大学化学工程与生物工程学院,浙江 杭州 310027
为了强化釜式氢化锂(LiH)合成反应器,采用计算流体力学(CFD)方法模拟了该坩埚反应器在静态操作、机械搅拌和气体鼓泡三种情况下的物质传递、化学反应和流体运动规律。模拟结果表明:自然对流对反应有较大的促进作用,其使LiH脱离反应界面,保证界面处“新鲜”金属Li与氢气的有效接触;另外,自然对流也促使反应器内物料良好混合;机械搅拌虽提高了反应物料的混合状况,但并不显著增加反应界面,过程强化程度有限;气体鼓泡可大幅度增加气液接触面积,反应时间大幅度缩减,是一种优选的LiH合成反应器构型。
氢化锂 釜式反应器 过程强化 计算流体力学
氢化锂是一种高能储氢材料,同时也是一种重要的核材料。氢化锂中氢的密度大于液氢,有希望成为燃料电池氢源[1,2]。氢化锂的中子吸收截面较大,是目前最有效的中子屏蔽材料,可用于空间核能装置的中子辐射屏蔽层[3]。另外,氢化锂的同位素,如氘化锂6是核聚变反应的主要原料。
氢化锂通常采用金属锂与氢气直接化合方法制备,反应条件比较苛刻,已有文献系统论述了氢化锂的制备方法,性质及用途[4]。廖世健等[5]在 25~50 ℃、常压的温和条件下,将金属锂和氢气在萘基衍生物和TiCl4催化下合成氢化锂。Howie等[6]在室温和50 MPa高压条件下的金刚石模具中合成氢化锂,所得产物化学稳定性较高。王宝明[7]等系统研究了金属锂吸氢速率与温度的关系,通过X射线衍射分析考察了杂质分布,获得了反应的最佳操作条件。Towndrow[8]提出一种合成氢化锂粉末的方法,并利用该粉末制备出不同几何形状的氢化锂器件。Napan等[9]和Lee等[10]利用从头计算法模拟了氢化锂的电子云分布,定量描述了锂和氢的反应能垒以及原子间的价键形式。综上所述,氢化锂合成的文献目前主要集中于化学反应特性的研究,对反应器及其反应过程中物料的“三传一反”规律鲜于见诸描述,缺乏系统研究。LiH合成过程涉及三个步骤,包括金属Li的提纯、Li与氢气反应、LiH冷却结晶与固化,其中合成反应是整个工艺的关键。Li与氢气反应生成的产物易于分解,且Li极为活泼,与氮气和氧气均可发生反应,反应一般在氩气或临氢条件下进行加氢。氢化锂合成反应过程涉及多相、变密度、强放热等复杂物理过程,本工作将利用计算流体力学方法对氢化锂合成反应器内物质传递、化学反应和流体运动进行深入研究,并以过程强化为目标,筛选反应器构型。
1 氢化锂合成反应器概述
现有LiH合成装置为静态坩埚,金属Li填充在坩埚内,升高温度后Li融化为液体,氢气由釜顶部引入,在气液界面处,金属Li与H2反应生成LiH产物,如图1所示。坩埚体积为8.6 L,有效体积5.74 L,底部直径105 mm,顶部直径175 mm,高550 mm。
LiH的沸点较高,因而反应过程中必须保持一定的温度(>700 ℃)以防止LiH在气液界面附近固化。LiH密度较大,会不断沉降到坩埚的底部,未反应的金属Li更新至气液界面,与氢气反应。反应结束后,温度自然降低,产物开始硬化结晶,冷却过程中保持一定氢气压力,以防止LiH发生分解反应。相关物性参数(反应温度725 ℃)示于表1。
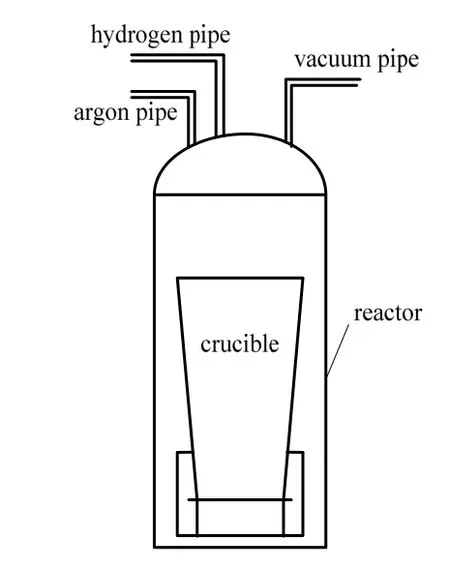
图1. LiH合成反应装置Fig.1 Synthetic reactor of LiH

表1 反应物性参数Table 1 Parameters of reactant properties
现有LiH合成装置的主要问题在于:气液界面较小,导致氢气的吸收速率不够,影响了合成效率;另外,自然对流促进流体混合和表面更新强度较低,LiH大量富集在气液界面,底部金属 Li未反应完全,本论文通过模拟机械搅拌和气体鼓泡,研究强制对流状态下LiH合成反应过程,提出新型高效的反应装置构型。
2 CFD数学模型
LiH合成涉及多个物理-化学过程,模拟的关键在于能够实时跟踪气液界面,掌握反应发生场所变化,本论文拟采用Fulent-VOF模型对该反应过程进行模拟。
2.1 流体力学本构方程
利用Navier-Stokes方程计算反应过程中的流场,然后求解反应-扩散方程获得组分浓度场,将反应与流动两类方程耦合联立求解[11]。

其中ρ为密度,kg/m3;u为速度,m/s;τ为粘度应力,N/m3;F为作用力,N/m3。
方程(1)~(3)适用于静态、搅拌和鼓泡反应器,三者不同之处主要体现为气液界面的处理方法不同。边界条件在壁面为无滑移边界,气液表面为压力边界。
首先计算出Li和LiH在液体中的浓度,得到液体密度和粘度数值,再带入运动方程求解流体速度,流体速度的改变反过来又影响了反应进程。氢化锂合成反应的速率r通过工业运行数据回归确定,得到排除扩散作用的动力学方程:

其中,r为反应速率,mol/(m3·s);PH2为氢气分压,Pa;Li为金属Li的质量分数;R为理想气体常数,J/(mol·K);T绝对温度,K;Di为扩散系数,m2/s。
氢气在液相Li中扩散系数根据Stocks-Einstein方程估算DH2为1.3×10-8m2/s。
2.2 界面跟踪
界面是反应发生的场所,需要实时跟踪和捕捉。拟采用流体体积分数法(VOF)[12]跟踪界面位置,VOF方法通过网格单元中流体和网格体积比函数(F)来确定自由面,追踪流体变化。若F为1,则该单元全部为液相流体所占据,若F为0,则该单元为气相流体单元,F在0与1之间时,则该单元为气液相界面所占据。
图2分别给出了现有静态反应装置及气体鼓泡装置内的气液分布情况,现有反应装置为静态反应器,液体处于反应器下部,反应发生在气液接触面处;气体鼓泡的情况比较复杂,气液接触面包含大量气泡,气泡呈一定尺寸大小分布,浮升过程中发生聚并和破碎,准确计算反应过程需要实时跟踪每一个气泡。

图2 气液界面Fig.2 Interface of gas-liquid phases

图3 网格划分及动网格Fig.3 Meshing configuration
2.3 网格的划分
LiH合成反应装置内的气液界面及网格划分如图3所示,整个反应装置布置于六面体网格系统内,流体流动控制方程在计算网格上离散,即将偏微分形式的流动控制方程转化为计算节点上的代数方程组。最后,通过求解大型代数方程组,得到流场变量的离散解。采用带搅拌桨的反应装置,流场的形状随边界运动而改变,必须预先定义初始网格、使用动网格技术自动更新每个迭代步中边界的变化,采用的方法为跟踪搅拌桨的空间位置,计算搅拌桨与网格的几何交错面,在六面体网格内移除交错面,并在运动方程中考虑边界运动的影响,动网格设置在Fluent软件内实现。网格划分为10万~30万个,并通过网格无关性检验。单个计算任务运行24 h,完成物理模拟时间500 s以上。
3 结果与讨论
采用上述计算方法对 LiH三种反应器构型进行模拟:现有静态反应器、带机械搅拌反应器、气体鼓泡式反应器。考察反应过程中流体运动与组分浓度变化规律,并针对该反应过程提出过程强化的措施。
3.1 静态坩埚反应器模拟
现有LiH合成装置为静态坩埚,反应原料Li在坩埚的下部,顶部通入氢气,并保持恒定的压力。反应主要发生在液相,反应过程中液相组成变化及其运动规律示于图4(a)~图4(e)。图中可以看到,产物LiH比金属Li具有更大的密度,在气液界面处生成的LiH由于重力作用而发生自然流动沉降到反应容器底部。自然对流对LiH合成过程有重要影响,一方面由于对流使得LiH脱离气液界面,促使界面处“新鲜”的金属 Li与氢气的接触;另一方面自然对流使反应器内物料运动,实现更好的混合,避免了死区等不良状况的发生。
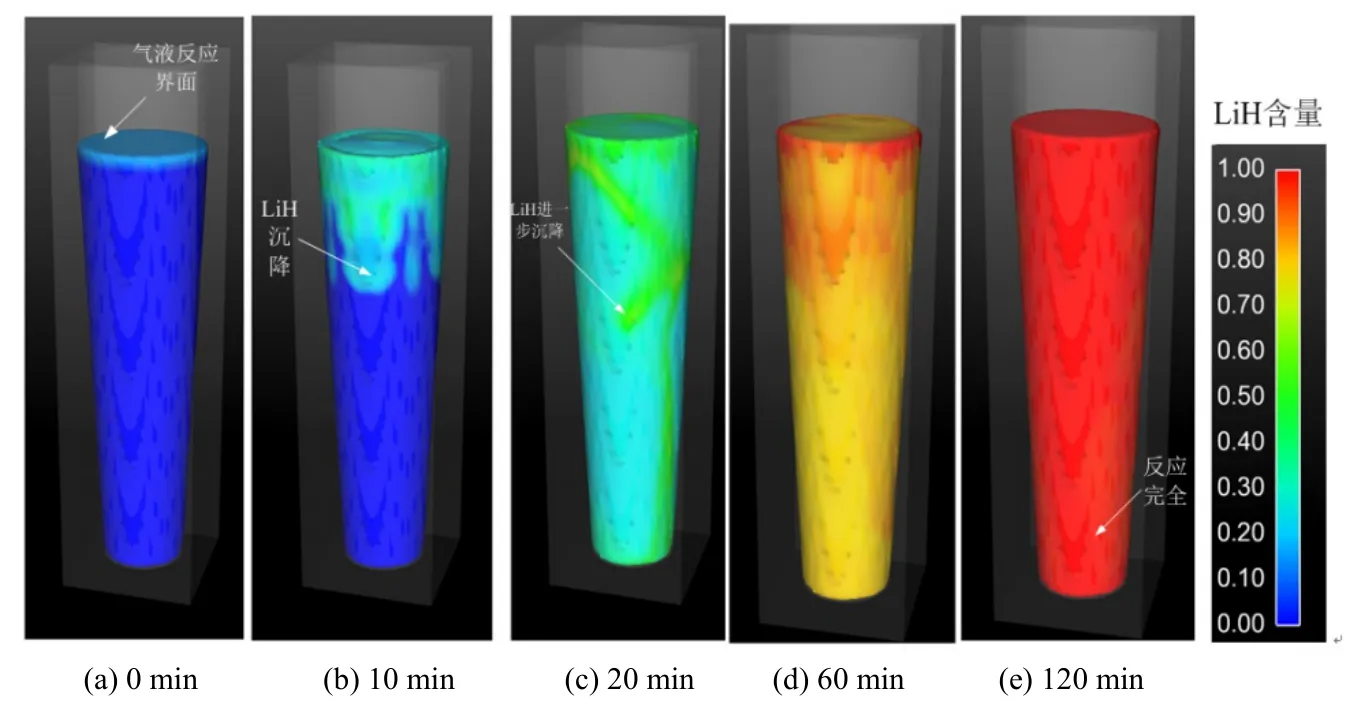
图4 合成装置内LiH浓度分布及变化规律Fig.4 Concentration distribution of LiH in synthetic reactor
如图4所示,反应初始阶段,LiH主要集中在气液界面附件,浓度较低;随着反应的进行,LiH含量提高,气液界面(上部)的密度大于底部,自然对流发生;反应中期,LiH依靠重力沉降到容器的下部;反应后期,随着氢化率的提高,密度差降低,自然对流运动下降,反应速率降低,该阶段需要的反应时间最长;反应终止时,金属Li基本反应完全。
3.2 机械搅拌式反应器模拟
机械搅拌是过程强化的有效手段,LiH合成的反应物系粘度较高,适合使用慢速搅拌桨,选用螺带桨构型,如图3所示。搅拌转速为5 r/min,机械搅拌下模拟得到反应过程中液相组成变化示于图5。由图5可见,由于离心力的作用,液体趋于向容器壁运动,周向的液位较高,另外螺带的迎风面的液体液位较高,而背风面的较低,液位起伏较大。与图4比较,机械搅拌虽提高了反应物料的混合程度,但抑制了自然对流,不能显著增加反应界面,过程强化程度有限,反应所需时间没有明显降低。
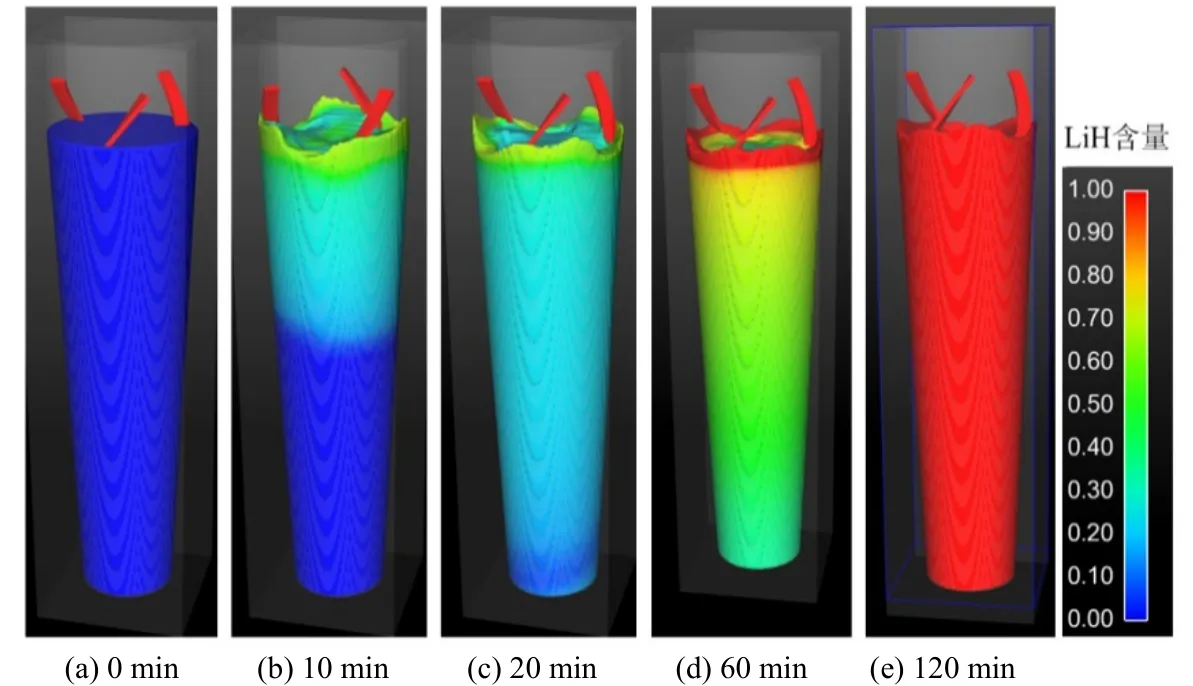
图5 机械搅拌反应器内LiH浓度分布及变化规律Fig.5 Concentration distribution of LiH in mechanical stirring reactor
3.3 气体鼓泡式反应器模拟
按照化学计量关系计算出的氢气用量中60%通过鼓泡通入反应器,40%由反应器上部引入,模拟得到反应过程中LiH浓度虽时间变化规律示于图6。进一步,反应器中轴截面处LiH组分浓度随时间变化如图7所示。

图6 鼓泡反应器内LiH浓度分布及变化规律Fig.6 Concentration distribution of LiH in bubbling reactor

图7 鼓泡反应器中轴截面处LiH浓度分布及变化规律Fig.7 Cross – section concentration of LiH in bubbling reactor
采用VOF方法跟踪每一个气泡浮升过程,研究气液接触面积的变化和界面更新情况。与现有反应器比较,不仅在上部气液界面处发生化学反应,而且在每一个气泡的界面也有反应发生,反应表面的增加使反应时间大幅度缩减。三种反应器的进一步比较示于图 8,图中可以看到,在三类反应器中,反应均呈现前期快,后期慢的特征,这主要是由于前期金属Li浓度高的缘故。三者比较,鼓泡反应器的反应效率最高,搅拌和现有静态反应器反应效率相当,反应较慢。在保持反应器基本形状不变条件下,以强化反应速率为目标适宜选用鼓泡反应装置。

图8 反应器效率的比较Fig.8 Reactor efficiency comparison
4 结 论
采用跟踪气液界面的VOF流体力学方法模拟了氢化锂合成反应器内流体运动和化学反应过程,考察了现有静态反应器、机械搅拌反应器、气体鼓泡式反应器内的反应速率和组分浓度分布。模拟表明,由于产物LiH比金属Li具有更大密度,现有静态反应器内发生强烈自然对流,促使了界面处“新鲜”的金属 Li与氢气的接触,强化了反应器内物料更好的混合。机械搅拌虽改善反应物料的混合,由于不能显著增加反应界面,与静态反应器比较没有明显优势。气体鼓泡式反应器是一种理想的LiH合成反应器类型,鼓泡强化了液体搅动和增大气液表面积,有利于反应过程强化。
[1]Rusman N A A, Dahari M. A review on the current progress of metal hydrides material for solid-state hydrogen storage application [J].Int J Hydrogen Energy, 2016, 41(28):12108-12126.
[2]Kong V C Y, Foulkes F R, Kirk D W, et al. Development of hydrogen storage for fuel cell generators [J]. Int J Hydrogen Energy, 1999,34(2):554-564.
[3]Zakirov V, Pavshook V. Russian nuclear rocket engine design for mars exploration [J]. Tsinghua Science and Technology, 2007,12(3):256-260.
[4]中国科学院原子核科学委员会,《氢化锂调研报告》 [R]. 北京, 1961.
[5]廖世健, 孔 巍, 刘和众, 等. 温和条件下氢化锂的催化合成 [J]. 化学学报, 1985, 43(8):752-756.Liao Shijian, Kong Wei, Liu Hezhong, et al. Catalyzed synthesis of LiH under mild conditions [J]. Journal of Chemical Industry and Engineering, 1985, 43(6):752-756.
[6]Howie R T, Narygina O, Guillaume C L, et al. High-pressure synthesis of lithium hydride [J]. Phys Rev B, 2012, 86(5):064108-1:8.
[7]王宝明, 张建东, 王力军. 氢化法制备氢化锂的工艺研究 [J]. 稀有金属, 2010, 34(8):786-790.Wang Baoming, Zhang Jiangdong, Wang Lijjun. Preparation of lithium hydride by hydrogenation [J]. Chinese Journal of Rare Metal,2010, 34(2):786-790.
[8]Towndrow P. Fabrication and handling aspects of highly reactive powders [J]. Powder Technol, 2007, 174(1):38-41.
[9]Napan R, Blanca E L P Y. First-principles studies of lithium hydride series for hydrogen storage [J]. Int J Hydrogen Energy, 2012,37(7):5784-5789.
[10]Lee B K, Stout J M, Dykstra C E. Ab initio calculations of lithium hydride [J]. J Mol Struct, 1997, 400(1):57-68.
[11]章梓雄, 董曾南. 粘性流体力学 [M]. 清华大学出版社, 2011:39-41.
[12]Guan X P, Li Z Q, Wang L J, et al. CFD simulation of bubble dynamics in bubble columns with internals [J]. Ind Eng Chem Res, 2014,53(4):16529-16538.
CFD Simulation and Process Intensification of LiH Synthesis Reactor
Jiang Tao1, Wang Lijun2
1. China Nuclear Power Engineering Company Limited, Zhengzhou Branch, Zhengzhou 45000, China;2. College of Chemical and Biological Engineering, Zhejiang University, Hangzhou 310027, China
In order to strength the Lithium Hydride (LiH) synthesis reactor, the material transfer, chemical reaction and fluid motion of the crucible reactor were simulated by the method of computing fluid dynamics(CFD) in static operation, mechanical stirring and gas bubbling. Simulation results showed that natural convection had a great effect on the chemical reaction which made LiH out of reaction interface and ensured the efficient contact between the “fresh” metal Lithium (Li) and the hydrogen at the interface. In addition,natural convection also facilitated good mixing of the materials in the reactor. Although the mechanical stirring increased the mixing of the reaction materials, but did not significantly increase the reaction interface,hence the degree of the process strengthening was limited. Gas bubbling can greatly increase the gas-liquid contact area and the reaction time was greatly reduced. Therefore, bubble reactor is a preferred LiH synthesis reactor configuration.
lithium hydride; tank reactor; process intensification; computing fluid dynamics
TQ021.4; TQ051
A
1001—7631 ( 2017 ) 03—0215—06
10.11730/j.issn.1001-7631.2017.03.0215.06
2017-04-14;
2017-05-29。
蒋 涛(1979—),男,高级工程师;王丽军(1976—),男,副研究员,通讯联系人。E-mail:wang_lijun@zju.edu.cn。

