基于上转换荧光共振能量转移的Hg2+侧流检测 模型的设计和应用
毕 畅, 迟丝雨, 李 贞
(1.生物医学分析化学教育部重点实验室,武汉大学化学与分子科学学院,湖北武汉 430072)
汞污染是一个严重的全球性问题,人类活动如矿石开采、垃圾焚烧、石油燃烧和化工生产等是造成无机汞过量排放的主要原因[1]。被释放出的单质汞蒸气通过大气扩散至各个地区,最终氧化为Hg2+,在植物、顶层土壤和水体中累积。部分土壤中的Hg2+会被土壤、水体甚至鱼类中的原核生物吸收,将无机汞转化为有机汞,在食物链中不断累积,对动植物的生命健康造成威胁[2]。
传统Hg2+定量检测手段一般包括原子吸收光谱法[3]、原子荧光光谱法[4]和气相色谱法[5]。这类方法均要求复杂的仪器和繁琐的样品处理过程,不利于对样品的快速和及时检测。纸基检测装置(PADs)具有造价低廉、方便携带和容易操作的特点,因此该检测装置非常适合实地、定点快速检测样品[6]。上转换纳米材料(UCNPs)具有近红外光激发,反斯托克斯位移荧光的特点,可以解决纸基内部荧光剂等物质产生的背景干扰问题[7]。将UCNPs作为能量供体应用于纸基检测装置,利用Hg2+可以使DNA的T碱基发生错配的性质[8],改变荧光共振能量转移(FRET)过程中的供受体距离,这是一种快速、简便的检测方法。
目前,已经有一系列利用较强的T-Hg2+-T作用力检测Hg2+工作的报道[9 - 11]。本文利用Hg2+诱导的T碱基错配,设计Hg2+适配体为识别分子,以金纳米粒子(AuNPs)为能量受体,构建上转换荧光共振能量转移(UC-FRET)纸基侧流检测模型。利用AuNPs在检测区的富集信号和相机收集的荧光信号,分别实现对Hg2+高灵敏的定性、定量分析,完成对样品中Hg2+的实地、裸眼可视化检测。
1 实验部分
1.1 仪器及试剂
LOS-BLD-0980-1.3 980 nm半导体近红外激光器(中国海特光电有限责任公司);RF-5301PC荧光分光光度计(日本,岛津公司);Zeiss SIGMA FESEM扫描电子显微镜(德国,Carl Zeiss 公司);UV-2550紫外/可见分光光度计(日本,岛津公司);Legend Micro 17R高速冷冻离心机(美国,Thermo Scientific 公司);Sartorius cn140硝化纤维(NC)膜、DB-6卡式底板、NJ-Y1样品垫、H5015吸收垫(中国杰一生物技术有限公司)。
Y2O3、Er2O3、Yb2O3(高纯试剂,上海国药集团);十八烯(分析纯,上海阿拉丁工业公司);一缩二乙二醇(分析纯,上海国药集团);聚丙烯酸(优级纯,Sigma-Aldrich);HAuCl4(分析纯,上海国药集团);三(2-羧乙基)膦(TCEP)(生化纯,萨恩化学技术有限公司);Hg2+适配体、Hg2+适配体互补链、延长序列互补链(生化纯,生工生物工程股份有限公司);链霉亲和素(生化纯,北京百灵威科技股份有限公司)。
1.2 夹心结构上转换纳米材料(SWUCNPs)的合成和修饰
根据文献报道方法[12 - 13]合成PAA修饰的夹心结构UCNPs(SWUCNPs):NaYF4∶Yb@NaYF4∶Yb,Er@NaYF4∶Yb。
1.3 AuNPs的合成与标记
以三柠檬酸钠为配体,合成AuNPs[14]。将50 mL 1 mmol/L HAuCl4加热至120 ℃回流,迅速注入5 mL 38.8 mmol/L柠檬酸三钠,待溶液逐渐变为血红色后,回流15 min。冷却至室温后,用0.22 μm无菌过滤器将溶液过滤,在4 ℃下储存。将231 μL 20 nmol/L TCEP加入至100 μmol/L 46.2 μL的M1溶液中(Tris-HCl缓冲溶液,pH=7.4)。避光、室温条件下孵化1 h。将混合溶液注入到10 mL AuNPs溶液中,避光室温搅拌16 h。向混合物中缓慢滴加2 mol/L NaCl 溶液,直至其浓度为0.05 mol/L。之后,继续避光搅拌24 h。在4 ℃、12 000 r/min条件下冷冻离心20 min。收集沉淀,并利用10 mmol/L Tris-HCl缓冲溶液(pH=7.4)洗涤沉淀2次。最后将收集到的M1-AuNPs分散在5 mL 10 mmol/L Tris-HCl缓冲溶液(pH=7.4)中。
1.4 UC-AuNPs侧流模型试纸条的构建
将样品垫、NC膜、吸水垫三部分依次粘贴于PVC垫板上,每部分与前一部分重叠2 mm。试纸条宽度为0.5 cm,总长6 cm:样品垫1.5 cm,NC膜 2.5 cm,吸水垫2 cm。再其上划定检测区(T)和参比区(C),两者区域直径均为3 mm,两者相隔1 cm。
利用亲和素-生物素反应[15],将单链DNA固定于检测区(T)和参比区(C)。为固定目标物检测适配体(M2)和延长序列互补链(C1),将5 μL 1 mg/mL 链霉亲和素溶液(10 mmol/L 磷酸盐缓冲溶液(PBS,pH=7.4)与35 μL 5 μmol/L生物素修饰DNA混合,避光条件下室温反应2 h后,6 000 r/min条件下离心20 min,将沉淀物分散在40 μL 10 mmol/L PBS(pH=7.4)中,在4 ℃下避光保存。在T区、C区分别固定经过生物反应后的5 μL M2和1 μL C1。在两区内各滴加1 μL 1.6 mg/mL SWUCNP和1%BSA溶液。最后,试纸条在37 ℃下烘干3 h,至表面完全干燥后,在4 ℃下储存。
1.5 UC-FRET侧流检测试纸条在缓冲体系中检测Hg2+的应用
利用pH=7.4的10 mmol/L Tris-HCl缓冲溶液(含100 mmol/L NaCl、1.75 mmol/L Mg2+、0.1%BSA和8%SDS),配制一系列Hg2+标准溶液(0、0.1、0.5、1、5、10、50、100、1 000 nmol/L)。将15 μL标记了M1的AuNPs提前负载在样品垫上,静置1 min。将40 μL待测溶液加在样品垫上,使其缓慢流过T区、C区。待检测样品完全流经整个试纸条后,用30 μL配制标准溶液的缓冲溶液洗涤试纸条两次。观察洗涤后的AuNPs在T区、C区富集程度,可判断Hg2+的存在,大致判断其浓度范围。将其放入烘箱,于37 ℃烘干30 min。待其表面完全干燥后,在暗室内,使用980 nm 激光激发T、C区荧光。使用相机记录荧光情况,并用Photoshop软件,读取RGB绿色通道内的荧光值,判断样品中Hg2+的含量。
考察该UC-FRET LFAs的选择性时,使用干扰物(Ca2+、Mg2+、Pb2+、Ni2+、Cu2+和Mn2+溶液)代替Hg2+为样品溶液,操作步骤同上。
2 结果与讨论
2.1 UC-AuNPs侧流模型构建原理
UCNPs-AuNPs适配体侧流试纸条的检测原理如图1。利用Hg2+可以导致T碱基错配的性质,设计两条T碱基丰富的单链DNA作为Hg2+适配体M1、M2。M1除含T碱基丰富链,还附加一段延长序列且5′端用巯基修饰,与AuNPs偶联,作为Hg2+识别部分。M2为只含T碱基的单链DNA,作为Hg2+适配体互补链,与UCNPs负载于检测区(T)。M1链上的延长序列互补链(C1)与UCNPs负载于C区,作为信号参考。在Hg2+存在条件下,AuNPs-M1与T区的M2配对,AuNPs富集于T区,形成信号,可利用比色法评估其浓度;同时,该富集行为拉近AuNPs与UCNPs距离,使FRET得以发生,由此猝灭UCNPs的荧光,通过荧光猝灭情况可判断Hg2+浓度。

图1 UCNPs-AuNPs适配体侧流试纸条的检测原理图Fig.1 Schematic illustration of the UCNPs-AuNPs aptamer lateral flow sensor.M1:Hg2+ aptamer with extended sequence(5′-SH-TTTTTTTTTTTCTGTCGGATGAG-3′);M2:Complementary strand for Hg2+ aptamer(5′-Biotin-TTTTTTTTTT-3′);C1:Complementary strand for extended sequence(5′-Biotin-CTCATCCGACAGC-3′)
2.2 SWUCNPs与AuNPs的表征
SWUCNPs利用层层种子介导方式进行合成。通过透射电镜图(图2)可以证明,经过层层组装后,UCNPs的晶像并未发生改变;每层的粒径大小比较均一。

图2 SWUCNPs的透射电镜(TEM)图。a.NaYF4内核;b.NaYF4@NaYF4∶Yb,Er核-内壳结构;c.NaYF4@NaYF4∶Yb,Er@NaYF4夹心结构Fig.2 TEM images of a.NaYF4;b.NaYF4@NaYF4∶Yb,Er;c.NaYF4@NaYF4∶Yb,Er@NaYF4
依据柠檬酸还原法,制备粒径在10~20 nm的AuNPs。根据图3,利用文献报道方法[16]计算,AuNPs的粒径为15 nm,浓度为6.93 nmol/L。AuNPs与M1的偶联通过Au-S键固定。根据图3(a)可见:AuNPs与M1偶联后,在520 nm处的等离子共振吸收峰有轻微红移,证明M1已成功修饰于AuNPs的表面。

图3 (a)AuNPs与AuNPs-M1的紫外-可见吸收光谱图;(b)UCNPs的荧光光谱图Fig.3 (a)UV-Vis absorption spectra of AuNPs and AuNPs-M1;(b)Fluorescence spectrum of UCNPs
2.3 UC-AuNPs侧流模型检测缓冲体系中的Hg2+
在样品垫上负载15 μL AuNPs-M1溶液,静置1 min,再负载50 μL Hg2+标准溶液。利用Photoshop的RGB格式提取绿光强度,可计算荧光的猝灭效率:(F0-F)/F0(F0:不加样品时,区域内的荧光强度;F:加入样品后,区域内的荧光强度)。
如图4(a),样品浓度在0.1~100 nmol/L范围内,Hg2+浓度的对数与T区荧光猝灭效率存在线性关系。检出限可达到0.1 nmol/L。该检出限低于目前文献报道的Hg2+侧流检测试纸条。在该浓度下,T区的荧光猝灭效率达到29.6%。这种对低浓度目标物的灵敏相应,可能来自于利用SWUCNPs构建的FRET体系。SWUCNPs的发光中心均集中于夹心结构的中间层,与能量受体的距离较近,因此FRET效率很高。C区(如图4(b))的荧光猝灭效率受Hg2+影响较小,在23.5%~37.8%之间。利用AuNPs在T区的富集而产生的颜色变化,可以利用比色法,粗略判断Hg2+浓度。如图4(c)所示,随Hg2+的浓度增加,T区的AuNPs颜色明显变深。
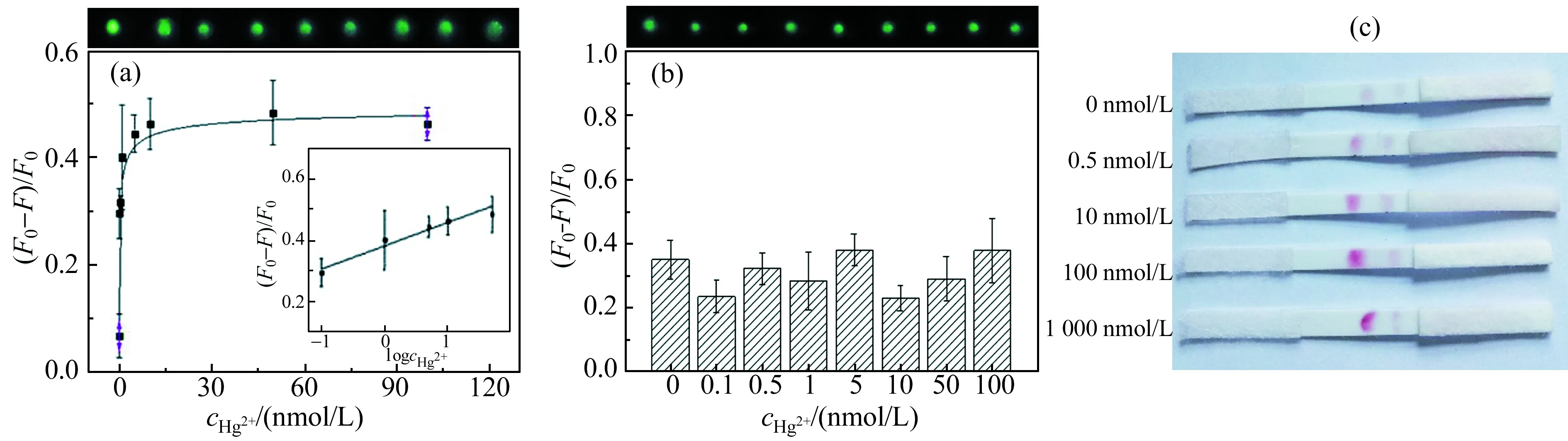
图4 不同Hg2+浓度下检测区(a)的猝灭效率以及参比区(b)和AuNPs在检测区、参比区的富集情况(c)Fig.4 The quenching efficiencyin of testing area(a) and reference area(b) and gathering of AuNPs in testing area and reference area (c) at different concentration of Hg2+

图5 SWUCNPs-AuNPs侧流检测试纸条的选择性考察Fig.5 The selectivity of SWUCNPs-AuNPs lateral flow sensor
为了考察该试纸条对Hg2+的选择性,本实验选择水体中可能存在的其它金属离子(Ca2+、Mg2+、Ni2+、Pb2+、Mn2+、Cu2+)与Hg2+进行对照试验。如图5所示,只有样品中含有Hg2+时,T区才存在明显的荧光猝灭,干扰物对检测所产生的影响很小。因此该试纸条针对样品中常见的金属离子具有良好选择性。Hg2+所用浓度为1 μmol/L,其余离子浓度均为10 μmol/L。
2.4 SWUCNPs-AuNPs侧流试纸条检测自来水中Hg2+
为考察SWUCNPs-AuNPs试纸条的检测能力,我们将该试纸条应用在实验室自来水中的Hg2+浓度检测上。由于自来水中的部分杂质可能对试纸条表面造成非特异性吸附,我们将自来水样品用10 mmol/L Tris-HCl缓冲溶液(含100 mmol/L NaCl、1.75 mmol/L Mg2+、0.1%BSA和8%SSC)将样品稀释至原浓度的0.6倍。测得自来水中的Hg2+浓度为0.14 nmol/L,同时我们利用标准加入法考察结果的可靠性,结果见表1。

表1 UC-FRET侧流检测试纸条确定自来水中Hg2+浓度Table 1 Detection of Hg2+ Concentration in tap water using SWUCNPs-AuNPs based lateral strips
2.5 结果讨论
现已报道的利用DNA适配体构建Hg2+固相荧光方法检测的FRET模型,对于目标物的检出限为2.8 nmol/L[17]。本文采用了两类纳米粒子上转换荧光材料和金纳米粒子作为能量供受体,提高FRET体系相应灵敏度,将其检出限降低至0.1 nmol/L。但由于纳米粒子之间的能量转移效率有限,最大只可达到60%,相较文献报道[18 - 19],UCNPs荧光猝灭效率较低,该模型线性范围较窄(0.1~100 nmol/L)。后续实验将通过调节能量受体金纳米粒子的尺寸以及上转换荧光材料的核壳结构方面,提高FRET效率,获得更大的目标物相应线性范围。
3 结论
本实验以AuNPs为能量受体,构建了以UCNPs为能量供体的UC-FRET侧流检测模型。将该模型应用于Hg2+的检测,证实了该侧流模型的可行性和SWUCNPs-AuNPs对目标物的高灵敏响应。该模型对Hg2+的响应具有较好的选择性,实现了目标物的可视化检测。在实地检测中,可以利用比色法快速半定量判断水样中Hg2+浓度;经过烘干处理后,可利用检测区荧光变化情况可准确判断Hg2+浓度。

