急性胸痛2例报道
袁 音, 黄 峰, 李 峰, 林 帆, 朱鹏立
急性胸痛2例报道
袁 音, 黄 峰, 李 峰, 林 帆, 朱鹏立
胸痛; 肺栓塞; 主动脉疾病
胸痛是急诊常见的一种急危症,其中致死性胸痛可严重威胁患者生命,如急性冠状动脉综合征(acute coronary syndromes, ACS)、主动脉夹层及肺动脉栓塞等造成的胸痛。如何快速诊断,避免误诊和漏诊,并进行及时救治,从而改善患者的预后,是胸痛诊疗的难点和重点。笔者科室于2016年收治胸痛患者2例,现回顾性分析其临床资料,并探讨胸痛的诊疗体会,报道如下。
1 病例介绍
1.1 病例1 患者,女性,71岁,因胸闷、气促2 d,胸痛11 h就诊于急诊科。入院前2 d,无明显诱因出现胸闷,伴活动后气促,夜间高枕卧位。入院前11 h晨起突发心前区刀割样痛,伴呼吸困难、濒死感,无咯血、晕厥。查体:体温36.3 ℃,脉搏107 min-1,血压104/67 mmHg(1 mmHg=133.3 Pa),血氧饱和度87%(吸入氧浓度21%)。神志清楚,口唇轻度紫绀,颈静脉充盈。双下肺可闻及湿啰音。心律齐,未及杂音。腹软,无压痛。双下肢无浮肿。既往有原发性高血压病史。入院前17 d曾于长途飞行后出现胸痛,查肌钙蛋白Ⅰ(cardiac troponin Ⅰ,cTnⅠ)为0.68 ng/mL,拟诊ACS收住院,冠状动脉造影示前降支中段弥漫性狭窄40%,前降支近端收缩期狭窄40%~50%、舒张期狭窄20%~30%。出院后不规律服用波立维及倍他乐克。曾有右下肢肿痛病史,行走后明显,于美国行局部理疗(具体不详)。患者入急诊抢救室后,辅助检查结果显示:cTnⅠ 0.09 ng/mL;N端前脑钠素(N-terminal pro-brain natriuretic peptide, NT-proBNP)2 147 pg/mL;血凝全套:纤维蛋白降解产物(fibrin degradation products, FDP)20.1 μg/mL,D-二聚体5.73 μg/mL,余未见异常;血气分析:吸入氧浓度21%,pH 7.42,血二氧化碳分压26.4 mmHg,血氧分压44.7 mmHg,乳酸3.9 mmol/L;心电图见图1。初步诊断:胸痛待查,ACS可能,Ⅰ型呼吸衰竭,原发性高血压病。治疗上双路给氧,扩容补液,去甲肾上腺素0.3 μg·kg-1·min-1升压,阿司匹林及氯吡格雷双联抗血小板,法安明抗凝,立普妥调脂稳定斑块。治疗后患者氧合情况未改善,因循环不稳定,逐渐增加去甲肾上腺素用量。4 h后复查cTnⅠ为0.87 ng/mL,NT-proBNP为10 386 pg/mL。进一步行肺动脉CT血管造影(CT angiography, CTA),示多发肺动脉栓塞(右上肺动脉、右肺中叶动脉近段及右下肺动脉干内多发充盈缺损,部分仅见细线样显影;左肺上叶动脉、左下肺动脉干及左肺下叶各基底段动脉内不同程度充盈缺损影)(图2)。诊断:急性肺动脉栓塞(高危)。收住院后立即给予溶栓、抗凝以及无创呼吸机辅助通气、强心利尿、抗感染、脏器支持等治疗。请心外科会诊,行双下肢深静脉造影术,术中见双侧髂静脉血栓形成并狭窄。为防止血栓脱落上行再次造成肺栓塞,行下腔静脉滤器置入术,终生服用华法林。
1.2 病例2 患者,男性,78岁,因反复胸部闷痛3年、加重1 d就诊于急诊科。3年来反复胸部闷痛发作,多位于心前区,呈刀割样,持续数分钟至数十分钟不等。3月前,因胸部闷痛再发,于美国行右冠状动脉造影+支架置入术,术后不规律服用抗血小板及调脂等药物,胸部闷痛有所改善。入院前1天无明显诱因胸部闷痛再发,以剑突下明显,性质较前加剧,含服速效救心丸后未缓解。急诊查cTnⅠ为0.02 ng/mL,NT-proBNP为97.07 pg/mL;心电图未见明显ST-T改变(图3)。拟诊冠心病,不稳定性心绞痛,并收住院。查体:体温36.3 ℃,脉搏59 min-1,血压152/77 mmHg,血氧饱和度95%(吸入氧浓度21%)。神志清楚,颈静脉无充盈。双肺呼吸音清,未闻及干湿性啰音。心律齐,未闻及杂音。腹软,无压痛。双下肢无浮肿。既往有原发性高血压病史。入院后检查:血常规及电解质正常;血凝全套:活化部分凝血活酶时间57.8 s,D-二聚体0.38 μg/mL;复查cTnⅠ 0.02 ng/mL,NT-proBNP 201.8 pg/mL,心电图未见明显改变。治疗上予以绝对卧床、吗啡止痛、硝酸甘油及地尔硫卓扩张冠状动脉、双联抗血小板、调脂等治疗。患者胸痛未明显缓解,持续烦躁伴出汗。进一步查胸主动脉及腹主动脉CTA,示腹主动脉腹腔干开口处小夹层形成,肠系膜上动脉近段夹层形成,其分支未见受累(图4)。调整治疗方案:考虑3月内置入支架,维持双联抗血小板药物的剂量;制动,控制性降压,收缩压控制于110~120 mmHg。病情稳定后转心外科行肠系膜上动脉支架置入术。
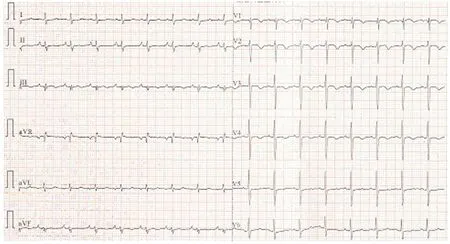
图中见窦性心动过速、电轴右偏、SⅠQⅢTⅢ及胸前导联T波改变.图1 病例1心电图Fig 1 Case 1 electrocardiogram result
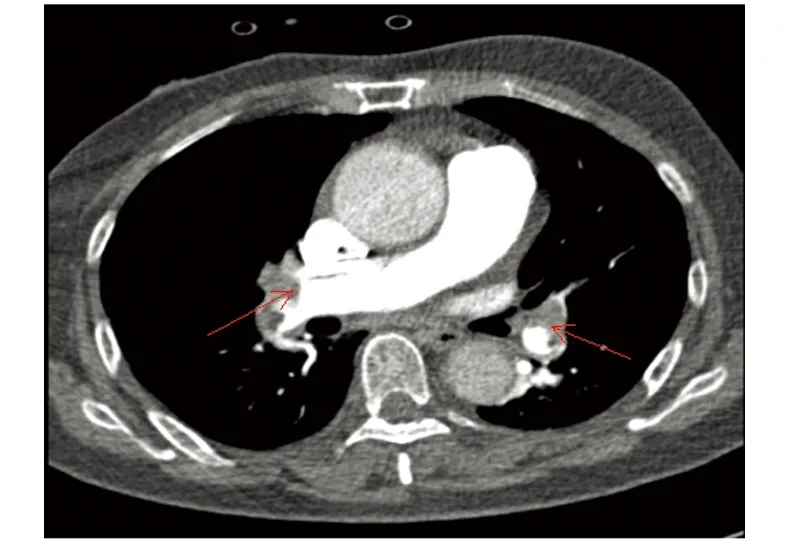
箭头所指为右肺动脉主干及左肺上叶动脉多发充盈缺损.图2 病例1的肺动脉CT血管造影Fig 2 Case 1 pulmonary artery CTA result
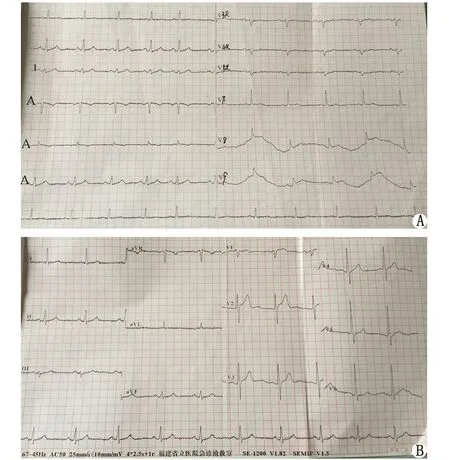
A,B:急诊18导联心电图.图3 病例2心电图Fig 3 Case 2 electrocardiogram results
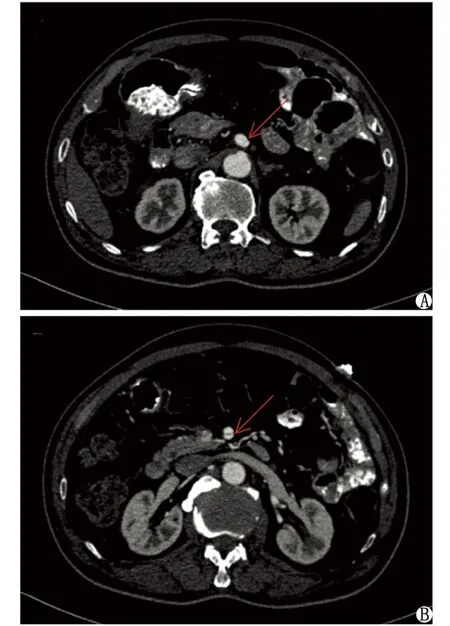
A:箭头所指为腹主动脉腹腔干开口处小夹层形成;B:箭头所指为肠系膜上动脉近段夹层形成.图4 病例2的胸、腹主动脉CT血管造影Fig 4 Case 2 thoracic and abdominal aorta CTA result
2 讨 论
急性胸痛的病因错综复杂且表现各异,其中不乏致死性疾病,若未及时识别病因并给予有效处理,可能贻误最佳救治时机而导致严重后果。现就误诊漏诊的可能原因以及诊治流程分析如下。
2.1 胸痛患者误诊漏诊的可能原因 病例1为老年女性,因胸痛、呼吸困难在17 d内2次就诊急诊科。患者具有高龄、高血压、动脉粥样硬化及下肢静脉血栓形成等肺栓塞易患因素,同时具有肺栓塞典型的临床表现,如胸痛、呼吸困难等,但无咯血,且首次检测cTnⅠ正常,心电图未见明显ST段抬高或有定位意义的Q波形成,在此条件下出现难以纠正的低氧血症及低血压状态。此时应大胆质疑ACS的诊断,不排除肺栓塞存在的可能。辅助检查方面,血气分析提示Ⅰ型呼吸衰竭,cTnⅠ阴性但BNP已升高,心电图提示典型窦性心动过速、电轴右偏、SⅠQⅢTⅢ及胸前导联T波改变,应高度怀疑急性肺栓塞可能,且非小面积栓塞可能性大。该疑诊最后经肺动脉CTA证实。患者首次就诊时以胸痛为主诉,缺乏典型的肺栓塞三联征表现,且无低血压及低氧血症,故对肺栓塞的诊断未存在警惕性。但如仔细推敲病史,患者胸痛发生于长途飞行十余小时制动后,且有下肢静脉血栓及推拿理疗史(人为移动血栓栓子),在冠状动脉造影未见明显冠状动脉分支狭窄时,若能进一步排查胸痛的可能原因,如查心脏彩超评估右心室负荷情况,动态复查cTnⅠ和BNP,并完善肺部影像学检查,或能发现早期肺栓塞的表现而进行早期处理,避免病情加重。
病例2既往有明确的冠心病及冠状动脉支架置入史,经腹主动脉CTA检查确诊为腹主动脉小夹层,在内科保守治疗2周后采取外科干预。主动脉夹层是以胸背部突发撕裂样疼痛为典型临床表现,但主动脉为全身供血主干血管,受内膜破口发生的部位和受累动脉分支的不同,其临床症状和体征复杂多变[1]。如夹层累及锁骨下动脉时,可出现左右上肢血压不等;冠状动脉开口受累时,可导致心肌缺血或梗死;累及肠系膜上动脉时,可导致急性腹痛、恶心、呕吐等。该患者胸痛位于剑突下,疼痛不易缓解,心电图未提示明显心肌坏死征象。该患者未出现典型的胸背部撕裂样疼痛或腹痛等症状,应该与夹层虽累及肠系膜上动脉,但范围较小、形成过程系慢性撕裂有关。同时,急诊首诊及收治病房的医师对胸背部及腹部血管杂音、四肢脉搏强弱及血压情况等未进行认真检查并书写记录,存在遗漏典型体征及延误诊断的可能。
2.2 在急性胸痛鉴别诊断时应重视辅助检查的作用 急性肺动脉栓塞时,心脏彩超能发现肺动脉压力升高、三尖瓣反流、室间隔异常运动、卵圆孔重新开放,甚至可见肺动脉或右心的栓子[2]。对于主动脉夹层,心脏超声可发现血管内膜破口,显示夹层真假腔及血流,并能及时发现主动脉弓分支供血情况以及有无冠状动脉受累、心包积液、主动脉瓣关闭不全及室壁运动异常等[3]。因其操作简单,可行床边检查,美国心脏学会和心脏协会(AHA/ACC)已将急性胸痛患者的早期心脏超声评价列为一级推荐,肯定了其在诊断和危险分层方面的重要性[4]。
对于疑似肺栓塞的患者,血浆D-二聚体结合临床评估是重要的初筛检查,可排除大约30%的患者,建议对门诊及急诊收治的中低度怀疑肺栓塞的患者执行。然而,对于高度怀疑肺栓塞者,即使使用高灵敏度的检测方法得到D-二聚体为正常值时,也不能完全排除肺栓塞的可能[5]。新近有关急性主动脉夹层的Meta分析指出,D-二聚体临界值取500 ng/mL时,灵敏度、特异度分别为95%(78.1%~98.8%),69.1%(43.7%~86.5%)[6]。可见在主动脉夹层的诊断方面,D-二聚体具有很高的灵敏度和一般的特异度。结合病例2,可见D-二聚体水平正常的高危患者并不能完全排除主动脉夹层,但对于非高危、主动脉夹层发生可能性低的患者,D-二聚体可作为血清学的排除标志物。
2.3 急性胸痛的高危识别与诊治流程 在我国急诊就诊的胸痛患者中,ACS高居致命性胸痛病因的首位[7]。因急性肺栓塞与主动脉夹层发生率低,临床上极易漏诊或误诊。其余高危胸痛还包括:心肌梗死机械性并发症(室间隔穿孔、乳头肌断裂甚至心脏破裂)、心脏压塞、张力性气胸等。它们的共同特点是病情进展迅速,极易出现不良预后甚至发生猝死。因此,早期识别致命性胸痛,对挽救高危患者的生命至关重要。“胸痛规范化评估与诊断中国专家共识”建议:接诊急性胸痛患者后,首先应进行生命体征监测,筛选危及生命的急重症;其次进行心电图、血液化验等快速简便的检查,二次筛选急重症;对高度怀疑急性肺栓塞、主动脉夹层、张力性气胸者可进行主动脉或肺动脉CTA检查以明确诊断;对于仅有胸闷、胸痛等临床症状,但无心电图或心肌标志物异常的疑似ACS患者,则建议急诊留院观察,每6 h复查心电图和心肌蛋白[8]。对于发病突然,诊断困难或不明确的胸痛患者,2016年AHA/ACC/美国放射学会等联合发布的“急诊科胸痛心血管影像学检查适用标准”中提及的三重排除法,即对急诊胸痛的患者行一次CTA来诊断或排除冠状动脉或主动脉病变及肺栓塞[2,9],其目的也在于迅速识别高危胸痛,及时采取措施。
[1] Erbel R, Aboyans V, Boileau C,etal. 2014 ESC Guidelines on the diagnosis and treatment of aortic diseases[J].EurHeartJ, 2014,35(41):2873-2926.
[2] 黄君龄, 陶振刚, 薛明明, 等.心超在评估急性肺栓塞患者预后中的价值[J]. 复旦学报(医学版), 2015,42(3):398-402.
[3] 郝 谦, 陈晓娟, 唐忠志. 急性主动脉夹层继发急性心肌梗死临床特点及文献分析[J]. 临床急诊杂志, 2017,18(1):44-47.
[4] Rybicki F J, Udelson J E, Peacock W F,etal. Appropriate utilization of cardiovascular imaging in emergency department patients with chest pain: a joint document of the American college of radiology appropriateness criteria committee and the American college of cardiology appropriate use criteria task forc[J].JAmCollCardiol, 2016,67(7):853-879.
[5] Konstantinides S V, Torbicki A, Agnelli G,etal. 2014 ESC guidelines on the diagnosis and management of acute pulmonary embolism[J].EurHeartJ, 2014,35(43):3033-3069.
[6] Cui J S, Jing Z P, Zhuang S J,etal. D-dimer as a biomarker for acute aortic dissection: asystematic review and meta-analysis[J].Medicine(Baltimore), 2015,94(4):e471.
[7] 向定成, 霍 勇, 方唯一. 中国胸痛中心认证标准[J]. 中国介入心脏病学杂志, 2016,24(3):121-130.
[8] 中华心血管病杂志编辑委员会. 胸痛规范化评估与诊断中国专家共识[J]. 中华心血管病杂志, 2014,42(8):627-632.
[9] Keenan N G, Pugliese F, Davies L C. The role of computed tomography in cardiovascular imaging: from X-ray department to emergency room[J].ExpertRevCardiovascTher, 2014,12(1):57-69.
(编辑:何佳凤)
2017-03-22
福建省立医院 老年科,福建省临床老年病研究所,福建医科大学 省立临床医学院,福州 350001
袁 音,女,主治医师,医学硕士
朱鹏立. Email:zpl7755@gmail.com
R311.121; R323.3; R441.1; R619
: B
: 1672-4194(2017)04-0259-03

