地西他滨联合不同化疗方案治疗复发难治性急性髓系白血病疗效观察
马洪霞
(河南省郑州市第三人民医院血液科,河南 郑州 450000)
·临床研究·
地西他滨联合不同化疗方案治疗复发难治性急性髓系白血病疗效观察
马洪霞
(河南省郑州市第三人民医院血液科,河南 郑州 450000)
目的 观察地西他滨联合不同化学治疗(化疗)方案治疗复发难治性急性髓系白血病(AML)的临床疗效。方法 选取医院2012年1月至2015年2月收治的复发难治性AML患者86例,按随机数字表法分为对照组和观察组,各43例。对照组患者给予地西他滨联合改良CAG(阿糖胞苷+阿克拉霉素+粒细胞集落刺激因子)方案治疗,观察组患者给予地西他滨联合减量FLAG(氟达拉滨+阿糖胞苷+粒细胞集落刺激因子)方案治疗。结果 观察组患者总有效率和死亡率分别为62.79%和16.28%,优于对照组的58.14%和18.60%,但组间比较均无显著性差异(2=0.19,0.08;P>0.05);治疗后,观察组患者总生存时间和无复发生存时间分别为(32.68±4.36)个月和(19.74±3.18)个月,优于对照组的(31.05±2.05)个月和(18.32±2.34)个月,但组间比较无显著性差异(t=5.84,10.04;P>0.05);两组患者血小板减少、中性粒细胞减少、恶心呕吐、感染等不良反应发生率均无显著性差异(P>0.05)。结论 采用地西他滨联合减量FLAG方案治疗和联合CAG方案治疗复发难治性AML的临床疗效相当,为该病恩环类化疗药物累积超量的患者提供了有效的化疗方案。
复发难治性急性髓系白血病;地西他滨;FLAG方案;CAG方案
急性髓系白血病(acute myeloid leukemia,AML)是目前临床较常见的血液系统恶性肿瘤,其发病率较高,且预后较差,病死率较高[1]。近年来随着医学技术水平的提高,该病的临床缓解率及患者的生存时间均有一定程度改善,但仍有部分患者不能完全缓解,进而导致复发。复发难治性AML是临床治疗中的一大难题。目前,临床对于复发难治性AML患者的治疗方案主要以氟达拉滨+阿糖胞苷+粒细胞集落刺激因子(FLAG)方案、大剂量阿糖胞苷联合蒽环类药物再诱导或FLAG方案联合去甲氧柔红霉素进行诱导,虽有一定临床疗效,但患者的缓解率仍较低,且有大量不良反应发生[2]。本研究探讨了地西他滨联合减量FLAG方案治疗复发难治性AML的临床疗效。现报道如下。
1 资料与方法
1.1 一般资料
纳入标准:符合《血液病诊断及疗效标准》[3]中关于复发难治性AML患者的诊断分型标准;根据体力状况(ECOG)进行评分,体能状态评分不超过3分,且一般状况良好;自愿签署知情同意书;该研究经过医学伦理委员会批准。
排除标准:有严重肝、肾、心功能障碍;患有代谢疾病;其他恶性肿瘤。
病例选择与分组:选取我院2012年1月至2015年2月收治的复发难治性AML患者86例,按随机数字表法均分为对照组和观察组,各43例。两组患者一般资料比较,差异无显著性(P>0.05),具有可比性。详见表1。

表1 两组患者一般资料比较(n=43)
1.2 方法
观察组给予地西他滨联合减量FLAG治疗:20 mg/m2地西他滨(Pharmachemie B.V.公司,进口药品注册证号H20140186,规格为每瓶50 mg)静脉滴注给药,第1~5天,每日 1次;25 mg/m2氟达拉滨(Bayer Schering Pharma AG公司,国药准字 J201400131,规格为每瓶50 mg)静脉滴注给药,第6~10天,每日1次,持续用药;氟达拉滨滴注后3 h静脉滴注给予1 g/m2阿糖胞苷(Actavis Italy S.P.A.公司,进口药品注册证号H20100594,规格为每支0.1 g),第6~10天,每日1次;皮下注射给予300 μg粒细胞刺激因子(哈药集团生物工程有限公司,国药准字S20000061,规格为每瓶900万U),每日1次,第5~10天,持续用药至患者中性粒细胞达到最低值后恢复>2×109/L。
对照组患者给予地西他滨联合减量CAG方案治疗:阿糖胞苷10 mg/m2,皮下注射,每12 h 1次,第1~14 d;阿克拉霉素(深圳万乐药业有限公司,国药准字H10910092,规格为每瓶20mg)10mg/(m2·d),静脉注射,第1~4 d;粒细胞集落刺激因子(GCSF)200 μg/(m2·d),皮下注射,第1~14 d,当中性粒细胞大于10×109/L时暂时减少或停用GCSF。两组患者均持续治疗4个疗程,对比两组临床疗效。
1.3 观察指标与疗效判定标准
根据《血液病诊断及疗效标准》[3]中的相关疾病疗效判断标准进行评价,临床疗效分为完全缓解(CR)、部分缓解(PR)、稳定(SD)和进展(PD)。总有效=CR+PR。观察两组患者不良反应发生情况,对患者进行随访,观察患者总生存时间和无复发生存时间及随访过程中的死亡情况。
1.4 统计学处理
2 结果
结果见表2至表4。

表2 两组患者临床疗效和死亡情况比较[例(%),n=43]
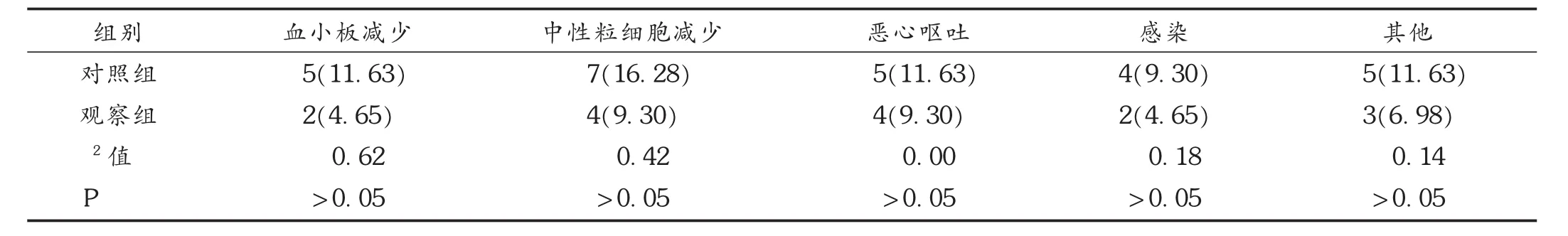
表3 两组患者不良反应发生情况比较[例(%),n=43]
3 讨论
AML是临床发病率较高的恶性肿瘤,随着临床新药的不断开发,治疗方案的不断完善,临床治疗有效率虽显著升高,但仍有部分患者会复发[4-5]。多数复发难治性AML患者临床治疗过程中均存在耐药性问题,进而导致复发后再次进行治疗时缓解率较低、患者生存期短等问题[6]。因此,提高该病的临床疗效,延长生存期是临床研究的重点和热点。目前,临床用于治疗复发难治性AML的常用经典方案为FLAG方案。其中,氟达拉滨可有效抑制白血病患者细胞DNA,RNA及蛋白质等物质的合成,促进S期内细胞脱氧胞苷激酶的活性,提高阿糖胞苷在机体内的浓度,从而对白血病细胞产生杀伤效果[7-8]。粒细胞刺激因子可促进白血病细胞静止期向细胞周期过渡,促进化疗药物对白血病细胞的杀灭作用[9]。虽然该方案是目前临床的常用方案,但其临床疗效一直备受争议[10]。因为在该方案的治疗过程中,随着阿糖胞苷剂量的增加,对患者的总生存期并无显著改善,反而导致临床毒副作用增加[11]。
表4 两组患者生存时间比较(±s,个月,n=43)

表4 两组患者生存时间比较(±s,个月,n=43)
组别对照组观察组t值P总生存时间31.05±2.05 32.68±4.36 2.22>0.05无复发生存时间18.32±2.34 19.74±3.18 2.36>0.05
地西他滨是一种去甲基化药物,主要活性成分为2′-脱氧胞苷类似物,可发挥双向调节作用,低浓度时可促进机体内细胞分化,高浓度时具有细胞毒作用[12]。药理学研究证明,该药物具有显著的抗肿瘤活性,主要作用机制为抑制DNA甲基转移酶,促进抑癌基因恢复至正常去甲基化状态,活化失活基因,最终达到治疗效果[13]。早期临床将地西他滨作为治疗 AML的一线药物,但大量临床数据显示,其对AML患者骨髓抑制的缓解率较低[14]。目前,临床提出采用减量FLAG方案联合地西他滨用于复发难治性AML患者的治疗,以期2种方案发挥协同增效的作用[15]。粒细胞刺激因子可促进AML患者细胞进入S期,加用地西他滨后可促进该效果更好地发挥。另外,地西他滨有助于白血病细胞对阿糖胞苷敏感性的增加,从而有助于阿糖胞苷更好地发挥治疗效果[16]。
本研究结果显示,两组患者临床疗效相当(P>0.05),观察组患者采用地西他滨联合减量FLAG方案治疗后不良反应发生率与对照组比较,无显著性差异(P<0.05);两组治疗后的总生存时间及无复发生存时间均无显著性差异(P<0.05)。
综上所述,采用地西他滨联合减量FLAG方案治疗复发难治性AML,可延长患者的存活期,且安全性高、效果显著,为临床治疗复发难治性AML蒽环类化疗药物累积超量的患者提供了一种有效的化疗方案。
[1]张红霞,吴广胜,王 燕.地西他滨联合半量CAG方案治疗老年急性髓系白血病的临床疗效[J].中国老年学杂志,2016,36(20):5058-5060.
[2]Nieto M,Demolis P,Béhanzin E,et al.The european medicines agency review of decitabine(dacogen)for the treatment of adult patients with acute myeloid leukemia:summary of the scientific assessment of the committee for medicinal products for human use[J].The oncologist,2016,21(6):692-700.
[3]张新华,黄有文.血液病诊断及疗效标准[M].北京:科学出版社,2007:29-34.
[4]Zheng RH,Xie BL,Wang CY,et al.D-CAG(decitabine followed by cytarabine,aclarubicin,and G-CSF)for relapsed acute myeloid leukemia after hematopoietic cell transplantation[J].Annals of Hematology,2016,95(1):157-159.
[5]蔡艳青.地西他滨联合CAG方案治疗老年急性髓系白血病临床疗效观察[J].山东医药,2016(5):90-91.
[6]高 苏,胡晓慧,仇惠英,等.地西他滨单药五天方案治疗复杂核型骨髓增生异常综合征和急性髓系白血病疗效观察[J].中华血液学杂志,2013,34(6):542-543.
[7]高 苏,仇惠英,金正明,等.地西他滨单药及联合半程和全程CAG方案治疗骨髓增生异常综合征和急性髓系白血病疗效观察[J].中华血液学杂志,2014,35(11):961-965.
[8]Kadia TM,Thomas XG,Dmoszynska A,et al.Decitabine improves outcomes in older patients with acute myeloid leukemia and higher blast counts[J].Am J Hematol,2015,90(7):E139.
[9]崔 巍,金正明,曹 晶,等.地西他滨联合HAAG方案治疗进展期急性髓系白血病疗效分析[J].第三军医大学学报,2016,38(12):1379-1384.
[10]郑卓军,朱远东,谢晓宝,等.地西他滨联合HIA方案治疗复发难治性急性髓系白血病的临床观察[J].临床肿瘤学杂志,2016,21(10):889-892.
[11]靖 ,朱成英,张 琪,等.地西他滨联合改良CAG方案治疗AML1-ETO阳性复发、难治急性髓系白血病的临床研究[J].中国实验血液学杂志,2014,22(5):1245-1250.
[12]柳凤芝,何 玲,王季石,等.地西他滨对白血病细胞DKK1基因去甲基化的实验研究[J].中国实验血液学杂志,2016,24(1):56-60.
[13]朱成英,刘世研,牛建花,等.地西他滨联合改良CAG方案治疗复发、难治型急性髓系白血病的临床研究[J].中国实验血液学杂志,2015,23(1):88-93.
[14]蔡艳青.地西他滨联合CAG方案治疗老年急性髓系白血病临床疗效观察[J].山东医药,2016,56(5):90-91.
[15]王 倩,陈冬梅,张 宏.地西他滨治疗继发于多发性骨髓瘤的急性髓系白血病1例[J].医药导报,2014,33(1):38-42.
[16]缪扣荣,倪 英,刘 澎,等.地西他滨联合减量FLAG方案成功高效诱导复发难治急性髓系白血病[J].南京医科大学学报(自然科学版),2015,10(1):93-95.
ClinicalObservation ofDecitabineCombined with DifferentChemotherapy Regimensin Treating Recurrent Refractory Acute M yeloid Leukemia
Ma Hongxia
(Department of Hematology,The Third People′s Hospital of Zhengzhou,Zhengzhou,Henan,China 450000)
Objective To investigate the clinical efficacy of decitabine combined with different chemotherapy regimens in treating recurrent refractory acute myeloid leukemia(AML).M ethods A total of 86 patients with recurrent refractory AML admitted to our hospital from January 2012 to February 2015 were randomly divided into the control group and the observation group according to the random number table method,43 cases in each group.The control group was given decitabine combined with CAG regimen(cytosine arabinoside+aclacinomycin+granulocyte colony-stimulating factor),while the observation group were treated with decitabine combined with reduced FLAG regimen(fludarabine+cytosine arabinoside+granulocyte colony-stimulating factor).Results The total effective rate and mortality rate of the observation group were 62.79% and 16.28%,respectively,which were better than 58.14% and 18.60% of the control group,but there was no significant difference between the two groups(χ2=0.19,0.08,P>0.05).After treatment,the survival time and recurrence-free survival time of the observation group were(32.68±4.36)months,(19.74±3.18)months,which were better than(31.05±2.05)months,(18.32±2.34)months of the control group,but there was no significant difference between the two groups(t=5.84,10.04,P>0.05).There was no significant difference in the incidence of adverse events such as thrombocytopenia,neutropenia,nausea and vomiting and infection(P>0.05).Conclusion The decitabine combined with reduced FLAG regimen and decitabine combined with CAG regimen for treatingrecurrentrefractory AML havecomparableclinicalefficacy,itcan providean effective chemotherapy regimen for patients with excess cumulative chemotherapy.
recurrent refractory acute myeloid leukemia;decitabine;FLAG regimen;CAG regimen
R969.4;R979.1
A
1006-4931(2017)16-0043-03
2017-04-30)
10.3969/j.issn.1006-4931.2017.16.014
马洪霞(1970-),女,大学本科,主治医师,研究方向为血液相关疾病的防治,(电子信箱)hnzzmhx@126.com。

