生脉注射液中人参皂苷Rb1在心绞痛患者体内的PK-PD结合模型研究*
夏素霞,杨瑞,唐思,张世良,董晓茜,靖博宇,李国信
生脉注射液中人参皂苷Rb1在心绞痛患者体内的PK-PD结合模型研究*
夏素霞,杨瑞**,唐思,张世良,董晓茜,靖博宇,李国信**
(辽宁省中医药研究院沈阳110034)
目的:建立生脉注射液中人参皂苷Rb1在心绞痛患者体内的PK-PD结合模型。方法:10名稳定性心绞痛受试者静脉滴注生脉注射液,连续给药14天,于给药后不同时间点采集血浆样品,采用质谱法检测人参皂苷Rb1的血药浓度,绘制药-时曲线,进行非房室模型拟合并计算PK参数;以受试者的收缩压和舒张压作为药效指标,进行PK-PD模型的拟合,计算PK-PD结合模型参数。结果:10名受试者静脉滴注生脉注射液后,人参皂苷Rb1在心绞痛受试者体内的药动学过程符合一室模型,生脉注射液中人参皂苷Rb1的降压效应滞后于血药浓度,效应与效应室浓度呈良好的相关性,符合Inhibitory Effect Imax模型。结论:该研究成功建立了生脉注射液中人参皂苷Rb1在心绞痛患者体内的PK-PD结合模型,可有效地用于评价生脉注射液的药效物质基础。
生脉注射液人参皂苷Rb1心绞痛液相色谱-质谱法药代动力学药代动力学-药效动力学
生脉注射液源于中药方剂“生脉散”,为一种新型的中药制剂,收载于部颁标准第十五册,主治气阴两虚,脉虚欲脱的心悸、气短、四肢厥冷、汗出、脉欲绝的心绞痛、心肌梗塞、休克等[1-4]。将散剂改剂型制备成注射液后可供静脉注射和肌肉注射使用,起效迅速,疗效显著。药理研究表明,生脉注射液可以增强缺氧心肌对缺氧的耐受性,有明显的稳压作用;能兴奋心肌β受体,促进合成代谢;抑制ATP酶的活性,提高心肌细胞膜对某些阳离子的主动运输能力,对心脏的复苏有一定促进作用;对血压有双向调节作用,可扩张冠状动脉,降低心肌耗氧量,抑制血小板聚集,促进纤溶,改善微循环,减少心肌缺血面积,减轻心肌缺血程度[5,6]。
人参皂苷Rb1[7]为原人参二醇型皂苷,具有中枢抑制、抗低温、降低细胞内钙浓度、抗氧化、抗衰老的功能。研究表明,人参皂苷Rb1可对心肌缺血的动物模型心肌起到保护的作用,是生脉注射液中含量最高的标志性成分。本研究拟通过对心绞痛患者体内人参皂苷Rb1的药代-药效动力学研究,初步探讨其体内动力学特征,证明其为药效物质基础。
1 材料与方法
1.1 仪器与试剂
1.1.1 主要仪器
Agilent 6410三重四级杆串联质谱仪,ESI离子源,Quantitative Analysis version B.01.04数据处理系统(美国安捷伦公司);XW-80A微型旋涡混合仪(上海沪西分析仪器厂);XS105分析天平(梅特勒-托利多仪器有限公司);SIGMA3-18 k低温高速离心机(德国SIGMA公司);Milli-Q Reference超纯水系统(德国默克公司);Haier超低温保存箱(青岛海尔公司);MTN-2 800 W氮吹浓缩装置(天津奥特赛恩斯仪器有限公司)。
1.1.2 药品与试剂
生脉注射液(1 mL生脉注射液含红参0.1 g、麦冬0.312 g、五味子0.156 g,规格:20 mL/支,四川省宜宾五粮液集团宜宾制药有限责任有限公司,批号:14090222)。葡萄糖注射液(规格:100 mL:5g,华仁药业股份有限公司,批号:040000147300)。
人参皂苷Rb1(中国食品药品检定研究院,批号:110704-201223);地西泮(内标,中国药品生物制品检定所,批号:171225-200302);甲醇、乙腈(色谱级,德国默克公司);超纯水(自制,Milli-Q Reference超纯水系统过滤)。
1.2 实验方法
1.2.1 受试者选择
气阴两虚的证慢性、稳定性、劳累性心绞痛患者,年龄45-70周岁,身高165±7 cm,体重68±9 kg,男女不限,试验前自愿签署知情同意书。诊断标准参照国际心脏病学会及世界卫生组织临床命名标准化联合专题组报告《缺血性心脏病的命名及诊断标准》,符合冠心病稳定型劳累性心绞痛诊断的患者;根据中药新药临床研究指导原则(2002版),符合中医气阴两虚证辨证的患者;参照《慢性稳定性心绞痛诊断与治疗指南》加拿大心血管学会心绞痛严重度分级,心绞痛严重程度评级为Ⅰ级-Ⅱ级的患者;8分≤心绞痛症状积分≤18分;每周发作2次或以上的冠心病心绞痛患者,排除不稳定型心绞痛患者及其他心肺疾病患者。
1.2.2 给药方案及样品采集
本试验采用随机、开放试验的设计方法。招募的符合入选标准的10名气阴两虚的证慢性、稳定性、劳累性心绞痛患者作为受试者。服药前禁食10 h以上,试验日晨每位受试者空腹静脉滴注生脉注射液60 mL(加入到5%葡萄糖注射液100 mL中),匀速静脉滴注,滴注时间1.5 h,连续给药14天,每天给药1次。于第1、12、13天早上用药前采集血样谷浓度以确定达稳态浓度的时间。于给药后第14天滴注前0 h、滴注开始后0.5 h和1 h,滴注结束后0、0.083(5 min)、0.5、1、2、4、6、8、12、24、48、96、144 h由静脉采血5.0 mL于肝素钠试管中,3 500 rpm离心10 min,分离血浆,分离出的血浆样本置于已标记好的试管中,在-70°C的冰箱中保存待测。
试验期间监测受试者生命体征,包括血压(收缩压、舒张压、平均血压)、心率、心电图、血常规、尿常规和血生化指标及受试者主诉。
1.2.3 血浆样品处理方法
精密量取200 μL血浆于2 mL空白离心管中,加入地西泮内标溶液(12.5 mg·L-1)10 μL,涡旋混匀30 s,加入乙腈400 μL,旋涡混匀3 min;14 000 r·min-1离心10 min,提取上清液,N2气吹干后,加100 μL流动相,涡旋混匀1 min,14 000 r·min-1离心5 min,取上清液10 μL进样分析。
1.2.4 血浆中人参皂苷Rb1分析方法
色谱柱:Agilent ZORBAX SB-C18Synergi POLARRP(3.5 μm,30 mm×2.16 mm);流动相为水(A)∶乙腈(B):0-5 min 15%-30%(B);5-18 mim 30%(B);18-19 min 30%-100%(B);19-26 min 100%(B),流速0.3 mL·min-1;柱温:40℃;进样量:10 μL。
ESI离子源;Gas Flow 9 L·mL-1,Gas Temp 350℃,Nebulizer 40 psi,Capillary 4 000 V;正离子方式检测,扫描方式为选择反应监测(SIM),用于定量的离子为人参皂苷Rb1,m/z 969.6,Fragmentor 320;内标地西泮,m/z 285.0,Fragmentor 165;扫描时间为200 ms。
1.2.5 PK模型的拟合
采用Pharsight Phoenix WinNonlin 6.3软件绘制药-时曲线,对受试者血浆中人参皂苷Rb1的血药浓度-时间关系进行药动学隔室模型拟合,以Akaike's信息标准AIC值、残差平方和(SSR)、拟合度(CORR)为指标筛选最佳房室模型。以AIC值越小、残差平方和值越小以及拟合度值越大为判断标准,并且综合考虑兼顾各个指标以及模型的简单性,确定人参皂苷Rb1的最佳房室模型。
1.2.6 PK-PD模型的拟合
以给药后受试者血浆中的人参皂苷Rb1的血药浓度为药代指标,分别以受试者的收缩压及舒张压为药效指标,在PK模型基础上建立PK-PD结合模型。通过考察不同的药效动力学模型,并输入PK参数,拟合出最佳PK-PD结合模型,描述药效动力学参数和药物浓度与药效之间的定量关系。
2 结果与分析
2.1 PK研究结果
受试者给予生脉注射液14天后,血浆中人参皂苷Rb1的血药浓度-时间关系经Pharsight Phoenix Win⁃Nonlin 6.3药代动力学隔室模型拟合,综合考虑AIC值、SSR、CORR,确定最佳房室模型为一室模型。人参皂苷Rb1的药-时曲线见图1,模型参数及药代参数见表1、表2。
2.2 PK-PD模型的拟合
采用效应室模型,通过效应室将血药浓度与效应相关联,分别以SBP和DBP为效应指标,以血药浓度作为PK指标进行模型的拟合,以AIC值作为筛选指标,对模型进行筛选,表明人参皂苷Rb1符合Inhibitory Ef⁃fect Imax模型,表示为:
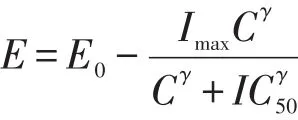
其中,C为效应室人参皂苷Rb1浓度,Imax为给药前最大效应,反映药物的内在活性,其值越大,内在活性也就越大;IC50为对应于50%最大效应时效应室的人参皂苷Rb1浓度,反映药物与受体的亲和力大小,IC50越小,则药物与受体的亲和力越大;γ为陡度系数,其大小与效应-浓度曲线的陡度有关。
由结果可知,人参皂苷Rb1的血药浓度与收缩压和舒张压的关系符合Inhibitory Effect Imax模型,呈良好的负相关性,随着血药浓度的升高,受试者舒张压和收缩压下降,血药浓度的达峰时间为给药后2.5 h,药物效应的达峰时间为给药后5.5 h,存在滞后现象,即效应与血药浓度不直接相关,表明人参皂苷Rb1与生脉注射液的降血压作用相关,可能是生脉注射液降血压作用的主要效应成分。
3 讨论
建立基于作用机制的PK-PD结合模型是PK-PD结合研究的发展趋势[8]。选择与作用机制相关,并且稳定的、可连续定量和可重复性的替代效应指标,寻找其与药物浓度的相关性是成功建立PK-PD结合模型的关键[9-12]。心绞痛的时候,因为情绪变化,疼痛刺激等,可以诱发肾上腺素分泌,导致血压上升。现代药理研究表明[13,14],人参皂苷Rb1具有能够阻断钙通道的能力,其中包括降低心肌细胞钙浓度,降低L-型全细胞钙电流,并且还能降低延迟外向钾电流,在心肌细胞内钙浓度下降的同时,可使心肌不应期延长,有利于终止兴奋的折反[15],起到降压的效果。研究中发现的药效滞后于血药浓度的现象,原因可能是生脉注射液静脉滴注后,血液中的人参皂苷Rb1逐渐向组织中(血管平滑肌、心肌细胞等)分布,分布速率较慢,导致药效的变化滞后于血药浓度的变化。本研究以受试者的收缩压和舒张压为药效评价指标,成功建立了人参皂苷Rb1在心绞痛患者体内的PK-PD结合模型,可有效的用于预测生脉注射液中人参皂苷Rb1的血药浓度和效应。
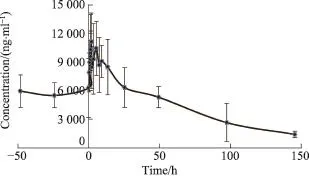
图1 心绞痛受试者静脉滴注生脉注射液后人参皂苷Rb1的药时曲线(n=10)
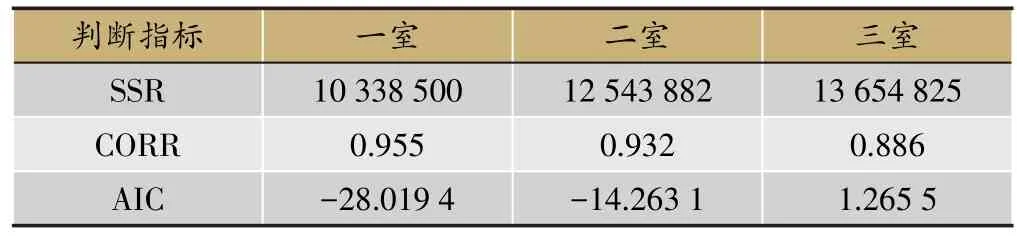
表1 人参皂苷Rb1的药动学隔室模型判断指标

表2 人参皂苷Rb1的房室模型PK参数
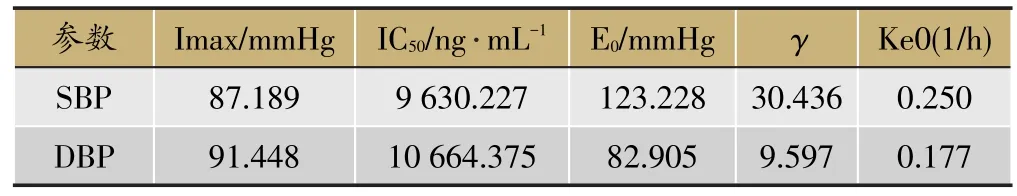
表3 生脉注射液中人参皂苷Rb1对舒张压和收缩压变化的PK-PD结合模型参数
1杨昌杰.心内科临床中生脉注射液的应用研究.心血管病防治知识(学术版),2015,10:102-103.
2刘君,徐志宏.生脉注射液的药理作用及临床应用.中国医院用药评价与分析,2013,13(11):1053-1054.
3张晓明,刘亚.生脉注射液的药理作用机制及临床应用.医学综述, 2013,19(15):2813-2816.
4范化杰.生脉注射液的药物作用机制及临床效果观察.北方药学,2016,13(6):137-137.
5袁碧文.生脉注射液的研究近况.中国药业,2000,9(11):62.
6王宝庭,李学军,刘雪山,等.生脉注射液治疗银屑病的疗效观察.华西药学杂志,2000,15(1):69.
7康安,钱静,单进军,等.人参总皂苷主要成分大鼠体内药动学研究.中草药,2015,46(20):3045-3050.
8Csajka C,Verotta D.Pharmacokinetic-pharmacodynamic modelling:history and perspectives.J Pharmacokinet Pharmacodyn,2006,33(3):227-279.
9Sheiner L B,Steimer J L.Pharmacokinetic/pharmacodynamic modeling in drug development.Annu Rev Pharmacol,2004,40(40):67-95.
10 Derendorf H,Lesko L J,Chaikin P,et al.Pharmacokinetic/pharmacodynamic modeling in drug research and development.J Clin Pharma⁃col,2000,40(12pt2):1399-1418.
11 Caruso A,Frances N,Meille C,et al.Translational PK/PD modeling for cardiovascular safety assessment of drug candidates:Methods and exam⁃ples in drug development.J Pharmacol Toxicol Methods,2014,70(1): 73-85.
12 Balaje R M,Sidhu P K,Kaur G,et al.Mutant prevention concentration and PK-PD relationships of enrofloxacin for Pasteurella multocida in buffalo calves.Res Vet Sci,2013,95(3):1114-1124.
13陈立波,佟力.人参总皂甙对心肌缺血再灌注损伤的保护作用实验研究.白求恩医科大学学报,1994,10(4):353-354.
14钟国赣,孙成文,李云义,等.人参二醇组皂甙Rb1、Rb2、Rb3、Rc和Rd的Ca2+通道阻制和抗自由基作用.中国药理学报,1995,16(3): 255-260.
15马越.人参皂甙单体Rb1对心肌缺血的保护作用及其机制.长春:东北师范大学硕士学位论文,2000.
Study on PK-PD Evaluation of Ginsenoside Rb1in Subjects withAngina Pectoris Following IntravenousAdministration of Shengmai Injection
Xia Suxia,Yang Rui,Tang Si,Zhang Shiliang,Dong Xiaoqian,Jing Boyu,Li Guoxin
(Liaoning Provincial Academy of Traditional Chinese Medicine,Shenyang 110034,China)
This study was aimed to establish the pharmacokinetics-pharmacodynamics(PK-PD)model of ginsenoside Rb1following the intravenous administration of Shengmai injection in subjects with stable angina pectoris.A total of stable angina pectoris were selected and
Shengmai injection for 14 days.Plasma samples were collected at different time points.Plasma concentrations of ginsenoside Rb1were determined by liquid chromatography-mass spectrometry(LC/MS).The concentration-time curves(AUC)were drawn,and then the PK parameters were calculated. The systolic pressure and diastolic pressure were monitored,and the combined PK-PD model was established based on the theory of effect compartment.The results showed that PK of ginsenoside Rb1conformed to a mono-compartment model.The effect of Shengmai injection lagged behind the concentrations of ginsenoside Rb1in plasma.The effect exhibited good correlation with ginsenoside Rb1in effect compartment.The relationship between effect and plasma concentrations fits the Inhibitory Effect Imax model.It was concluded that the study successfully established the combined PK-PD model of ginsenoside Rb1in subjects with angina pectoris.The model can efficiently evaluate the effective substance of Shengmai injection.
Shengmai injection,ginsenoside Rb1,angina pectoris,chromatography-mass spectrometry,pharmacokinet⁃ics,pharmacokinetics-pharmacodynamics
10.11842/wst.2017.05.021
R285.5
A
(责任编辑:马雅静,责任译审:王晶)
2017-05-15
修回日期:2017-05-20
*科学技术部国家“十二五”重大新药创制项目(2012ZX09303-017):中药新药临床评价研究技术平台,负责人:李国信;国家中医药管理局国家临床重点专科建设项目经费资助(2013年),负责人:李国信;国家中医药管理局临床中药学重点学科(2009年),负责人:李国信;辽宁中医药大学杏林学者青蓝工程(2013年),负责人:李国信。
**通讯作者:杨瑞,副研究员,主要研究方向:药代动力学及药物新制剂;李国信,主任医师,主要研究方向:临床药理。

