抗肿瘤药物不良反应临床分析
吴如成,邹秀芬
江苏省金湖县人民医院药剂科,江苏金湖 211600
抗肿瘤药物不良反应临床分析
吴如成,邹秀芬
江苏省金湖县人民医院药剂科,江苏金湖 211600
目的 探讨抗肿瘤药物不良反应(ADR)表现及一般特点,为临床合理用药提供数据参考。 方法 从2013年8月—2016年7月于该院行住院化疗的恶性肿瘤患者中随机抽取394例为研究对象,统计抗肿瘤药物相关性ADR发生率,观察不良反应患者的性别、年龄、用药种类及途径、损害器官组织部位及表现等。结果 394例患者发生ADR 203例(51.52%),男性49.02%,女性54.26%(P>0.05);51~70岁是ADR发生的集中年龄段;ADR患者抗肿瘤用药分布前三位依次为铂类(49.26%)、紫杉醇类(24.14%)和氟嘧啶类(14.78%);ADR患者不良反应损害部位主要为皮肤及附件(21.18%)、消化系统(19.70%)和全身性损害(17.73%)。结论 抗肿瘤药物不良反应涉及系统广且表现多样,临床制定用药方案时应综合考虑患者年龄、药物种类、给药途径等因素,在确保疗效的同时尽量减少可能发生的不良反应,以提高用药安全性及患者生存质量。
抗肿瘤药物;不良反应;临床分析
大多数抗肿瘤药物都具有毒性反应,作用于肿瘤细胞的同时也会对正常器官组织造成毒性和损害,从而引起不同程度的药物不良反应(ADR),影响化疗进程及患者生命健康和生存质量[1]。该研究现对2013年8月—2016年7月于该院行住院化疗的394例恶性肿瘤患者抗肿瘤药物相关性ADR表现及一般特点进行分析和研究,旨在为临床合理应用抗肿瘤药物,减少药源性损害提供借鉴和参考,现报道如下。
1 资料与方法
1.1 一般资料
从于该院行住院化疗的恶性肿瘤患者中随机抽取394例为研究对象,患者临床资料齐全完整。男206例,女188例,患者年龄15~96岁,平均年龄(63.42±5.17)岁,其中 40岁以下 11例(2.79%),41~50岁 68例(17.26%),51~60岁92例(23.35%),61~70岁135例(34.26%)71~80岁 77例(19.54%),81~96岁 11例(2.79%)。
1.2 方法
根据国家卫生部药品不良反应监测中心指定原则,统计抗肿瘤药物相关性药品不良反应(ADR)患者例数及发生率,ADR评价标准为同时符合以下3项[2]:①ADR诊断明确符合抗肿瘤药物不良反应类型;②ADR发生在服用抗肿瘤药物后;③药物停用后,ADR症状有所减轻和改善。搜集ADR患者性别、年龄、肿瘤类型、用药种类、ADR损害器官组织部位及表现等临床资料进行汇总分析。
1.3 统计方法
资料归类和汇总采用Excel数据表格软件和Access关系数据库,以SPSS 17.0统计学软件进行统计学分析,计数资料以率(%)表示,进行χ2检验,P<0.05为差异有统计学意义。
2 结果
2.1 ADR发生率与性别、年龄分布
统计结显示,394例患者中ADR发生数203例,发生率51.52%。ADR患者中,男性101例,发生率49.02%(101/206),女性102例,发生率54.26%(102/188)。女性ADR发生率略高于男性,但比较差异无统计学意义(P>0.05)。ADR患者年龄分布见表1,统计显示年龄在51~70岁的患者ADR发生率高于平均水平,是ADR发生的集中年龄段。

表1 ADR患者年龄分布
2.2 ADR 患者抗肿瘤用药分布
751例 ADR患者中,使用铂类药物者最多,占49.26%,使用紫杉醇类和氟嘧啶类药物者次之,分别占24.14%和14.78%。其中,铂类和紫杉醇类均为细胞毒性药物,是肿瘤患者最常用抗肿瘤药物类型,见表2。

表2 ADR患者抗肿瘤用药分布
2.3 ADR损害器官组织部位及表现
统计显示,抗肿瘤药物ADR损害以皮肤及附件损害最为常见,占21.18%,消化系统和全身性损害次之,分别占19.70%和17.73%,见表3。
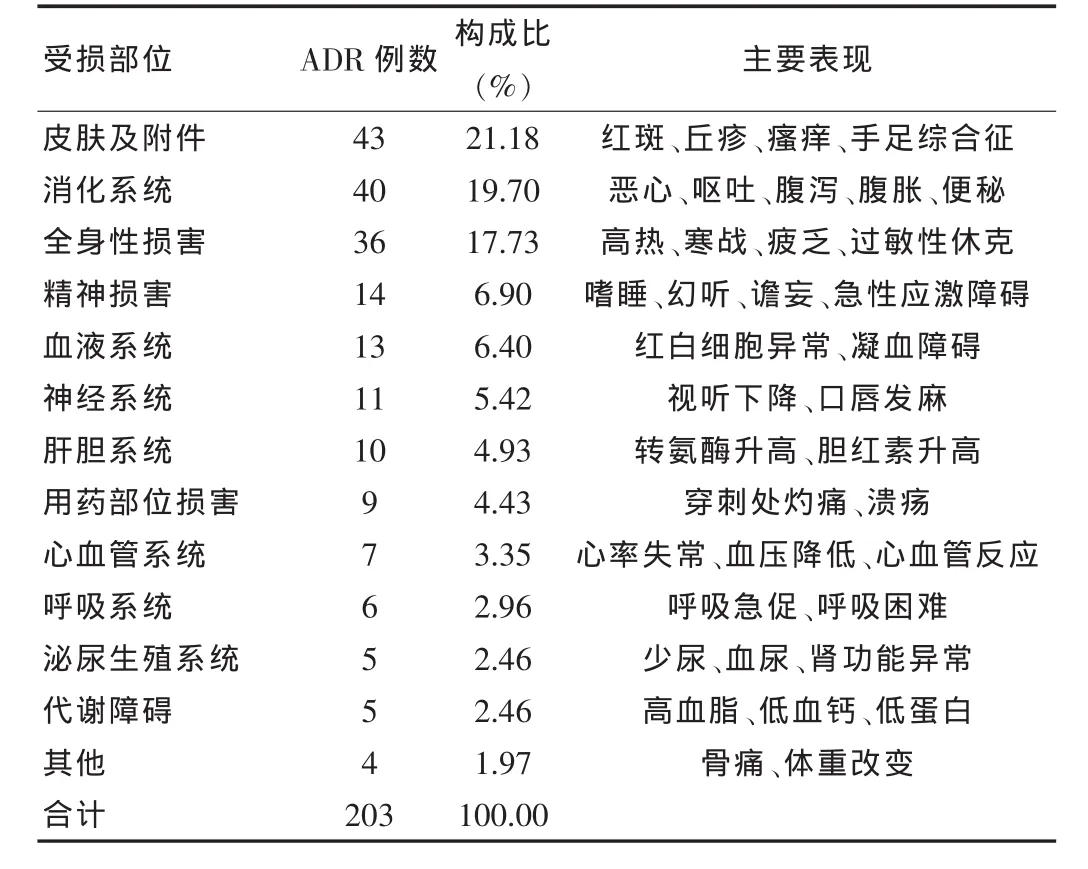
表3 ADR损害器官组织部位及表现
2.4 ADR给药途径及分布
静脉滴注是用药抗肿瘤患者出现不良反应的最主要给药途径,占病例数的42.86%,静脉注射和口服给药次之,分别为27.59%和15.27%,见表4。

表4 ADR给药途径及分布
3 讨论
肿瘤化疗患者是ADR高发人群,这与化疗所用抗肿瘤药物的药理、药性存在直接关系。肿瘤细胞在生理、生化、形态特征等方面有别于正常细胞,但两者基础周期代谢比较相似,这导致抗肿瘤药物作用于机体时对肿瘤细胞的特异性选择较差,故杀灭肿瘤细胞的同时也会对正常细胞造成毒性损害,从而引发症状[3]。
目前,临床关于抗肿瘤药物相关ADR的发生率报道不一,这与抗肿瘤药物不良反应评价标准及上报情况有关,目前文献报道普遍集中于45%~65%[4]。该次调研的 394例肿瘤化疗患者中,ADR患者 203例,占51.52%,符合上述报道结论。在ADR与年龄分布方面,该次调研中,男性ADR发生率 (49.02%)低于女性(54.26%),与李纳新等人[5]报道的男性化疗患者ADR发病率46.30%的研究结论相近,考虑可能与男性和女性生理机能差异有关。该次调研的患者年龄多集中于51~70岁,考虑原因为中年高发的癌症手术适应证强,患者术后化疗增加药物敏感性,而老年患者生理机能下降,对药物的敏感性降低,故不良反应不明显。
顺铂类药物、紫杉醇类药物和氟嘧啶类药物是现阶段临床治疗肿瘤疾病的一线药物,其中卡培他滨、奥沙利铂等治疗胃肠道肿瘤疾病效果明确,紫杉醇、卡铂等治疗生殖系统肿瘤、头颈肿瘤、乳腺癌等疗效良好。这些药物适用范围广,在肿瘤科临床使用量较大、频度也很高,因此相关性ADR发生率也较高。该次调研中,ADR患者抗肿瘤用药列居前三的药物种类依次为铂类(49.26%)、紫杉醇类(24.14%)和氟嘧啶类(14.78%),与钟润娴等人[6]报道的各类抗菌药物使用率(抗肿瘤用药不良反应较多的抗菌药物为铂类50.13%、紫杉醇类24.82%、氟嘧啶类15.02%)基本相符,这也从侧面反映了各类临床肿瘤发病率及治疗情况。
抗菌药物相关ADR表现方面,该次调研结果显示,ADR主要累及皮肤及附件(21.18%)、消化系统(19.70%)和全身性损害(17.73%)。有研究指出,铂类、紫杉醇类抗肿瘤药物相关ADR多表现为皮肤炎性反应和消化系统症状[7],这与该研究中铂类、紫杉醇类药物用量大,皮肤及附件、消化系统不良反应发生率高的结论相对应,也与目前临床所用抗肿瘤药物以细胞毒类药物为主存在相关性。该研究中,铂类和紫杉醇类均为细胞毒性药物,两种使用率约占病例总数的70%。此外,通过观察给药途径发现,抗肿瘤药物相关ADR患者主要用药途径为静脉滴注(42.86%)、静脉注射(27.59%),其原因一方面在于临床静脉给药化疗方案居多,另一方面也与静脉给药,药品直接参与体循环,药效药性产生迅速且更为激烈有关[8]。
综上所述,抗肿瘤药物不良反应涉及系统广且表现多样,临床制定用药方案时应综合考虑患者年龄、药物种类、给药途径等因素,在确保疗效的同时尽量减少可能发生的不良反应,以提高用药安全性及患者生存质量。
[1]黎国栋.抗肿瘤药物的不良反应及临床防治措施[J].实用癌症杂志,2016,31(5):866-868.
[2]谢冬梅,王群.该院抗肿瘤药物致不良反应65例报告分析[J].临床合理用药杂志,2013,6(1):5-6.
[3]王燚.抗肿瘤药物的不良反应及防治[J].临床和实验医学杂志,2012,11(10):746-747.
[4]陈海云.474例抗肿瘤药品不良反应/事件报告分析 [J].中国药物警戒,2013,10(11):676-678,682.
[5]李纳新,徐华,付志,等.该院抗肿瘤药物不良反应报告分析[J].中国当代医药,2012,19(33):147-148.
[6]钟润娴,单钰齐,朱结桃,等.抗肿瘤药物不良反应调查与分析[J].北方药学,2015,12(10):144-145.
[7]崔琪,闫素英.抗肿瘤药物引起的严重不良反应报告分析[J].中国临床药理学杂志,2015,11(8):654-656.
[8]唐友平,唐友明.某院常用抗肿瘤药物不良反应分析[J].中华全科医学,2013,11(3):473-474.
Clinical Analysis of Adverse Reactions of Antitumor Drugs
WU Ru-cheng,ZOU Xiu-fen
Department of Pharmacy,Jinhu People’s Hospital,Jinhu,Jiangsu Province,211600 China
ObjectiveTo discuss the manifestations and general features of antitumor drugs and provide reference for the clinical rational medication.Methods394 cases of patients with malignant tumors in our hospital from August 2013 to July 2016 were randomly selected and the incidence rate of antitumor drugs related ADR was counted and the gender,age,medication type and way,injured organ site and manifestations of adverse reaction patients were observed.ResultsADR was in 203 cases of 394 cases (51.52%),including 49.02%males and 54.26%females(P>0.05),and 51~70 years old was the concentrated age phase of ADR,and the top three of antitumor drugs of ADR patients were in turn platinum(49.26%),taxanes(24.14%)and fluoropyrimidine(14.78%),and the injured sites of adverse reactions of ADR patients were mainly skin and appendage(21.18%),digestive system(19.70%)and general damage(17.73%).ConclusionThe system involved of adverse reactions of antitumor drugs is wide and the manifestation is multiple,and we should comprehensively consider the age,drug type and administration way when making the clinical medication,and it can ensure the curative effect and try to reduce the potential adverse reactions thus improving the medication safety and survival quality of patients.
Antitumor drugs;Adverse reactions;Clinical analysis
R979
A
1674-0742(2017)06(c)-0084-03
10.16662/j.cnki.1674-0742.2017.18.084
2017-03-23)
吴如成(1963-),男,江苏金湖人,本科,副主任药师,研究方向:医院药学。

