气相色谱法同时测定水中12种挥发性消毒副产物
张忠祥+赵琦+刘玉蕾+马军+齐晶瑶+任芝军

摘 要 建立液-液萃取气相色谱法电子捕获检测器(GC/ECD)同时测定饮用水中12种挥发性消毒副产物(Disinfection byproducts, DBPs)的方法。采用过程标准校正降低预处理过程中引入的误差,方法检出限为0.08~0.21 μg/L, 全部组分在21.50 min内测定完成。不同浓度的DBPs在自来水和地表水中的回收率为80.9%~115.7%,相对标准偏差在0.9%~9.9%之间。各组分在0.5~200 μg/L浓度范围内线性关系良好,相关系数R>0.99。应用本方法测定了饮用水和地表水及其氯化后样品中DBPs的含量。本方法简便、快速、稳定,满足饮用水中挥发性DBPs的检测要求。
关键词 消毒副产物; 气相色谱; 挥发性; 氯消毒; 饮用水
1 引 言
饮用水消毒是20世纪最有效的公共健康措施之一[1]。氯消毒由于具有经济性和便捷性的特点,成为世界上使用最广泛的消毒方式[2]。然而研究人员发现, 氯消毒在杀灭病原体的同时会产生消毒副产物(Disinfection byproducts, DBPs),对人体健康构成新的威胁[3]。自1974 年Rook发现饮用水中含有三卤甲烷后,饮用水中DBPs的生成就成为了人们关注的焦点[4]。
目前,已知的DBPs超过600多种[5],水中常见的挥发性消毒副产物主要包括三卤甲烷(THMs)、卤乙腈(HANs)、卤代醛(HAs)、卤代酮(HKs)以及卤代硝基甲烷(HNMs)类等[6]。挥发性消毒副产物具有特殊气味,一般通过呼吸、皮肤接触和饮用途径进入人体,这些DBPs具有致癌性和其它毒性。例如,THMs的各组分具有明显的致突变作用或遗传毒性,且存在良好的剂量反应关系[7];HANs的毒性研究多集中于其遗传毒性,DCAN已被确认具有致癌、致畸、致突变毒性[8];HNMs的动物细胞遗传毒性甚至超过了致诱变化合物,它还具有强烈的致突变性等[3]。因此,许多国家和世界卫生组织(WHO)都对饮用水中消毒副产物含量进行了严格限制。WHO规定饮用水中三氯甲烷(TCM)含量不超过0.3 mg/L[9],我国国标要求TCM含量不超过0.06 mg/L[10],美国环保署(US EPA)则规定4种THMs的总量不超过0.08 mg/L[11]。
气相色谱法是测定挥发性DBPs的主要方法。赵鹏等[12]采用顶空-气相色谱法测定了4种THMs和四氯化碳;Vallejo-Vargas等[13]采用顶空-固相微萃取-气相色谱法测定了4种THMs;曹爱丽等[14]采用衍生-吹扫捕集-气相色谱质谱法(GC/MS)测定了三氯乙醛。现有检测方法测定的种类较为单一,顶空等预处理方法虽然减少了溶剂用量,但增加了设备投入。李海青等[15]采用GC/MS测定了3种卤乙腈;Liu等[16]采用液液萃取-气相色谱双串质谱法测定了三卤甲烷、卤乙腈、卤代酮和三氯硝基甲烷。GC-MS灵敏度低于气相色谱-电子捕获检测器(GC/ECD)[17],而气相色谱双串质谱法检测灵敏度较高,但仪器价格昂贵。消毒副产物种类众多,危害严重,因此有必要开发一种适合中小水厂使用、 方便快捷的检测方法,以满足快速测定多种DBPs的要求。本研究建立了一种液液萃取-气相色谱-电子捕获检测器同时测定水中12种常见挥发性消毒副产物的方法。本方法操作简单、 灵敏度高、 测定结果稳定,能为饮用水和水源水检测消毒副产物和进行安全风险评价提供技术支持。
2 实验部分
2.1 仪器与试剂
安捷伦6890 N型气相色谱仪(美国安捷伦公司); Milli-Q超纯水机(美国Millipore公司);XK96-A型漩涡振荡器(新康公司)。
标准品: 4种三卤甲烷混合标准样品(三氯甲烷、一溴二氯甲烷、二溴一氯甲烷和三溴甲烷)、7种卤代挥发性有机物混合标准样品(二氯乙腈、三氯乙腈、氯溴乙腈、二溴乙腈、二氯丙酮、三氯丙酮和三氯硝基甲烷)以及水合三氯乙醛标准样品,均购自美国Sigma-Supelco公司。各种DBPs及其结构式见表1。
甲基叔丁基醚(MTBE)、甲醇、丙酮(色谱纯,美国TEDIA公司);无水Na2SO4、抗坏血酸(分析纯,国药试剂公司)。无水Na2SO4于550℃烘烤2 h后备用。
2.2 检测条件
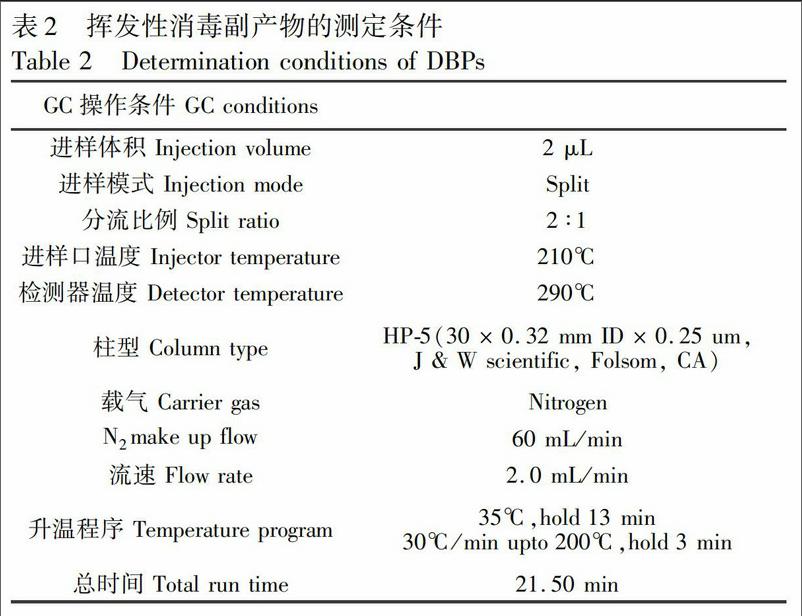
采用毛细管色谱柱分离目标物,采用电子捕获检测器(ECD)测定目标物的响应值。采集的数据通过Chemstation B.02软件进行分析。色谱柱升温程序及其它气相色谱条件见表2。
2.3 样品预处理与保存
液-液萃取法是水质分析中常用的预处理方法[6]。参照US EPA 551.1[18],本实验采用液-液萃取法对水样进行预处理。取20 mL待测水样至40 mL螺口带聚四氟乙烯瓶盖的瓶子中,加入4 mL MTBE,再立刻加入8 g经550℃干燥2 h的无水Na2SO4,充分振荡2 min后静置30 min,移取上层有机层1 mL,进行GC/ECD分析。
样品采集前应在取样瓶中加入过量抗坏血酸终止氯化反应。自来水取自饮用水水龙头,将水流放至水温恒定后取样;地表水取自松花江哈尔滨段,取江面下约10 cm的水样,沉淀除去泥沙后备用;矿泉水为随机市售矿泉水; 游泳池水为室内游泳池水;含藻水为人工培养的铜绿微囊藻。取样后若不能立即分析,需在4℃冷藏保存,并于7天内尽快测定。
3 结果与讨论
3.1 色谱条件优化
色谱峰的出峰时间和分离度主要受载气流速、初始温度和升温速率等色谱条件的影响。将3种混合标准样品用MTBE稀释混合,配制成含有12种挥发性DBPs的混合标准样品,直接进样到气相色谱,优化检测条件,确定各组分的保留时间。
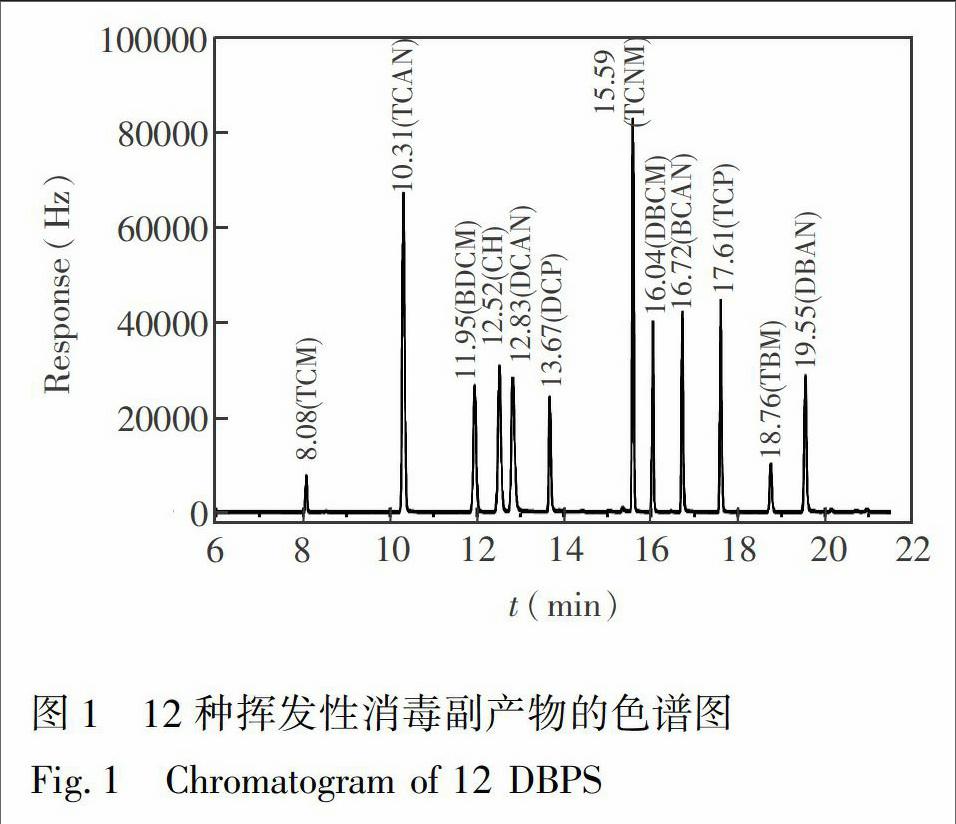
根據各组分的保留时间对水样中所含有的DBPs进行定性分析。最先出峰的物质是三氯甲烷(RT:8.08 min),最后出峰的物质是二溴乙腈(RT:19.55 min),方法共运行21.50 min。其中三氯乙醛(RT:12.52 min)与二氯乙腈(RT:12.83 min)的出峰时间较为接近,通过降低初始温度,延长初温保留时间等对色谱条件进行优化,获得了良好的分离效果。各挥发性DBPs浓度为100 g/L时的色谱图见图1。
3.2 标准曲线和方法检出限
为了抑制预处理过程对目标物测定产生的干扰,本方法采用过程标准校正(Procedural standards calibration)绘制标准曲线。将特定浓度的DBPs标准品加入到超纯水中混合均匀,按照实际样品的处理方法,通过液液萃取将目标物回收后进行测定,绘制标准曲线,从而降低回收率对绘制标准曲线的影响[18]。根据待测组分的峰面积通过外标法进行计算,得出被测水样中DBPs的含量。
首次测定时应验证测定过程中使用的容器与药品不会产生干扰。本实验用超纯水现用现制,玻璃器皿和无水Na2SO4都经高温碳化后使用。经验证,空白样品中不含待测DBPs。各DBPs的保留时间和标准曲线见表3。
由表3可见,12种挥发性DBPs在0.5~200 g/L的浓度范围内具有良好的线性相关性,各组分线性方程的相关系数R>0.99。
本方法的方法检出(Method detection limit, MDL)采用EPA[18]的方法进行计算,MDL=SD × t(n-1,1-α=0.99)。式中n为重复测量的样品个数,SD为n次测量的标准偏差,1-α为置信水平, t为自由度(n-1), 置信度为99%时的t分布值(单侧),当n=7时,t=3.14。各组分的方法检出限为0.08~0.21g/L, 表明本方法具有良好的检测灵敏度。
3.3 方法回收率与精密度
实际水体中的背景成分复杂,可能会产生基质效应,影响目标物的测定[19]。本方法通过向自来水和地表水中分别加入5 μg/L和50 μg/L的混合标准样品,计算方法的回收率和相對标准偏差(RSD),考察不同背景水体对本方法测定DBPs可靠性的影响, 测定结果见表4。
由表4可见,本方法对各组分在自来水中的回收率和精密度分别为80.9%~113.8%和0.9%~8.9%,在地表水中的回收率和精密度分别为81.2%~115.7%和2.9%~9.9%。Ma等[20]采用分散液液微萃取,气相色谱质谱法测定饮用水中7种HANs,得到的RSD为7.8%~10.2%,回收率为 79%~105%;Spyros等[21]采用液液萃取,气相色谱质谱法测定地表水中4种THMs得到的回收率为60%~144%。各组分在自来水和地表水中的回收率和精密度良好,说明过程标准校正可以有效降低目标物在不同背景水体中回收率的波动。其中,地表水中各种DBPs的回收率波动高于自来水,对各种DBPs的测定影响较大。
3.4 实际样品分析
河流和湖库是主要的饮用水水源,以江水代表河流水,含藻水模拟受水华影响的湖泊和水库水,测定两种水源水的氯化DBPs, 并测定了市售矿泉水和自来水两种饮用水,以及室内游泳池水,测定结果见表5。市售矿泉水和江水中只检测到微量的三氯甲烷。自来水中分别检出了三氯甲烷10.21 μg/L、一溴二氯甲烷0.88 μg/L,远低于国家标准[10]中规定的60 μg/L的限值。游泳池水中各种挥发性DBPs的含量较高,其中TCM含量最高,达到68.23 μg/L,其次为三氯乙醛,含量达到23.84 μg/L。泳池中DBPs的种类与含量与Tardif等[22]检测结果范围一致。氯化后的江水DBPs含量明显增加,并生成了毒性较大的溴代消毒副产物,说明江水中含有一定浓度的溴离子,当以江水作为水源水应注意溴离子的去除。含藻水生成了大量的DBPs,说明藻细胞是重要的DBPs前体物,当以湖库水为水源时应注意水华的防控。
4 结 论
采用液-液萃取GC/ECD同时测定12种挥发性消毒副产物,分离效果良好,方法运行总时间为21.5 min。在0.5~200 μg/L的范围内,12种分析物具有良好的线性关系,相关系数R均大于0.99,方法检出限在0.08~0.21 g/L之间。测定了自来水和地表水两种不同背景水体中高、低两种不同浓度DBPs的回收率为80.9%~115.7%,RSD为0.9%~9.9%。江水和含藻水氯化后DBPs含量增加,并且江水氯化后生成了毒性较高的溴代DBPs,说明以地表水为水源时应注意溴离子去除和水华的防控。实验结果证明, 本方法具有简便、快速、稳定的优点,适合自来水和地表水水体中挥发性消毒副产物的测定。
References
1 Boorman G, Dellarco V, Dunnick J K, Chapin R E, Hunter S, Hauchman F, Gardner H, Cox M, Sills R C. Environ. Health Persp., 1999, 107(Suppl 1): 207-217
2 Sedlak D L,Von Gunten U. Science, 2011, 331(6013): 42-43
3 Liew D, Linge K L, Joll C A. Environ. Monit. Assess, 2016, 188(9): 518
4 Rook J J. Water Treat. Exam., 1974, 66(12): 703-706
5 Krasner S W, Weinberg H S, Richardson S D, Pastor S J, Chinn R, Sclimenti M J, Onstad G D, Thruston A D. Environ. Sci. Technol., 2006, 40(23): 7175-7185
6 Kanchanamayoon W. Chromatographia, 2015, 78(17): 1135-1142
7 Richardson S D, Plewa M J, Wagner E D, Schoeny R, DeMarini D M. Mutat. Res-Rev. Mutat., 2007, 636(1-3): 178-242
8 Ahmeda A E,Aronsonb J, Jacoba S. Toxicol. in Vitro, 2000, 14(3): 199-210
9 Guidelines for Drinking Water Quality. 4th ed., Word Health Organisation, 2011
10 Standard forDriking Water Quality. National Standards of the People's Republic of China. GB 5749-2006
生活饮用水卫生标准. 中华人民共和国国家标准. GB 5749-2006
11 National Primary Driking Water Regulations, Stage 2 Disinfection and Disinfection Byproducts Rule, United States Environmental Protection Agency, 2006
12 ZHAO Peng, QIU Li-Xiao, JIN Xiao-Xia, WU Jie. Chin. J. Health Lab. Tec., 2014, 24(4): 476-478
赵 鹏, 裘立晓, 金晓霞, 乌 杰. 中国卫生检验杂志, 2014, 24(4): 476-478
13 Vallejo-Vargas O I, Beltrán L, Franco P, Montoya-Navarrete C H, Alzate-Rodríguez E J, Reyes H. Revista Colombiana de Química, 2015, 44(1): 23-29
14 CAO Ai-Li.Guangzhou Chemical Industry, 2013, 41(13): 183, 184, 248
曹爱丽. 广州化工, 2013, 41(13): 183, 184, 248
15 LI Hai-Qing, CAI Ye, ZHANG Li-Ming, QIAN Xiao-Yan, YUAN Hai-Lang, LI Gang. The Administration and Technique of Environmental Monitoring, 2014, 26(5): 37-39
李海青, 蔡 烨, 张利明, 钱晓燕, 袁海浪, 李 刚. 环境监测管理与技术, 2014, 26(5): 37-39
16 Liu Y, Duan J, Li W, Lai Q, Saint C P, Mulcahy D. Anal. Lett., 2014, 48(1): 188-203
17 Weinberg H S.Philos. T. Roy. Soc. A, 2009, 367(1904): 4097-4118
18 Determinationof Chlorination Disinfection Byproducts, Chlorinated Solvents, and Halogenated Pesticides/Herbicides in Drinking Water by Liquid-Liquid Extraction and Gas Chromatography with Electron-Capture Detection. United States Environmental Protection Agency 551.1, 1995
19 LIU Jin-Jin, LIAO Xiao-Bin, ZHOU Zhen-Ming, LI Fei, YUAN Bao-Ling. Chinese J. Anal. Chem., 2015, 43(4): 497-501
劉津津, 廖晓斌, 周真明, 李 飞, 元宝玲. 分析化学, 2015, 43(4): 497-501
20 Ma H, Li Y, Zhang H, Shah S M, Chen J. J. Chromatogr. A, 2014, 1358(1): 14-19
21 Golfinopoulos S K, Nikolaou A D. Desalination, 2005, 176(1): 13-24
22 Tardif R, Catto C, Haddad S, Simard S, Rodriguez M. Environ. Res., 2016, 148: 411-420

