CalliSpheres载药栓塞微球治疗中晚期肝癌临床效果评价
姜松 李桂杰 周祝谦 牛威
·肿瘤介入·
CalliSpheres载药栓塞微球治疗中晚期肝癌临床效果评价
姜松 李桂杰 周祝谦 牛威
目的:探讨CalliSpheres载药栓塞微球治疗中晚期肝癌的临床效果和安全性。方法:对25例中晚期肝癌患者行导管肝动脉化疗栓塞术(TACE),并使用CalliSpheres载药栓塞微球进行栓塞,采用改良实体瘤疗效评价标准(mRECIST)评价治疗效果,比较患者治疗前后肝功能变化,记录不良反应及并发症发生情况。结果:本组25 例患者均顺利接受CalliSpheres载药栓塞微球治疗,技术成功率为100%;25例患者随访6个月,根据mRECIST标准,3个月疾病缓解率(CR+PR)为80%,疾病控制率(CR+PR+SD)为88%,6个月疾病缓解率(CR+PR)为72%,疾病控制率(CR+PR+SD)为80%。术后3 d,肝功能变化主要表现为谷丙转氨酶(ALT)、谷草转氨酶(AST)及总胆红素升高,与术前差异有统计学意义,白蛋白变化不明显,与术前差异无统计学意义,术后3个月,肝功能基本恢复正常水平,与术前比较差异无统计学意义,所有患者均未出现胆汁漏并发感染、肝脓肿、肿瘤破裂出血及消化道出血等严重并发症。结论:对中晚期肝癌患者,应用CalliSpheres载药栓塞微球是一个新的选择,近期临床疗效及安全性良好,远期疗效尚待进一步观察。
肝动脉化疗栓塞术; 肝癌; 可载药栓塞微球; CalliSpheres
经动脉化疗栓塞治疗是将化疗药物和栓塞材料同时应用,从而能产生协同效应治疗肿瘤,主要用于高血运性肿瘤,例如肝细胞癌和肿瘤肝转移,国外2006年首次报道将载药栓塞微球植入在肿瘤血液循环中的这种方法应用于结直肠癌肝转移(colorectal cancer liver metastases, CRLM)的治疗[1]。已取得较为良好的效果[2]。载药微球长期以来一直受到国内外研究者的普遍关注,但目前成功上市的载药栓塞微球仅有DC Bead、Hepasphere等产品,CalliSpheres载药微球作为国内自主研发的新型产品,与DC Bead和Hepasphere等同类产品相比,具有载药速度快、载药量大、缓释时间久、无需溶涨等优势。然而,对于CalliSpheres载药微球的近期临床疗效及安全性,目前尚无文献报道。本研究应用CalliSpheres载药栓塞微球治疗中晚期肝癌,并探讨其近期临床疗效及安全性。
资料与方法
一、一般资料
选取2016年6月—2017年2月我院收治的经临床或病理明确诊断明确的中晚期肝癌患者25例,全部病例均经临床、影像学(超声、CT、磁共振成像)、甲胎蛋白(AFP)等检查诊断为肝癌。其中男20例,女5例;年龄38~81岁,中位年龄57岁。所有患者均接受肝动脉化疗栓塞术(transcatheter arterial chemoembolization,TACE)治疗,患者术前资料见表1。
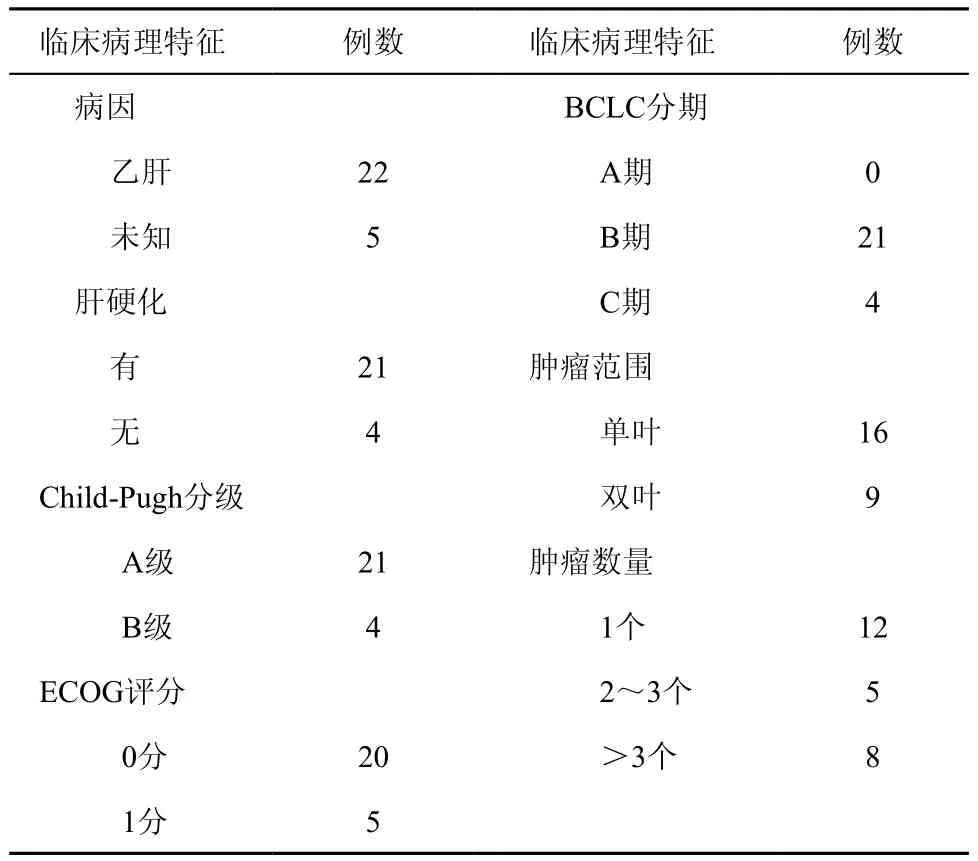
表1 患者术前资料
二、纳入标准及排除标准
纳入标准:(1)外科不能手术切除原发性病灶及转移性病灶;(2)肝功能Child- Pugh分级为A、B级;(3)门静脉主干未完全阻塞,或虽然门静脉主干完全阻塞,但肝门有较多代偿性侧支血管形成。排除标准:(1)肝功能Child-Pugh分级为C级;(2)凝血功能严重减退,且无法纠正;(3)门静脉主干完全由癌栓阻塞,侧支血管形成少或门静脉高压伴逆向血流;(4)合并感染,如肝脓肿不能同时得到治疗;(5)肿瘤全身广泛转移,估计患者生存期<3个月。
三、方法
1. CalliSpheres微球载药过程:(1)用20 ml注射器把7 ml CalliSpheres可载药微球(100~300 μm,江苏恒瑞公司)全部抽出,然后将注射器竖立放置2~3 min,直至微球沉降,分层明显,将上部清液推出,最后剩余载药微球约3~4 ml。(2)用10 ml注射器抽取注射用水或葡萄糖水溶解40 mg表柔比星,建议配制浓度20 g/L,确认化疗药完全溶解(化疗药浓度越高,微球吸附速度越快,起始加药量越高,微球吸附量就越大)。(3)用装有微球的20 ml注射器把化疗药全部抽出,让微球与化疗药混合进行载药,每5 min轻摇1次,共6次,载药时间30 min。(4)载药微球吸附表柔比星完毕后,按体积1∶1加入非离子型对比剂,轻轻摇匀,在烧杯中静置5 min后即可开始使用。
2. 手术过程:所有病例均在美国GE数字减影血管造影机上进行。应用Seldinger穿刺技术,穿刺成功后,常规动脉插管与血管造影,了解肿瘤供血特点。用2.7F Progrea(tTERUMO,Japan)超选插管至靶血管,用1 ml或2 ml注射器抽取载药微球表柔比星和对比剂混合液,经微导管注射到超选部位,注射时采用脉冲式注射,注射速度1~2 ml/min。待对比剂流速缓慢甚至停滞时,停止栓塞。再次造影,染色灶消失,结束手术。
3.术后处理:介入术后给予患者保肝、支持、止吐、镇痛等对症治疗3~5 d;酌情使用抗生素,静脉应用制酸药3 d。记录患者术中及术后出现的不良反应及并发症,并复查患者肝功指标,包括白蛋白、谷草转氨酶(AST)、谷丙转氨酶(ALT)及总胆红素。
4.术后随访方案及内容:①告知患者术后每月来院复查1次,根据改良实体瘤疗效评价标准(mRECIST)进行评价[3],分为完全缓解(CR)、部分缓解(PR)、疾病稳定(SD)和疾病进展(PD),疾病缓解为CR+PR,疾病控制为CR+PR+SD。②对比患者治疗前与术后随访时的肝功能变化;③根据术后不良反应及并发症,记录患者治疗过程中的不良反应及并发症(包括发热、疼痛、呕吐、肝破裂、上消化道出血、肝肾功能衰竭等)情况。
三、统计学处理
本研究采用SPSS 19.0 统计分析软件。计量数据采用x±s表示,治疗前后肝功能变化采用t检验,P<0.05为差异有统计学意义。
结 果
一、介入治疗情况
本组25例患者均顺利接受CalliSpheres载药栓塞微球治疗,技术成功率为100%,患者平均术后住院时间3~7 d。
二、介入治疗效果比较
25例患者随访6个月,疾病控制率为80%,见表2;术前肿瘤直径中位数为6.0 cm,术后肿瘤直径中位数为4.0 cm,较术前均有不同程度缩小,见图1。
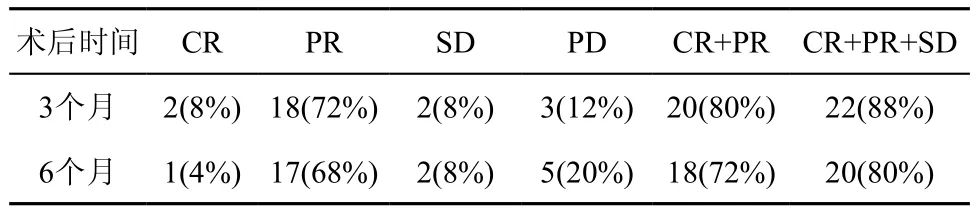
表2 术后不同时间的随访结果 例(%)
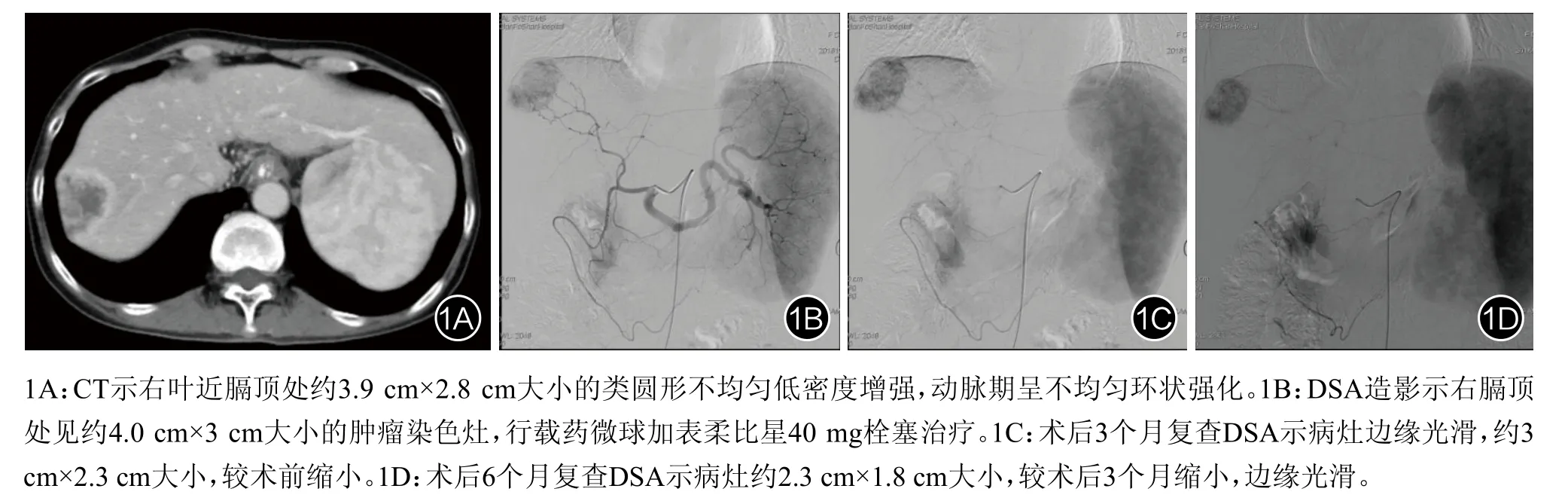
图1 典型病例手术前后CT及造影图
三、手术前后肝功能变化
术后3 d,肝功能变化主要表现为ALT、AST及总胆红素升高,与术前差异有统计学意义,白蛋白变化不明显,与术前差异无统计学意义,术后3个月,肝功能基本恢复正常水平,与术前比较差异无统计学意义,见表3,根据CTCAE4.0标准,患者术后肝功能Grade 1 级10例,Grade 2级8例,Grade 3级7 例。
四、并发症
术后最常见临床反应主要表现为轻度恶心呕吐、发热、6 h内出现轻度腹部疼痛。其中有6例患者严重腹痛和发热,对症处理后症状消失。术后所有患者均未出现肝肾功能衰竭、胆汁漏并发感染、肝脓肿、腹腔出血、肿瘤破裂出血、消化道出血、骨髓抑制及心脏毒性表现等严重并发症。
表3 患者治疗前后肝功能变化比较 ()

表3 患者治疗前后肝功能变化比较 ()
*P<0.05,a与术前比较P<0.05
时间 白蛋白(g/L)ALT(U/L) AST(U/L)总胆红素(μmol/L)术前 40.0±3.0 31.5±12.0 39.0±17.0 13.5±4.5术后3 d 37.0±5.6 86.0±53.0a132.0±82.0a 19.0±7.7a术后3个月 38.0±4.6 33.5±10.0 42.0±15.5 14.5±6.5 F 0.64 6.37* 15.54* 9.75*
讨 论
肝癌是我国常见的恶性肿瘤之一,手术切除仍然是最有效的治疗方法,5年生存率从29%到70%不等[4-5]。然而手术切除仅适用于约25%的患者中,即使患者接受切除手术后,复发率仍高达75%[6]。因此,仍然需要姑息治疗和可以将肿瘤降低至可手术切除程度的治疗方法。对于不能接受手术切除的中晚期肝癌患者的治疗方法推荐TACE[7],使用现代血管成像技术的化疗栓塞可以选择性地将材料送达至肿瘤,从而减少了化疗药剂释放到周围组织中[8],而且这是一项微创和可重复的操作过程。传统TACE中常用碘油加阿霉素或其他化疗药物混合给药,这种传统乳剂可导致化疗药物进入全身循环系统,增加了全身的不良反应并且降低了局部治疗效果[9]。
在肝癌介入治疗中,药物的持续释放及肿瘤内部药物浓度的维持起着重要的作用,载药栓塞微球在一定程度上解决了该问题,这种新型栓塞剂可以和化疗药物混悬,在TACE 的治疗过程中动脉内注射[10]。有研究发现,载药栓塞微球可以负载阿霉素,在肝癌细胞中达到较高的浓度并且延长阿霉素与肿瘤细胞的作用时间[11]。CalliSpheres载药栓塞微球作为一种新型可加载化疗药物的栓塞材料,能与蒽环类药物(阿霉素或表柔比星等)结合。与传统TACE 的栓塞材料碘油相比,CalliSpheres可载药栓塞微球的剂量远大于碘油,且安全性较高;具有缓释效应,可较长时间持续释放阿霉素。本研究中选用的微球为300~100 μm,目前国际上应用最小的微球直径为30~60 μm,尚未在国内上市。目前国外已有HepaSphere 微球治疗原发性肝癌的报道,Malagari等[12]使用加载阿霉素的直径30~60 μm的HepaSphere微球治疗原发性肝癌,结果显示3个月疾病缓解率为68.9%,疾病控制率为88.9%。结合本研究结果可以看出,与HepaSphere 微球相比,CalliSpheres可载药栓塞微球对于中晚期肝癌也具有良好的治疗效果。有国内文献报道,与普通碘油栓塞治疗原发性肝癌相比,应用载药栓塞微球治疗能取得更好的治疗效果及较少的并发症[13]。本研究随访结果显示,CalliSpheres治疗肝癌的3个月疾病缓解率(CR+PR)为80%,疾病控制率为88%,随着时间的延长,疾病缓解率及疾病控制率均出现不同程度的下降。主要原因可能是:肿瘤侧支循环的再建立和栓塞血管的再通。目前已有随机对照临床试验报道,微球栓塞与传统TACE相比,术后并发症及栓塞术后腹痛程度与传统TACE比较无明显差异,肝功能变化主要表现为术后1周内转氨酶轻度升高[14]。本研究结果显示在术后3 d转氨酶较术前轻度升高,但术后3个月时肝功能基本恢复至术前水平。虽然几乎所有患者在栓塞后3~7 d会出现肝脏转氨酶的轻度升高,这在传统TACE 中也是经常发生的。90%以上的患者在传统TACE 治疗后都会出现栓塞术后综合征(postembolizationsyndrome,PES),但使用微球栓塞治疗的患者都表现出了较好的耐受性。本研究中患者术后大多出现轻度的栓塞后综合征,主要为轻度腹痛、发热及呕吐。有文献报道,使用微球栓塞的并发症发生率为4.2%~11.4%,包括胸膜渗出、胃溃疡出血、食管静脉曲张出血、肝功能衰竭、胆囊炎及肝脓肿形成[15]。与治疗相关的病死率为0~3.7%,造成死亡的原因有肝功能衰竭、肝破裂、肝脓肿和胆囊炎等。本研究所有患者均未出现肝功能衰竭、胆汁漏、感染、肝脓肿、肿瘤破裂出血、消化道出血、骨髓抑制及心脏毒性等严重并发症。
总之,载药后的CalliSpheres用于中晚期肝癌的治疗可获得良好的收益,但一些结论仍需大量的随机对照试验证实。尽管如此,与传统的TACE相比,CalliSpheres载药栓塞微球仍有其明显的优势,在临床上值得推广。
1 Aliberti C, Tilli M, Benea G, et al. Trans-arterial chemoembolization (TACE) of liver metastases from colorectal cancer using irinotecaneluting beads: preliminary results[J]. Anticancer Res, 2006,26:3793-3795.
2 Thirion P, Michiels S, Pignon JP, et al. Modulation of fluorouracil by leucovorin in patients with advanced colorectal cancer: an updated metaanalysis[J]. J Clin Oncol, 2004, 22:3766-3775.doi: 10.1200/ JCO.2004.03.104.
3 Rees M, Tekkis PP, Welsh FK, et al. Evaluation of longterm survival after hepatic resection for metastatic colorectal cancer: a multifactorial model of 929 patients[J]. Ann Surg, 2008, 247:125-135. doi: 10.1097/ SLA.0b013e31815aa2c2.
4 Smith MD, McCall JL. Systematic review of tumour number and outcome after radical treatment of colorectal liver metastases[J]. Br J Surg, 2009, 96:1101-1113. doi: 10.1002/bjs.6735.
5 Bhattacharjya S, Aggarwal R, Davidson BR. Intensive follow-up after liver resection for colorectal liver metastases: results of combined serial tumour marker estimations and computed tomography of the chest and abdomen—a prospective study[J]. Br J Cancer, 2006, 95:21-26.doi: 10.1038/sj.bjc.6603219.
6 Hurwitz H, Fehrenbacher L, Novotny W, et al. Bevacizumab plus irinotecan, fluorouracil, and leucovorin for metastatic colorectal cancer[J]. N Engl J Med, 2004, 350:2335-2342.doi: 10.1016/ j.clcc.2016.07.013.
7 Tang Y, Taylor RR, Gonzalez MV, et al. Evaluation of irinotecan drug-eluting beads: a new drug-device combination product for the chemoembolization of hepatic metastases[J]. J Control Release, 2006, 116:e55-e56. doi:10.1016/j.jconrel.2006.09.047.
8 Sobrero AF, Maurel J, Fehrenbacher L, et al. EPIC: phase III trial of cetuximab plus irinotecan after fluoropyrimidine and oxaliplatin failure in patients with metastatic colorectal cancer[J]. J Clin Oncol, 2008, 26: 2311-2319. doi: 10.1200/JCO.2007.13.1193.
9 赵艳,韩国宏,白苇,等.药物缓释微球肝动脉化疗栓塞治疗肝癌研究进展[J].介入放射学杂志,2012,21(1):79-83.doi:10.3969/ j.issn.1008-794X. 2012.01.020
10 Jordan O, Denys A, de Baere T, et al. Comparative study of chemoembolization loadable beads: in vitro drug release and,physical properties of DC bead and hepasphere loaded with doxorubicin and irinotecan[J]. J Vasc Interv Radiol, 2010, 21:1084-1090.doi: 10.1016/ j.jvir.2010.02.042.
11 邵海波,张曦彤,李红,等. 栓塞微球在肝癌介入治疗中的应用[J].介入放射学杂志,2008,17:776-778.doi:10.3969/j.issn.1008-794X.2008.11.005.
12 Malagari K, Pomoni M, Moschouris H, et al. Chemoembolization of hepatocellular carcinoma with HepaSphere 30-60 μm. Safety and efficacy study[J]. Cardiovasc Intervent Radiol, 2014, 37: 165-175.doi: 10.1007/s00270-013-0777-x.
13 段峰,阎洁羽,刘凤永,等.装载阿霉素的DC- Beads 经导管化疗栓塞治疗不可切除性原发性肝癌的初步经验[J].中华肿瘤杂志,2014,36: 314-315.doi:10.3760/cma.j.issn.0253-3766.2014.04.016.
14 Golfieri R, Giampalma E, Renzulli M, et al. Randomised controlled trial of doxorubicin- eluting beads vs conventional chemoembolisation,for hepatocellular carcinoma [J]. Br J Cancer, 2014,111: 255-264.doi: 10.1038/bjc.2014.199.
15 Malagari K, Pomoni M, Spyridopoulos TN, et al. Safety profile of,sequential transcatheter chemoembolization with DC Bead:,results of 237 hepatocellular carcinoma (HCC ) patients [J]. Cardiovasc Intervent Radiol, 2011, 34: 774-785.doi: 10.1007/s00270-010-0044-3.
Interventional chemoembolization with CalliSpheres-loaded microspheres for the treatment of advanced hepatocellular carcinoma
Jiang Song, Li Guijie, Zhou Zhuqian, Niu Wei. Department of Interventional Radiology,Qianfoshan Hospital attached Shandong University, Jinan 250014, China
Zhou Zhuqian ,Email: zhouzhuqian@126.com
Objective:To evaluate the safety and clinical short-term efficacy of interventional embolization with CalliSpheres-loaded microspheres in treating advanced hepatocellular carcinoma.Methods:A total of 25 patients with advanced hepatocellular carcinoma underwent transcatheter arterial chemoembolization (TACE) plus using CalliSpheres-loaded microspheres treatment. The clinical and imaging data, complications of interventional treatment and prognosis were summarized and analyzed by modified response evaluation criteria in solid tumors (mRECIST); follow-up was performed on all patients.Results:The follow-up lasted 6 months. According to mRECIST, the 3-month objective response rate (CR+PR) was 80% and disease control rate (CR+PR+SD) was 88%; the 6-month objective response rate (CR+PR) was 72% and disease control rate (CR+PR+SD) was 80%. At day 3 after the procedure, the levels of ALT, AST and TBIL were increased, with a statistical significance compared with those before the operation. However, there was no significant difference in the level of albumin. At 3 months postoperatively, the indications of liver function returned to the normal level. And there was no significant difference between preand post-operation. No severe complications, such as bile leak with infection, liver abscess, abdominal hemorrhage, bleeding due to tumor rupture and gastrointestinal bleeding occurred in these patients.Conclusion:TACE performed with CalliSpheres-loaded microspheres is a novel and safe option for patients with advanced hepatocellular carcinoma. Its clinical short-term efficacy was satisfied, yet its long-term efficacy needs further studies.
Transcatheter arterial chemoembolization; Hepatocellular carcinoma; Drug-loaded microspheres; CalliSpheres
2017-04-16)
(本文编辑:闫娟)
10.3877/cma.j.issn.2095-5782.2017.03.013
250014 山东济南,山东大学附属千佛山医院介入科
周祝谦,Email: zhouzhuqian@126.com
姜松,李桂杰,周祝谦,等. CalliSpheres载药栓塞微球治疗中晚期肝癌临床效果评价[J/CD].中华介入放射学电子杂志,2017,5(3):174-178.

