冠心病合并二尖瓣中度关闭不全患者冠状动脉旁路移植术联合二瓣置换术的效果
王岳峰 杨 鹏 邬 飞 杨雪峰 石 磊 祝沪军 许日昊
(大庆油田总医院胸心外科二病房,黑龙江 大庆 163001)
冠心病合并二尖瓣中度关闭不全患者冠状动脉旁路移植术联合二瓣置换术的效果
王岳峰 杨 鹏 邬 飞 杨雪峰 石 磊 祝沪军 许日昊1
(大庆油田总医院胸心外科二病房,黑龙江 大庆 163001)
目的 总结冠心病(CAD)合并二尖瓣中度关闭不全患者外科手术治疗病例及手术经验。方法 27例就诊于大庆油田总医院胸心外科的冠心病合并二尖瓣中度关闭不全患者,其中单纯行冠状动脉旁路移植术(CABG)22例,同期行二尖瓣置换(MVR)手术5例。观察患者术前、术中、术后瓣膜反流程度、左室射血分数(LVEF)及左室大小。结果 全组患者无死亡,术后瓣膜反流程度、左心室大小较术前均减轻(P<0.05),MVR组较CABG组在左室大小和LVEF方面改善更明显。结论 对于CAD合并二尖瓣中度关闭不全的患者,术式的选择需综合考虑瓣膜反流原因、心脏改变情况、反流束情况、心功能以及术中食道超声检查结果。
冠心病;二尖瓣关闭不全;冠状动脉旁路移植术
冠心病(CAD)患者因心肌缺血或心肌梗死会造成二尖瓣的缺血从而导致二尖瓣关闭不全(MR)。据报道〔1〕,CAD引起的乳头肌缺血或坏死已成为引起MR的第二位原因,占10%~27%。而在进行冠状动脉旁路移植术(CABG)的同期是否行二尖瓣手术目前尚有争议,尤其对合并中度MR的患者是否需同期行二尖瓣手术尚无明确手术指征。本研究经外科手术治疗此类患者27例,观察患者出院前后心脏状况并与术前进行对比。
1 资料与方法
1.1 一般资料 选取2013年1月至2016年6月大庆油田总医院外科手术治疗的27例患者,均行冠状动脉造影确诊为符合搭桥指征,体重50~97〔平均(70.96±12.22)〕kg,年龄43~75〔平均(60.7±8.44)〕岁。术前均有不同程度的前胸后背针刺样疼痛并伴有胸闷、气短、心悸等症状,9例有不稳定心绞痛病史,12例有心肌梗死病史,入院后心前区听诊可闻及Ⅱ~Ⅲ级收缩期杂音,纽约心脏病协会(NYHA)心功能分级:Ⅱ级18例,Ⅲ级8例,Ⅳ级1例。心脏彩超提示左心室舒张期末内径48~ 64 mm,平均(54.56±5.08)mm,射血分数(EF)(53.89±4.62)%,其中EF小于0.5者2例。根据反流面积判定其反流程度,轻度反流2~4 cm2,中度反流5~8 cm2,重度反流>8 cm2。患者临床诊断均为CAD合并MR。单纯行CABG手术22例,同期行CABG+二尖瓣置换(MVR)手术5例。
1.2 手术方法 手术均在全麻体外或非体外循环下进行,胸骨正中切口。8例在体外循环下进行,其中包括同期行MVR者5例及单纯行CABG者3例,其余均在非体外循环下进行。CABG病例先进行左乳内动脉与前降支吻合,然后行大隐静脉与冠状动脉远端序贯桥吻合,最后在升主动脉侧壁钳下完成近端吻合。CABG+MVR病例首先经主动脉及上、下腔静脉插管建立体外循环,阻断升主动脉、心脏停搏后,先行大隐静脉与冠状动脉远端序贯桥吻合,然后行二尖瓣人工瓣膜置换,然后行大隐静脉与主动脉端侧吻合,最后在心脏停搏或不停搏时完成乳内动脉与冠状动脉前降支吻合。3例体外循环下单纯行CABG病例均为因术中心率、血压不能有效维持而转为体外循环辅助下心脏不停跳CABG手术。
1.3 统计学处理 应用SPSS19.0软件行t检验。
2 结 果
表1可见,全组病例术后30 d内无在院死亡,旁路移植血管(2.74±0.45)支,移植血管材料包括大隐静脉、 乳内动脉,同期二尖瓣机械瓣膜置换5例,均痊愈出院。术后使用多巴胺平均剂量为3.0~10.0 μg·kg-1·min-1,硝酸甘油平均剂量为0.3~0.15 μg·kg-1·min-1,部分应用肾上腺素的平均剂量(0.03~0.15 μg·kg-1·min-1)支持心脏功能。出院时心功能Ⅰ 级23例,Ⅱ 级4例。单纯CABG和CABG+MVR组左室大小、二尖瓣反流面积均较术前缩小,术后左室射血分数(LVEF)值较术前升高(均P<0.05)。术后6个月两组病例二尖瓣反流面积均得到明显改善,而CABG+MVR左室缩小和LVEF升高程度更加显著(P<0.05)。
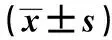
表1 两组术前、术中、术后心脏彩超情况
与术前比较:1)P<0.05
3 讨 论
CAD患者中约有20%患者伴有二尖瓣反流〔1〕,此类患者较单独患有缺血性心脏病患者预后更差,手术风险较高。缺血性二尖瓣反流是因心肌缺血或梗死导致室壁运动异常,以致乳头肌位置改变,腱索长度发生相对变化,从而导致瓣膜的关闭不全,但患者瓣叶形态、结构正常。对此类患者中轻度反流的患者可单独行CABG治疗,因为心肌再血管化后可使心肌恢复灌注,瓣膜功能得到恢复从而使反流减轻或消失。有学者认为,在行CABG时,轻度的MR可以不处理,其远期生存率不受影响〔2〕。而同时伴有重度的二尖瓣反流患者一般需同期行CABG+MVR/MVP,但对于同时伴有中度的二尖瓣反流患者是否需行二尖瓣手术目前争议较大〔3〕。研究认为同期行CABG+MVR/MVP短期和中期的随访效果均较好〔4〕,提倡同期行二尖瓣手术,但是也有研究认为单独行CABG患者在术后死亡率、中期生存率、心功能分级和同期行CABG+MVR的患者没有明显区别〔5〕。还有研究认为单独CABG能够提高LVEF,减小二尖瓣反流程度,提高生存率〔6〕。搭桥手术同期行瓣膜手术必然使手术复杂且涉及心脏停搏,导致风险增高,其死亡率高于单独行搭桥手术。相关研究认为,对于重度MR同期行CABG+MVP手术治疗与单纯行CABG相比手术死亡率增加,且术后二尖瓣反流情况差异不大〔7〕。因此,在手术之前需要对瓣膜病变做出详细评估,是缺血性病变导致还是器质性病变,血管重建后是否能改善瓣膜缺血从而使瓣膜病变改善,从而分析出是否需要同期处理瓣膜病变。
对于CAD患者瓣膜反流是否应搭桥术同期对二尖瓣进行干预,不能单以反流程度作为是否进行二尖瓣手术的唯一标准,二尖瓣本身反流原因、反流束数量(单束或多束)和反流性质(中心性或偏心性)都应在考虑范围之中。反流原因包括器质性(瓣环扩大,腱索断裂,瓣叶风湿性改变等)和功能性(瓣膜及瓣下结构缺血)。瓣膜器质性病变以及多束、偏心性反流等必然需同期行二尖瓣手术治疗。而瓣膜形态结构正常伴单束、中心性反流且反流量处于中度时,还要考虑左室大小,左室扩大可引起MR,瓣环周径扩大超过正常的10 mm时常导致MR,此外LVEF值也需考虑。Nanley等〔8〕认为术前心功能、EF值均影响手术死亡率。术前存在较严重心力衰竭症状的患者大多伴有二尖瓣中度反流,入院后暂给予强心、利尿、扩冠、补充电解质补钾营养心肌等对症支持治疗,待调整后如心力衰竭症状消失或复查心脏彩超EF升高,瓣膜反流面积减少,提示心肌尚有大量处于顿抑状态或冬眠状态的心肌,血管重建后瓣膜缺血状态可改善,可考虑单纯行CABG;如心力衰竭改善不明显或复查超声心动EF升高及瓣膜反流面积减少不明显需同期行CABG+MVR/MVP手术。对于CAD合并二尖瓣中度关闭不全的患者,MR还可能是功能性的可逆性心肌缺血造成,在血管化后因乳头肌及腱索功能改善关闭不全有可能改善,此类病例可单独行CABG术,术后同样可取得较好效果。因此,术前评价MR是功能性的还是器质性的十分重要。
另外,MR反流程度的评估本身受到多方面的影响,比如超声心动机器、操作人员水平及经验、患者接受检查时体循环血流动力学的变化对二尖瓣反流速度图像的影响等,因此获得对二尖瓣关闭不全严重程度的准确评价较为困难。特别是经胸超声心动图检查时受肥胖、肺部气体、胸壁畸形等诸多因素的影响,约20%的患者常不能获得比较清晰满意的图像,致使诊断受限。而绝大多数CAD患者同时伴有肥胖,致使经胸心脏彩超的结果在肥胖的CAD患者中的精确性更加受到质疑。经食道超声心动能更加准确的评估二尖瓣病变情况,反流面积多较经胸心脏彩超面积小。
对于CAD合并MR患者术式的选择:(1)对于术前常规行经胸食道超声二尖瓣轻度及以下关闭不全且为中心性反流患者,如无二尖瓣器质性病变,多选择单纯CABG治疗,术中食道超声非必须检查。(2)对于术前常规行经胸食道超声二尖瓣存在器质性病变以及重度反流患者应在CABG同期行二尖瓣手术,因二尖瓣重度反流患者多合并腱索断裂等器质性二尖瓣病变且反流常为两束以上的偏心性反流。(3)对于二尖瓣手术,报道一般认为首选瓣膜成形术〔9〕,同时成形术后应用术中食道超声及时评价成形效果,风湿性病变应首选瓣膜置换术。但瓣膜成形手术对术者经验及手术技巧要求较高且不适合较严重的慢性缺血性MR〔10〕。本组中二尖瓣处置办法在取得患者及家属同意后均选用二尖瓣置换术。但此类患者需注意术后抗凝治疗及监测,避免抗凝意外。(4)术前常规行经胸食道超声,对于二尖瓣中度关闭不全且未见明显器质性病变的患者,需经术中食道超声进一步证实二尖瓣反流程度,如术中食道超声证实反流二尖瓣为单束中心型且反流量确实在中度以下或较术前经胸超声有明显改善者,同时左室大小在65 mm以下,则单纯给予CABG,术后出院前复查及中期随访效果良好。对术中食道超声证实二尖瓣反流为多束或偏心型,以及反流量较术前经胸超声无明显改善者,考虑CAD所致的慢性缺血性病变对二尖瓣及周围结构损伤较严重且单纯恢复血供逆转不佳,故同期给予二尖瓣手术处置。此类术前经胸超声中度二尖瓣反流的患者,术中食道超声发挥了较关键的作用。(5)综合考虑患者术前状态,如患者术前左室大小≥65 mm,EF值<0.5,且有明显心力衰竭症状者,此类患者多伴有二尖瓣中度以上反流,同时瓣膜病变较严重。此类患者手术风险较大,术前一般需经系统改善心功能治疗且术式选择时需谨慎。一般建议同期行二尖瓣手术处置以提高术后心功能及生活质量,但手术风险相应增加。
1 Gillinov AM,Wierup PN,Blackstone EH,etal.Is repair preferable to replacement for ischemic mitral regurgitation〔J〕?J Thorac Cardiovasc Surg,2001;122(6):1125-41.
2 Harris KM,Sundt TM,Aeppli D,etal.Can late survival of patients with moderate ischemic mitral regurgitation be impacted by intervention on the valve〔J〕? Ann Thorac Surg,2002;74(5):1468-75.
3 Adams DH,Filsoufi F,Aklog L.Surgical treatment of the ischemic mitral valve〔J〕.J Heart Vavlve Dis,2002;11(Suppl 1):S21-S25.
4 Chan KM,Punjabi PP,Flather M,etal.Coronary artery bypass surgery with or without mitral valve annuloplasty in moderate functional ischemic mitral regurgitation:final results of the Randomized Ischemic Mitral Evaluation(RIME)trial〔J〕.Circulation,2012;126:2502-10.
5 Diodato MD,Moon MR,Pasque MK,etal.Repair of ischemic mitral regurgitation does not increase mortality or improve long-term survival in patients undergoing coronary artery revascularization:a propersity analysis〔J〕.Ann Thorac Surg,2004;78:794-9.
6 Hamner CE,Sundt TM.Trends in the surgical management of ischemic mitral regurgitation〔J〕.Curr Cardiol Rep,2003;5:116-24.
7 Kang DH,Kim MJ,Kang SJ,etal.Mitral valve repair versus revascul arization alone in the treatment of ischemec mitral regurgitation〔J〕.Circulation,2006;11(Suppl 1):I499-I503.
8 Nanley DL,Grunkemeier GL,Starr A.Aortic valve replacement with coronary bypass grafting.Significant determinants of ten-year survival〔J〕.Thorac Cardiovasc Surg,1983;85:705-11.
9 鲍春荣,梅 举,王宜青,等.冠心病伴缺血性二尖瓣关闭不全27例手术治疗分析〔J〕.上海交通大学学报,2008;28(3):326-8.
10 麦明杰,陈星权,郑少忆,等.冠心病合并重度缺血性二尖瓣关闭不全的外科治疗早期疗效分析〔J〕.南方医科大学学报,2011;31(6):1072-4.
〔2017-02-07修回〕
(编辑 郭 菁)
王岳峰(1982-),男,主治医师,主要从事心脏瓣膜病和冠心病的外科治疗研究。
R65
A
1005-9202(2017)14-3468-03;
10.3969/j.issn.1005-9202.2017.14.038
1 吉林大学第二医院心血管外科

