线性探针联合HPLC研究六锐胶囊中没食子酸的眼部药代动力学
郭俊国,王兴荣,2,赵晴,宋继科,毕宏生,2
·论著:实验研究·
线性探针联合HPLC研究六锐胶囊中没食子酸的眼部药代动力学
郭俊国1,王兴荣1,2,赵晴3,宋继科3,毕宏生1,2
目的建立线性探针联合高效液相色谱(HPLC)测量兔前房没食子酸的方法,探讨六锐胶囊中没食子酸的眼部药代动力学参数。方法6只新西兰大白兔前房植入微透析线性探针(CMA402),灌胃给予六锐胶囊(20ml/kg)。以乙腈和0.1%醋酸水为流动相梯度洗脱,283 nm检测没食子酸浓度,DAS 2.0分析没食子酸的药代动力学参数。结果没食子酸检测限为0.67μg/ml,定量限为1.34μg/ml,在1.34~20.13μg/m l间线性关系良好,精密度和稳定性的相对标准差(RSD)分别为0.77%和2.21%,体内回收率为50.78%。没食子酸前房药代动力学符合二室模型,生物半衰期为54min,达到最大浓度时间为80min。结论采用线性探针联合HPLC实时测量兔眼没食子酸前房浓度准确可靠;六锐胶囊中的没食子酸可以进入兔眼前房,其药代动力学符合二室模型特征。
六锐胶囊;没食子酸;线性探针;高效液相色谱;药代动力学
六锐胶囊为藏药,由诃子、红花、巴夏嘎、木香、安息香、人工麝香六种药物组成,具有清热凉血、明目退翳功效,主要用于血、胆、疬引起的头痛病,云翳等眼科疾病[1]。临床发现六锐胶囊对白内障、糖尿病性视网膜病变、眼底出血及渗出等均有较好的临床疗效,但其作用机制和药效物质基础仍不明确[2-4]。我们前期研究发现,六锐胶囊可通过减轻前房炎症渗出和炎症细胞浸润,保护眼部组织结构,增强机体抗氧化能力,调节免疫状态,发挥对葡萄膜炎的治疗作用[5]。诃子主要含有没食子酸、诃子酸等化学成分,没食子酸具有抗炎、抗氧化、抗自由基等多种生物学活性,是六锐胶囊的有效化学成分之一[6]。微透析采样技术可以提供眼前房组织游离药物浓度的实时、连续、在线监控,同步进行检测前房内药物浓度变化[7]。本研究旨在通过微透析CMA402探针实时取样房水,高效液相色谱法(high performance liquid chromatography,HPLC)检测没食子酸的浓度,探讨其眼部药代动力学。
1 材料与方法
1.1 材料
新西兰大白兔6只,雌雄兼有,体质量2.0~2.5 kg,山东大学动物实验中心提供,动物许可证号SYXK(鲁)2003-0020。在室温20~26℃,相对湿度40%~70%,光照12 h明暗交替的环境中饲养。
六锐胶囊(西安大唐制药集团有限公司提供,国药准字:Z20090461);没食子酸对照品(中国药品生物制品检定院,A0110);乙腈和甲醇(色谱级,Productof Tedia,United States America);其它试剂均为分析纯。
戴安U-3000液相色谱仪(UltiMate 3000自动进样器,UltiMate 3000泵,UltiMate 3000二极管阵列检测器,UltiMate 3000 RS柱温箱);EL204电子天平(德国梅特勒有限公司);MS205DU十万分之一天平(德国梅特勒公司);FW135高速粉碎机(北京市永光明医疗器械有限公司);KQ5200B型超声波清洗器(昆山市超声仪器有限公司)。微透析线性探针(CMA 30,瑞典CMA公司)。
1.2 样品制备与灌胃
取六锐胶囊内容物在真空干燥箱中干燥8 h,高速粉碎后过60目药筛。称取100 g,置三角烧瓶中,加25%甲醇200ml,称定质量,超声处理30min,滤过,取续滤液浓缩至1ml相当于1 g药材。采用兔用开口器进行灌胃,剂量为20ml/kg。
1.3 没食子酸对照品溶液的制备
精密称取没食子酸对照品4.63mg,置10ml棕色容量瓶中,加25%甲醇溶解并定容,得对照品储备液。精密量取对照品储备液1.0ml,置10ml棕色容量瓶中,加25%甲醇溶解并定容,得对照品溶液46.3μg/ml。 1.4色谱条件与系统适用性
色谱柱:Acclaim 120 A C18色谱柱(5μm,4.6 mm×150mm),流动相A为乙腈,流动相B为0.1%醋酸水,梯度洗脱:0min 97%B;5min 95%B;10min 55%B;20min 75%B;25min 97%B;流速为1.0ml· min-1,检测波长为283 nm,柱温30℃进样量5μl。
1.5 探针植入方法
术前3 d常规抗生素眼液点眼,术前30min耳缘静脉注射肝素钠(100U/kg),防止前房炎性渗出。腹腔注射1%戊巴比妥纳(1mg/kg)麻醉实验兔,将其侧卧固定于解剖台上,开睑器开睑,5号针头沿睑裂方向于角巩膜缘处进针,做贯通前房穿刺,导入探针,使探针渗析窗全部浸入房水中[8](图1)。
微透析探针植入兔眼部后,约2 h前房恢复,以生理氯化钠溶液为灌注液,流速设定为1μl/min,冲洗0.5 h后,开始灌胃,并将流速设定为2μl/min,每一样品收集20min,HPLC色谱法测定渗析液中没食子酸含量。
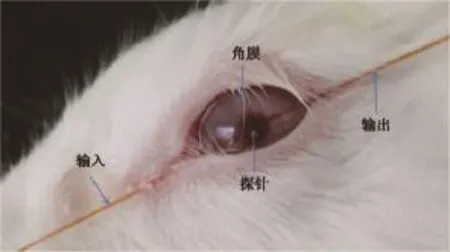
图1 眼部微透析线性探针植入图
1.6 方法学考察
工作曲线:分别精密吸取浓度为40.26μg/ml的没食子酸对照品各0.5、1、2.5、3.75、5.0ml,置10ml棕色容量瓶中,加25%甲醇溶解并定容,精密吸取5 μl,注入液相色谱仪测定。以没食子酸浓度为横坐标,以吸光度为纵坐标,绘制工作曲线。
检测限和定量限:将没食子酸对照品溶液依次稀释至不同浓度,按照1.4的色谱条件分别测定。以信噪比3∶1作为检测限,以信噪比10∶1作为定量限。
精密度和稳定性:取浓度为6.671μg/mL没食子酸对照组溶液,按照1.4的色谱条件连续进样5次,计算精密度。分别于0、2、4、8、12、24 h,按照1.4的色谱条件分别进样,计算稳定性。
回收率:微透析探针植入家兔眼部后,约2 h前房恢复,以零净通量法,分别以6.671μg/mL和20.13μg/mL的没食子酸溶液进行灌注,流速设定为1μl/min,更换灌注液后,至少冲洗0.5 h才开始取样,每一样品收集20min,HPLC色谱法测定渗析液中没食子酸含量,计算探针在体回收率(Rinvivo)。Rinvivo=(Cd-Cp)/(Cm-Cp)×100%。Cd为渗析液药物浓度,Cp为灌注液中的药物浓度,Cm为组织中的药物浓度[9]。
1.7 药物动力学分析
药代动力学软件DAS 2.0进行前房药物的药时动力学分析;用灌胃器将六锐胶囊样品溶液灌到动物胃内,流速设定为2μl/min,每一样品收集20 min,收集360min共18个样品,按照1.4的色谱条件分别测定。以没食子酸浓度和时间绘制曲线,以lgC-t判断房室模型。
2 结果
2.1 专属性
实验结果表明,所建立的样品处理方法和检测条件下,没食子酸对照品和样品图谱保留时间一致,微透析线性探针对没食子酸的保留时间无影响(图2~图4)。
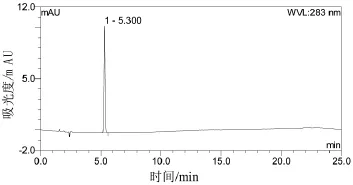
图2 没食子酸对照组色谱图(高效液相色谱法)。数字1标示了没食子酸的保留时间
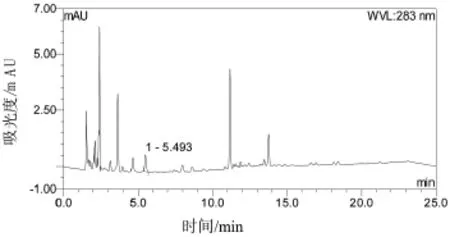
图3 六锐胶囊样品溶液色谱图(高效液相色谱法)。数字1标示了没食子酸的保留时间
2.2 工作曲线
没食子酸在1.34~20.13μg/ml范围线性关系良好,回归曲线为y=0.0106x+0.0012,r=0.9999。见图5。
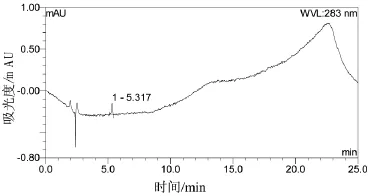
图4 六锐胶囊微透析溶液色谱图(高效液相色谱法)。数字1标示了没食子酸的保留时间
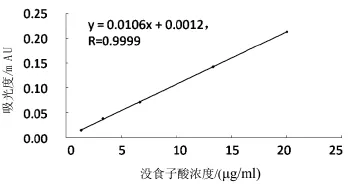
图5 没食子酸线性范围
2.3 检测限和定量限
没食子酸的检测限为0.67μg/ml,定量限为1.34μg/ml。
2.4 精密度和稳定性
没食子酸连续进样5针,峰面积分别为0.0744、0.0737、0.0734、0.0735、0.0728,相对标准差(RSD)值为0.77%,表明仪器的精密度良好。没食子酸不同时间的峰面积分别为0.0741、0.0733、0.0748、0.0715、0.0711,RSD值为2.21%,说明没食子酸溶液在24 h内稳定性良好。
2.5 探针回收率
探针植入兔眼前房后测得体内回收率为50.78%±3.02%,表明探针回收率良好。
2.6 没食子酸药代动力学
由没食子酸在新西兰大白兔前房的参数和lgC-t曲线,其药代动力学符合二室模型,生物半衰期为54min,达到最大浓度时间为80min。具体结果见表1,图6和图7。表明六锐胶囊中没食子酸可以进入新西兰大白兔前房。
3 讨论
为证实六锐胶囊中诃子的有效成分没食子酸是否可进入前房发挥治疗作用,本研究应用线性微透析探针实时取样技术,建立没食子酸的HPLC检测方法,并采用DAS 2.0分析前房没食子酸的药代动力学参数。微透析技术是一项完善的在体取样技术,可实现不同组织同时取样,为阐明药物的体内过程及作用机制提供依据,原理是基于物质的自由扩散,降低生物样本个体差异,结合高灵敏度的分析检测技术,达到连续监测动态变化的目的[10-12]。方法学考察的结果显示,没食子酸检测限为0.67μg/mL,定量限为1.34μg/mL,在1.34μg/mL~20.13μg/mL范围线性关系良好,精密度和稳定性的RSD值分别为0.77%和2.21%,探针体内回收率为80.78%,说明微透析联合HPLC检测技术可以实时准确地测定动物眼前房中的没食子酸浓度,是进行眼部药代动力学研究的便捷工具。本研究发现,六锐胶囊中的没食子酸可以进入新西兰大白兔前房,药代动力学符合二室模型,生物半衰期为54min,达到最大浓度时间为80min。但六锐胶囊中没食子酸如何进入前房,原因尚未深入研究,可能与六锐胶囊中的芳香开窍药人工麝香和安息香有关。
综上所述,线性探针联合HPLC连续测量动物眼没食子酸前房浓度准确可靠;六锐胶囊中的没食子酸可以进入兔眼前房,其药代动力学符合二室模型特征。
表1 六锐胶囊灌胃给药实验兔前房内没食子酸的药物动力学参数(±s,n=6)

表1 六锐胶囊灌胃给药实验兔前房内没食子酸的药物动力学参数(±s,n=6)
参数单位参数值t1/2βmin54.21±2.17 AUC(0-360)mg·L-1·min38.79±1.58 AUC(0-∞)mg·L-1·min42.50±3.12 MRT(0-∞)min180.11±9.76 Tmaxmin80.00±5.34 CLz/FL·min-1·kg-10.04±0.01 Cmaxmg·L-10.25±0.03
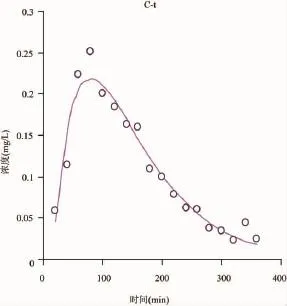
图6 没食子酸在实验兔前房的药物浓度-时间曲线
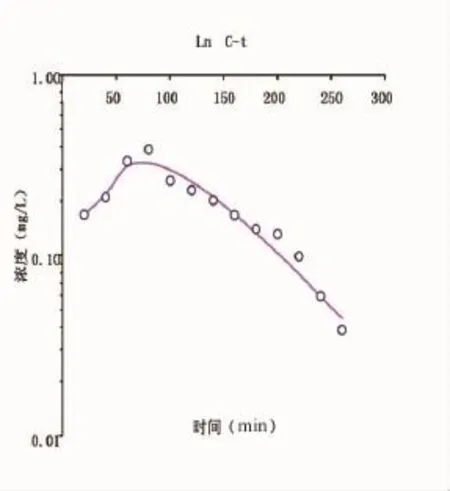
图7 没食子酸在实验兔前房的lgC-t曲线
[1]武向锋,刘俊,沈娟,等.六锐胶囊的质量标准研究[J].解放军药学学报,2009,25(5):410-414.
[2]仝警安,王西欧.六锐胶囊结合西药治疗白内障的疗效观察[J].陕西中医,2016,37(1):80-81.
[3]王军.六锐胶囊联合视网膜激光光凝治疗糖尿病视网膜病变临床研究[J].亚太传统医药,2015,11(12):100-102.
[4]罗晓阳.六锐胶囊治疗眼底出血及渗出疗效探讨[J].中医眼耳鼻喉杂志,2014,4(1):22-24,37.
[5]郭俊国,赵晴,王兴荣,等.六锐胶囊对葡萄膜炎大鼠血清SOD? MDA和NT-3含量的影响[J].眼科新进展,2016,36(4):334-335; 344.
[6]王嘉伦,王培杰,易智威,等.诃子的化学成分、药理作用及炮制配伍应用研究进展[J].中医药信息,2016,33(3):123-126.
[7]Song J,BiH,Xie X,etal.Naturalborneolenhancesgeniposideophthalmic absorption in rabbits[J].Int JPharm,2013,445(1-2):163-170.
[8]宋继科,毕宏生,郭俊国,等.冰片对盐酸青藤碱滴眼液角膜透过性的影响[J].时珍国医国药,2013,24(6):1321-1323.
[9]郑达敏,吕耿彬,王利胜,等.雷公藤甲素微透析体外回收率的研究[J].中国医药导报,2013,10(13):17-19.
[10]马金龙,姜国斌,姚善泾,等.微透析技术在植物生理生化研究中的应用[J].湖北农业科学,2013,52(12):2733-2736.
[11]董冉冉,王萌,刘志东,等.微透析技术在中药成分体内分析研究中的应用[J].中草药,2015,46(20):3117-3124.
[12]Boddu SH,Gunda S,Earla R,etal.Ocularmicrodialysis:a continuoussampling technique to study pharmacokineticsand pharmacodynamics in theeye[J].Bioanalysis,2010,2(3):487-507.
Study on ocular pharmacokinetics of gallic acid from Liurui capsule by line probe combined w ith HPLC
GUO Junguo,WANG Xingrong,ZHAOQing,et,al.Eye Institute of Shandong University of Traditional ChineseMedicine,Jinan 250002,China
OBJECTIVE To establish themeasurementmethod ofgallic acid in rabbitanterior chamber by line probe combined high performance liquid chromatography(HPLC),and to study the ocular pharmacokinetics of gallic acid of Liurui capsule.METHODS Six New Zealand white rabbits were implanted with linear probemicro dialysis(CMA402)in anterior chamber,Liurui capsule(20ml/kg)was given by intragastric administration.The acetonitrile and 0.1%acetic acid waterwere used formobile phase gradient elution,the gallic acid concentration was detected at283 nm wavelength,the pharmacokinetic parametersofgallic acid were analyzed by DAS 2.0.RESULTS Limitof detection ofgallic acid was 0.67μg/mL,limitofquantitation was 1.34μg/mL;From 1.34μg/mL to 20.13μg/ mL,the linear relationship was fine;The relative standard deviation(RSD)of precision and stabilitywere 0.77%and 2.21%respectively,and RSD of line probe recovery ratewas50.78%.The pharmacokinetic ofgallic acid in anterior chamber conformed to the two chambermodel,the biological half-lifewas 54min,themaximum concentration time was80min.CONCLUSIONS The line probe combined with HPLC technology could accurately determine the concentration of gallic acid in anterior chamber,and it from Liurui capsule entered into the anterior chamber which meant itspharmacokineticswas consistentwith featuresof two compartmentmodels.
Liuruicapsule;gallic acid;line probe;high performance liquid chromatography;pharmacokinetic
R776.1
A
1002-4379(2017)02-0083-04
10.13444/j.cnki.zgzyykzz.2017.02.004
山东省重点研发计划(2015GGH319001);山东省自然科学基金(2014ZRB14483);山东省中医药科技发展计划普通项目(2013-106)
1山东中医药大学眼科研究所,济南250002 2山东中医药大学附属眼科医院,济南250002 3山东中医药大学眼科与视光医学院,济南250355
毕宏生,E-mail:hongshengbi1@163.com

