效应面法优选甜茶素提取工艺
吴婕,吴超,宫江宁,廖莉玲,*
(1.贵州师范学院化学与生命科学学院,贵州贵阳550018;2.贵州师范大学化学与材料科学学院,贵州贵阳550001)
效应面法优选甜茶素提取工艺
吴婕1,吴超1,宫江宁2,廖莉玲2,*
(1.贵州师范学院化学与生命科学学院,贵州贵阳550018;2.贵州师范大学化学与材料科学学院,贵州贵阳550001)
为了甜茶素的工业化生产,在甜茶叶中提取甜茶素的单因素试验基础上,采用效应面法优选出甜茶素的提取工艺参数,建立关于甜茶素提取率的二项式拟合方程,得到的最佳提取工艺参数:乙醇体积分数54.45%,提取温度70.21℃,液料比15.13 mL/g,提取时间2.1 h,甜茶素提取率的预测值3.615 3%。同时为了检验此工艺条件在实际工业生产中的可靠性,改进工艺条件为:提取温度70℃,乙醇体积分数55%,提取时间2.0 h,液料比15 mL/g,得到甜茶素提取率的实际值与其二项式拟合方程的预测值偏差仅为1.24%。故效应面法优选出的甜茶素的提取工艺参数,方法简便、可靠。
甜茶;提取工艺;甜茶素;效应面法
甜茶是一种蔷薇科悬钩子属的落叶,其叶味甜,故名“甜茶”。甜茶不仅具有人体所必需的氨基酸、维生素C以及矿物质等成分,还含有甜茶素、茶多酚和黄酮等活性成分。甜茶的甜味来源于甜茶素(Rubusoside,又名甜茶甙),其分子式为C32H50O13,它是葡萄糖和斯替维醇结合生成的四环二萜甙,其化学结构与甜叶菊甙非常相似。甜茶素的甜度是蔗糖的300倍,然而热值却为蔗糖的1%,故可作为一种天然的甜味剂,成为肥胖症和糖尿病患者的糖类替代物质,广泛应用于食品和医药等行业[1],具有广阔的市场前景。
提取甜茶素的方法主要有微波提取法、大孔树脂吸附分离法和有机溶剂提取法等[2-5],本试验采用有机溶剂乙醇冷凝回流法提取甜茶叶的甜茶素。在甜茶叶中提取甜茶素的单因素试验基础上,以甜茶素提取率为研究对象,以乙醇溶剂的体积分数、液料比、提取甜茶素温度和提取甜茶素的时间为考察因素,借助实验设计软件Design-Expert.7.0的Box-Behnken模式,研究各考察因素对甜茶素提取率的单独作用和交互作用,建立关于甜茶素提取率的回归方程数学模型,为甜茶素的工业化生产优选出最佳工艺条件。
1 材料与方法
1.1 主要试验材料与试剂
甜茶叶:贵州健康茶科技有限公司;甲醇(色谱纯)德国进口;无水乙醇为分析纯。
1.2 主要器材
Aglient1200高效液相色谱仪:美国安捷伦公司;A200S型电子天平:泉州市长新电子有限公司;101-1A型电热恒温鼓风干燥箱、FZ102微型植物粉碎机:天津市泰斯特仪器有限公司;KDM型控温电热套:山东鄄城华鲁电热仪器有限公司。
1.3 方法
1.3.1 提取甜茶素的工艺流程
清洗甜茶叶→烘干(35℃)→研碎→过40目筛→备用
称取甜茶叶粉末2.0 g→提取→冷凝回流→过滤→离心(4 200 r/min)→合并滤液→定容→测定甜茶素的质量浓度
1.3.2 甜茶素含量的测定[6]与计算
高效液相色谱法测定甜茶素含量。检测器:Aglient 1200;色谱柱:迪马 C1(8 250 mm×4.6 mm×5 μm;柱温:30℃;色谱甲醇 ∶水=85∶15(体积比);流速:1.0 mL/min;检测波长:210 nm;进样量:10 μL。
甜茶素的提取率Y/%=C×V/M×100,式中:C为甜茶素质量浓度,mg/mL;V为甜茶素体积,mL;M为甜茶叶质量,mg。
2 结果与讨论
2.1 单因素试验
以甜茶素提取率为研究对象,分别以不同的溶剂乙醇的体积分数、料液比、提取甜茶素的温度和提取甜茶素的时间为考察因素,进行3次平行试验,得到甜茶素提取率的平均值,从而确定各考察因素的合适取值范围。
2.1.1 乙醇溶剂的体积分数对甜茶素提取率的影响
称取2.0 g甜茶叶,液料比10 mL/g,提取时间1.5 h,提取温度55℃,选取不同的体积分数乙醇溶液(30%、40%、50%、60%、70%)分别提取甜茶素,试验结果如图1所示。
由图1可以得出,甜茶素提取率随着乙醇溶剂体积分数的增大而增大;但是当乙醇溶剂的体积分数超过50%时,甜茶素提取率反而有下降的趋势。因为甜茶素易溶于乙醇极性溶剂,它的溶解量随着乙醇溶剂体积分数的增大而增大,但是其他可以溶于乙醇溶剂的杂质,如色素、黄酮类物质,它们的溶解量也随着乙醇溶剂体积分数的增大而增大,当乙醇溶剂体积分数超过50%时,可溶于乙醇溶剂的杂质溶出量超过甜茶素的溶出量,在单位体积的乙醇溶剂中,甜茶素的提取率反而降低了[7]。此外,乙醇溶剂体积分数较大时其挥发性较强,工业生产利用率较低。故选择有机溶剂50%的乙醇为宜。
2.1.2 液料比对甜茶素提取率的影响
称取2.0 g甜茶叶,乙醇体积分数50%、提取时间1.5 h和温度 70 ℃,选取不同液料比(5、10、15、20、25 mL/g)分别提取甜茶素,试验结果如图2所示。
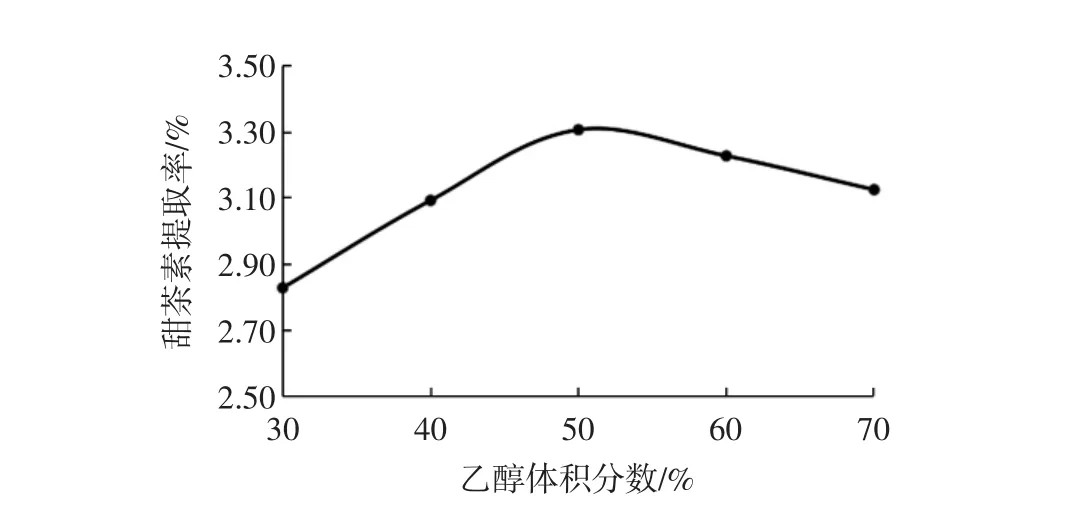
图1 乙醇体积分数对甜茶素提取率的影响Fig.1 Effects of ethanol volume percentage on extraction rate of rubusoside
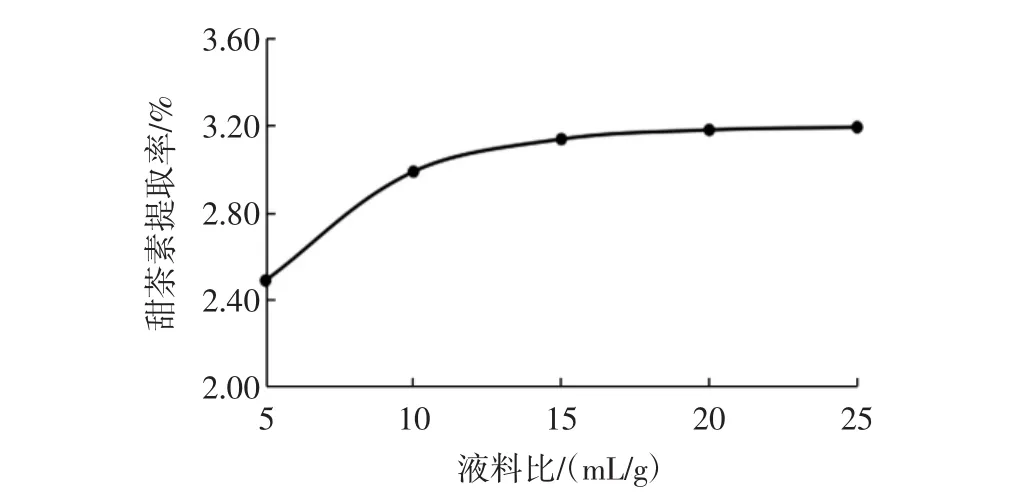
图2 液料比对甜茶素提取率的影响Fig.2 Effects of liquid-material ratio on extraction rate of rubusoside
由图2可以得出,甜茶素的提取率随着液料比的增大而升高,特别是液料比在15 mL/g以下,甜茶素提取率升高较快,而液料比超过15 mL/g,甜茶素提取率的曲线变化不明显。因为液料比的增加实质是乙醇溶剂量的增加,增加的液料比导致物料内外溶液的甜茶素质量浓度差增大,从甜茶叶中溶出的甜茶素增多,故甜茶素提取率增大;但是当液料比超过15 mL/g时,单位质量的甜茶叶中甜茶素已经基本溶出,甜茶素提取率变化不明显;并且不合适的增加液料比不仅不利于提高甜茶素提取率,反而会对后续的浓缩工艺造成困难。故选择液料比为15 mL/g较好。
2.1.3 提取甜茶素的时间对其提取率的影响
称取2.0 g甜茶叶粉末,乙醇体积分数50%,液料比15 mL/g,提取温度70℃,选取不同的提取时间(1.0、1.5、2.0、2.5、3.0 h)分别提取甜茶素,试验结果如图3所示。
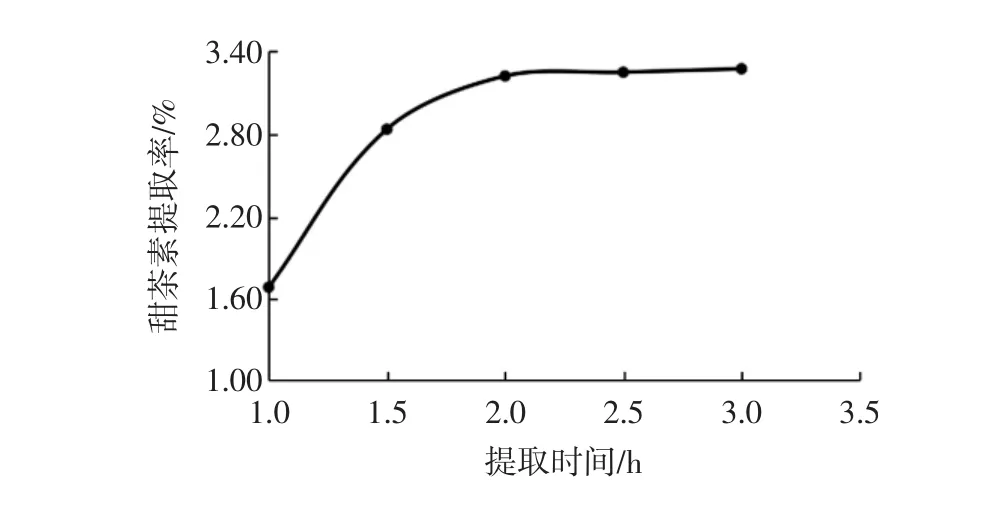
图3 提取时间对甜茶素提取率的影响Fig.3 Effects of extraction time on extraction rate of rubusoside
从图3可以得出,在2 h内甜茶素提取率迅速增长,但是超过2 h后,甜茶素提取率变化趋于平缓。因为在2 h时此溶液体系的传质过程已经基本达到动态平衡,溶出的甜茶素质量浓度也基本趋于稳定,导致甜茶素提取率也趋于稳定。故选择提取时间2 h效果为佳。
2.1.4 提取甜茶素的温度对其提取率的影响
称取2.0 g甜茶叶,乙醇体积分数50%,提取时间2 h,液料比 15 mL/g,选择不同的提取温度(60、65、70 、75、80℃)分别提取甜茶素,试验结果如图4所示。

图4 温度对甜茶素提取率的影响Fig.4 Effects of temperature on extraction rate of rubusoside
由图4可以得出,甜茶素提取率随着提取温度的升高逐渐增大。在60℃~70℃之间,甜茶素提取率增加的速率较大,而在70℃~80℃之间,甜茶素提取率的变化趋于平缓。因为在一定的时间和液料比范围之内,温度的升高有利于甜茶素分子在甜茶叶溶液中扩散,提取的甜茶素质量浓度会增加,甜茶素提取率也会升高;但是当温度升高到一定值时,扩散作用使得从甜茶叶中溶出的甜茶素质量浓度达到恒定,导致甜茶素提取率几乎不再变化。故选择提取温度70℃比较合适。
2.2 提取甜茶素工艺条件的效应面优化
2.2.1 效应面因素分析及水平选取
在提取甜茶素的单因素试验结果基础上,以乙醇体积分数(A)/%、提取温度(B)/℃、液料比(C)/mL/g、提取时间(D)/h为考察因素,以甜茶素提取率(Y)/%为效应值,应用Design-Expert.7.0软件设计4个考察因素3个水平的Box-Behnken分析试验。
为了简化数据,把各考察因素水平转化为标准函数。水平变换公式为:
乙醇体积分数:A/%=(A*-50)/10
提取温度:B/℃=(B*-70)/10
液料比:C/(mL/g)=(C*-15)/5
提取时间:D/h=(D*-2.0)/5
本试验的提取甜茶素考察因素各水平代码值及实际操作物理量,如表1所示。
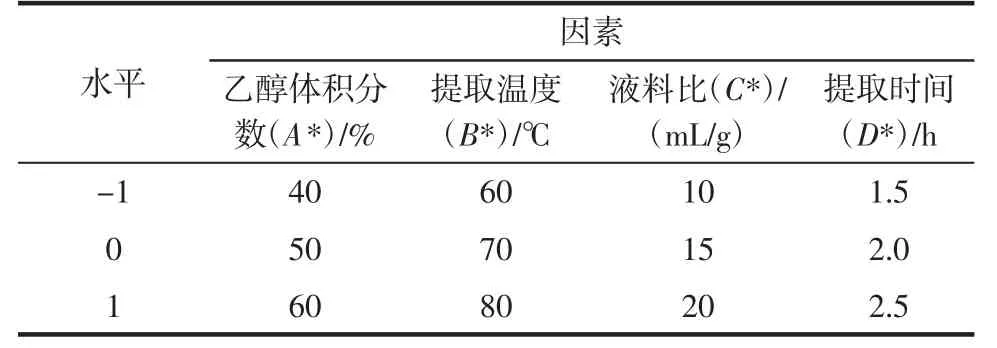
表1 考察因素各水平代码值及实际操作物理量Table 1 Code value and physical practice of independent variables levels
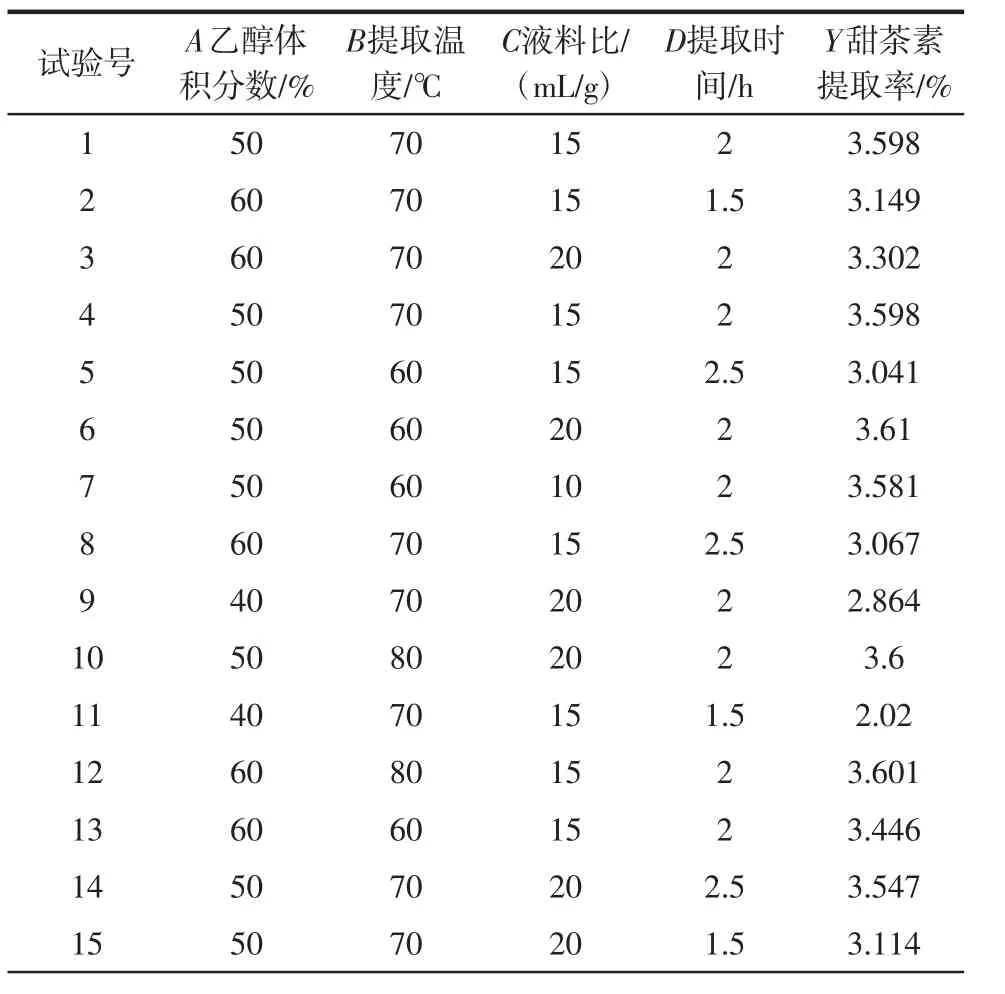
表2 星点设计及结果Table 2 Central composite design and results
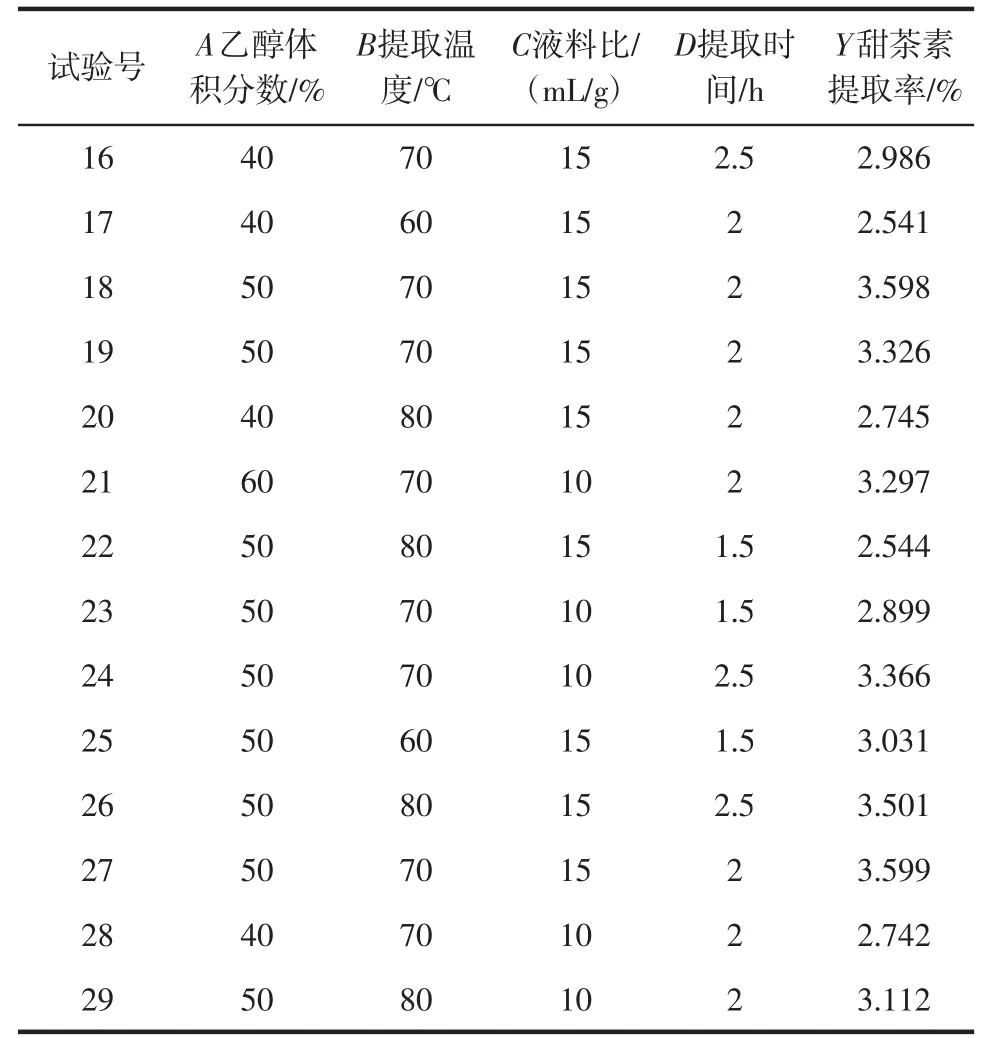
续表2 星点设计及结果Continue table 2 Central composite design and results
2.2.2 数学回归模型拟合与显著性检验
运用Design-Expert.7.0软件进行效应面分析,Box-Behnken设计出29个试验点。将试验所得数据带入Box-Behnken中,以各总评归一值(甜茶素提取率/%)对各考察因素[乙醇体积分数/%、提取温度/℃、液料比/(mL/g)和提取时间/h]进行多元线性回归和二项式拟合,拟合的甜茶素提取率数学回归模型如下:
Y=3.54+0.33A-0.012B+0.087C+0.23D-0.012AB-0.029AC-0.26AD+0.11BC+0.24BD-0.008 5CD-0.41A2-0.088B2-0.002 9C2-0.35D2
对拟合的数学模型进行F检验方差分析,其结果如表3所示。从整体上看,拟合的数学回归模型反映了各考察因素[乙醇体积分数/%、提取温度/℃、液料比/(mL/g)和提取时间/h]对甜茶素提取率的单独作用和交互作用,其中 A、B、C、D、A2、B2、C2、D2项代表 4 个考察因素对甜茶素提取率的单独作用,而AB、AC、AD、BC、BD、CD项代表不同的考察因素对甜茶素提取率的交互作用。

表3 二项式拟合回归模型的方差分析Table 3 Analysis of variance for binomial fitting quadratic regression model
从表3可以看出:第一,该模型的P<0.000 1,相关系数R2=0.932 0,表示数学回归模型达到极显著水平,该模型与实际情况拟合度好,它能够解释各考察因素与甜茶素提取率的关系;第二,失拟项P=0.314 3>0.05,S/N(信噪比)=15.720 0>4,表示该模型与实际拟合中的非正常误差所占的比例很小,该模型模拟出的甜茶素的最佳提取工艺具有很高的可信度。第三,在F值中,各考察因素对甜茶素提取率的影响程度大小顺序为:乙醇体积分数/%>提取时间/h>液料比/(mL/g)>提取温度/℃。第四,在P值中,一次方项的乙醇体积分数对甜茶素提取率影响非常显著,二次方项的乙醇溶剂体积分数和提取甜茶素的时间对其提取率影响非常显著。
2.2.3 提取甜茶素工艺优化与预测
Design-Expert.7.0软件可以根据星点试验设计的结果绘制效应值(甜茶素提取率/%)与任意两个考察因素[乙醇体积分数/%、提取温度/℃、液料比/(mL/g)、提取时间/h]的三维效应面。通过三维效应面能直观的看出各考察因素交互作用对甜茶素提取率效应值的影响[6,8]。本研究的三维效应面见图5~图10。
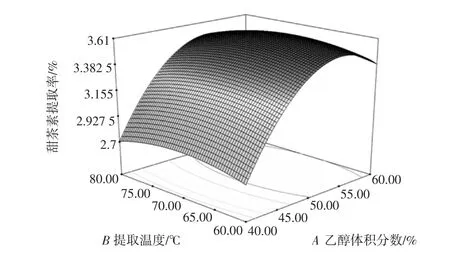
图5 提取温度和乙醇体积分数对甜茶素提取率的效应面Fig.5 Response surface for the effect of cross interaction between extraction temperature and ethanol volume percentage on extraction rate of rubusosides
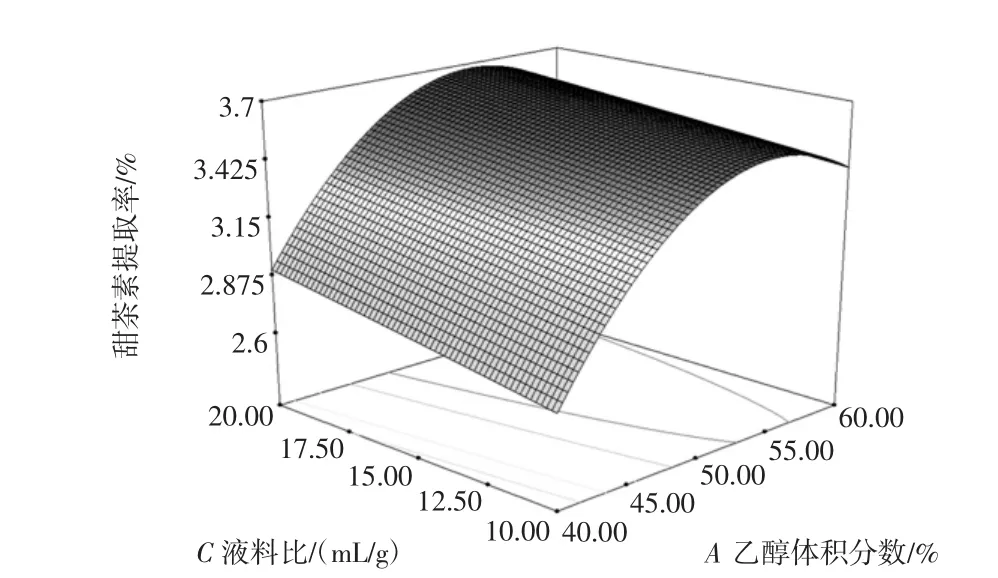
图6 乙醇体积分数和液料比对甜茶素提取率的效应面Fig.6 Response surface for the effect of cross interaction between ethanol volume percentage and liquid-material ratio on extraction rate of rubusosides
由图5可以看出,乙醇体积分数和提取甜茶素的温度的交互作用不显著。虽然甜茶素提取率随着乙醇溶剂体积分数和提取温度的增加而逐渐升高,但是当它们增加达到一定值时,甜茶素提取率表现降低的趋势。
由图6可以看出,乙醇溶剂的体积分数和液料比这两个考察因素的交互作用不十分显著。当乙醇体积分数一定时,甜茶素提取率随着液料比的增大而升高,但是升高的幅度很小;当液料比一定时,乙醇溶剂体积分数的增大,甜茶素提取率也增加,但是乙醇溶剂体积分数超过55%时,甜茶素提取率反而呈现降低的趋势。
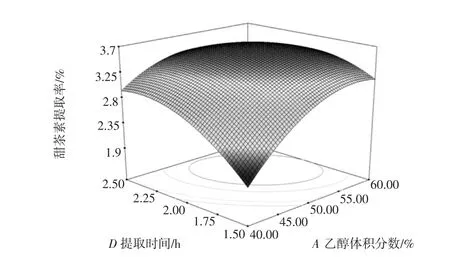
图7 乙醇体积分数和提取时间对甜茶素提取率的效应面Fig.7 Response surface for the effect of cross interaction between ethanol volume percentage and extraction time on extraction rate of rubusosides
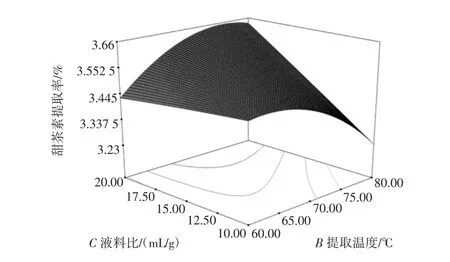
图8 提取温度和液料比的效应面Fig.8 Response surface for the effect of cross interaction between extraction temperature and liquid-material ratio on extraction rate of rubusoside
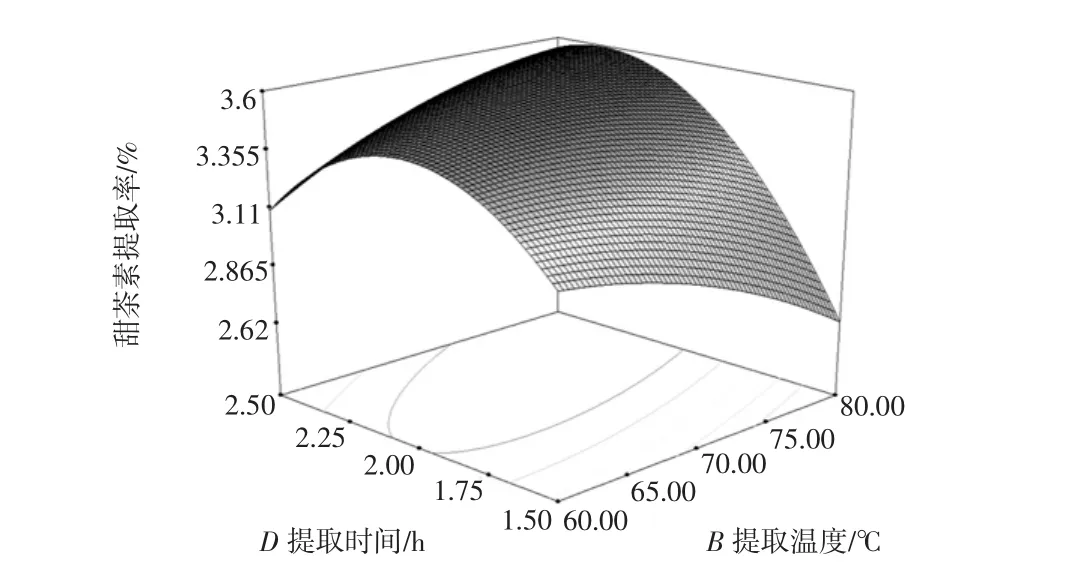
图9 提取温度和提取时间的效应面Fig.9 Response surface for the effect of cross interaction between extraction temperature and extraction time on extraction rate of rubusosides
由图7可以看出,乙醇溶剂体积分数和提取时间这两个考察因素的交互作用非常显著,它们微小的变化就会引起甜茶素提取率的变化。当乙醇体积分数和提取时间分别在55%和2.25 h之内,甜茶素提取率随它们的增大而显著提高;若分别超过其临界值,甜茶素提取率则呈现下降的趋势。
由图8可以看出,提取甜茶素的温度和甜茶素的液料比这两个考察因素交互作用不显著。当提取温度一定时,液料比的增加对甜茶素提取率的增长影响不大;当液料比一定时,甜茶素提取率随着提取温度的升高而增加,但是提取温度超过70℃,甜茶素提取率反而降低。

图10 提取时间和液料比对甜茶素提取率的效应面Fig.10 Response surface for the effect of cross interaction between extraction time and liquid-material ratio on extraction rate of rubusosides
由图9可以看出,提取甜茶素的温度和时间的交互作用极显著;当提取甜茶素的时间一定时,提取率随着提取温度的增加先增加而后减小;当提取甜茶素的温度一定时,提取率随着提取时间的延长而增加,但是超过2.0 h,甜茶素提取率反而降低。
由图10可以看出,甜茶素的提取时间和液料比这两个考察因素的交互作用较不显著。当液料比一定时,甜茶素提取率会随着提取时间的延长而明显增加,但是提取时间超过2.25h时,甜茶素提取率则呈现降低的趋势;当提取时间一定时,甜茶素提取率随着液料比的增加有上升的趋势,但是升高的幅度不是很大。
综上所述,数学回归模型预测的最佳工艺条件为:乙醇体积分数54.45%,提取温度70.21℃,液料比15.13(mL/g),提取时间 2.1 h,甜茶素提取率预测值3.615 3%。为了检验此工艺条件在实际工业生产中的可靠性,改进工艺条件为:提取温度70℃,乙醇体积分数 55%,提取时间 2.0 h,液料比 15(mL/g),平行试验3次,得到甜茶素提取率的平均验证值3.570 6%,可以得出甜茶素提取率的验证值与预测值的相对偏差较小(约1.25%),故认为星点设计效应面法选择的最佳甜茶素的提取工艺,拟合结果准确,可信度高。
3 结论
为了寻求最佳的考察因素水平,一般采用没有明确的函数表达式的线性数学模型——正交设计,但是它无法在设定的考察因素范围内找到最佳组合[9-10]。效应面法可以克服正交设计的缺点,建立效应值与考察因素的回归数学模型,试验选连续变量,所得试验结果更加接近回归数学模型预测值[11],并且可以从效应面上选择最佳的效应值,回推出最优的考察因素组合。
本研究,在提取甜茶素的单因素试验基础上,利用试验设计软件Design-Expert.7.0对考察因素乙醇体积分数(A)/%、提取温度(B)/℃、液料比(C)/(mL/g)、提取时间(D)/h与甜茶素提取率(Y)/%的数学模型进行了回归分析,其相关性极显著,它能有效地预测甜茶素的最佳工艺条件:乙醇体积分数54.45%,提取温度70.21℃,液料比为 15.13(mL/g),提取时间 2.1 h,甜茶素提取率的理论值3.615 3%。为了检验此工艺条件在实际工业生产中的可靠性,改进工艺条件为:提取温度70℃,乙醇体积分数55%,提取时间2.0 h,液料比15(mL/g),平行试验3次,得到甜茶素提取率的平均验证值为3.570 6%,得出甜茶素提取率的验证值与预测值的相对偏差较小(约1.24%),可以认为该模型预测的最佳工艺条件合理可靠。
[1] 李祝,陈蓉,李献,等.广西甜茶中甜茶素的提取工艺研究[J].食品工业,2013,34(2):93-95
[2] 司佳,吴正奇,万端极,等.从甜茶叶中制备甜茶素的工艺研究[J].食品科技,2013,38(4):262-265
[3] 刘洋,杨磊,郝婧玮,等.响应面法优化匀浆提取刺五加主要酚苷及苷元的工艺[J].化工进展,2010,29(4):745-752
[4] 李萍.大孔吸附树脂在中草药有效成分研究中的应用[J].天津药学,2002,14(3):9-11
[5] 吴婕,鲍晨阳,杜莹,等.SA-3大孔树脂纯化甜茶素的研究[J].食品研究与开发,2014,35(23):36-38
[6] 卢昕,张新申,刘承伟.反相高效液相色谱法测定广西甜茶中甜茶素[J].色谱,2003,21(3):260-262
[7] 马建春,何伟,伍振峰.甜茶素的研究进展[J].食品与药品,2008,10(5):73-75
[8] 陈莉,屠康,王海,等.采用响应曲面法对采后红富士苹果热处理条件的优化[J].农业工程学报,2006,22(2):159-163
[9] 朱家校,何伟,李勇,等.响应面分析法优化川芎藁本内酯提取工艺的研究[J].中成药,2011,33(12):2172-2175
[10]于淼,柏云娇,代岐昌,等.响应曲面法优化文殊兰中生物碱的提取工艺[J].中草药,2013,44(10):1286-1289
[11]吕维,吴恋,罗红丽,等.星点设计-效应面法优化川芎提取工艺[J].药物评价研究,2014,37(1):53-57
Optimization of Extraction Process of Rubusoside by Response Surface Method
WU Jie1,WU Chao1,GONG Jiang-ning2,LIAO Li-ling2,*
(1.College of Chemistry and Life Science,Guizhou Normal College,Guiyang 550018,Guizhou,China;2.School of Chemistry and Material Science,Guizhou Normal University,Guiyang 550001,Guizhou,China)
Based on the single factor test of extraction rubusoside,response was used to explore the optimum extraction parameters of rubusoside for industry.The rubusoside extraction regression equation was established and the optimal extraction processing parameters were determined.The optimal conditions of extraction process were followed:extraction temperature of 70.21℃,ethanol concentration of 54.45%,extraction time of 2.1 h and liquid-material ratio of 15.13 mL/g.Under this condition,the rubusoside extraction rate was 3.615 3%.In order to test the reliability of the process condition in industry,the best verification processing parameters were followed:extraction temperature of 70℃,ethanol concentration of 55%,extraction time of 2.0 h and liquidmaterial ratio of 15 mL/g.The variance between the result of the best verification test and the binomial fitting equation forecast value was nearly 1.24%.Thus,The optimized extraction parameters were simple and reliable.
sweet tea;extraction technology;rubusoside;response method
2016-10-09
10.3969/j.issn.1005-6521.2017.11.014
吴婕(1982—),女(土家),副教授,博士研究生,主要从事化学天然产物和环境科学研究。
*通信作者:廖莉玲,教授,硕士,主要从事化学天然产物和材料化学研究。

