丹七片的研究进展
蒋秋香柳州食品药品检验所,广西 柳州 545006
文献综述
丹七片的研究进展
蒋秋香
柳州食品药品检验所,广西 柳州 545006
丹七片具有活血化瘀、通脉止痛的功效,是活血化瘀类药物的代表药,临床应用广泛,其质量关系到用药的安全性和有效性。笔者通过查阅中国知网、万方及维普等数据库,对2001~2015年涉及丹七片的制备工艺、显微鉴别、薄层色谱鉴别、含量测定、指纹图谱、药理作用及临床应用等方面的36篇文献进行分析、归纳和整理,以期为丹七片的质量评价及开发应用提供参考和依据。
丹七片;鉴别;含量测定;指纹图谱;药理作用;研究进展
丹七片由丹参和三七两味中药组成,具有活血化瘀、通脉止痛的功效,用于瘀血闭阻所致的胸痹心痛、眩晕头痛、经期腹痛。其制法是将三七粉碎成细粉,丹参经水煮、滤过、浓缩、加入三七细粉及淀粉、糊精,压片,包衣即得。现行版质量标准是《中国药典》2015年版一部[1],其中规定了丹七片的处方、制法、性状、鉴别、检查、含量测定、功能与主治、用法与用量、注意、规格和贮藏。目前国内有41个不同的厂家生产丹七片,涉及的地域宽广,原料药材来源和品种多样化。为了更好地控制丹七片的质量,为临床合理应用提供科学依据,笔者对丹七片的质量研究、药理作用及临床应用进行综述,为丹七片质量评价研究及临床用药安全提供参考。
1 制备工艺
《中国药典》收载的丹七片由丹参和三七组成:丹参通过水煎煮,滤液浓缩,再加入三七细粉,混匀,干燥,压片。丹参的主要活性成分有水溶性的丹酚酸类化合物及脂溶性的丹参酮类化合物,其中丹酚酸B在丹参根中含量最高[2],水提转化率较高,但是脂溶性成分提取不充分。岳国超等[3]将丹七片的工艺进行了改进:将丹参分别用90%乙醇6倍量提取1h、4倍量提取0.5h,浓缩之后加三七细粉,混匀,干燥,压片。按高效液相色谱法,对原工艺和改进后工艺生产的各3批丹七片进行丹参酮IIA含量的测定,结果显示,改进工艺后,丹参酮IIA的含量较原工艺提高了4.1~5.2倍。制粒过程在片剂的制备工艺中是非常关键的步骤,因中药成分非常复杂,浸膏中除有效成分外,还有淀粉、糖类、黏液质、蛋白质等,这些物质多具有一定的粘性,给制粒带来影响。韩超等[4]应用流化床制粒技术,改善颗粒的溶解度、孔隙率、比表面积,降低能耗、减少物料损失,提高处方中不稳定成分的稳定性,并通过正交试验法,筛选丹七片流化床制粒工艺参数,形成最佳制粒工艺。丹七片压片后,可包糖衣或薄膜衣,按照传统的包糖衣技术,各个批次之间的包衣厚度、色泽等差异较大。肖晏婴等[5]改进包糖衣工艺,使包衣工序的每个操作环节都有量化标准:粉衣层包15层,糖衣层8层,有色糖衣层8层,从而保证该制剂质量均一,外形美观。
2 定性鉴别
2.1 显微鉴别 根据《卫生部药品标准中药成方制剂》[6]规定,鉴别丹七片中三七的方法为显微鉴别,其鉴别主要对象为淀粉粒。2010年版药典[7]将显微特征鉴别对象定为含黄色分泌物的三七树脂道碎片。现行版药典[1]规定的显微鉴别也是三七树脂道碎片。
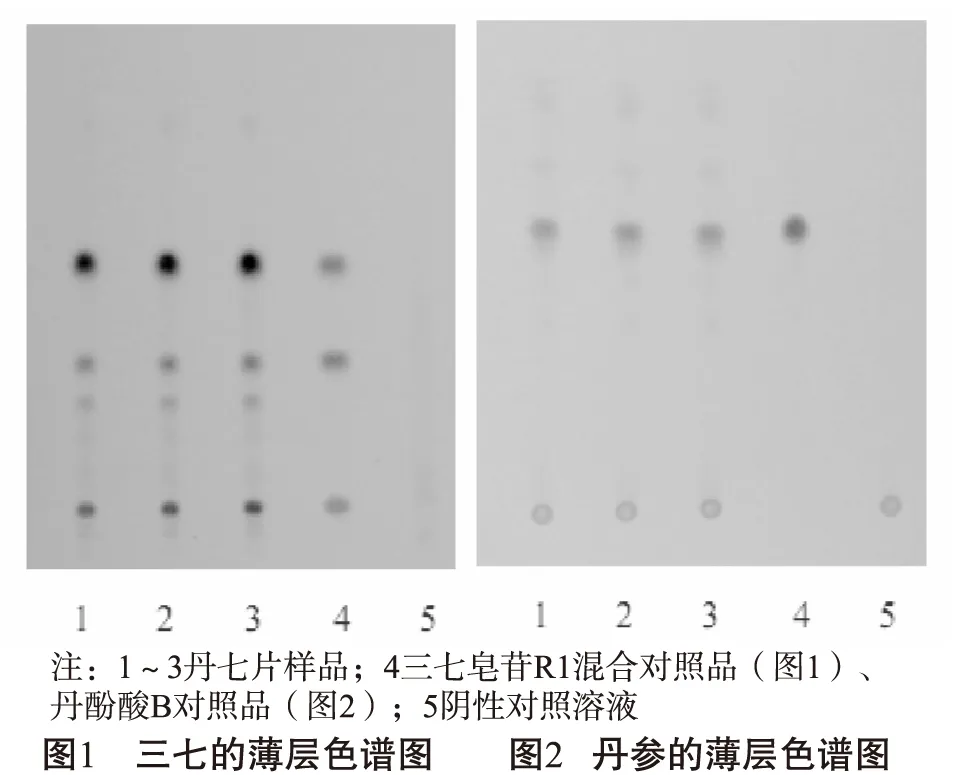
2.2 薄层色谱鉴别 在已有的研究丹七片质量标准的文献报道中[8-12],薄层色谱鉴别法作为主要的鉴别方法被采用。其中三七的有效成分三七皂苷R1、人参皂苷Rg1、人参皂苷Rb1作为主要的鉴别对象,通过“取样品,加水1mL,搅匀,再加以水饱和的正丁醇8mL,密塞,振摇10min,放置2h,离心,取上清液,加正丁醇饱和的水25mL,摇匀,取正丁醇层,蒸干,残渣加甲醇1mL使溶解,作为供试品溶液”等步骤提取,薄层板为硅胶G板,展开剂有正丁醇-乙酸乙酯-水(4∶1∶5)的上层溶液[9]、三氯甲烷-乙酸乙酯-甲醇-水(15∶40∶23∶10)在10℃以下放置的下层溶液[10]、1,2-二氯甲烷-正丁醇-甲醇-水(6∶8∶3∶5)的下层溶液(薄层色谱图见图1)[11]等。也有研究者[12]通过“取样品,加甲醇30mL,超声处理45min,滤过,滤液蒸干, 残渣加水20mL溶解,用稀盐酸调节pH值约为2,用醋酸乙酯20mL振摇提取,弃去醋酸乙酯液,水层以水饱和正丁醇萃取2次,每次30mL,合并正丁醇液,再用氨试液40mL洗涤,分取正丁醇液,以水40mL洗涤2次,弃去水液,蒸干,残渣加甲醇1mL使溶解,作为供试品溶液”提取,展开剂为氯仿-乙酸乙酯-甲醇-水(15∶40∶22∶10)10℃以下放置12h的下层溶液。显色剂为10%硫酸乙醇溶液,在105℃加热至斑点显色清晰,分别置日光和紫外光灯下检视,在与对照品相应的位置上,显相同颜色的斑点和荧光斑点。对于丹参的鉴别方法相对较少,冯彬彬等[10]用以下方法提取:取样品,加水20mL,超声处理20min,加稀盐酸调节pH值至3~4,用乙醚提取3次,每次20mL,合并乙醚液,用无水硫酸钠脱水,挥干,残渣加无水乙醇1mL使溶解,作为供试品溶液,丹参对照药材做同样处理。薄层板使用硅胶GF254板,以甲苯-三氯甲烷-乙酸乙酯-甲醇-甲酸(2∶3∶4∶0.5∶2)为展开剂,于紫外光254nm下检视,在与丹参对照药材相应的位置上显相同颜色的荧光斑点。另有鉴别丹参水溶性成分丹酚酸B的报道[11],用70%乙醇超声处理提取之后,滤过,蒸干,残渣加乙酸乙酯溶解,跟丹酚酸B对照品点于同一硅胶G薄层板上,以乙酸丁酯-水-甲酸(14∶2∶3)的上层溶液展开,喷以1%三氯化铁溶液与1%铁氰化钾溶液的等量混合溶液,在与丹酚酸B相应的位置上,显相同颜色的蓝色斑点(薄层色谱图见图2)。2015年版药典[1]鉴别(2)项下规定,鉴别丹酚酸B的提取方法为70%乙醇超声提取之后,滤过,浓缩,作为供试品溶液,其薄层板、展开系统和显色剂与上述鉴别丹参水溶性成分丹酚酸B的报道相同。
3 含量测定
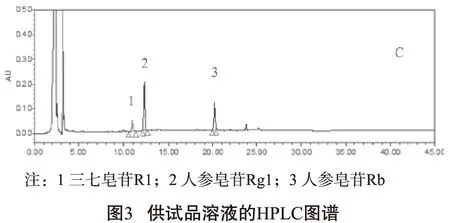
3.1 三七 三七为五加科植物三七Panaxnotoginseng(Burk.)F.H.Chen 的干燥根和根茎[1],其成分复杂多样,目前已确定的成分有百余种,其中有效成分以皂苷类和三七素类为主[13]。三七作为丹七片的一味主药,现行版质量标准[1]规定,将丹七片样品用50%甲醇超声提取30min,按高效液相色谱法试验,在203nm波长下,以乙腈-水为流动相进行梯度洗脱,测定三七的有效成分三七皂苷R1、人参皂苷Rg1和人参皂苷Rb1的总量,每片不得少于12.0mg。梁少强等[11]进行的丹七片质量标准研究中,三七的主要成分三七皂苷R1、人参皂苷Rg1和人参皂苷Rb1作为研究的目标成分,用50%甲醇超声提取,使用高效液相色谱法,检测波长为203nm,以乙腈-水为流动相梯度洗脱分离,测定(高效液相色谱图见图3)。孙英英等[14]也采用50%甲醇超声提取的方法,以乙腈-水为流动相,使用超高效液相色谱法分离测定丹七片中的三七皂苷R1、人参皂苷Rg1和人参皂苷Rb1,此方法能在6分钟内将三种待测成分完全分离。蔡向阳等[15]采用“取样品,精密加入水饱和的正丁醇50mL,密塞,称定重量,超声处理30min,放冷,称定重量,用水饱和的正丁醇补足减失的重量,摇匀,滤过,精密量取续滤液10mL,置分液漏斗中,加氨试液洗涤2次,每次10mL,取正丁醇液,蒸干,残渣加甲醇使溶解,转移至10mL量瓶中,加甲醇至刻度,摇匀,滤过,取续滤液,即得。”提取丹七片中的三七皂苷R1和人参皂苷Rg1,以乙腈-水-磷酸为流动相,对三七皂苷R1和人参皂苷Rg1进行分离测定。也有进行单独的人参皂苷Rg1含量的测定[16-17],以甲醇-水为流动相,将检测波长设为280nm,进行测定。殷召军[18]采用HPLC-ELSD检测丹七片中人参皂苷Rg1和人参皂苷Rb1的含量,用乙腈-水为流动相梯度洗脱,漂移管温度110℃,载气流速3.0mL/min,也能将人参皂苷Rg1和人参皂苷Rb1进行较好的分离检测。
3.2 丹参 丹参为唇形科植物丹参SalviamiltiorrhizaBge.的干燥根和根茎[1]。其化学成分主要有脂溶性和水溶性成分两大类。丹七片的现行版质量标准中只有丹参的水溶性成分丹酚酸B的薄层色谱鉴别要求,无含量测定标准。但是丹酚酸B的含量测定方法已有文献报道,其提取方法多样:(1)取样品0.25g,加水10mL溶解,用稀盐酸调节pH至1~2,乙酸乙酯萃取3次,每次20mL,合并萃取液并蒸干,残渣用75%甲醇溶解至10mL,再吸取1mL至10mL量瓶中,加75%甲醇稀释至刻度[19]。(2)取样品0.3g,加50%乙醇25mL,超声处理30min,过滤,即得[12,20,21]。(3)取样品0.15g,置25mL量瓶中,加水适量,超声处理20min,用水定容至刻度,即得[9]。(4)取样品0.1g,加75%甲醇50mL,加热回流1h,过滤,即得[10]。但高效液相色谱条件基本一致:流动相组成为甲醇-乙腈-甲酸-水,检测波长286nm。丹参的水溶性成分除了丹酚酸B外,目前已知的还有丹参素和原儿茶醛[22],骆秀平等[23]将丹七片样品经过甲醇超声提取,使用高效液相色谱法,检测波长280nm,以甲醇-1.5%冰醋酸水溶液为流动相,分离测定原儿茶醛。但是梁民琦[24]使用的提取方法跟原儿茶醛的水溶性性质更相符:取样品5g,加水50mL,超声处理30min,滤过,取滤液25mL,用稀盐酸调pH至2.2,用水饱和的醋酸乙酯提取4次(20、20、15、10mL),合并醋酸乙酯液,蒸干,残渣用甲醇溶解,即得,其使用的流动相为甲醇-0.2mol·L-1醋酸铵(用HCl调pH至2.2),检测波长313nm。对于丹参素的测定,魏淑萍[25]将样品用50%乙醇超声提取30min,使用高效液相色谱法,在280nm波长下,以乙腈-水-磷酸将丹参素分离测定。而潘锋[26]将丹七片样品用10%甲醇溶液超声提取30min,在高效液相色谱条件下,检测波长为281nm,使用甲醇-1%醋酸溶液能将丹参素与原儿茶醛同时分离检测。
4 指纹图谱研究
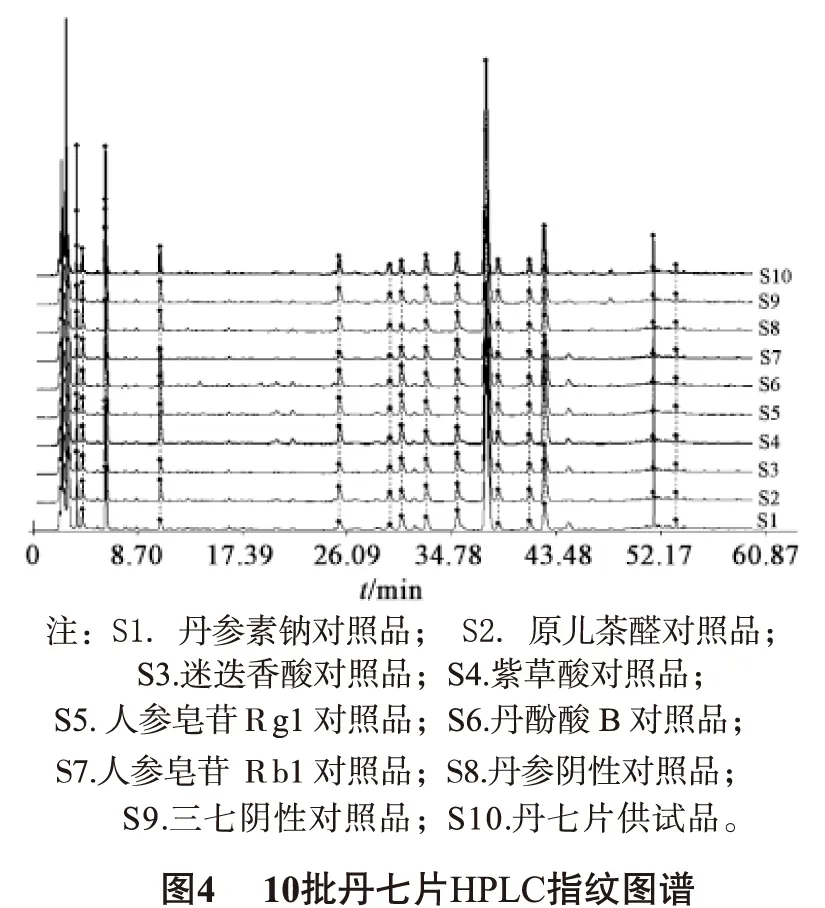
郑文忠等[27]将丹七片样品经75%甲醇超声处理30min提取后,使用高效液相色谱法,在210nm的波长下检测,以乙腈-0.06%磷酸溶液进行梯度洗脱,对10批次的丹七片样品进样分析,采集色谱图,建立指纹图谱,得到10个共有峰,以“中药色谱指纹图谱相似度评价系统(2004A)”进行相似度计算,结果发现10批次的丹七片相似度均在0.90以上(见图4)。
5 药理作用和临床应用
徐懿乔等[28]以家兔和大鼠为实验对象,发现丹七片可明显抑制由凝血酶和胶原蛋白诱导的血小板聚集,可升高凝血酶作用下的血小板内cAMP含量。丹七片作为活血化瘀类药物的代表在临床心脑血管疾病治疗中应用广泛,郭淑贞等[29]采用心血管系统与人类最为接近的小型猪作为实验动物,为丹七片干预心肌缺血的作用机制阐释了新的线索与证据。在有效控制冠状动脉粥样硬化的发生和发展、减轻或消除冠心病病人的临床症状和降低血脂方面,丹七片是一种理想的药品选择[30-33]。王玉龙等[34]根据自发性高血压大鼠(SHR)和正常WKY大鼠尿液的代谢组学差异,研究丹七片对SHR血压及尿液中差异性代谢物的影响,发现丹七片可降低SHR血压,且可通过干预SHR尿液中与高血压发生相关的差异性代谢物分布状态来达到治疗高血压的作用。此外,在与复明片联合用药后,对原发性开角型青光眼的治疗具有更佳的临床疗效,值得临床推广应用[35-36]。
6 结语
丹七片具有活血化瘀、通脉止痛的功效,常用于冠心病、动脉粥样硬化、高脂血症的治疗。丹七片中的三七和丹参皆为常用中药,方中丹参味苦性微寒,善于活血祛瘀、凉血消肿、清心除烦,三七味甘微苦、性温,功擅活血祛瘀、消肿定痛。药典收载的丹七片规定了三七的显微鉴别,丹酚酸B、三七皂苷R1、人参皂苷Rg1和人参皂苷Rb1的薄层色谱鉴别,三七皂苷R1、人参皂苷Rg1和人参皂苷Rb1的含量测定,但是,因三七、丹参种质资源复杂,不同地区采收时间各异,其他成分的含量也各有不同,仅凭现有的质量标准控制,并不能较好的反映药材和制剂的品质与疗效。另外,药典上规定的制法工艺要求丹参水煎煮3次,煎液滤过,浓缩之后入药,与三七细粉直接入药相比,其工艺相对复杂,这给一些不法厂家有机可乘,若将丹参直接以细粉入药,以现有的定性定量质量标准检测,无法判定其制作工艺的合法性。因此,笔者考虑是否能将“异性有机物”的检查也纳入丹七片的质量标准控制项目,即除三七原药材组织外,不得检出其它植物组织,这也是笔者下一步将继续探索的课题。
[1]国家药典委员会.中华人民共和国药典(2015年版一部)[S].北京:中国医药科技出版社,2015:676.
[2] 肖培根.新编中药志[M].北京:化学工业出版社,2002:212.
[3] 岳国超,焦玉.丹七片制备工艺改进[J].湖北中医杂志,2011,33(12):68.
[4] 韩超,马琳.正交设计法研究丹七片流化床制粒工艺[J].陕西中医,2009,30(3):343.
[5] 肖晏婴,黄德红,王洪军.丹七片包糖衣工艺改进[J].湖北中医杂志,2015,37(1):70.
[6] 卫生部药典委员会编.卫生部药品标准中药成方制剂(第1册)[M].北京:人民卫生出版社,1989:48
[7] 国家药典委员会.中华人民共和国药典(2010年版第一增补本)[S].北京:中国医药科技出版社,2010:14.
[8] 黄玉芍.丹七片(胶囊)的薄层色谱鉴别[J].时珍国医国药,2001,12(4):339.
[9] 郝自新,程世云,张正虎.丹七片质量标准研究[J].安徽医药,2009,13(11):1329.
[10] 冯彬彬,张建海,祝慧凤.丹七片的质量标准研究[J].浙江中医药大学学报,2010,34(1):84.
[11] 梁少强,谢仕伟,李国荣.丹七片质量标准的研究[J].中国医药指南,2009,7(24):57.
[12] 廖名爱.丹七片质量标准研究[J].中国药业,2010,19(10):28.
[13] 夏鹏国,张顺仓,梁宇锁,等.三七化学成分的研究历程和概况[J].中草药,2014,45(17):2564.
[14] 孙英英,郭玉海,林华庆,等.UPLC测定丹七片中三七皂苷R1、人参皂苷Rg1和人参皂苷Rb1的含量[J].中国生化药物杂志,2015,35(1):148.
[15] 蔡向阳,夏金华.RP-HPLC法同时测定丹七片中三七皂苷R1和人参皂苷Rg1的含量[J].中国药房,2007,18(36):2837.
[16] 金银芝,金朝阳,应佳.HPLC测定丹七片中丹七片中人参皂苷Rg1的含量[J].浙江中医药大学学报,2009,33(6):884.
[17] 应佳,包玮鹫,李冰岚,等.HPLC测定丹七片中人参皂苷Rg1的含量[J].中成药,2007,29(8):21.
[18] 殷召军.HPLC-ELSD测定丹七片中人参皂苷Rg1和人参皂苷Rb1含量[J].内蒙古中医药,2010,9(21):126.
[19] 夏明.RP-HPLC法测定丹七片中丹酚酸B的含量[J].中华中医药杂志,2010,25(11):1880.
[20] 黄湘,刘丹,文萍.HPLC测定丹七片中丹酚酸B的含量[J].现代中药研究与实践,2007,21(6):43.
[21] 席仲洪,胡仁胜,帅银花,等.丹七片中丹酚酸B的含量测定[J].江西中医药,2007,38(4):62.
[22] 赵艳威,杨宣,董璨珠,等.丹参素及原儿茶醛研究进展[J].武警医学院学报,2009,18(3):260.
[23] 骆秀平,王术玲,郑艳平.HPLC法测定丹七片中原儿茶醛的含量[J].中药新药与临床药理,2005,16(2):130.
[24] 梁民琦.丹七片中原儿茶醛的含量测定[J].中国临床药学杂志,2005,14(3):186.
[25] 魏淑萍.HPLC法测定丹七片中丹参素的含量[J].辽宁中医杂志,2005,32(5):472.
[26] 潘锋.HPLC同时测定丹七片中丹参素和原儿茶醛的含量[J].药物分析杂志,2006,26(4):531.
[27] 郑文忠,邓红,林华庆,等.丹七片HPLC指纹图谱[J].中国实验方剂学杂志,2014,20(10):80.
[28] 徐懿乔,刘杰,谢笑龙.丹七片对动物血小板聚集的抑制作用及其机制研究[J].华西药学杂志,2012,27(3):267.
[29]郭淑贞,啜文静,王勇,等.丹七片干预心肌缺血的血浆蛋白质组学研究[J].中西医结合心脑血管病杂志,2014,12(11):1355.
[30] 龚道凯,张学敏.丹七片治疗冠心病的临床观察[J].中国民族民间医药,2009,18(21):125.
[31] 高静民,马莉.丹七片治疗高脂血症及预防动脉粥样硬化[J].首都医药,2004,10(2):43.
[32] 龙军.丹七片对冠状动脉粥样硬化性心脏病患者血脂代谢的影响[J].中国药业,2015,24(24):36.
[33] 张延华,沈凌霞,马成兰.丹七片治疗冠状动脉粥样硬化性心脏病28例[J].中国药业,2016,25(2):112.
[34] 王玉龙,吕光耀,王娅妮,等.基于1H-NMR的丹七片对自发性高血压大鼠尿液代谢组学分析[J].中国实验方剂学杂志,2017,23(4):102.
[35] 付禄新.复明片与丹七片联合治疗原发性开角型青光眼临床观察研究[J].中国卫生产业,2013,10(19):91.
[36] 魏红,王慧博.复明片与丹七片联合治疗原发性开角型青光眼临床观察[J].中国中医急症,2010,19(6):947.
蒋秋香(1983-),女,汉族,本科,在职研究生,主管中药师,研究方向为药品、食品、化妆品、保健食品的检验和标准研究。E-mail:67370082@qq.com
R286.0
A
1007-8517(2017)12-0037-04
2017-04-10 编辑:陶希睿)

