获得性凝血因子Ⅴ缺乏症的临床诊治
陈云飞, 刘 葳, 刘晓帆, 付荣凤, 黄月婷, 薛 峰, 张 磊, 杨仁池
中国医学科学院血液病医院(血液病研究所),天津 300020
·论 著·
获得性凝血因子Ⅴ缺乏症的临床诊治
陈云飞, 刘 葳, 刘晓帆, 付荣凤, 黄月婷, 薛 峰, 张 磊, 杨仁池*
中国医学科学院血液病医院(血液病研究所),天津 300020
目的: 总结获得性凝血因子Ⅴ缺乏症(acquired factor Ⅴ deficiency, AFⅤD)的临床诊治经验。方法: 回顾性分析10例获得性凝血因子Ⅴ缺乏症患者的临床资料,分析临床特点,总结临床诊治经验。结果: 10例患者中男性7例,女性3例,年龄51~71岁,中位年龄60岁,均无遗传性凝血因子缺乏病史及家族史,临床表现为牙龈出血、鼻衄、血尿、黑便,甚至颅内出血。10例患者均有凝血酶原时间(PT)、活化部分凝血活酶时间(APTT)显著延长,凝血因子Ⅴ活性降低,抑制物定性或定量试验阳性,均诊断为获得性凝血因子Ⅴ缺乏症。10例患者均输注新鲜冰冻血浆控制出血症状,并采用糖皮质激素或联合环磷酰胺、硫唑嘌呤免疫抑制治疗,其中5例患者(5/10)缓解,未再出现出血症状;3例患者(3/10)应用糖皮质激素及环磷酰胺治疗效果差,随后加用利妥昔单抗治疗均有效,其中2例经治疗后凝血因子Ⅴ(factor Ⅴ,FⅤ)浓度恢复正常,未再出现出血症状,1例患者需用小剂量利妥昔单抗维持治疗;2例患者(2/10)死于颅内出血。结论: AFⅤD是一种罕见疾病,临床出血症状轻重不一,经糖皮质激素及环磷酰胺、利妥昔单抗治疗有助于缓解症状
获得性因子Ⅴ缺乏;免疫抑制剂;糖皮质激素
获得性凝血因子Ⅴ缺乏症(acquired factor Ⅴ deficiency, AFⅤD)是一种罕见的凝血障碍性疾病,主要由血浆中产生凝血因子Ⅴ(factor Ⅴ,FⅤ)抑制物导致[1-2]。其临床表现多种多样,可仅为实验室指标异常而无临床症状,亦可出现患者各部位、器官出血,甚至致命的严重出血,如颅内出血等[2-3]。由于该病临床发病率较低,且患者往往首诊于非血液专科医院,易误诊或漏诊延误病情。因此,本研究对我中心近年来10例AFⅤD患者进行回顾性分析,总结临床诊治经验,以提高临床医师对该病的认识,提高对该病的临床诊治水平。
1 资料与方法
1.1 一般资料 选择中国医学科学院血液病医院2004年2月至2016年12月诊治的AFⅤD患者10例,其中男性7例,女性3例;年龄51~71岁,中位年龄60岁。基本临床资料具体见表1。既往均无遗传性凝血因子缺乏病史及家族史,无出血病史。首诊时均有不同程度的多部位出血,其中伴有皮肤黏膜出血共9例(牙龈出血3例、鼻衄3例、皮肤瘀3例),伴有肉眼血尿4例,下肢肌肉血肿及腹股沟血肿1例,阴道出血1例,消化道出血1例,右侧胸腔血性积液1例,颅内出血1例;2种及2种以上部位出血共5例患者。
10例患者中有高血压病史5例,高血压肾病1例,糖尿病病史3例,胆囊炎及胆结石病史2例,阑尾炎手术史3例,颈椎椎管狭窄手术1例,但近1年均无手术史。其中1例为急性胰腺炎治疗后20 d发现凝血功能异常,其间应用头孢他啶抗感染治疗,入院时合并肺感染、右侧胸腔血性积液;1例患有风湿性心脏病,并于16年前行二尖瓣、主动脉瓣置换术,术后华法林抗凝治疗14年,后停药2年。

表1 患者一般临床资料
1.2 治疗方法 10例患者入院后均接受了新鲜冰冻血浆(fresh frozen plasma,FFP)输注及糖皮质激素治疗,糖皮质激素为甲泼尼龙(methylprednisolone,MP;7/10)、地塞米松(dexamethasone,DXM;1/10)或泼尼松(prednisone,Pred;1/10),激素等量换算后均为1 mg/(kg·d),中位治疗天数14.5 d(5~45 d)。5例患者应用糖皮质激素联合环磷酰胺(cyclophosphamide,CTX)治疗,环磷酰胺剂量为100 mg/d或200 mg 隔日1次输注,输注剂量中位数2 200 mg(200~6 000 mg)。3例患者应用激素或激素联合环磷酰胺治疗效果欠佳或病情复发,应用利妥昔单抗(rituximab,RTX)治疗,其中2例患者利妥昔单抗剂量为100 mg/周,共4次,1例患者利妥昔单抗剂量为375 mg/m2,共1次。
10例患者出院后均应用糖皮质激素口服维持治疗,逐步减量至停药,中位维持时间3个月(2~12个月)。2例患者应用硫唑嘌呤(azathioprine,AZA)100 mg/d维持治疗,维持时间分别为40个月及6个月。1例应用利妥昔单抗治疗后症状持续缓解,但3~6个月后出血症状反复,应用利妥昔单抗100 mg输注维持治疗,输注频率为3~4个月输注1次。
2 结 果
2.1 实验室检查指标 结果(表2)表明:10例患者入院后血常规示血小板均正常。凝血功能检查:中位凝血酶原时间(prothrombin time, PT)为81.35 s(63.8~124.4 s),中位部分凝血活酶时间(activated partial thromboplastin time, APTT)为163.5 s(119.9~211.7 s),均较正常值延长;纤维蛋白原中位值3.807 g/L(2.017~6.0 g/L),水平均正常或增高。凝血因子浓度检查FⅡ、FⅦ、FⅧ、FⅨ、FⅩ、FⅩⅠ浓度均正常,而FⅤ浓度中位值0.7%(0.3%~2.0%)。凝血因子抑制物定性均为阳性,抑制物定量中位值4.8 BU/mL(0~32 BU/mL)。
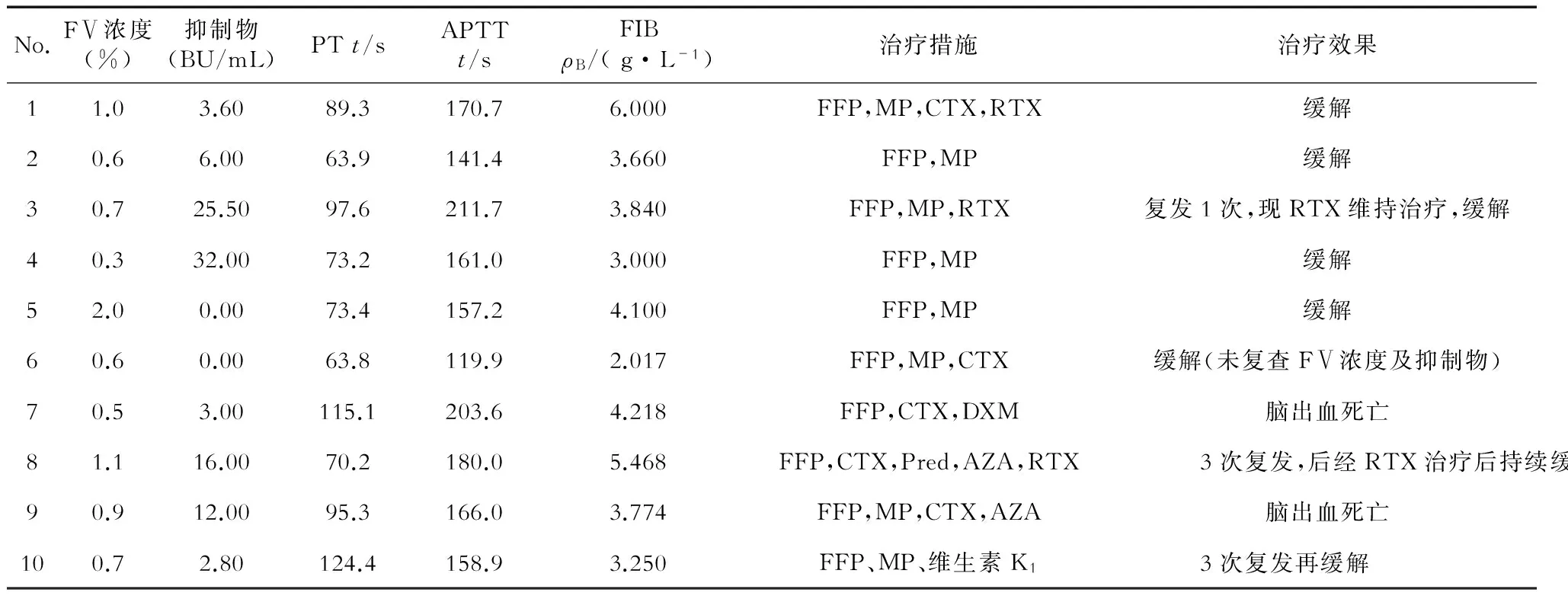
表2 患者实验室检查结果
2.2 随访结果 10例患者中位随访时间22.5个月(2~156个月),在治疗过程中出血症状均有所好转或消失。7例患者在治疗一段时间后复查FⅤ浓度,恢复为50%以上;FⅤ浓度恢复为50%以上所需治疗中位时间为23 d(13 d~35个月)。1例患者维持治疗1年后停用激素,后间断口服激素,仍有间断牙龈出血症状,未进一步复查凝血功能及FⅤ浓度、抑制物定性定量,随访83个月,近1年自诉未再出现出血症状。2例患者死亡,1例患者为出院后2个月出血仍未控制,突发颅内出血死亡;1例患者经我院治疗后出血症状消失,维持治疗半年后自行停药,后间断出现皮肤出血症状,自行间断口服激素治疗,半年后出现颅内出血死亡。3例患者在随访过程中病情复发,1例患者经激素、环磷酰胺、硫唑嘌呤治疗后病情控制,维持治疗近3年余停药,停药4年余后再次出现出血症状,入院应用激素及硫唑嘌呤治疗后出血症状缓解,FⅤ浓度恢复正常,应用激素及硫唑嘌呤维持治疗3个月后停药,3个月后再次复发,应用利妥昔单抗治疗后随访4年余未再发生出血症状;1例患者激素治疗效果欠佳,经利妥昔单抗治疗后出血症状控制,FⅤ浓度恢复正常后停用激素,但停药后3个月余再次出现出血症状,经输注利妥昔单抗后出血症状再次控制,后出血症状每3~6个月反复出现,应用利妥昔单抗100 mg输注维持治疗,输注频率为3~4个月输注1次,随访近2年未再发生出血症状;1例患者激素治疗后FⅤ浓度恢复正常,停药5个月后再次出现出血症状,应用激素治疗后FⅤ浓度再次恢复正常,半年后再次出现出血症状,应用激素治疗后FⅤ浓度再次恢复正常,后随访8个月余未再发生出血症状。
3 讨 论
AFⅤD最早于1955年由Hörder等[3]报道,迄今文献[4]报道仅有200多例。获得性FⅤ抑制物的产生常分为以下3种情况:第1种为同种抗体,见于先天性FⅤ缺乏症患者,因多次接受异体血液制品后产生特异性FⅤ异型抗体;第2种为异种抗体,见于牛凝血酶(bovine thrombin,BT)暴露后患者;第3种为自发产生的抗FⅤ抗体,见于既往凝血指标正常患者,常见相关因素为抗生素的应用、恶性肿瘤、近期外科手术及自身免疫性疾病、输血等[5]。Knöbl等[6]回顾分析了1955~1997年105例FⅤ抑制物病例,牛凝血酶制剂暴露后产生的占45.9%。Wang等[4]回顾分析了1955~2016年共200例FⅤ抑制物病例,其中有74例因牛凝血酶暴露诱导产生,其余126例均为非牛凝血酶(non-bovine thrombin,NBT)暴露诱导产生。后者包括抗生素(头孢他啶[7]、环丙沙星、哌拉西林他唑巴坦等,42例,33%),手术(33例,26%),肿瘤(21例,17%),自身免疫性疾病(14例,11%),感染(22例,17%),器官移植(6例,5%),除抗生素外药物(胺碘酮、华法林、达比加群酯、氯吡格雷,5例,4%),特发性(29例,23%)。近年来因BT临床不再使用导致其暴露诱导产生FⅤ抑制物的病例明显减少。Wang等[4]回顾分析了2010—2016年共52例FⅤ抑制物病例,其中仅4例BT暴露后FⅤ抑制物阳性病例。本研究10例AFⅤD患者中,1例为急性胰腺炎治疗后20 d发现凝血功能异常,近期有头孢他啶治疗史,入院时合并肺感染,故肺感染、头孢他啶[5]均为FⅤ抑制物可能诱因,而其余9例患者均无明显已报道诱因存在。
AFⅤD多见于老年患者,临床表现多种多样,可仅为实验室指标异常而无临床出血症状,亦可出现患者各部位、器官的出血,甚至致命的严重出血,如颅内出血[5]。有研究[8]显示,患者出血倾向与血浆剩余FⅤ浓度有关,但另外一些研究[9-10]却显示患者出血程度与FⅤ浓度、FⅤ抑制物并无明显相关性。部分患者甚至出现血栓并发症,提示FⅤ在促凝和抗凝过程中均扮演重要角色[5,11]。大多数牛凝血酶诱导的FⅤ抑制物患者常表现为凝血指标的异常,并没有出血表现,且抗体多可在短期内自行消失[12]。本研究10例患者首诊时均有不同程度的多部位出血,其中皮肤黏膜出血及血尿较常见。轻者表现为皮肤黏膜出血,重者起病时即出现消化道出血、胸腔出血甚至颅内出血,10例患者无关节出血表现。AFⅤD的诊断除了以出血症状为主要临床,还依赖于凝血功能相关检查。患者如既往无出血史及家族病史,血小板水平及功能正常,如出现PT和APTT明显延长,FⅤ活性水平明显降低,其余凝血因子活性正常,抑制物定性或定量试验阳性可以确诊[5]。
治疗AFⅤD主要在于控制出血和清除自身抗体或抑制物[13]。部分患者无明显出血症状,抑制物可自行消失,多见于牛凝血酶暴露后FⅤ抑制物阳性患者,往往无需治疗[5]。对于有出血症状的患者,可应用新鲜冰冻血浆、浓缩血小板、凝血酶原复合物等输注控制出血症状[13]。有20%的FⅤ存在于血小板α颗粒中[7],因而部分患者输注浓缩血小板止血效果明显[5]。此外,重组人凝血因子ⅤⅡa(recombinant activated factor ⅤⅡa,rFⅤⅡa)对于部分有严重出血症状的患者止血效果较好[14-15]。清除抗体或抑制物可应用免疫抑制治疗(如糖皮质激素、环磷酰胺、硫唑嘌呤、利妥昔单抗等)、大剂量静脉人免疫球蛋白(intravenous immunoglobulin,IVIG)、血浆置换、免疫吸附治疗等[5]。对于严重出血患者,与血浆置换和免疫吸附治疗相比,免疫抑制治疗起效更快、FⅤ抑制物滴度下降亦更为迅速[16-18]。此外,IVIG的应用也可以提高Ⅴ因子活性[19-20]。AFⅤD患者的整体预后较好,但不同发病机制者差异较大[5]。有研究[6]认为,牛凝血酶制剂暴露后患者预后相对较好。本研究10例患者中仅1例可能与抗生素(头孢他啶)有关,目前病情持续缓解。
综上所述,由于AFⅤD临床少见,且患者常首诊于非血液专科医院,易误诊或漏诊延误病情。本病发病机制尚不明确,临床出血症状轻重不一,治疗方案及疗效均限于个案报道,目前尚缺乏最佳治疗方案的指南与共识,值得进一步研究。
[ 1 ] HIRAI D, YAMASHITA Y, MASUNAGA N, et al. Acquired factor Ⅴ inhibitor[J].Intern Med, 2016,55(20):3039-3042.
[ 2 ] GAVVA C, YATES S G, RAMBALLY S, et al. Transfusion management of factor Ⅴ deficiency: three case reports and review of the literature[J].Transfusion,2016,56(7):1745-1749.
[ 3 ] HÖRDER M H. Isolierter factor Ⅴ- mangel bedingt durch einen spezifischen Hemmkörper [J]. Acta Haematol,1955,13(4):235-241.
[ 4 ] WANG X, QIN X, YU Y, et al. Acquired factor Ⅴ deficiency in a patient with a urinary tract infection presenting with haematuria followed by multiple haemorrhages with an extremely low level of factor Ⅴ inhibitor: a case report and review of the literature [J]. Blood Coagul Fibrinolysis, 2016. [Epub ahead of print].
[ 5 ] 杨艳辉,王宏梅,薛 峰,等.获得性凝血因子Ⅴ抑制物患者三例报告并文献复习[J].中华血液学杂志,2012,33(4):294-298.
[ 6 ] KNÖBL P,LECHNER K.Acquired factor Ⅴ inhibitors [J].Baillieres Clin Haematol,1998,11(2):305-318.
[ 7 ] CUI Q Y, SHEN H S, WU T Q, et al.Development of acquired factor Ⅴ inhibitor after treatment with ceftazidime: a case report and review of the literature [J]. Drug Des Devel Ther, 2015,9: 2395-2398.
[ 8 ] EMORI Y, SAKUGAWA M, NIIYA K, et al. Life-threatening bleeding and acquired factor Ⅴ deficiency associated with primary systemic amyloidosis[J].Blood Coagul Fibrinolysis,2002, 13(6):555-559.
[ 9 ] WIWANITKIT V. Spectrum of bleeding in acquired factor Ⅴ inhibitor: a summary of 33 cases [J].Clin Appl Thromb Hemost, 2006,12(4): 485-488.
[10] MORRIS C J, CURRY N. Acquired factor Ⅴ inhibitor in a critically ill patient [J]. Anaesthesia, 2009,64(9): 1014-1017.
[11] LU L, LIU Y, WEI J,et al. Acquired inhibitor of factor Ⅴ: first report in China and literature review [J]. Haemophilia, 2004,10(5): 661-664.
[12] LIPPI G,FAVALORO E J,MONTAGNANA M, et al.Inherited and acquired factor Ⅴ deficiency[J]. Blood Coagul Fibrinolysis, 2011,22(3): 160-166.
[13] ANG A L,KUPERAN P, NG C H,et al.Acquired factor Ⅴ inhibitor. A problem-based systematic review[J]. Thromb Haemost,2009,101(5):852-859.
[14] TESSIER-MARTEAU A,CROQUEFER S,MEZIANI F, et al. Acquired factor Ⅴ inhibitor in a context of sepsis and disseminated intravascular coagulation[J].Am J Hematol,2010, 85(2):145-146.
[15] FRANCHINI M, LIPPI G. Recombinant activated factor Ⅶ:mechanisms of action and current indications[J]. Semin ThrombHaemost, 2010, 36(5):485-492.
[16] TRIBL B, KNÖBL P, DERFLER K, et al.Rapid elimination of a high-titer spontanoues factor Ⅴ antibody by extracorporeal antibody-based immunoadsorption and immunosuppression[J]. Ann Hematol, 1995, 71(4):199-203.
[17] FU Y X, KAUFMAN R, RUDOLPH A E, et al. Multimodality therapy of an acquired factor Ⅴ inhibitor [J].Am J Hematol, 1996, 51(4):315-318.
[18] JANSEN M, SCHMALDIENST S, BANYAI S, et al. Treatment of coagulation inhibitors with extracorporeal immunoadsorption(Ig-Therasorb) [J].Br J Haematol, 2001, 112(1):91-97.
[19] BUCLIN T, SCHMIDT PM, HAUERT J, et al.Acquired factor Ⅴ inhibitor treated with intravenous immunoglobulins [J].Schweiz Med Wochenschr, 1992, 122(51-52): 1968-1970.
[20] DE RAUCOURT E, BARBIER C, SINDA P, et al. High-dose intravenous immunoglobulin treatment in two patients with acquired factor Ⅴ inhibitors[J].Am J Hematol,2003, 74(3):187-190.
[本文编辑] 叶 婷, 贾泽军
Clinical analysis of acquired coagulation factor Ⅴ deficiency
CHEN Yun-fei, LIU wei, LIU Xiao-fan, FU Rong-feng, HUANG Yue-ting, XUE Feng, ZHANG Lei, YANG Ren-chi*
Institute of Hematology and Blood Diseases Hospital, Chinese Academy of Medical Sciences & Peking Union Medical College, Tianjin 300020, China
Objective: To conclude the clinical experience of acquired factor Ⅴ deficiency (AFⅤD). Methods: Clinical data of 10 cases with acquired coagulation factor Ⅴ deficiency were analyzed retrospectively, the clinical features were analyzed and clinical experiences were concluded. Results: The 10 patients included 7 males and 3 females. Their ages varied from 51 to 71 with a median age of 60 years. No one had hereditary coagulation factor deficiency or family history. Patients with acquired coagulation factor Ⅴ deficiency had different manifestations, including spontaneously mucous bleeding, epistaxis, hematuresis, melena and encephalic bleeding. Laboratory test showed that all patients had prolonged prothrombin time (PT) and activated partial thromboplastin time (APTT), decreased FⅤ activity, positive results of inhibitor qualitative or quantitative test. They were all diagnosed with acquired coagulation factor Ⅴ deficiency. All patients had fresh frozen plasma transfusions and were treated with steroid and immunosuppressive agents. There were 5 of the 10 patients had a remission and stopped bleeding, 3 of the 10 patients had poor therapeutic effect with steroid and cyclophosphamide, but had effective result with rituximab, 2 of the 3 patients had a normal level of FⅤ activity after treatment of rituximab and stopped bleeding, 1 of the 3 patients needed maintenance treatment of low dose rituximab, 2 of the 10 patients died of encephalic bleeding. Conclusions: Acquired factor Ⅴ inhibitor is a rare coagulation disorder with variable clinical symptoms. Steroid, cyclophosphamide and rituximab may be effective to eliminate the inhibitors.
acquired factor V inhibitor; immunosuppressive regimens; glucocorticoid
2017-03-22 [接受日期] 2017-04-15
国家重点研发计划(2016YFC0901503),天津市自然基金面上项目(16JCYBJC26700),中国医学科学院医学与健康科技创新工程经费资助(2016-I2M-1-002). Supported by the National Key Research and Development Program of China(2016YFC0901503), Tianjin Municipal Science and Technology Commission Grant(16JCYBJC26700), and CAMS Innovation Fund for Medical Sciences(CIFMS,2016-I2M-1-002).
陈云飞,硕士,主治医师. E-mail: opalfly@163.com
*
Corresponding author). Tel: 022-23909009, E-mail: rcyang65@163.com
10.12025/j.issn.1008-6358.2017.20170237
R 544
A

