初中生化学微粒观构建的实践反思
钱海如+赵华
摘要:微粒观的构建是初中生学习化学需要形成的基本认识能力。初中生学习“物质构成的奥秘”普遍感到较难,尤其是“离子”的内容,学习过程中经常出现20项问题,采取以下教学策略:以实验探究引领学生走进微观世界,以模型运用帮助学生搭建认知桥梁,以理论建立锻炼学生运用逻辑推理,就可以增强学生对微粒本身的认识,引导学生建立微粒表征、符号表征、宏观表征的有机联系,使学生形成科学认识方式,构建微粒观。同时,在教学中还要注意避免内容空洞贫乏,忽视先前经验,随意拔高教学要求等问题。
关键词:课程标准;初中化学;微粒观;教学策略
文章編号:1005–6629(2017)5–0035–06 中图分类号:G633.8 文献标识码:B
初中化学教学实践中发现,初中生学习“物质构成的奥秘”普遍感到较难,在认识上难以实现从宏观到微观的转变,尤其是学习到“离子”的内容,虽然师生平时花费了大量的时间讲解和训练,学生微粒观的构建效果仍不明显,这一现象引起了我们的思考:问题究竟出在哪里?怎样有效地解决?本文从《义务教育化学课程标准(2011年版)》(以下简称《课程标准》)的基本要求入手,侧重于从教学的实践层面,分析学生学习过程中出现的常见问题,并以“离子”为例谈谈初中生化学微粒观构建的教学策略。
1 课程标准对微粒观的基本要求
《课程标准》指出,化学学科应通过具体化学知识和概念的学习,促进学生形成化学学科思想和基本观念,逐步使学生从单一的定性与定量、宏观与微观的物质认识过程,过渡到定性与定量相结合、宏观与微观相结合的物质认识过程。从宏观到微观、从定性到定量,体现了化学学科发展的趋势。对物质组成的微观研究和定量研究使化学逐步成为能在实验和理论两个方面同时发展的一门自然科学[1]。“课程内容”在有关的一、二级主题中对微粒观的构建有明确的要求,具体见表1所示[2]。义务教育教科书《化学(九年级上、下册)》(以下简称《教科书》)[3]在有关章节中呈现了关于“离子”的学习内容,具体见表2所示。
微粒观就是人们对物质微粒性的基本看法,表现为自觉地在原子、分子、离子的水平上认识常见物质的组成、结构、性质、用途和变化现象的思维倾向。从表1可以看出,在《课程标准》中使用了“知道”、“认识”、“解释”等行为动词,这些行为动词涵盖了“认知性学习目标的水平”中的初级、中级、高级水平[4]。从表2可以看出,自从在第3章学习了离子以后,在后续的学习中要进一步认识到离子与其他粒子之间的关系,然后基于这些微粒的认识再去体会物质的组成和分类,去理解物质的物理性质、物理变化、化学性质和化学变化等的本质。可以看出,微粒观的构建,有利于学生形成认识物质的思路:深入到物质内部去看物质的本质,然后跳出来再看它的一些外观特征、变化的规律。微粒观是《课程标准》的基本要求,是学生学习化学必须形成的核心化学观念。
2 学生学习离子出现的常见问题
“离子”的教学是建立在学生已经知道了物质是由微粒构成的,初步建立了分子、原子模型,在此基础上,继续深入到原子的内部,从核外电子的分层排布入手,介绍离子的形成和离子构成物质,使学生对构成物质的微粒有一个完整系统的认识,是对学生微粒观的丰富。由于内容比较抽象,对于以形象思维为主的初中生来说就显得比较困难。学生在具体内容的学习过程中经常出现的问题有以下20项(见表3)[5]。
以上所列的问题类型中,“对离子本身的认识”共5项,“离子及其符号表征的联系”共3项,“离子符号表征与宏观物质的联系”共12项,可以看出“离子符号表征与宏观物质的联系”是学生出现的重点问题,但这些重点问题实际上是对离子的初步应用层次,而问题的根源却在“对离子本身的认识”和“离子及其符号表征的联系”,这些内容恰恰是学生开始学习“物质构成的奥秘”时的缺失引起的。因此,我们需要加强“对离子本身的认识”的教学,让学生对物质的微观构成了解非常清楚,在此基础上再对微粒表征和符号表征建立有机联系,于是,学生对“离子符号表征与宏观物质的联系”就会水到渠成了。
3 教学策略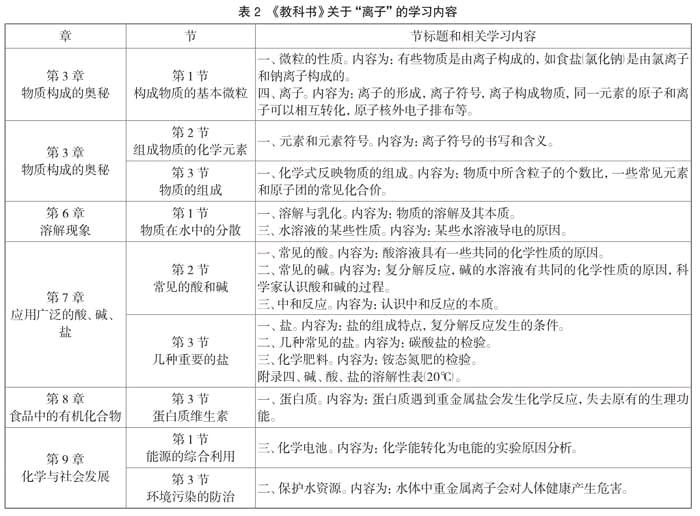
微粒观构建的教学价值在于培养学生由表及里、由现象到本质、由宏观到微观的科学认识方式,锻炼学生的逻辑推理思维和理论思维。需要我们妥善运用观察、想象、类比、模型化、探究和实践活动等方法,帮助学生逐步理解化学现象的本质。教学中,我们可以采取以下策略:
3.1 以实验探究引领学生走进微观世界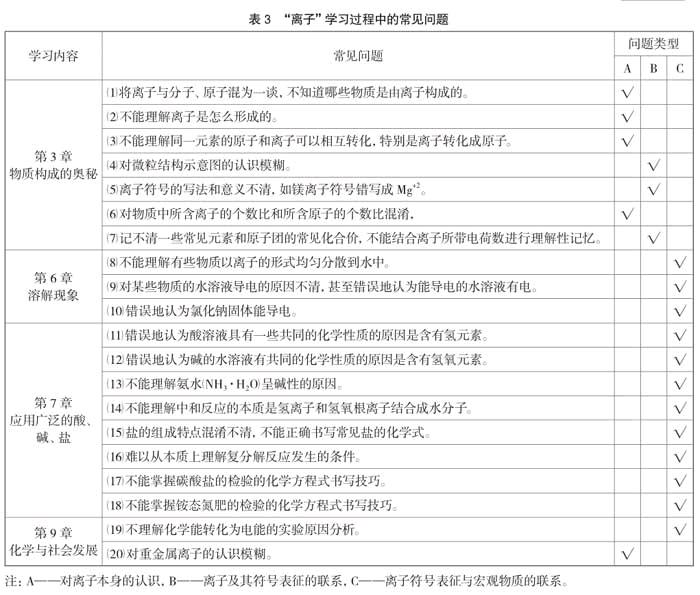
实验探究,可以培养学生的学习兴趣和实证意识。在初中阶段学生建立的微粒观的核心内容主要包括:宏观物质都是由原子、分子、离子等肉眼看不见的基本粒子构成的;构成物质的微粒是极其微小的,并且存在着质量、体积大小不同的差异;微粒是不断运动的;微粒之间存在间隔;构成物质的微粒之间存在相互作用。这些核心内容是学生头脑中原先没有的,学生原有的看法往往是“眼见为实”,如何转变学生原来的看法是难点,对教师的要求也较高,如果处理不当,学生在此就出现分化。《教科书》编排“物质构成的奥秘”的思路是“微粒的性质→分子→原子(原子结构)→离子(原子核外电子排布)→元素→化合价”,从编排上可以看出,“微粒的性质→分子→原子(原子结构)”是学习“离子”的基础和铺垫,更是“前戏”,对“离子”的教学起到至关重要的作用。所以在“分子、原子”中,首先要充分利用身边的现象和简单实验,例如,氨分子的运动、水与酒精混合的体积变化、比较空气和水在被压缩时的体积变化情况、观察并解释浓氨水和浓盐酸相互接近时的“空中生烟”现象、品红的扩散等;其次,还要利用科学家们做过的实验视频资料,例如,STM(扫描隧道显微镜)与“原子操纵”技术,卢瑟福的粒子散射实验等;在“离子”教学中演示“金属钠在氯气中燃烧”的实验,播放“熔融氯化钠导电”实验视频。这些简单可行的实验可以激发学生的学习兴趣,是引导学生走进微观世界的好帮手,而视频资料能展示科学的进步,化学技术的发展,化学家们的追求,微观世界的真实,还能激发学生的求知欲望。简单实验及视频资料都是宏观到微观的一些具体现象和实证,不仅引导学生承认微观粒子的存在,还帮助学生慢慢打开微观世界的大门,走进微观世界,这是帮助学生形成科学认识方式的基础。
3.2 以模型运用帮助学生搭建认知桥梁
模型运用,便于打通学生的宏观思维和微观想象。化学可以说是应用宏观与微观结合、思维与实践结合的方法研究实物材料(化学物质)的组成、结构、性质和变化,以及它们的相互联系,为人类利用自然、改造自然、保护自然、提高生活质量和生存安全服务,满足人类的实际需要以及有关的好奇心和兴趣的科学[6]。科学的认识方式是人们在认识和改造世界中遵循或运用的、符合科学一般原则的各种途径和手段,模型运用就是其中之一。著名物理学家钱学森曾说:“模型就是通过我们对问题的分析,利用我们考察来的机理,吸收一切主要因素,略去一切非主要因素所创造出来的一幅图画。”对于“离子”的教学,模型运用可以从三个方面入手:
3.2.1 尽量使用实物模型和动画模型
实物模型和动画模型就是让学生体验“真实感”,实现“宏观世界”与“微观世界”的连接。例如,在学习“氯化钠”的形成过程时,出示钠原子和氯原子的核外电子的分层排布的原子结构模型,如果再配上钠原子和氯原子“甩掉(失去)”、“捕捉(得到)”电子的形象动画,能够将复杂的核外电子分层运动的理论和离子的形成“可视化”。在学习“物质的溶解”时,配上氯化钠溶于水的微观动画,学生能形象地“观察”钠离子和氯离子在水分子的作用下,分散到水中,此时得到的水溶液中存在三种微粒(钠离子、氯离子、水分子),并且在不断运动(自由移动),这对于学生建立“宏观物质氯化钠溶于水”到“离子分散到其他微观粒子之间”很有帮助,有利于学生快速理解物质溶解的本质,避免了教师的单纯讲解,使学生感到枯燥无味,脱离初中生的实际,也避免了涉及高中阶段的教学要求,超出课标的要求。
3.2.2 着力构建概念模型和图示模型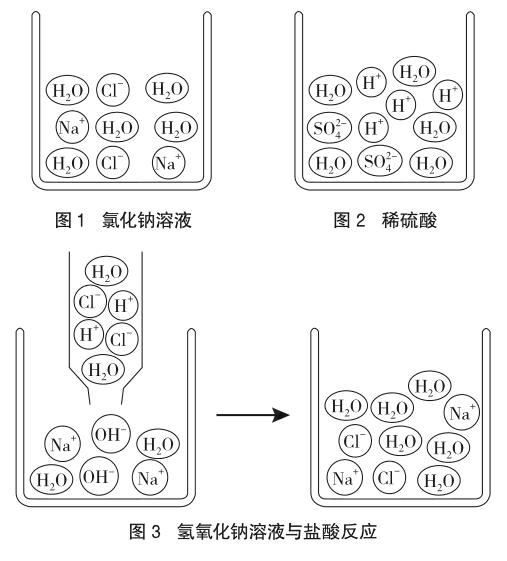
概念模型和图示模型都是思维模型的一种,都属于一种科学操作和科学思维的基本方法。作为化学学科核心素养的关键能力,其中包括化学信息能力(如结构化、变换、推理等),化学学习能力(如宏微结合、分类研究等化学认知策略及能力等)[7]。这里就涵盖了化学思维模型,需要我们逐步培养学生的化学学科的模型认知素养,即能认识化学现象与模型之间的联系,能运用多种模型来描述和解释化学现象。(1)关于概念模型的构建。例如,在“离子”概念教学中,尽管教科书中这样提出:“在化学变化中,电中性的原子经常因得到或失去电子而成为带电荷的微粒,这种带电的微粒称为离子[8]”,我们还要增加以下问题:①离子与分子、原子有什么区别和联系?②原子转化成离子后,所带电荷不同,怎样分类?③离子怎样才能转化成原子?④以原子为中心,怎样将原子、分子、离子、物质联系起来?这些问题可以帮助学生领会离子概念的含义和实质,充分运用比较与分类的思维方法,进行概念学习的思维建模,以达到准确理解概念、科学应用概念解决实际问题的目的。(2)关于图示模型的构建。例如,在“物质的溶解”、“水溶液的某些性质”、“中和反应”教学中,呈现下列图示(如图1、2、3所示),图1反映了物质(氯化钠)溶于水中微粒的种类以及钠离子和氯离子的数目比,图2反映了稀硫酸中存在的微粒种类以及氢离子和硫酸根离子的数目比,图3反映了氢氧化钠溶液与盐酸反应后的微观粒子的种类和数目的变化情况,建立这样的图示模型是揭示物质溶解过程和化学反应过程本质的重要手段,可以将实验与观察、微观想象也解决不了问题更加形象,使得分析思路更加清晰。
3.2.3 巧妙利用数学模型和过程模型
数学模型和过程模型都是一种有效的学习模型,它们能以不变应万变,让学生更好地理解化学物质。(1)关于数学模型的利用。化学上的许多基本概念与理论,看起来都是定性描述与规定,实际上都涉及到量的比较和定量计算。例如,关于粒子所带电荷数的教学中,可以依据核外电子数和质子数建立一种数学模型,即n=(-1)×a+(+1)×b(其中,n:粒子所带电荷数,a:核外电子数,b:质子数)。当n=0时,呈电中性;当n=-x时,属于阴离子,带x个单位负电荷;当n=+y时,属于阳离子,带y个单位正电荷。利用该数学模型还可以解决学生“错误地认为能导电的水溶液有电”的问题,以及解决今后学习中的“电荷守恒”问题。另外,学生在学习离子符号的写法时,经常错写离子符号(如镁离子符号错写成Mg+2)。可以借助数学上“同类项合并”模型,方法是:①钠离子带1个单位正电荷,在Na的右上方标出1个“+”,写作:Na+;②镁离子带2个单位正电荷,在Mg的右上方标出2个“+”(Mg++),规范写作:Mg2+;③铝离子带3个单位正电荷,在Al的右上方标出3个“+”(Al+++),规范写作:Al3+,以此类推。实践证明,使用这样的教法,学生的错误率较低。(2)关于过程模型的利用。过程模型就是根据学生的认知心理逻辑发展规律,结合人类一般认识过程和化学知识学习的过程,注重宏观物质与微观抽象结构相结合,微观抽象结构与宏观物质模型结构结合,将获得的理论模型信息(比如化学符号),与宏观物质结构模型相结合,实现由物质模型向思想模型(观念)的转换[9]。例如,在“氯化钠的形成过程”教学中,采取下列流程:①提问:氯化钠是由什么微粒构成的?②演示实验:钠在氯气中燃烧;③展示氯化钠固体和氯化钠结构模型;④展示钠离子和氯离子结构示意图;⑤指引学生观察模型、知觉所表征的意义(微粒图式和离子结构示意图);⑥组织交流讨论;⑦引导学生联系整合;⑧指导学生画出氯化镁的微粒图式和离子结构示意图。这一教学程序强调学生的原有知识经验,注重“整体——部分——整体”的认识过程,在教师的组织和引导下,通过师生、生生的相互交流,让学生主动建构属于自己的学习模型,构建了微粒观,并能将其运用到后续更广泛的学习当中。
3.3 以理论建立锻炼学生运用逻辑推理
理论建立,能够培养学生的逻辑思维和推理能力。所谓的理论思维是一个具有广泛涵义的概念,它既含有哲学思维(即世界观和方法论)和逻辑思维,又含有自然科学中的理论(科学概念、原理、定律)和假说,以及联想和想象力等。中国科学院院士、吉林大学冯守华教授在一次讲座中提到:“化学习惯于从结构的观点看问题”。这就告诉我们,学习化学需要深入到物质内部去看物质的本质。在进行“原子”教学时,适宜以时间为序展开:古代东方哲学认为的阴阳五行论→德谟克利特的古典原子论→牛顿的粒子学说→道尔顿的原子理论→阿伏伽德罗的分子理论→汤姆逊发现电子(原子的枣糕模型)→卢瑟福行星模型→发现质子和中子(原子核模型)。在进行“离子”教学时,从卢瑟福原子结构相关知识开始,适当介绍原子核外电子排布,介绍科学家的猜想、核外电子的真实运动情况、科学家研究手段和方法,展示核外电子的分层排布的原子结构模型,并简化为原子结构示意图,侧重分析1-18号元素的原子核外电子排布的特点。然后介绍原子的稳定结构理论,引导学生分析鈉原子和氯原子结构特点,进而发现钠原子和氯原子的结构不稳定,于是在化学变化中,这些电中性的原子经常因得到或失去电子而成为带电荷的微粒——离子(阳离子、阴离子),带有相反电荷的钠离子和氯离子之间相互作用,构成了氯化钠。学生在具体的科学史实中不仅了解到科学家的严谨求实的科学态度,而且领悟了科学家们的“提出问题、实验分析、建立模型、解释现象”的逻辑思维,在潜移默化中培养了学生的逻辑思维和推理能力。
4 教学中应注意的问题
化学的核心是其基本观念以及相应的思维和实践[10]。离子的教学是在学生形成对物质宏观和微观的初步认识的基础上,建立微粒表征、符号表征、宏观表征的有机联系,帮助学生形成“宏观(物质特征、现象)→微观(微粒结构、符号)→宏观(物质特征、变化)”的认识物质的思路。当前在离子教学中出现了一些不良倾向,主要表现在教学内容贫乏、忽视学生基础、随意拔高要求等,给学生学习造成了障碍,加重了学生学习的负担,不利于培养学生的微粒观。因此,教学中应注意以下问题[11~13]。
4.1 忌内容空洞贫乏
化学是在原子、分子水平上研究物质的,“物质构成的奥秘”旨在引导学生用微粒的观点来学习化学,学习内容比较抽象,微观概念较难建立,涉及到离子的内容又分散于各个章节中,知识零散,难以系统学习。因此,在教学中要秉承教师的“教”是为学生的“学”服务的观点,充分结合学生实际,创设生动直观的情境,从分析身边的一些现象和简单实验入手,并充分利用现代教育技术,激发学生的学习兴趣,提高学生的想象能力;同时要让学生动手绘制微观示意图或制作模型,尝试解释一些簡单的化学现象。此外,还要介绍科学家探索物质微观世界、认识酸和碱的过程的科学史料,拓展学生视野,学习科学家严谨求实的科学态度。防止在课堂上“就知识讲知识”、“从理论到理论”,内容空洞贫乏,既忽视了初中生的心智特点,又达不到微粒观构建的基本要求。
4.2 忌忽视先前经验
学生在学习“物质构成的奥秘”前,已经从媒体、科普杂志和书籍上接触过“分子、原子、离子、质子、中子”等词汇,从物理课上学习了有关分子的知识,如分子在不停地做无规则运动、分子之间存在相互作用力等,这些先前经验需要我们在教学时激活。同时在教学过程中要注意与学生的交流对话,进一步了解他们原有的看法,充分抓住关键点上构建微粒观的时机,巧妙利用先前经验的“同化”和“认同”作用,避免在学习过程中产生“相异构想”。如对课堂提问答案判断后进行如下追问:你是怎么想的?你从哪个角度想到的?你为什么有这样的答案?你在记忆过程中有哪些技巧?通过学习,你觉得你原来的哪些看法是不科学的?以后在应用时要注意什么?
4.3 忌拔高教学要求

初中生微粒观的构建就是要在教学过程中加强学生对微粒本身的认识,引导学生建立微粒表征、符号表征、宏观表征的有机联系,从而使学生形成科学认识方式,在此基础上学生才能逐步理解物质及其变化的本质,逐步理解物质的多样性和统一性,逐步形成核心化学观念并发展探究物质及其变化的兴趣。
参考文献:
[1][2][4]中华人民共和国教育部制定.义务教育化学课程标准(2011年版)[S].北京:北京师范大学出版社,2011.
[3][5][8]中学化学国家课程标准研制组.义务教育课程标准实验教科书·化学(九年级)(上、下册)[M].上海:上海教育出版社,2015.
[6][7][10]吴俊明.关于核心素养及化学学科核心素养的思考与疑问[J].化学教学,2011,(11):3~8,23.
[9]文庆城,李凤.中学化学物质结构学习过程模型建构[J].教学与管理,2006,(9):77~78.
[11]吴星,沈怡文.给化学教师的101条建议[M].南京:南京师范大学出版社,2006.
[12]钱海如.初中化学课程中化学计算的教学策略[J].化学教学,2013,(11):9~12,81.
[13]钱海如,闵蓉蓉.基于化学学科本质的有效教学实践[J].化学教与学,2014,(6):15~17.

