电子止吐仪联合昂丹司琼预防乳腺癌延迟性化疗相关恶心、呕吐的效果观察
冯小娟,胡小霞,陈合波
电子止吐仪联合昂丹司琼预防乳腺癌延迟性化疗相关恶心、呕吐的效果观察
冯小娟,胡小霞,陈合波
[目的]观察电子止吐仪联合昂丹司琼预防乳腺癌延迟性化疗相关恶心、呕吐的疗效。[方法]将63例接受中、高致吐性化疗药物治疗的乳腺癌病人分为两组,试验组(31例)应用电子止吐仪联合昂丹司琼治疗,对照组(32例)应用昂丹司琼治疗,观察并记录两组乳腺癌病人化疗结束后第1天~第3天的恶心、呕吐情况。[结果]试验组和对照组在第1天~第3天呕吐控制有效率分别为64.5%和28.1%、74.2%和50.0%、96.8%和87.5%,呕吐控制情况第1天、第2天比较差异有统计学意义(P<0.05),第3天比较差异无统计学意义(P>0.05)。试验组和对照组在第1天~第3天恶心控制有效率分别为51.6%和25.0%、80.6%和56.3%、87.1%和81.3%,恶心控制情况第1天、第2天比较差异有统计学意义(P<0.05),第3天比较差异无统计学意义(P>0.05)。且两组的不良反应轻微,主要有头晕、头痛、乏力、便秘等,不良反应发生率差异无统计学意义。[结论]电子止吐仪联合昂丹司琼预防乳腺癌延迟性化疗相关恶心、呕吐的作用优于单用昂丹司琼,且不良反应可以耐受。
乳腺癌;化疗;恶心;呕吐;电子止吐仪;昂丹司琼
乳腺癌是中国女性发病率最高的癌症,中国总计有超过169 452 例新发浸润性乳腺癌,所有浸润性乳腺癌病人中大约 81.4%接受了化疗[1]。化疗相关性恶心呕吐(chemotherapy-induced nausea and vomiting,CINV)是化疗中最常见和最让病人难以忍受的不良反应,严重影响病人的生活质量及治疗依从性[2-3]。美国国家癌症研究所统计数据表明,在没有使用药物的情况下,有约90%的乳腺癌化疗病人会经历不同程度的CINV[4]。昂丹司琼是一种5-羟色胺3 (5-HT3 )受体拮抗剂,主要通过竞争性地与5-HT3 受体结合,从而阻断消化道嗜铬细胞释放出5-羟色胺产生的致呕作用,对急性CINV控制率为52.9%~68.8%,但对延迟性CINV的控制率仅为28%左右[5]。电子止吐仪是一种经皮神经电刺激治疗仪,发出周期性低频双向脉冲波通过刺激手腕部正中神经并向上传递到呕吐中枢,达到调节导致神经性呕吐的信号和往返于胃部迷走神经信号,减轻呕吐、恶心、厌食症状[6]。国内鲜有针对乳腺癌病人的延迟性CINV的研究,而控制延迟性CINV对于数量众多的乳腺癌病人有重要意义。我院于2015年2月—7月完成电子止吐仪联合昂丹司琼预防乳腺癌病人中、高致吐性化疗药物所致迟发型CINV的观察,观察结果报告如下。
1 资料与方法
1.1 一般资料 63例病人来自2015年2月—7月某大型三级甲等医院普外科,均为乳腺癌行化疗病人。采用完全随机方法随机分为试验组(31例)、对照组(32例)。试验组:男1例,女30例,年龄48.68岁±10.64岁,术前新辅助化疗4例,术后化疗27例。对照组:男1例,女31例,年龄46.63岁±9.35岁,术前新辅助化疗2例,术后化疗30例。两组乳腺癌化疗病人一般资料比较差异无统计学意义(P<0.05),具有可比性。
1.2 纳入标准 ①年龄为18岁~70岁,病理报告确诊为乳腺癌病人。②行含中、高致吐性化疗药物(顺铂、表柔比星、环磷酰胺)的化疗方案至少1周期。化疗方案为氟尿嘧啶+表柔比星+环磷酰胺6个周期、表柔比星+环磷酰胺4个周期后序贯紫杉醇4个周期、表柔比星+环磷酰胺4个周期后序贯紫杉醇+顺铂6个周期。药物剂量:表柔比星 100 mg/m2, 环磷酰胺500 mg/m2~600 mg/m2,紫杉类175 mg/m2, 顺铂2 mg/kg, 氟尿嘧啶500 mg/m2。③化疗前白细胞>3.5×109/L,天门冬酸氨基转移酶<100 U/L,丙氨酸氨基转移酶<100 U/L,肌酐清除率>65 mL/min。④化疗前24 h无恶心、呕吐,未使用其他止吐药物。⑤自愿使用电子止吐仪并签署知情同意书。
1.3 排除标准 ①有乳腺癌或其他肿瘤脑转移者;②有其他疾病,如部分或完全性肠梗阻、电解质紊乱、尿毒症、胃动力障碍、前庭功能障碍等易引起恶心、呕吐疾病;③有植入心脏起搏器、血糖仪、人工耳蜗等金属仪器;④对金属过敏;⑤有认知障碍或精神疾病者。
1.4 治疗方法 试验组:病人在输注化疗药物前30 min、结束后4 h使用昂丹司琼注射液(欧贝)8 mg加生理盐水100 mL静脉输注;第2天使用昂丹司琼注射液8 mg加生理盐水100 mL静脉输注。同时在化疗前30 min佩戴电子止吐仪(法罗适),直到第2天取下,共佩戴24 h。佩戴位置为非乳腺癌侧手腕,仪器的金属板应紧贴腕部(在桡侧腕屈肌和掌长肌之间距离远侧碗横纹2 cm~3 cm处的腕部正中位置),调节档位至病人舒适、耐受档。
对照组:病人在输注化疗药物前30 min、结束后4 h使用昂丹司琼注射液8 mg加生理盐水100 mL静脉输注;第2天使用昂丹司琼注射液8 mg加生理盐水100 mL静脉输注。
1.5 疗效标准 根据WHO抗癌药物毒副反应分级,将呕吐程度分为6个等级,将恶心分为4个等级[7],见表1。

表1 呕吐与恶心程度分级表
一次呕吐事件定义为持续时间大于1 min,两次呕吐之间至少缓解5 min[7]。呕吐有效控制率(RR)=(0级例数+Ⅰ级例数)/总例数×100%。呕吐完全控制率(CR)=0级例数/总例数×100%。恶心有效控制率(RR)=(0级例数+Ⅰ级例数)/总例数×100%。恶心完全控制率(CR)=0级例数/总例数×100%。因本调查未出现呕吐Ⅳ级、Ⅴ级情况,故在之后的统计表中不列出。
1.6 统计学方法 采用 SPSS 23.0统计软件对数据进行分析处理。 计数资料采用百分比描述,两组恶心、呕吐有效控制率的变化采用χ2检验,以P<0.05为差异有统计学意义。
2 结果
2.1 两组病人恶心、呕吐控制率比较 研究结果显示:试验组和对照组的呕吐有效控制率在化疗后第1天、第2天比较差异有统计学意义(P<0.05),试验组的呕吐有效控制率高于对照组,两组的呕吐有效控制率在化疗后第3天差异无统计学意义,见表2。试验组和对照组的恶心有效控制率在化疗后第1天、第2天比较差异有统计学意义(P<0.05),试验组恶心有效控制率高于对照组,两组的恶心有效控制率在化疗后第3天差异无统计学意义,见表3。
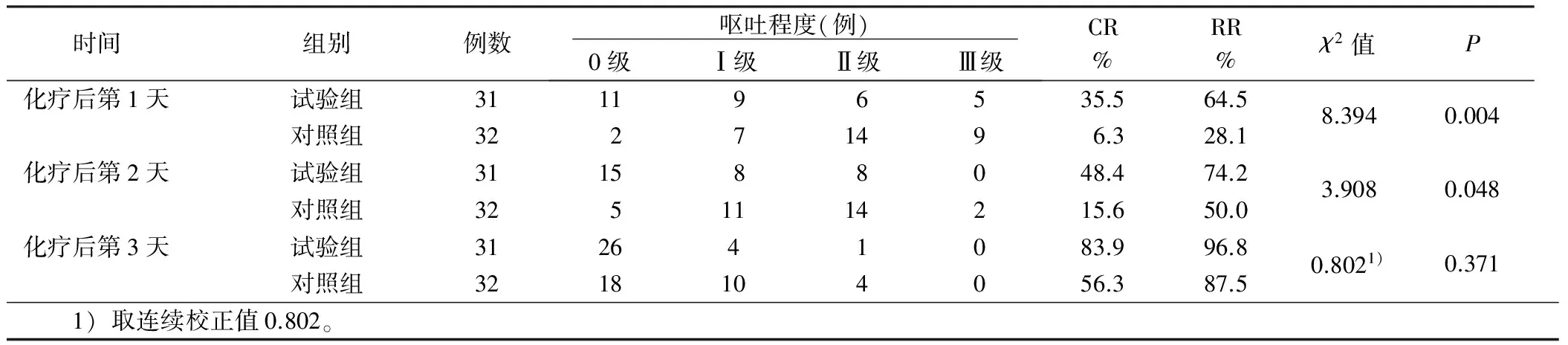
表2 两组病人呕吐控制率比较

表3 两组病人恶心控制率比较
2.2 不良反应 本研究中有部分病人出现头晕、头痛、乏力、便秘、指尖发麻等不良反应,反应较轻,且试验组和对照组差异无统计学意义,见表4。由此可以看出,电子止吐仪联合盐酸昂丹司琼对化疗后恶心、呕吐的控制安全,有一定效果。
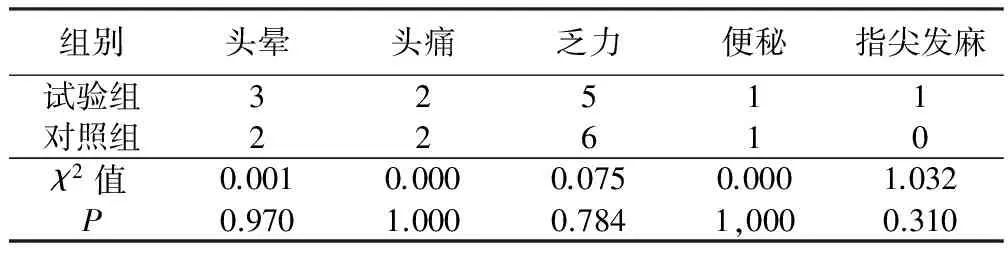
表4 两组病人的不良反应比较 例
3 讨论
CINV可分为急性、延迟性、预期性、突破性、难治性5类[8]。延迟性CINV是指发生在化疗24 h后发生的恶心、呕吐[8]。接受中、高致吐风险的化疗药物病人,延迟性CINV一般持续2 d~3 d[9],发生率分别为19%~33%和49%~75%[2]。近年来认为 5-HT是在急性CINV中发挥重要作用的递质,在迷走神经传入纤维、CTZ及孤束核中均有多种5-HT受体;而延迟性CINV则与P物质联系紧密[10]。另外,年轻(低于55岁)、女性、低乙醇摄入、不吸烟、体力状态较差、便秘、晕动病史及妊娠期呕吐者更易发生呕吐[11]。因此,乳腺癌病人更易发CINV,对于预防延迟性CINV的需求更为迫切。
昂丹司琼是一种外周神经元及中枢神经系统 5-HT3受体的高效、高选择性竞争拮抗剂,通过与内脏神经和迷走神经上的5-HT3受体结合,阻断胃肠道嗜铬细胞释放的5-HT与5-HT3受体结合,从而抑制迷走神经传入兴奋起到止吐作用[12]。昂丹司琼一般耐受良好,少数有头痛、头晕、便秘、乏力、腹泻等不良反应。电子止吐仪是一种新型体外经皮神经电刺激性医疗器械。它的外观类似于手表的电脉冲发生器,使用时佩戴在手腕部,仪器背部的两个金属板紧贴腕部桡侧腕屈肌和掌长肌之间距离远侧碗横纹2 cm~3 cm处的正中(内关穴)。仪器发出的低频脉冲通过腕部的正中神经到达大脑皮层的高级中枢,调节来自各种生物和物理通道的导致神经性呕吐的信号,同时也会调节胃部的迷走神经信号,阻止或者延缓大脑向胃部传输呕吐信号,减缓胃部异常蠕动的频率[6]。电子止吐仪能抑制5-HT过量释放和下调5-HT3受体表达,从而减轻CINV[13]。Taspinar等[14]发现应用按摩腕带对P6穴位(内关穴)的刺激减少了CINV。国内一些学者如周愚等[15-17]也指出经皮电刺激内关穴能够改善术后疼痛和恶心、呕吐。
本研究结果显示:对于乳腺癌病人化疗期间发生的延迟性恶心、呕吐,试验组对于恶心和呕吐的有效控制率均优于对照组。而试验组和对照组的不良反应均较轻微,说明电子止吐仪联合昂丹司琼预防CINV是安全的。这可能是电子止吐仪与昂丹司琼二者之间存在协同作用,增加了止吐、抗恶心的作用。还发现,CINV中恶心比呕吐更难以控制,这与Hesketh等[18]报道的结果类似。
综上所述,电子止吐仪联合昂丹司琼在预防乳腺癌延迟性化疗相关性恶心、呕吐方面疗效确切,减轻了乳腺癌病人化疗过程中的不适,保证了化疗的顺利进行,值得在临床推广。但目前对于乳腺癌病人延迟性CINV的控制仍不够理想,如何进一步减少延迟性CINV的发生率,需要广大医务人员的进一步研究与努力。
[1] Fan L,Strasser-Weippl K,Li JJ,etal.Breast cancer in China[J].Lancet Oncol,2014,15(7):e279-289.
[2] Wickham R.Evolving treatment paradigms for chemotherapy-induced nausea and vomiting[J].Cancer Control,2012,19(2 Suppl):3-9.
[3] Janelsins MC,Tejani MA,Kamen C,etal.Current pharmacotherapy for chemotherapy-induced nausea and vomiting in cancer patients[J].Expert Opin Pharmacothe,2013,14(6):757-766.
[4] Jordan K,Schaffrath J,Jahn F,etal.Neuropharmacology and management of chemotherapy-induced nausea and vomiting in patients with breast cancer[J].Breast Care(Basel),2014,9(4):246-253.
[5] Jorden K,Hinke A,Grothey A,etal.A meta-analysis comparing the efficacy of four 5-HT3 -receptor antagonists for acute chemotherapy-induced emesis[J].Support Care Cancer,2007,15(9):1023-1033.
[6] 刘君,肖扬, 郭建雄,等.电子止吐仪联合盐酸帕洛诺司琼预防高致吐化疗药物所致延迟性呕吐的研究[J].重庆医学,2015,44(8):1087-1090.
[7] US Department of Health and Human Services.Common terminology criteria for adverse events (CTCAE) version 4.0[S].National Cancer Institute:National Institutes of Health,2009:1.
[8] 陈歆妮,陈映霞,秦叔逵.化疗相关性恶心呕吐(CINV)的药物防治及指南指导下的临床实践[J].临床药物治疗杂志,2014,12(5):7-11.
[9] National Comprehensive Cancer Network.NCCN Clinical Practice Guidelines in Oncology:antiemesis,version1,2015[EB/OL].[2016-01-20].http://www.nccn.org//professionals/physician_gls/f_guidelines.asp#antiemesis.
[10] Bergstrom M,Hargreaves RJ,Burns HD,etal.Development of aprepitant,the first neurokinin-1 receptor antagonist for the prevention of chemotherapy-induced nausea and vomiting[J].Ann NY Acad Sci,2011,1222:40-48.
[11] Sekine I,Segawa Y,Kubota K,etal.Risk factors of chemotherapy-induced nausea and vomiting:index for personalized antiemetic prophylaxis[J].Cancer Sci,2013,104(6):711-717.
[12] 王楹,林英城.延迟性化疗相关性恶心呕吐的治疗进展[J].临床肿瘤学杂志,2014,19(10):945-949.
[13] 王德山,柴继严,谢鑫,等.电子止吐仪对顺铂诱发呕吐猫CTZ区5-HT含量及受体表达影响[C].2013年全国中医肿瘤学术年会.北京:中华中医药学会,2013:945-948.
[14] Taspinar A,Sirin A.Effect of acupressure on chemotherapy-induced nausea and vomiting in gynecologic cancer patients in Turkey[J].Eur J Oncol Nurs,2010,14(1):49-54.
[15] 周愚,王蔚,黄宏辉,等.自控经皮穴位电刺激对妇科腹腔镜术后恶心呕吐的影响[J].临床麻醉学杂志,2014,30(6):592-593.
[16] 高军龙,李玉兰.浅谈经皮穴位电刺激在围麻醉期的多种作用[J].中国针灸,2015,35(3):269-273.
[17] 吕改华,王海燕,韩冲芳,等.韩氏穴位神经刺激仪对妇科腹腔镜术后疼痛与恶心呕吐的影响[J].中国疼痛医学杂志,2012,18(9):537-540.
[18] Hesketh PJ,Grunberg SM,Gralla RJ,etal.The oral neurokinin-1 antagonist aprepitant for the prevention of chemotherapy-induced nausea and vomiting:a multinational,randomized,double-blind,placebo-controlled trial in patients receiving high- dose cisplatin--the Aprepitant Protocol 052 Study Group[J].J Clin Oncol,2003,21:4112-4119.
(本文编辑孙玉梅)
Effect observation on electronic antiemetic acupuncture combined with ondansetron in prevention of tardive chemotherapy- induced nausea and vomiting in breast cancer patients
Feng Xiaojuan,Hu Xiaoxia,Chen Hebo
(West China Hospital,Sichuan University,Sichuan 610041 China)
冯小娟,护师,本科,四川大学华西医院;胡小霞、陈合波单位:610041,四川大学华西医院。
信息 冯小娟,胡小霞,陈合波.电子止吐仪联合昂丹司琼预防乳腺癌延迟性化疗相关恶心、呕吐的效果观察[J].护理研究,2017,31(16):2039-2041.
R473.73
A
10.3969/j.issn.1009-6493.2017.16.037
1009-6493(2017)16-2039-03
2016-03-16;
2017-05-12)

