HPLC-CAD法同时测定葡萄糖氯化钠注射液中葡萄糖和氯及钠的含量
孙良广 郭振旺
广西壮族自治区梧州食品药品检验所,广西 梧州 543001
HPLC-CAD法同时测定葡萄糖氯化钠注射液中葡萄糖和氯及钠的含量
孙良广 郭振旺*
广西壮族自治区梧州食品药品检验所,广西 梧州 543001
目的:建立高效液相色谱-电喷雾检测器(HPLC-CAD)法同时测定葡萄糖氯化钠注射液中葡萄糖、氯和钠的含量。方法:采用Thermo U3000-Corona CAD测定,用超纯水溶解葡萄糖氯化钠注射液,过滤后注入液相色谱仪测定。色谱柱为Thermo Mixed-Mode Hilic-1柱(3μm 2.1×150mm);柱温:40℃;流动相:50mmol/L醋酸铵和乙腈梯度洗脱;流速:0.3mL/min;进样体积:10μL。结果:葡萄糖的线性范围为0.05~1.00mg/mL(r=0.9993),氯和钠的线性范围为0.09~1.80mg/mL(r=0.9999)。方法回收率均>99.8%,精密度RSD均<2.0%,超纯水中ClO-、NO3-对葡萄糖氯化钠的含量测定几乎没有干扰。结论:该方法准确,快速、简便,可用于葡萄糖氯化钠注射液中葡萄糖、氯和钠的测定及其质量控制,对其类似化合物的测定具有参考价值。
葡萄糖氯化钠注射液;高效液相色谱;电喷雾检测器
葡萄糖氯化钠注射液(Glucose and sodium chloride injection)是常用的补充热能和体液的复方制剂,内含葡萄糖与氯化钠,用于各种原因引起的进食不足或大量体液丢失[1]。2015年版《中国药典》二部中葡萄糖氯化钠注射液的含量测定方法繁琐耗时,分别用旋光度法测定葡萄糖含量,硝酸银滴定法测定氯化钠中氯含量。目前,葡萄糖的检测方法中高效液相色谱法准确、快速,得到广泛采用[2]。常采用示差折光率检测器(RID)[3-4]和蒸发光散射检测器(ELSD)检测器[5]。为了缩短测定时间且同时对葡萄糖和氯化钠含量进行分析,笔者采用HPLC-CAD法[6-7]同时测定葡萄糖氯化钠注射液中葡萄糖、氯离子和钠离子的含量[8-10]。该方法更加快速、简便、准确地对葡萄糖氯化钠注射液进行了定量分析。
1 仪器与材料
1.1 仪器 Thermo-U3000高效液相色谱仪(美国热电公司,附带Corona Ultra电喷雾检测器),色谱柱为Thermo Mixed-Mode Hilic(2.1×150mm 1.3μm)。
1.2 材料 醋酸铵(分析纯,上海阿拉丁生化科技股份有限公司);葡萄糖对照品(批号:E1407051, Aladdin,含量≥99.5%);氯化钠对照品(批号:GBW(E)060024,中国计量科学研究院,含量=99.99%);250mL葡萄糖氯化钠注射液(批号:E131102K2,湖南科伦制药有限公司;批号:131228804,安徽双鹤药业有限责任公司;批号:H13121609,广西裕源药业有限公司),乙腈(色谱纯,美国Sigma-aldrich公司),水为超纯水。
2 方法与结果
2.1 色谱条件 色谱柱:Thermo Mixed-Mode Hilic(2.1mm×150mm 1.3μm);流速:0.3mL/min,柱温40°C,进样量10μL,流动相为A(50mmol/L醋酸铵):B(乙腈)。详见表1。
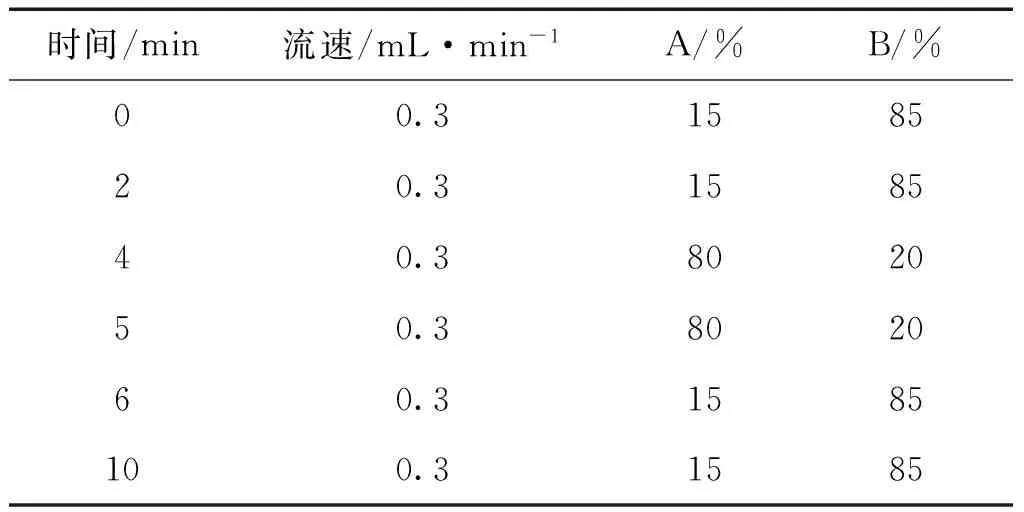
表1 梯度洗脱
2.2 供试品溶液的制备 取“1.2”项下葡萄糖氯化钠注射液,精密移取各1mL分别置于1000mL容量瓶中,加超纯水稀释并定容至刻度,摇匀,滤过,滤液过0.45μm滤膜,即得。
2.3 对照品溶液的制备 参照2015年版《中国药典》二部中葡萄糖氯化钠注射液规格(7)项下[1]配制,取葡萄糖12.5g和氯化钠2.25g,精密称定,置于250mL量瓶中,加水溶解并稀释至刻度,摇匀,即得。作为对照品贮备液。
2.4 标准曲线的制备 精密移取对照品贮备液1mL置于10mL量瓶中,加超纯水稀释并定容至刻度,摇匀,再精密移取各1mL分别置于100、50、25、10、5mL量瓶中,加超纯水稀释并定容至刻度,摇匀,即得。制成下表所示线性溶液(见表2)。葡萄糖、Cl-、Na+分离度良好,且不受溶剂超纯水中杂质ClO-等干扰,色谱图见图1。精密量取上述“2.2”和“2.3”项下供试品溶液和对照品溶液,分别精密吸取10μL,注入液相色谱仪,记录峰面积,以对照品浓度为横坐标,以峰面积为纵坐标,绘制标准曲线,进行线性回归。葡萄糖在0.5~1.0mg/mL范围内与峰面积线性关系良好,回归方程Y=125.8386X+ 1.2101(r= 0.9993);氯、钠在0.09~1.80mg /mL范围内与峰面积线性关系良好,回归方程分别为Y= 33.6836X+ 0.6429(r= 0.9999)、Y= 17.3087X+ 0.0395(r= 0.9999)。
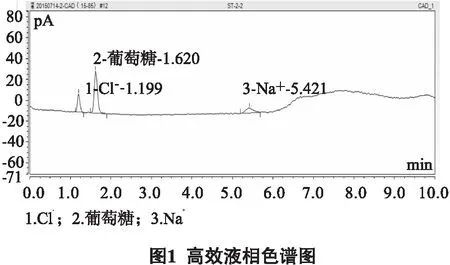

表2 标准工作曲线的样品浓度 (n=5)
2.5 精密度试验 精密精取同一对照品溶液,连续进样6次,记录峰面积,分别计算葡萄糖、Cl-和Na+的RSD,分别为0.25%、0.11%、0.14%。结果表明,仪器精密度良好。
2.5 重复性试验 取样品6份,按“2.2”供试品方法制备,测定峰面积。分别计算6份样品中葡萄糖、Cl-和Na+的平均含量,分别为12.51g/250mL、2.25g/250mL、2.25g/250mL,RSD分别为1.50%、0.95%和1.58%。结果表明,本方法重复性良好。
2.6 稳定性试验 取样品,在0、4、8、12、16、20、24h内进样,测定峰面积,分别计算样品中不同时间点的葡萄糖、Cl-和Na+含量,RSD为0.93%、0.85%、1.04%。结果表明,供试品溶液在24h内稳定。
2.7 回收率试验 取已知含量的样品6份,每份约1mL,精密称定。分别精密加入“2.3”项下对照品储备液1mL,按“2.2”供试品方法制备,测定,结果见表3。葡萄糖氯化钠注射液中葡萄糖、Cl-和Na+的平均回收率分别为100.4%、99.8%、100.1%,RSD分别为1.11%、1.02%、1.15%。见表3至表5。

表3 葡萄糖的加样回收实验 (n=6)

表4 葡萄糖的加样回收实验 (n=6)

表5 葡萄糖的加样回收实验 (n=6)
3 讨论
3.1 定量方法的选择 由于葡萄糖和氯化钠没有紫外吸收官能团,不能通过常规的高效液相色谱-紫外检测法(HPLC-UV)同时进行检测。本文建立了一种准确、快速、简便的高效液相色谱-电喷雾检测器法同时测定葡萄糖氯化钠注射液中葡萄糖、氯和钠的含量,可应用于其质量控制和稳定性研究,对其类似化合物的测定也具有参考价值,也可作为医院常用的葡萄糖氯化钠注射液含量检测的一种有效手段[12-13]。
3.2 色谱条件的选择 由于Thermo Mixed-Mode Hilic-1 3μm 2.1×150mm色谱柱具有混合模式固定相结合反相(RP)和亲水性交互(HILIC)两种属性。高效的硅胶基质的混合模式固定相由疏水性烷基链组成,末端是二醇基团。疏水性基团提供反相保留,末端的二醇基团则促进亲水相互作用。其独特组合提供可调节的选择性,卓越的分离度和峰的不对称性,适用于各种极性和非极性分子,使同时测定氯和钠两种阴阳离子成为可能。
3.3 CAD检测器的优势 电喷雾检测器(CAD)是近年发展起来的一种新型通用检测器,在灵敏度、重现性和线性方面均具有优异的性能,且操作简便。基于其独特的检测原理,它的检测范围不受制于化合物的分子结构,可应用于任何非挥发或半挥发化合物[11,12],在不具有示差折光检测器和离子色谱的情况下,能完成对葡萄糖和氯化钠2个阴阳离子的检测[13]。
3.4 实际应用性 2015年版《中国药典》二部采用的含量测定方法繁琐耗时,分别用旋光度法测定葡萄糖含量,硝酸银滴定法测定氯化钠中氯含量[1]。研究改用HPLC-CAD法进行测定,样品用超纯水直接溶解上机,大大节省了前处理时间,同时检测三个成分含量,保证了结果的准确性和耐用性。且葡萄糖、氯和钠的分离效果好,此方法抗干扰能力强,适宜推广应用。
[1]国家药典委员会.中华人民共和国药典(二部)[S].北京:中国医药科技出版社,2015:1271.
[2]董晓东,候宛玲,苏绍哲,等.高效色相色谱法测定葡萄糖和甘露醇[J].分析化学,2000,28(5):656.
[3]孙雪,黄元礼,柯林楠.高效液相色谱-示差折光检测法测定辅助生殖培养液中果糖和葡萄糖的含量[J].中国组织工程研究,2014,18(30):4873-4877.
[4]董玮,陈加罡,陆斌.HPLC-RID法测定转化糖电解质注射液中果糖和葡萄糖含量[J].中国药师,2014,17(11):1883-1885.
[5]张淋洁,王如伟,何厚洪,等.高效液相色谱-蒸发光散射法测定铁皮石斛中单糖和双糖[J].医药导报,2013,32(4):517-520.
[6]梁慧敏,欧妮.高效液相色谱-电喷雾检测器法测定贞芪扶正颗粒中黄芪甲苷含量[J].中国药业,2016,25(5):55-56.
[7]郭婷,董莉,魏秀丽,等.小叶黄杨中环维黄杨星D含量测定的两种高效液相色谱法评价[J].中国临床药理学杂志,2016,32(19):1797-1799.
[8]杨勇,吴琳琳,罗奕,等.HPLC-CAD法测定乳制品中果糖、葡萄糖、蔗糖、乳糖、半乳糖和麦芽糖含量的不确定度评定[J].中国食品添加剂,2015,9:172-180.
[9]游正琴,杨勇,许乾丽,等.HPLC-CAD法同时测定乳制品中糖类[J].中国乳品工业,2015,43(6):55-57.
[10]Almeling S, Ilko D, Holzgrabe U.Charged aerosol detection in pharmaceutical analysis[J].J Pharm Biomed Anal, 2012, 69:50-63.
[11]刘兴国,李丽红,李仁勇,等.新型电喷雾式检测器CAD与蒸发光散射检测器ELSD用于分析黄芪甲苷的对比研究[J].中国药事,2010,24(6):290-294.
[12]张凤妹,王建.HPLC-电喷雾检测器测定硫酸阿米卡星中卡纳霉素和硫酸盐的含量[J].中国抗生素杂志.2015,40(5):354-358.
[13]刘路,高旋,杨永健.HPLC-电雾式检测器的应用[J].中国医药工业杂志,2012,43(3):227-231.
Determination of Glucose,Cl-and Na+in Glucose and Sodium Chloride Injection by High Performance Liquid Chromatography with Charge Aerosol Detection(HPLC-CAD)
SUN Liangguang GUO Zhenwang*
Guangxi Wuzhou Institute for Food and Drug Control, Wuzhou 543001,China
Objective To establish a high performance liquid chromatographic with charge aerosol detection(HPLC-CAD) method for the determination of Glucose,Cl-and Na+in Glucose and sodium chloride injection.Methods An Thermo U-3000 HPLC system with a charged aerosol detector was used.The Glucose and sodium chloride injection samples were dissolved by water and injected into a Thermo Mixed-Mode Hilic-1(3μm 2.1×150mm)column at 40℃.The mobile phase was composed of 50 mmol·L-1ammonium acetate-acetonitrile with a flow rate of 0.3mL·min-1.The injection volumn was 10μL.Results The methodology recovery was higher than 99.8%.TheRSDwere less than 2.0%.The calibration curve was linear at 0.05~1.00mg·mL-1, with coefficient of determination over 0.9999.Glucose and sodium chloride injection was detected with little interference from the excipient blend of water.Conclusion The method is accurate,rapid and convenient for releage and stability test of Glucose,Cl-and Na+in Glucose and sodium chloride injection and may be used as reference for similar compounds.
Glucose and Sodium Chloride Injection; HPLC;CAD
孙良广(1985-),男,汉族,主管中药师,研究方向为食品药品检验。E-mail:sunliangguang@163.com
郭振旺(1984-),男,汉族,硕士,药师,研究方向为食品药品检验。E-mail:gzhw2005214@163.com
R917
A
1007-8517(2017)10-0018-03
2017-03-21 编辑:陶希睿)

