中频交变电流联合紫杉醇抗乳腺癌MCF-7细胞作用的研究
谢 青,王晓文,汪 悦,张北山,张丽岩,路晓光,毛 昀,唐劲天,李利亚⋆
(1.北京中医药大学,北京 100029;2.中日友好医院 中西医结合肿瘤科,北京 100029;3.清华大学工程物理系 医学物理与工程研究所医疗新技术实验室,北京 100084)
中频交变电流联合紫杉醇抗乳腺癌MCF-7细胞作用的研究
谢 青1,2,王晓文3,汪 悦3,张北山3,张丽岩3,路晓光2,毛 昀2,唐劲天3,李利亚2⋆
(1.北京中医药大学,北京 100029;2.中日友好医院 中西医结合肿瘤科,北京 100029;3.清华大学工程物理系 医学物理与工程研究所医疗新技术实验室,北京 100084)
目的:研究中频交变电流联合紫杉醇抗人乳腺癌MCF-7细胞的作用。方法:将对数生长期的乳腺癌细胞分别暴露于电刺激、紫杉醇、电刺激与紫杉醇联合作用下,采用cck8法检测细胞存活率,并运用流式细胞技术分析各组实验作用下对细胞凋亡/死亡、细胞周期的影响。结果:中频交变电流(100kHz,110mA,30min)作用MCF-7细胞后,细胞存活率为70±5.24%,联合紫杉醇(IC50)治疗后,细胞存活率为24±1.81%(P<0.01);中频交变电流联合紫杉醇能够增加细胞凋亡率,阻滞细胞于S期、G2/M期。结论:中频交变电流单独使用可以抑制MCF-7细胞增殖,联合紫杉醇应用时能表现出协同抑制肿瘤细胞生长的作用。
中频交变电流;紫杉醇;人乳腺癌MCF-7细胞;细胞周期;凋亡
Author’s addressBeijing University of Chinese Medicine,Beijing 100029,China
中频交变电场(100~300kHz,1~2V/cm),亦称肿瘤治疗电场(tumor treating fields,TTFields),在抗肿瘤作用领域具有独特的生物学机制和效应,如引起Septin 2、6、7蛋白定位障碍[1],干扰α/β微管聚合,影响纺锤体的形成,使肿瘤细胞有丝分裂中期异常中断[2,3],减少 CD34(+)细胞,抗血管生成[4,5]和p53依赖,引起肿瘤细胞免疫原性死亡,且副反应较低,已被FDA批准正式应用于临床治疗复发脑胶质母细胞瘤[6,7]。而交变电流不仅具有抗肿瘤作用[8],还可以减少耐药蛋白在肿瘤细胞中的表达,增加肿瘤细胞对化疗药物的摄取,协同化疗药物抑制肿瘤细胞增殖[9]。电流和电场具有的生物学效应,在医学上的运用越来越广[10]。目前已针对不同类型肿瘤,如脑胶质母细胞瘤[11]、非小细胞肺癌[12]、胰腺癌[13]、前列腺癌[14]等开展了一系列基础实验及临床研究,并取得一定的抗肿瘤效果。
本实验室自2008年开始,首次将中频电场和电流结合,即中频交变电流(alternating current at intermediate frequency,ACIF)。已证实中频交变电流对人肝癌HepG2细胞、BEL-7402细胞、人神经胶质瘤细胞U251、乳腺癌MCF-7细胞等具有不同程度的抑制作用[15]。化疗药物紫杉醇能够抑制细胞微管解聚,促进微管聚合并稳定微管,阻滞细胞于G2/M期,达到抗肿瘤目的。然而,近年来肿瘤细胞对紫杉醇耐药性逐渐增加,迫切需要找到新的方法与紫杉醇联合使用,增加抗肿瘤疗效。因此,本实验将进一步研究ACIF联合紫杉醇抗人乳腺癌MCF-7细胞作用效果。
1 材料
1.1 细胞株
人乳腺癌MCF-7细胞株,由北京协和细胞库提供。
1.2 仪器设备
中频交变电流治疗仪,清华大学医疗新技术实验室研发;电极:铂金材质。多功能读数仪-酶标仪,美国Thermo Scientific公司;BD FACSCalibur型流式细胞分析仪,美国BD公司。
1.3 药品与试剂
紫杉醇(紫素),批号:国药准字H10980069,购自北京协和药厂;cck8试剂盒,日本同仁化学研究所;RPMI-1640培养基,美国Gibco公司;胎牛血清(FBS),美国Hyclone公司;细胞DNA含量(细胞周期)即时检测试剂盒,南京凯基生物科技发展有限公司;Annexin V-FITC/PI双染细胞凋亡检测试剂盒,南京凯基生物科技发展有限公司。
2 方法
2.1 细胞培养
将人乳腺癌MCF-7细胞以1×104/ml浓度接种于25cm2培养瓶中,加入含10%胎牛血清的RPMI 1640培养基,放置于37℃、5%CO2的培养箱中培养。进行细胞实验时,将处于对数生长期的细胞用PBS洗3次,胰酶消化后,加入含10%胎牛血清的RPMI 1640培养基终止消化,吹打混匀(避免气泡产生),吸入到离心管中离心,倒掉上清液,加入适量的培养基,调整所需细胞浓度至1.5×104/ml。
2.2 不同中频交变电流对MCF-7细胞增殖的研究
设置对照组:正常培养细胞;电刺激组:选取中频交变电流参数100kHz、30min,分别予50mA、70mA、90mA、110mA、130mA、150mA的电流刺激细胞,每个电刺激组设置4个复孔。取对数生长期的MCF-7细胞,调整细胞浓度至1×104/ml,每孔2ml,接种于24孔板中,37℃、5%CO2的培养箱中培养24h后,分别予中频交变电流刺激MCF-7细胞,每隔24h刺激1次,共3次。刺激结束后,弃去培养基,每孔避光加入 0.5ml的cck8工作液,37℃、5%CO2的培养箱中避光孵育2h,用酶标仪检测450nm波长处各孔的OD值。细胞存活率(%)=实验组OD/对照组OD×100%。
2.3 不同紫杉醇药物浓度抑制MCF-7细胞的生长情况
设置对照组:正常培养细胞;紫杉醇组:调整紫杉醇的药物培养基浓度分别为:0.01、0.1、1、10、100、1000nmol/L,每一物质的量浓度设置4个复孔。取对数生长期的MCF-7细胞,调整细胞浓度至1×104/ml,每孔2ml,接种于24孔板中,37℃、5%CO2的培养箱中避光培养24h后,换上含有上述紫杉醇的药物培养基避光培养。培养72h后,测定各组的OD值(方法同“2.2”项)。
2.4 中频交变电流联合紫杉醇对MCF-7细胞增殖的影响
设置对照组:正常培养细胞;电刺激组:刺激参数为100kHz,110mA,30min;紫杉醇组:物质的量浓度为31nmol/L(IC50);联合组:电刺激+紫杉醇组。取对数生长期的MCF-7细胞,调整细胞浓度至1×104/ml,每孔2ml,接种于24孔板中,每组4个复孔,37℃、5%CO2的培养箱中避光培养24h后,紫杉醇组与联合组分别换上31nmol/L的紫杉醇药物培养基。每隔24h分别予中频交变电流作用于电刺激组与联合组1次,共3次。刺激结束后,测定各组的OD值(方法同“2.2”项)。
2.5 中频交变电流联合紫杉醇抑制MCF-7细胞后的恢复时间研究
分组方法同“2.4”项。各实验组细胞分别在24h内暴露于电刺激、紫杉醇药物及联合作用,再换上正常培养基。分别于24、48、72h检测各组的OD值(方法同“2.2”项)。
2.6 流式细胞术检测MCF-7细胞凋亡/死亡及细胞周期
分组方法同“2.4”项。取对数生长期的MCF-7细胞,调整细胞浓度至1.5×104/ml,每孔2ml,接种于24孔板中,每组8个复孔,37℃、5%CO2的培养箱中避光培养24h后,紫杉醇组与联合组分别换上31nmol/L的紫杉醇药物培养基。每隔24h分别予中频交变电流作用于电刺激组与联合组1次,独立实验共3次。

表1 不同ACIF刺激后肿瘤细胞的存活率(%)

表2 不同浓度紫杉醇对MCF-7细胞增殖的影响
2.6.1 细胞凋亡/死亡
各组细胞用不含EDTA的胰酶消化搜集到离心管,于2000r/min离心10min,弃去上清液,用PBS洗涤2次,加入500滋l的Binding Buffer悬浮细胞,予5滋l Annexin V-FITC混匀后,再加入5ul Propidium Iodide混匀,室温避光反应10 min,流式细胞仪检测。
2.6.2 细胞周期
各组细胞用胰酶消化搜集到离心管,于2000r/min离心10min,弃去上清液,用PBS洗涤细胞1次,于2000r/min离心5min,搜集并调整细胞浓度为1×106/ml,取1ml单细胞悬液离心,弃去上清液,在细胞中加入体积分数为70%的冷乙醇500ul固定2h,4℃保存。2000r/min离心10min,弃去上清液,加入100滋l RNase A 37℃水浴30min,再加入400滋l PI染色混匀,4℃避光30min,流式细胞仪检测。
2.7 统计学方法
应用SPSS20.0统计软件,数据间比较采用t检验。
3 结果
3.1 不同中频交变电流对MCF-7细胞增殖的影响
随着电流增加,乳腺癌MCF-7细胞的存活率越来越低,表明中频交变电流对MCF-7人乳腺癌细胞具有较好的抑制作用(见表1)。
3.2 不同紫杉醇药物浓度抑制MCF-7细胞的生长情况
随着紫杉醇药物浓度的增加,其对MCF-7人乳腺癌细胞的抑制率越来越强,紫杉醇对MCF-7细胞的IC50为31nmol/L(见表2)。
3.3 中频交变电流联合紫杉醇对MCF-7细胞增殖的影响
中频交变电流联合紫杉醇(IC50)作用于MCF-7细胞,细胞存活率为24±1.81%,相对于紫杉醇组:52±3.97%,MCF-7人乳腺癌细胞存活率明显降低(P<0.01)。由此可知,中频交变电流(ACIF)联合紫杉醇对MCF-7人乳腺癌细胞具有协同杀伤作用。
3.4 对MCF-7细胞治疗24h后恢复时间过程的影响
各实验组在24h内治疗后,均可见对MCF-7细胞有不同程度的抑制作用。其中与对照组相比,电刺激组及紫杉醇组的人乳腺癌MCF-7细胞减少近30%,联合组的人乳腺癌MCF-7细胞减少近50%,达到半数抑制量。在接下来的48h期间,电刺激组相对于药物组,细胞恢复较快;联合组、药物组恢复较慢;其中,联合组细胞存活率最低,仅33%(见图1)。
3.5 对MCF-7细胞凋亡/死亡的影响
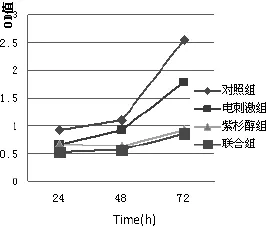
图1 各组作用24h内的恢复时间
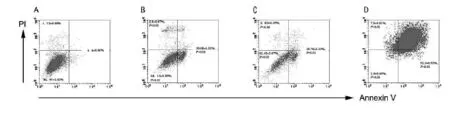
图2 中频交变电流联合紫杉醇对MCF-7细胞凋亡/死亡的影响(A:对照组;B:电刺激组;C:紫杉醇组;D:联合组)
流式细胞仪分析结果显示,单独电刺激组及紫杉醇组能够促进MCF-7细胞凋亡,在中频交变电流联合紫杉醇作用后,人乳腺癌MCF-7细胞凋亡率明显增加,与其它3组相比有显著性差异,说明中频交变电流联合紫杉醇能诱导MCF-7细胞凋亡(见图2)。
3.6 对MCF-7细胞周期的影响
流式细胞仪分析结果显示,治疗3d后,各实验组G0/G1期细胞明显减少,S期细胞明显增多,其中,联合治疗组G2/M期细胞明显增多,说明中频交变电流联合紫杉醇能改变MCF-7细胞周期,将MCF-7人乳腺癌细胞阻滞于S期、G2/M期(见图3,封二)。
4 讨论
中频交变电流(ACIF)结合了电流和电场的特性,是本实验室首创。研究表明[8,10],中频交变电流可以影响人乳腺癌MCF-7细胞周期,使细胞分裂滞后,诱导细胞凋亡,且对正常细胞没有明显的影响。另外,微管在细胞有丝分裂进程中有着重要的作用,中频交变电场能够干扰肿瘤细胞微管,影响纺锤体形成,抑制细胞有丝分裂[16]。大多数以微管为作用靶点的药物,如紫杉醇类、长春碱类、秋水仙碱、自念珠藻环肽,能阻止细胞分裂于G2/M期,Artelastin、龙葵素等干扰细胞于 S期[17,18],诱导细胞凋亡。而紫杉醇是临床指南推荐使用的治疗复发乳腺癌的常用化疗药物,还没有进行中频交变电流与紫杉醇联合作用于乳腺癌MCF-7细胞的研究。因此,本实验为首次探究中频交变电流联合紫杉醇抗人乳腺癌MCF-7细胞的作用效果。
本实验通过cck8法测得中频交变电流联合紫杉醇 (IC50)对MCF-7细胞的存活率为24± 1.81%,表明中频交变电流能协同紫杉醇增加细胞毒作用;流式细胞仪检测显示,经中频交变电流联合紫杉醇治疗3d后,G0/G1期细胞百分比明显减少,仅占18.53±3.25%,而S期细胞及G2/M期细胞百分比(分别为50.94±3.11%、30.53±2.09%,P<0.01)明显增多,因此推断中频交变电流联合紫杉醇能将MCF-7细胞阻滞在S期、G2/M期。细胞周期的紊乱是肿瘤发生发展的重要特征[19]。研究发现[20,22],在乳腺癌发生发展过程中,细胞周期蛋白(cyclin)D1可以缩短G1期,使细胞进入S期,过度表达可致乳腺导管增生和导管癌;cyclin E过度表达可以缩短G1期,形成不稳定的染色体,诱导肿瘤细胞生成、恶化。细胞周期蛋白依赖性激酶 (cyclin-dependent kinase,CDK)抑制剂p21、p27能够与cyclin-CDK结合,抑制其催化活性,使细胞周期停滞[23]。我们猜测,中频交变电流联合紫杉醇能将MCF-7细胞阻滞于S、G2/M期,可能与cyclin D1、E及CDK抑制剂p21、p27有一定的关系。在流式细胞仪检测细胞凋亡/死亡中,联合组正常细胞百分比仅占1.3±0.45%,而凋亡细胞百分比高达91.3±0.93%,可以看出,中频交变电流能够协同紫杉醇促进MCF-7细胞凋亡。我们猜测,中频交变电流能够协同紫杉醇促进细胞微管聚合,防止其解聚,阻滞细胞于S期、G2/M期,使肿瘤细胞有丝分裂中断,共同发挥着诱导人乳腺癌MCF-7细胞凋亡的作用。
中频交变电流(ACIF)无创或微创的疗法,可显著抑制人乳腺癌MCF-7细胞的增殖,并提高化疗效果,为乳腺癌的治疗和乳腺癌化疗的增敏提供了新的思路。
[1] Gilden JK,Peck S,Chen YC,et al.The septin cytoskeleton facilitates membrane retraction during motility and blebbing[J].J Cell Biol,2012,196(1):103-114.
[2] Giladi M,Schneiderman RS,Voloshin T,et al.Mitotic spindle disruption by alternating electric fields leads to improper chromosome segregation and mitotic catastrophe in cancer cells[J].Sci Rep,2015,5:18046.
[3] Lok E,Swanson KD,Wong ET.Tumor treating fields therapy device for glioblastoma:physics and clinical practice considerations[J].Expert Rev Med Devices,2015,12(6):717-726.
[4] Orecchioni S,Gregato G,Martin-Padura I,et al.Complementary populations of human adipose CD34+progenitor cells promote growth,angiogenesis,and metastasis of breast cancer [J].Cancer Res,2013,73(19):5880-5891.
[5] Maschio LB,Madallozo BB,Capellasso BA,et al.Immunohistochemical investigation of the angiogenic proteinsVEGF,HIF-1α and CD34 in inva sive ductal carcinoma of the breast[J].Acta Histochem,2014,116(1):148-157.
[6] Swanson KD,Lok E,Wong ET.An overview of alternating electric felds therapy(NovoTTF Therapy)for the treatment of malignant glioma[J].Curr Neurol Neurosci Rep,2016,16(1):8.
[7] Rehman AA,Elmore KB,Mattei TA.The effects of alternating electric fields in glioblastoma:current evidence on therapeutic mechanisms and clinical outcomes[J].Neurosurg Focus,2015,38(3):E14.
[8] JQ Tong,RT Liu,LY Zhao,et al.Inhibiting human breast cancer cells(MCF-7)with alternating micro-current at intermediate frequency (ACIF)in Vitro and in Vivo[C].World Congress on Medical Physics and Biomedical Engineering. Beijing,China:Springer Berlin Heidelberg,2013.1596-1599.
[9] Janigro D,Perju C,Fazio V,et al.Alternating current electrical stimulation enhanced chemotherapy:a novel strategy to bypass multidrug resistance in tumor cells[J].BMC Cancer,2006,6:72.
[10] 谢青,李利亚.交变微电流与电场抗肿瘤作用研究进展[J].中日友好医院学报,2016,30(1):44-46.
[11] Stupp R,Taillibert S,Kanner AA,et al.Maintenance therapy with tumor-treating fields plus temozolomide vs temozolomide alone for gli oblastoma:A randomized clinical trial[J]. JAMA,2015,314(23):2535-2543.
[12] Weinberg U,FarberO,GiladiM,etal.194TiP:LUNAR: Phase III study of front-line chemotherapy with TTFields for advanced squamous NSCLC[J].J Thorac Oncol,2016,11(4 Suppl):S141.
[13] Giladi M,Schneiderman RS,Porat Y,et al.Mitotic disruption and reduced clonogenicity of pancreatic cancer cells in vitro and in vivo by tumor treatingfields[J].Pancreatology,2014,14(1):54-63.
[14] KoreckijTD,HillC,AzureL,etal.Low dose,alternating electric currentinhibits growth ofprostate cancer[J]. Prostate,2010,70(5):529-539.
[15] 马俊,王然,唐劲天.中频交变电流抑制肿瘤细胞的体外增殖[J].现代生物医学进展,2014,14(11):2032-2036.
[16] Kirson ED,Gurvich Z,Schneiderman R,et al.Disruption of cancer cell replication by alternating electric fields[J].Cancer Res,2004,64(9):3288-3295.
[17] Pedro M,Ferreira MM,Cidade H,et al.Artelastin is a cytotoxic prenylated flavones that disturbs microtubules and interferes with DNA replication in MCF-7 human breast cancer cells[J].Life Sci,2005,77(3):293-311.
[18] 钟伟枫,刘思平,潘斌,等.龙葵素通过诱导细胞周期G1/S阻滞抑制裸鼠前列腺癌细胞Du145移植瘤生长[J].南方医科大学学报,2016,36(5):665-670.
[19] MassaguéJ.G1cell-cycle controland cancer[J].Nature,2004,432(7015):298-306.
[20] Zhang H,Zhu L,Zuo W,et al.The ClC-3 chloride channel protein is a downstream target of cyclin D1 in nasopharyngealcarcinoma cells [J].IntJ Biochem CellBiol,2013,45(3):672-683.
[21] Roy PG,Thompson AM.Cyclin D1 and breast cancer[J]. Breast,2006,15(6):718-727.
[22] Huth HW,Albarnaz JD,Torres AA,et al.MEK2 controls the activation ofMKK3/MKK6-p38 axisinvolved in the MDA-MB-231 breast cancer cell survival:Correlation with cyclin D1 expression[J].Cell Signal,2016,28 (9):1283-1291.
[23] Ye D,Luo H,Lai Z,et al.ClC-3 chloride channel proteins regulate cell cycle by up-regulating cyclin D1-CDK4/6 through suppressing p21/p27 expression in nasopharyngeal carcinoma cells[J].Sci Rep,2016,6:30276.
Inhibiting human breast cancer MCF-7 cells proliferation with alternating current at intermediate frequency combined with paclitaxel in vitro/
/
XIE Qing,WANG Xiao-wen,WANG Yue,et al//Journal of China-Japan Friendship Hospital,2017 Feb,31(1):26-30
Objective:To investigate the effect of alternating current at intermediate frequency(ACIF)in combination with Paclitaxel on cell proliferation of MCF-7 cells in vitro.Methods:Cell proliferation in culture was studied in human breast MCF-7 cell lines exposed to ACIF,Paclitaxel separately and in combinations.The growth rate of MCF-7 cells was evaluated by cck8 assay;cell apoptosis/death and cycle of MCF-7 cells were analyzed by a flow cytometry.Results:The survival rate of MCF-7 cells exposed to ACIF(100kHz,110mA,30 min)was 70±5.24%,but significantly decreased to 24±1.81%in combination with Paclitaxel(P<0.01).Moreover,ACIF in combination with Paclitaxel could promote MCF-7 cells apoptosis and induce cell growth arrest in S phase and G2/M phase.Conclusion:ACIF alone could inhibit MCF-7 cells proliferation and enhance the inhibitory effect ofpaclitaxel.
alternating current at intermediate frequency;Paclitaxel;human breast MCF-7 cells;cell cycle;apoptosis
R730.59;R454.1
A
1001-0025(2017)01-0026-05
10.3969/j.issn.1001-0025.2017.01.007
国家自然科学基金(81372412)。
2* 本文通讯作者。
谢 青(1991-),男,硕士研究生。
2016-08-17
2016-12-08

