四肢骨折内固定术后感染病原菌特点和耐药性分析
白博++郑恬++吴子祥+郇科++苏菲++梁娟++桑宏勋
[摘要] 目的 研究四肢骨折内固定手术患者术后感染的病原菌特点和耐药情况。 方法 收集2013年1月~2016年1月第四军医大学西京医院骨科收治的四肢骨折行内固定术的患者资料,发生术后感染共39例患者,取组织标本进行细菌培养和药敏试验。 结果 39例术后感染患者细菌培养阳性率为87.18%(34/39),细菌培养结果阳性的34例患者共分离出38株细菌,4例(10.53%)分离出2种细菌。导致骨折内固定术后感染的病原菌主要为革兰阳性菌(57.89%,22/38),其中,金黄色葡萄球菌(47.36%,18/38)所占比例最高;革兰阴性菌占39.47%,真菌占2.63%。52.63%(20/38)术后感染患者病原菌为多重耐药菌(MDR),70.00%(14/20)的MDR是耐甲氧西林金黄色葡萄球菌,其对青霉素、左氧氟沙星、克林霉素和红霉素等呈较高的耐药性,对万古霉素和利奈唑胺均敏感。 结论 骨折内固定术后感染的主要病原菌为金黄色葡萄球菌,且MDR占很高比例。应尽早进行细菌培养和药敏试验明确病原菌,根据药敏试验结果及时调整抗生素使用方案,对降低院内感染发病率、控制抗生素滥用、有效控制感染和提高治愈率有重要意义。
[关键词] 骨折;内固定术;术后感染;病原菌;多重耐药菌
[中图分类号] R969.3 [文献标识码] A [文章編号] 1673-7210(2017)04(b)-0004-04
[Abstract] Objective To study the pathogenic characteristics and drug resistance for surgical site infection after limb fracture internal fixation surgery. Methods Data of patients with limb fracture underwent internal fixation in Department of Orthopedics, Xijing Hospital, the Fourth Military Medical University, from January 2013 to January 2016 were selected. 39 cases had suffered from postoperative infection. Bacterial cultures and drug sensitive tests were conducted.
Results The positive culture rate of 39 patients with infection after surgery was 87.18% (34/39). Altogether 38 pathogenic strains were cultured from the 34 infected wound, and 2 kinds of bacteria were cultured from 4 patients (10.53%). The pathogenic bacteria causing infection after internal fixation surgery were mainly gram-positive bacteria,which accounted for 57.89% (22/38) of the total strains. Staphylococcus aureus (47.36%, 18/38) was the main pathogenic bacteria. Gram-negative bacteria (39.47%) and fungi (2.63%) were followed. 52.63% (20/38) patients with infection after surgery was multi-drug resistant. The main multi-drug resistant bacteria which caused postoperative infection was methicillin-resistant Staphylococcus aureus, accounting for 70.00% (14/20). The drug resistance of methicillin-resistant Staphylococcus aureus was relatively high to Penicillin, Levofloxacin, Clindamycin and Erythromycin, but sensitive to Vancomycin and Linezolid. Conclusion Staphylococcus aureus is the main pathogen causing postoperation infection of the limb fracture internal fixation surgery. The multi-drug resistant organism account for a high proportion. Clarify the pathogens by the bacteria culture and drug sensitive test in the early stage is essential. Adjust the antibiotics according the result of the drug sensitive test can reduce the nosocomial infection control, effectively control the abuse of infection and improve the cure rate.
[Key words] Fracture; Internal fixation surgery; Postoperative infection; Pathogen; Multi-drug resistant bacteria
感染是骨折内固定术后“灾难性”的并发症,术后一旦发生手术部位感染(surgical site infection,SSI),尤其内固定材料导致的感染或骨髓炎,治疗十分棘手,常需行翻修手术,取出内固定,严重时需行截肢术甚至危及生命,严重影响骨折愈合和康复效果,给患者带来巨大的身心痛苦和沉重的经济负担[1-3]。本研究通过回顾性分析2013年1月~2016年1月第四军医大学西京医院(以下简称“我院”)骨科收治的四肢骨折接受内固定手术治疗术后发生感染的患者资料,对感染的病原菌特点和耐药性进行调查研究。
1 资料与方法
1.1 一般资料
选取我院39例四肢骨折接受内固定手术治疗术后发生感染的患者,其中,男28例,女11例;初次手术年龄为21~73岁,平均44.2岁;受伤原因:车祸伤26例,摔伤4例,重物砸伤4例,高处跌落伤3例,机器绞伤2例;受伤至手术平均时间为37.2 h;术后出现感染时间为5~91 d,平均21.6 d;受伤部位:胫腓骨骨折24例,股骨骨折11例,跟骨骨折1例,桡骨骨折2例,尺骨骨折1例。
1.2 纳入与排除标准
纳入标准:①开放或闭合性四肢骨折在我院行切开复位内固定手术治疗,资料完整并经实验室、影像学检查明确诊断为术后感染患者;②符合原卫生部制订的《外科手术部位感染预防与控制技术指南(2010年)》标准[4]。排除标准:①未行内固定术,如行骨牵引、骨折清创术、截肢患者;②术前已经发生骨折部位感染者;③资料不完整患者。
1.3 标本采集、细菌培养及药敏试验
严格按照无菌操作原则取感染伤口周围分泌物,将标本送至我院检验科,严格按照《全国临床检验操作规程》进行细菌分离和培养,进行菌种鉴定,以K-B纸片扩散法和琼脂平板稀释法进行抗生素药敏试验。以美国临床实验室标准委员会规定的标准(clinical and laboratory standards institute,CLSI)為依据进行结果判定,病原菌鉴定应用半自动或全自动病原菌鉴定仪。
2 结果
2.1 病原菌分布情况
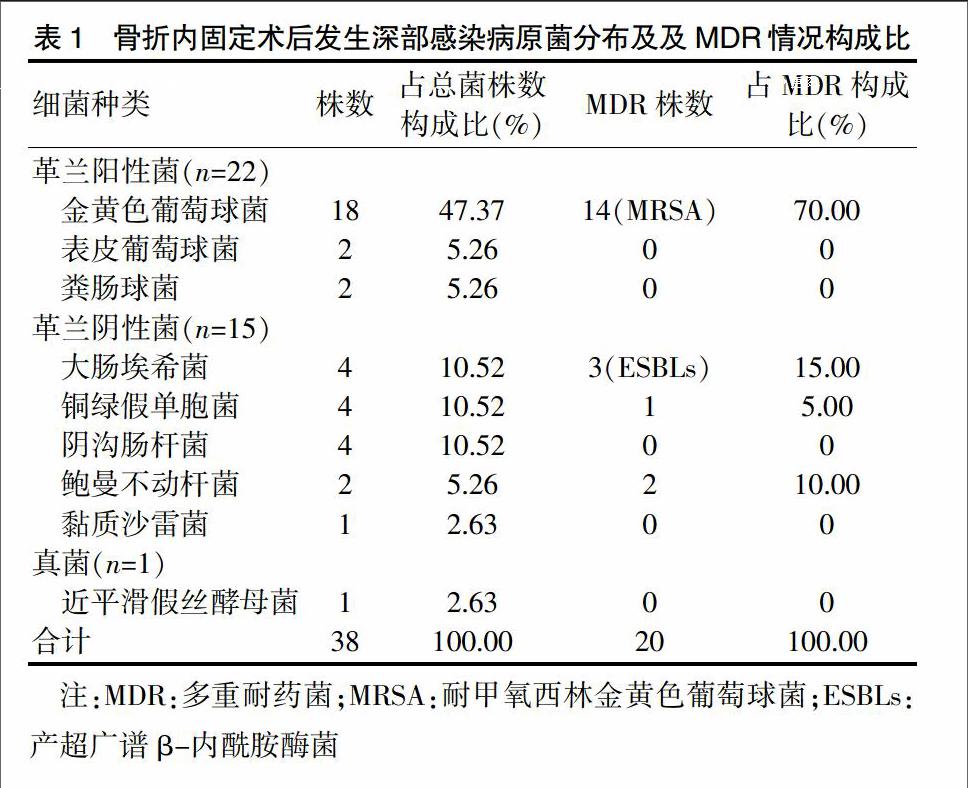
将标本送至我院检验科进行细菌培养加药敏试验进行分析,结果显示:4125例接受骨折内固定术患者中39例发生术后感染,术后感染的总体发生率约为0.95%。39例患者标本细菌培养阳性率为87.18%,其中5例未培养出病原菌。细菌培养阳性的34份标本中共分离出38株细菌,其中4份(10.53%)分离出两种细菌。分离出的病原菌中,革兰阳性菌占57.89%,革兰阴性菌占39.47%,真菌占2.63%。革兰阳性菌中,金黄色葡萄球菌比例最高。革兰阴性菌中,大肠埃希菌、铜绿假单胞菌和阴沟肠杆菌均有4株,鲍曼不动杆菌2株,黏质沙雷菌1株。真菌仅1株,为近平滑假丝酵母菌。38株细菌中,多重耐药菌(multi-drug resistant bacteria,MDR)为20株,其中,耐甲氧西林金黄色葡萄球菌(methicillin-resistant Staphylococcus aureus,MRSA)占金黄色葡萄球菌的比例达77.78%,余为产超广谱β-内酰胺酶(extender spectrum Beta-lactamases,ESBLs)菌、鲍曼不动杆菌和铜绿假单胞菌。见表1。
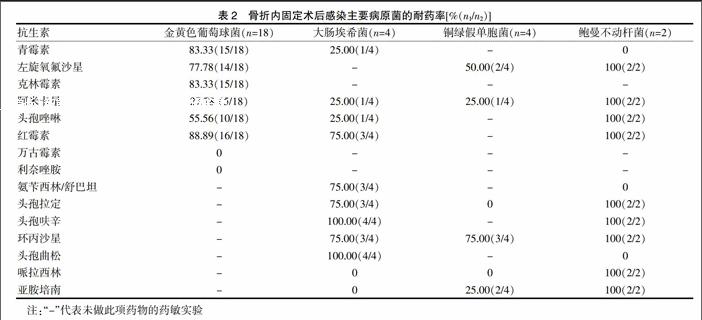
2.2 主要病原菌耐药性分析
革兰阳性菌中,金黄色葡萄球菌对临床常用的青霉素、左氧氟沙星、克林霉素和红霉素等抗菌药物呈现出较高的耐药性;MRSA对万古霉素和利奈唑胺的耐药性为0。革兰阴性菌中,大肠埃希菌对红霉素、氨苄西林/舒巴坦、头孢拉定和头孢呋辛、环丙沙星和头孢曲松表现出较高的耐药性;铜绿假单胞菌对环丙沙星和左旋氧氟沙星耐药率较高;鲍曼不动杆菌对左旋氧氟沙星、克林霉素、头孢唑啉,甚至亚胺培南均呈100%耐药。见表2。
3 讨论
骨折内固定术后感染是临床中常见和棘手的并发症,由于诊治的复杂性,其成为骨科医生持续关注的热点。骨折内固定术后感染受到患者自身免疫状态、围术期、手术和术后等多种相关因素的综合影响[4],其总体发生率为0.4%~16.1%[6],开放性骨折则高达1%~55%[7-8]。随着抗生素滥用现象越来越严峻,多重耐药菌感染的比例逐年增加,使抗生素的治疗效果大打折扣,一旦发生术后感染,治疗难度和成本大幅增加[9]。同时,有学者认为内固定材料表面形成黏附力极强的细菌生物膜,使细菌难以清除,大大增强对抗生素的抵抗力,感染更难控制[10-11]。
本研究通过对我院骨科行内固定术的住院患者伤口分泌物进行培养和药敏试验,统计分析了术后感染病原菌的分布和耐药性,目的是为早期抗生素的经验用药提供科学依据,降低院内感染发病率,减少抗生素滥用,有效控制感染和提高术后感染的治愈率。本研究共回顾分析我院4125例接受骨折内固定术患者资料,其术后感染的总体发生率约为0.95%。根据统计结果,革兰阳性菌22株,占57.89%,革兰阴性菌15株,占39.47%,真菌1株,占2.63%;位居前4位的病原菌分别为金黄色葡萄球菌、大肠埃希菌、铜绿假单胞菌和阴沟肠杆菌,病原菌分布规律基本同国内外研究结果一致[12-14]。39例患者中5例未培养出病原菌,可能为取材方式不同对培养结果阳性率影响较大。据报道,血培养阳性率仅为50%,细针穿刺取材活检阳性率为60%~70%,骨组织活检的阳性率为90%以上[15]。标本采集时可能仅取到脓性分泌物,而未取周围坏死组织进行培养,也有可能与部分厌氧菌培养条件要求比较高有关。
MDR是指对3类(如氨基糖苷类、β-内酰胺类、大环内酯类、喹诺酮类)或3类以上抗生素同时呈现耐药性的病原菌[16]。常见的MDR有MRSA、ESBLs菌和泛耐药的鮑曼不动杆菌等,本研究分离出的38株病原菌中MDR占19株(50.00%),其中MRSA比例最高,占所有金黄色葡萄球菌感染患者的比例达77.78%,对青霉素、左氧氟沙星、克林霉素和红霉素等抗生素均有较强的耐药性,但比较乐观的是其对万古霉素和利奈唑胺敏感性均较高。鉴于金黄色葡萄球菌及MRSA感染的普遍性,提示如果病情严重,细菌培养及药敏试验结果未回报之前,如患者自身肾功能良好,可考虑敏感性较高的万古霉素或利奈唑胺。分离出ESBLs有3株,占所有大肠埃希菌的75.00%,对大环内酯类、喹诺酮类和β-内酰胺类抗生素均呈现较高的耐药性,对哌拉西林和亚胺培南较敏感。对于非发酵革兰阴性菌,鲍曼不动杆菌属于条件致病菌,广泛存在于自然界的水、土壤及医院环境中,对各类抗生素普遍耐药,应引起足够重视[17]。同时,受伤和手术的创伤降低了患者的免疫力,条件致病菌会导致感染的发生,病房人员流动大,病原菌、患者与医疗环境相互影响,交叉感染的概率增加,容易引起感染。对于革兰阴性菌所致的感染,应尽早进行细菌培养和药敏试验,尽量避免经验用药,以免造成耐药菌的产生使感染复杂难控。
感染是骨折内固定术后严重的并发症,危险因素较多,包括年龄、合并基础疾病(低蛋白血症、糖尿病、高血压等)、开放性骨折、伤口污染情况、手术时间、引流管放置时间、住院时间等[18-23]。对于开放性骨折,在彻底清创、稳定骨折、改善血运、消灭死腔的基础上,科学、合理、有效的抗生素使用是控制感染的重要手段,但需要根据不同类型的伤口特点、细菌耐药的流行病学资料,结合患者自身状况和伤口愈合情况,尽早采集标本进行细菌培养和药敏试验,明确病原菌。除此之外,在治疗期间,应反复、多次进行细菌培养和药敏试验,提高标本培养的准确性,减少因污染产生的误差,根据体外药敏试验结果及时调整抗生素使用方案,对降低院内感染发病率、控制抗生素滥用、有效控制感染和提高治愈率有重要意义。
[参考文献]
[1] Matos MA,Lima LG,De Oliveira LAA. Predisposing factors for early infection in patients with open fractures and proposal for a risk score [J]. Journal of Orthopaedics and Tra?鄄umatology,2015,16(3):195-201.
[2] 姜楠,覃承诃,余斌.骨折内固定术后感染诊断与治疗的研究进展[J].中华创伤骨科杂志,2015,17(9):764-769.
[3] 费军,王爱民.骨科固定物与感染治疗新进展[J]. 中华创伤骨科杂志,2007,9(12):1189-1191.
[4] 中华人民共和国卫生部.外科手术部位感染预防与控制技术指南[S].2010.
[5] Mabit C,Marcheix PS,Mounier M,et al. Impact of a surgical site infection(SSI)surveillance program in orthopedics and traumatology [J]. Orthopaedics & Traumatology:Sur?鄄gery & Research,2012,98(6):690-695.
[6] Zimmerli W. Clinical presentation and treatment of orthopaedic implant-associated infection [J]. Journal of Internal Medicine,2014,276(2):111-119.
[7] Hogan A,Heppert VG,Suda AJ. Osteomyelitis [J]. Archives of Orthopaedic and Trauma Surgery,2013,133(9):1183-1196.
[8] Ojo OD,Oluwadiya KS,Ikem IC,et al. Superficial swab cultures in open fracture management:insights from a resource-poor setting [J]. Journal of Wound Care,2010,19(10):432-438.
[9] Kardas P,Devine S,Golembesky A,et al. A systematic review and meta-analysis of misuse of antibiotic therapies in the community [J]. International Journal of Antimicrobial Agents,2005,26(2):106-113.
[10] Rodney M,Donlan JWC. Biofilms:Survival Mechanisms of Clinically Relevant Microorganisms [J]. American Society for Microbiology,2002,15(2):167-193.
[11] Mauffrey C,Herbert B,Young H,et al. The role of biofilm on orthopaedic implants: the“Holy Grail”of post-traumatic infection management? [J]. European Journal of Trauma and Emergency Surgery,2016,42(4):411-416.
[12] Trampuz A,Zimmerli W. Diagnosis and treatment of infections associated with fracture-fixation devices [J]. Injury,2006,37(Suppl 2):S59-S66.
[13] 芦永华,黄新玲,何文英,等.四肢骨折手术部位感染危险因素多中心调查[J].中国感染控制杂志,2016,15(6):393-396.
[14] Vieira GD,Mendonca HR,Alves TC,et al. Survey of infection in orthopedic postoperative and their causative agents: a prospective study [J]. Rev Assoc Med Bras,2015, 61(4):341-346.
[15] Islam G,Tomlinson J,Darton T,et al. Bone and joint infections [J]. Surgery,2013,31(4):187-192.
[16] Magiorakos AP,Srinivasan A,Carey RB,et al. Multidrug-resistant,extensively drug-resistant and pandrug-resistant bacteria: an international expert proposal for interim standard definitions for acquired resistance [J]. Clinical Microbiology and Infection,2012,18(3):268-281.
[17] Kaye KS,Pogue JM. Infections Caused by Resistant Gram-Negative Bacteria: Epidemiology and Management [J]. Pharmacotherapy,2015,35(10):949-962.
[18] 蔡程名,駱倩倩,张洪芹,等.植骨对伴骨膜缺损的胫骨骨折愈合的影响[J].中国医药科学,2016,6(6):192-195.
[19] 周玉萍,李志建,黄少华,等.骨科手术切口感染发生率及相关危险因素回顾性调查分析[J].中华医院感染学杂志,2013,23(13):3158-3160.
[20] 严芝敏,邓小波,林民贵,等.剃毛备皮和脱毛剂备皮在骨科手术中的应用效果观察[J].中国医药科学,2016,(1):106-108.
[21] Parkkinen M,Madanat R,Lindahl J,et al. Risk Factors for Deep Infection Following Plate Fixation of Proximal Tibial Fractures [J]. The Journal of Bone and Joint Surgery,2016,98(15):1292-1297.
[22] Greene LR. Guide to the elimination of orthopedic surgery surgical site infections: An executive summary of the Association for Professionals in Infection Control and Epid?鄄emiology elimination guide [J]. American Journal of Infe?鄄ction Control,2012,40(4):384-386.
[23] Willey M,Karam M. Impact of Infection on Fracture Fixation [J]. Orthopedic Clinics of North America,2016,47(2):357-364.
(收稿日期:2016-12-22 本文编辑:程 铭)

