参麦注射液预防化疗所致心脏毒性的系统评价
万光升,刘丽丽,李敬瑜,孙 珏
参麦注射液预防化疗所致心脏毒性的系统评价
万光升,刘丽丽,李敬瑜,孙 珏
目的 系统评价参麦注射液预防化疗所致心脏毒性的有效性。方法 计算机检索中国知网、中国生物医学文献数据库、维普数据库、万方数据库、Pubmed、Web of Science等数据库,检索时间限定为建库至2016年8月,检索所有参麦注射液预防化疗所致心脏毒性的随机对照试验,并追索纳入研究的参考文献,通过与本领域专家、通讯作者联系以求获取灰色文献。由研究人员对文献进行筛选和数据提取,并用Revman5.3进行Meta分析。结果 最终纳入15篇文献,共2 042例病人。Meta分析结果:与对照组比较,参麦注射液可减少心电图、心肌酶、心脏功能性损伤等异常情况,降低心脏不良反应。结论 参麦注射液有助于预防化疗所致的心脏毒性。
心脏毒性;化疗;参麦注射液;Meta分析
随着环境污染和人口老龄化,癌症发病率和死亡率呈现增长趋势。据国家癌症中心最新数据显示,2012年全国新发恶性肿瘤358.6万例,发病率达264.85/10万,死亡病例218.7万例,累积死亡率达12.61%[1]。目前,化疗、手术、放疗是癌症治疗的3大常用手段。化疗药物主要通过干扰细胞代谢或直接破坏细胞结构实现抑制癌细胞目的,由于化疗药选择性较低,引起毒性作用,人体正常细胞不可避免地受到损伤,而心肌损伤是重要的一方面。一般认为,蒽环类药物、烷化剂、铂类金属络合物、抗代谢药等临床常用化疗药均产生不同程度的心脏毒性[2]。队列研究表明,大剂量应用蒽环类药物、与曲妥珠单抗联用、联合放疗等因素可能增加病人心脏毒性风险[3]。
参麦注射液由红参、麦冬提炼而成,具有益气固脱,养阴生津的功效。一项随机、双盲、多中心、安慰剂对照的临床研究认为,参麦注射液可治疗充血性心力衰竭合并冠心病[4]。随机对照试验Meta分析提示,参麦注射液可能对慢性肺心病心力衰竭有辅助治疗作用[5]。近年来,参麦注射液广泛用于防治化疗所致的心脏毒性,但目前仍缺乏循证医学证据支撑。为此,本研究采用Cochrane系统评价方法,全面收集国内外发表的有关参麦注射液防治化疗所致心脏毒性的临床随机对照研究,评价其研究质量,并进行Meta分析,以期为参麦注射液防治化疗所致心脏毒性提供循证医学证据。
1 资料与方法
1.1 文献纳入和排除标准
1.1.1 研究对象 临床随机对照试验(Randomized Controlled Trial,RCT),无论是否采用盲法及分配隐藏。语种限中文和英文。
1.1.2 结局指标 ST-T改变、QT-QTc延长、QRS低电压等心电图表现;期前收缩、房室传导阻滞、心律失常、心功能不全等心脏病变表现;乳酸脱氢酶(LDH)、肌酸激酶(CK)、肌酸激酶同工酶(CK-MB)等心肌酶谱检测;阿霉素(ADM)累积剂量与心电图异常改变关系;世界卫生组织(WHO)化疗心脏毒性分级。
1.1.3 纳入标准 经病理/细胞学检查明确诊断为原发性肝癌;临床随机对照试验;基本干预措施为化疗,以参麦注射液作为研究对象,且有相关结局指标。
1.1.4 排除标准 非随机对照试验;回顾性研究、动物实验及综述类文献;中英文以外的文献;组间均衡性差,无法进行有效的组间比较;无相关结局指标的研究;重复发表的研究;干预措施为参麦注射液混合其他中药注射剂的研究;病人有心脏功能性、器质性病变或心肌酶谱异常,非化疗引起的心脏毒性反应;研究质量较差的文献,文献版面不足1页、每组病例不足30例的研究。
1.2 文献检索策略 采用电子检索数据库包括中国知网、中国生物医学文献数据库、维普数据库、万方数据库、Pubmed和Web of Science。中文主题词检索式为“参麦注射液 AND (心肌保护 OR 心脏毒性 OR 心肌损害) AND 化疗”,英文主题词检索式为“chemotherapy and cardiotoxicity” and “Shenmai Injection”。检索时间为各数据库建库起至2016年8月止。灰色文献检索:与本领域专家、通讯作者联系,以获取以上检索未发现的信息。
1.3 文献筛选、数据提取和文献方法学质量评价 文献筛选由两位评价者分别独立阅读检索所获得文献的题目和摘要,剔除明显不符合纳入标准的文献。对潜在符合纳入标准的文献进行全文阅读,依据纳入和排除标准确定是否最终纳入研究,并进行交叉核对。如遇分歧讨论解决,若仍不能解决的交由第三位评价者仲裁。数据提取由两位评价者分别独立完成,提取以下数据:①ST-T改变、QT-QTc延长、QRS低电压等心电图表现;②期前收缩、房室传导阻滞、心律失常、心功能不全等心脏病变表现;③LDH、CK、CK-MB等心肌酶谱的检测;④ADM累积剂量与心电图异常改变的关系;⑤WHO化疗心脏毒性分级。文献方法学质量评价由两位评价者采用修改后的Jadad量表(1分~3分为低质量,4分~7分为高质量)分别评价纳入研究的方法学质量,评价项目包括随机序列的产生、随机化隐藏、盲法、撤出与退出。
1.4 统计学处理 统计学分析采用Cochrane协作网提供的Revman 5.3软件进行数据汇总分析。结局指标采用相对危险度(relative risk,RR)进行合并统计量分析,同时报告统计结果的95%可信区间(confidence intervals,CI)。通过χ2检验计算纳入研究间的异质性,当P≥0.05,I2≤50%时异质性较小,采用固定效应模型合并分析;当P<0.05,I2>50%时异质性较大,采用随机效应模型进行合并分析。
2 结 果
2.1 文献检索结果 共检索到146篇文献,中国知网51篇,中国生物医学文献数据库37篇,维普数据库16篇,万方数据库42篇,Pubmed 0篇,Web of Science、灰色文献0篇。剔除89篇重复检索的文献后,阅读题目和摘要剔除22篇不符合要求的文献,然后获取全文进行阅读,最终纳入15篇文献,共2 042例病人。文献筛选流程详见图1,纳入文献的基本特征见表1。
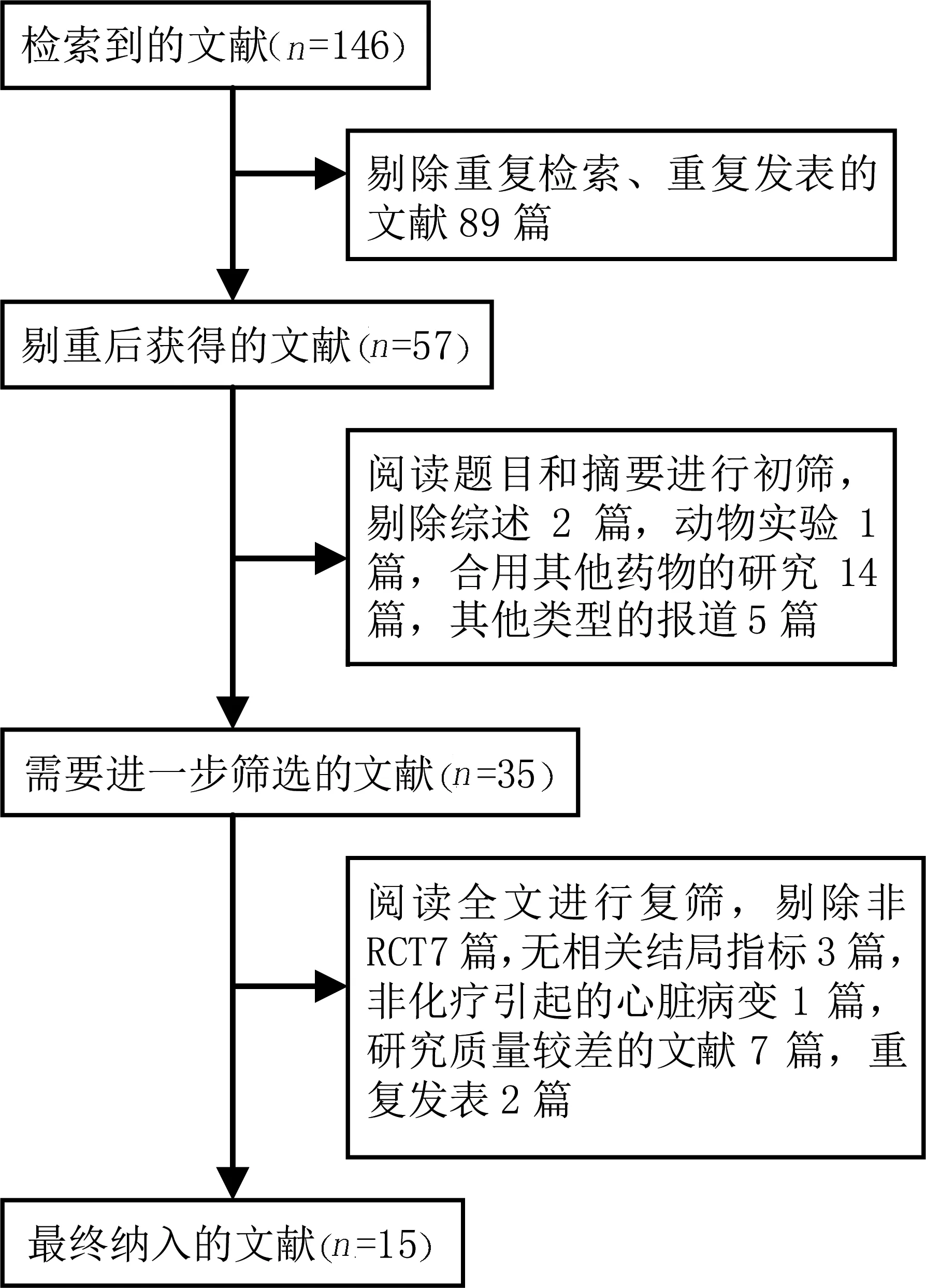
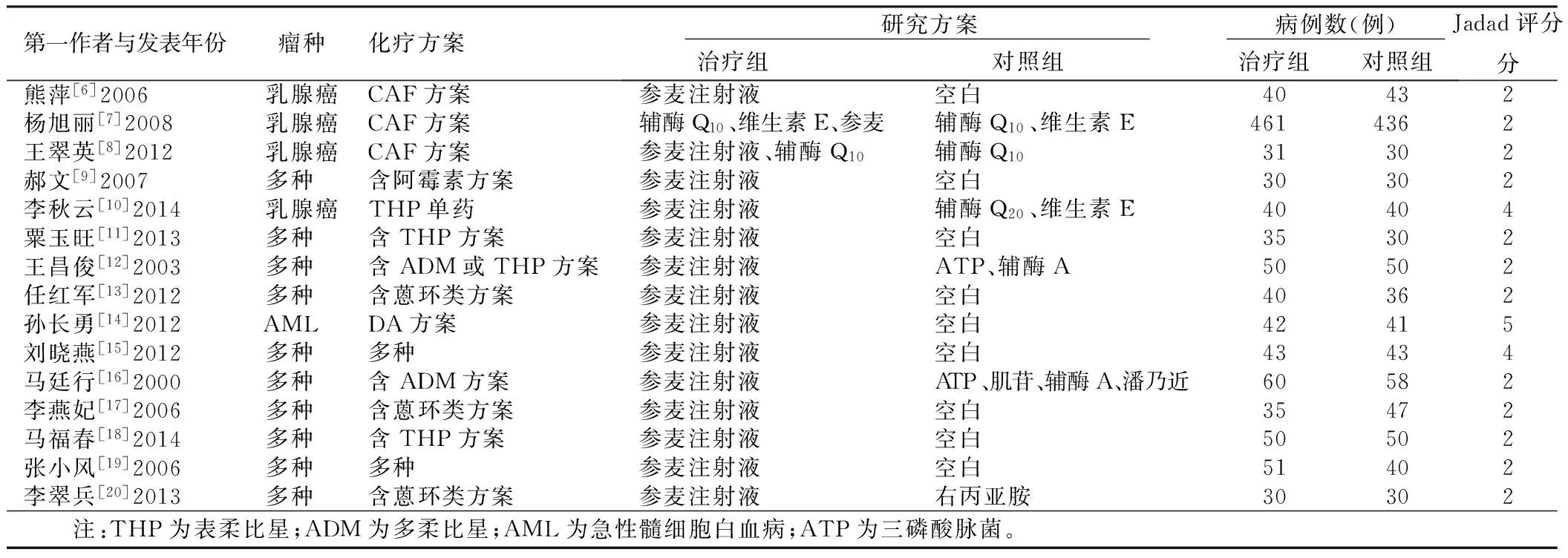
图1 文献筛选流程表1 纳入研究的基本信息
2.2 纳入文献的质量评价 两位评价者通过交叉核对评价,发现纳入研究的文献质量普遍不高,仅3项属于高质量的研究[10,14-15](详见表1)。对于随机分组序列的产生方式,仅3项研究[10,14-15]明确表述为使用随机数字表法,其他研究均仅出现“随机”字样,存在选择性偏倚。关于治疗方案的分配隐藏和盲法的使用所有文献均未提及,存在实施偏倚。在随访方面,仅3项研究[7,14-15]进行随访,其中仅1项提及退出和失访的情况[14],存在失访偏倚。
2.3 Meta分析结果
2.3.1 心电图异常 共8篇文献[6-8,10-12,14-15]具体报道病人出现心电图异常情况。根据报道的ST-T改变、QT-QTc延长、QRS压低等不同情况,采用亚组分析。由于各亚组以及总的异质性检验结果均显示P≥0.05,I2≤50%,故采用固定效应模型进行meta分析。ST-T改变亚组(P<0.01)、QT-QTc延长亚组(P<0.05)、QRS压低亚组(P<0.05)及总的心电图异常组(P<0.01)统计学结果均支持参麦注射液有助于预防化疗引起的ST-T改变、QT-QTc延长、QRS压低等心电图异常改变。详见图2。
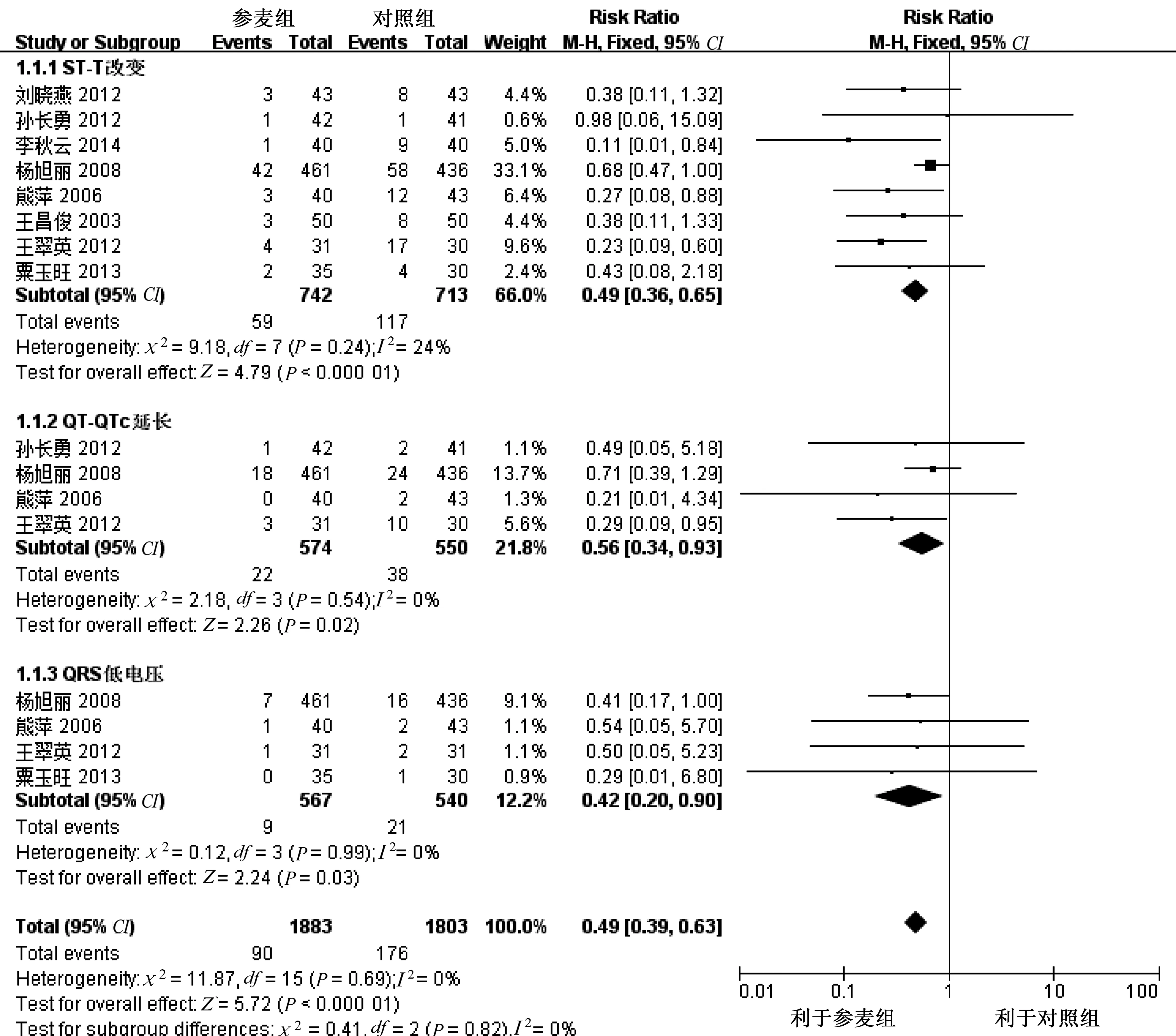
图2 心电图异常的森林图
2.3.2 心肌酶异常 共3项研究[7,11-12]报道包括LDH、CK-MB、肌钙蛋白T(cTnT)在内的心肌酶异常情况。根据各亚组和总的异质性检验结果,采用固定效应模型,结果显示LDH亚组、CK-MB亚组(P<0.01)、cTnT亚组(P<0.05)和总的心肌酶(P<0.01)均有统计学意义,说明参麦注射液能有效地降低LDH、CK-MB、cTnT心肌酶的异常表达。详见图3。
图3 心肌酶异常的森林图
2.3.3 心脏功能性损伤 共10项研究[6-15]报道期前收缩、房室传导阻滞、心律失常等心脏功能性损伤。根据各亚组和总的异质性检验结果,采用固定效应模型,结果显示期前收缩亚组、心律失常亚组和总的心脏功能性损伤组均差异有统计学意义(P<0.01),但房室传导阻滞亚组差异无统计学意义(P>0.05)。参麦注射液可预防化疗引起的包括期前收缩和心律失常在内的心脏功能性损伤,但对房室传导阻滞的预防效果证据不足。详见图4。
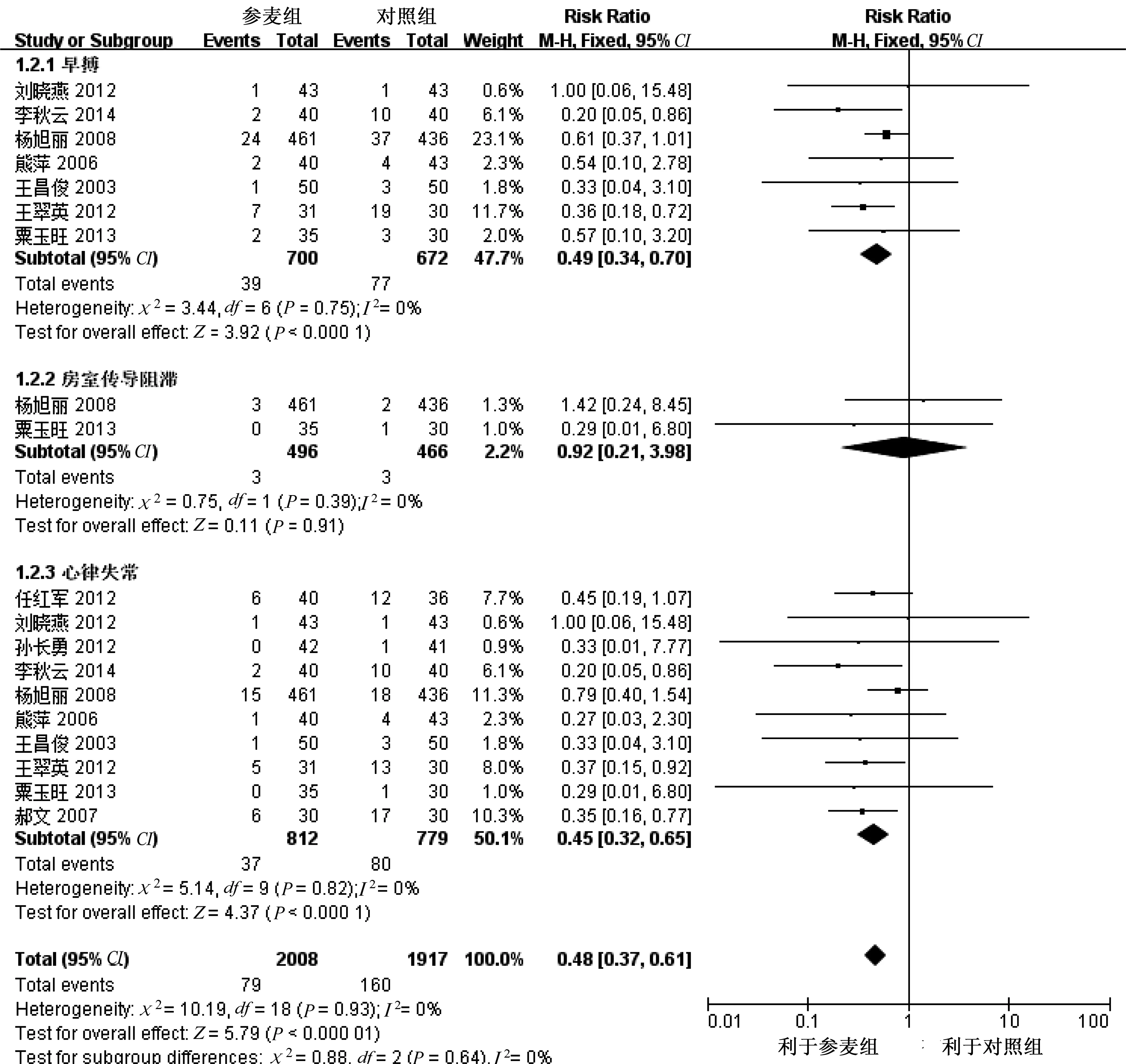
图4 心脏功能性损伤的森林图
2.3.4 心功能不全 共有3项研究[9,12-13]报道病人发生心功能不全。根据异质性检验结果,采用固定效应模型,结果显示参麦注射液组与对照组差异无统计学意义(P>0.05)。说明基于目前证据,尚不足以证明参麦注射液有助于防止化疗引起的心功能不全。详见图5。
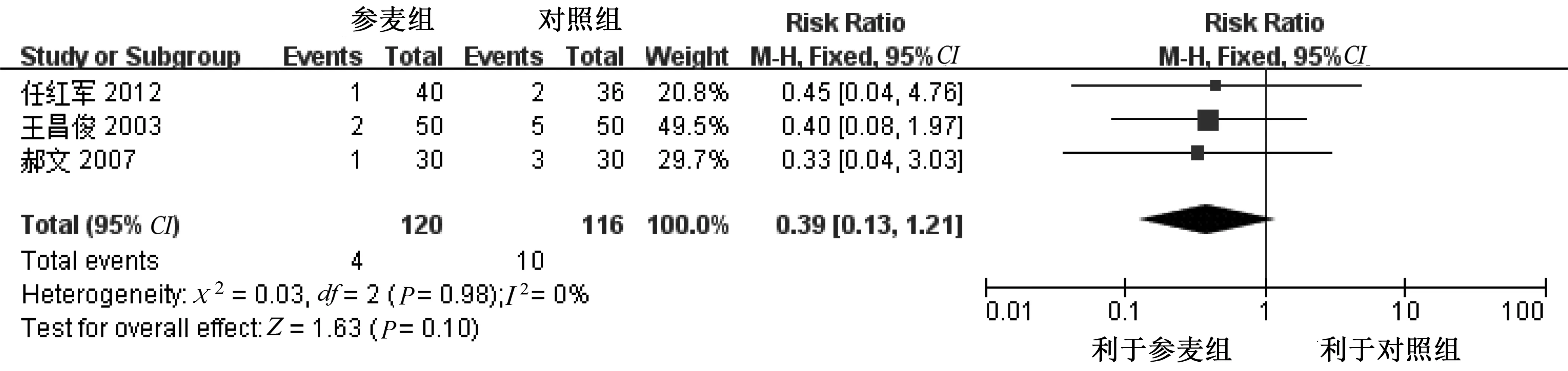
图5 心功能不全的森林图
2.3.5 心脏不良反应分级 共5项研究[15-19]根据WHO化疗心脏毒性分级标准[21]进行报道。根据异质性检验结果,采用固定效应模型,结果显示Ⅰ级和Ⅳ级病例差异无统计学意义(P>0.05),但除0级以外病例汇总结果差异有统计学意义(P<0.01)。依据WHO化疗心脏毒性分级标准,参麦注射液能预防化疗引起的心脏毒性,但对于Ⅰ级和Ⅳ级病例证据不足。详见图6。
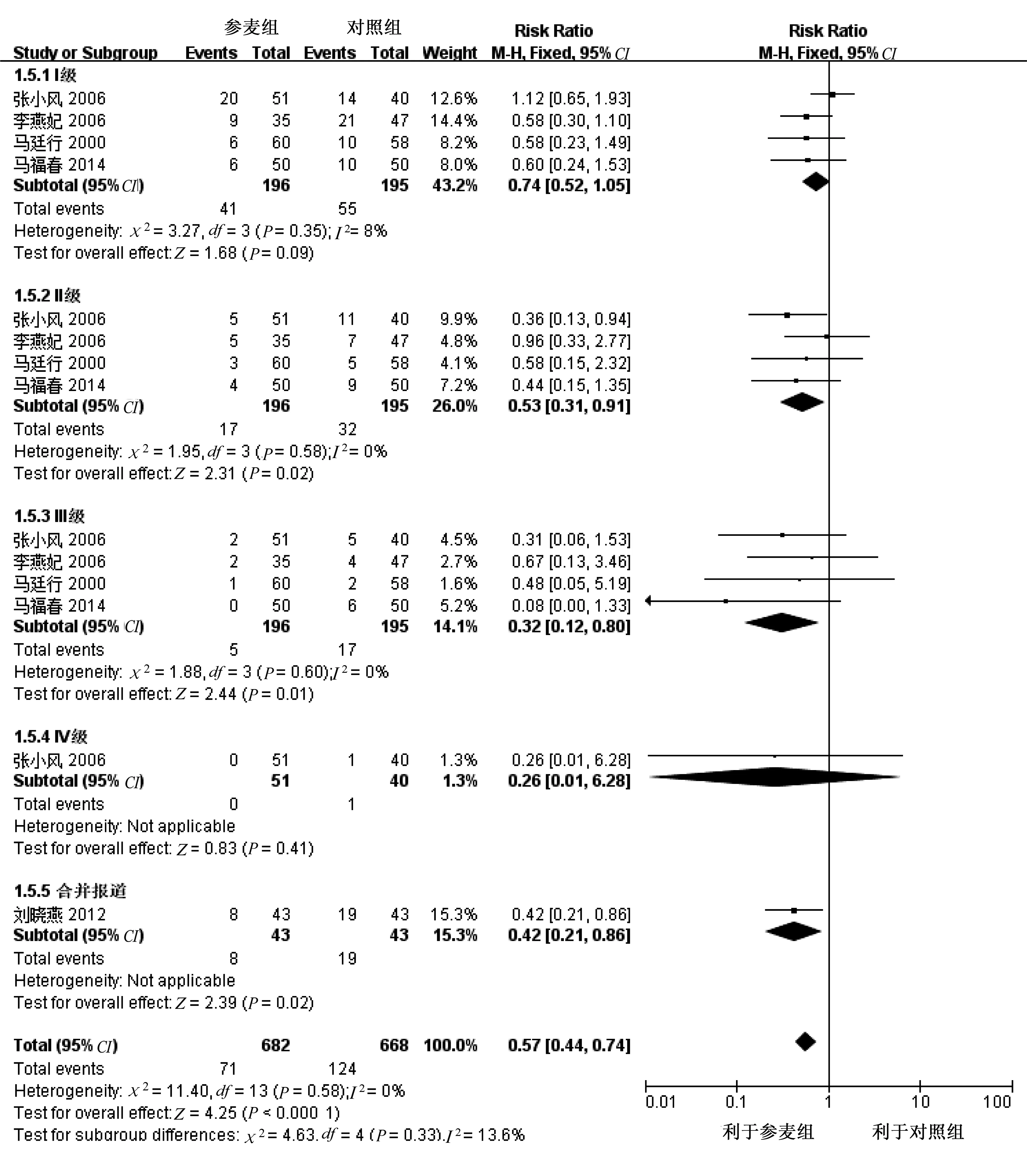
图6 心脏不良反应分级的森林图
3 讨 论
心脏毒副作用是蒽环类药物的常见不良反应,特别是其毒性程度与蒽环类剂量的累积呈正相关,这极大地限制蒽环类药物的临床使用。目前临床上公认的抗心脏毒性药物包括血管紧张素转换酶抑制剂、β受体阻滞剂、二甲双胍、右丙亚胺等,应用最广泛的是右丙亚胺,已有Meta分析认为其能有效降低心脏毒副作用的发生率[22]。美国和部分欧洲国家已批准为晚期和/或转移性乳腺癌病人接受阿霉素化疗时的心肌保护剂。2007年有研究认为右丙亚胺增加儿童癌症患儿发生继发性急性髓系白血病(AML)的可能性[23]。此后有回顾性队列研究[24]认为右丙亚胺暴露与继发性AML发病率增加不相关,但最新发表对多个RCT的Meta分析[25]认为右丙亚胺增加罹患继发性AML的风险。儿童病人使用右丙亚胺的安全性仍需进一步研究验证。因此,中医药防治化疗所致的心脏毒性有重要意义。
参麦注射液作为中医药现代化的研究成果之一,越来越多运用于化疗心脏毒副作用的临床工作。有研究认为[26],参麦注射液对阿霉素引起的心肌细胞损伤可减少乳酸脱氢酶漏出量和心肌细胞内丙二醛含量,并改善心肌细胞活力和搏动频率,其机制可能与抑制阿霉素引起的脂质过氧化损伤有关。本研究通过对多个RCT的meta分析提示,参麦注射液有助于减少化疗引起的心电图异常改变、心肌酶的高表达,降低早搏和心律失常的发生率,降低心脏不良反应分级。
本研究的局限性:①由于纳入研究的方法学质量较差,得出的结论仅供参考;②对照措施使用不当,仅一项研究采用临床公认的右丙亚胺作为对照组[20],其他研究采用空白对照,或使用辅酶Q10、维生素E等抗氧化剂,影响组间的可比性,考虑到蒽环类心脏毒性的作用机制可能是形成蒽环-Fe3+复合物,诱导产生大量氧自由基,引起心肌细胞线粒体与内质网过氧化,使用抗氧化剂对照的方式也有一定的理论支持;③纳入的文献均未报道使用参麦注射液的不良反应,存在一定的安全隐患,据国家药品不良反应中心自发呈报系统的数据显示[27],参麦注射液不良反应发生率为0.093%,主要表现为“憋气”、“过敏样反应”和“潮红”,此外,注射前连续使用前列地尔、环磷腺苷,合并用喹诺酮类、青霉素类药物均可能增加不良反应机会;④纳入的文献中仅一项提及病例脱落情况[14],其他研究均未提及退出和失访,也未采用意向治疗分析,这种情况认为有夸大疗效的可能[28];⑤参麦注射液的厂家、批号、临床用量等信息均未见报道。
综上所述,参麦注射液能有效预防化疗所致的心脏毒性,但限于纳入研究的方法学质量问题,该结论仍有待更多高质量、多中心、大样本、随机、双盲临床试验加以验证,为参麦注射液的临床运用提供更多循证医学证据。
[1] 陈万青,郑荣寿,张思维,等.2012年中国恶性肿瘤发病和死亡分析[J].中国肿瘤,2016,25(1):1-8.
[2] 覃业语,苏素文.抗肿瘤药物心脏毒性作用机制研究进展[J].海南医学,2015,26(24):3661-3664.
[3] 薛剑.化疗药物心脏毒性危险因素与预测因素分析[D].北京: 中国人民解放军军事医学科学院,2015.
[4] Xian S,Yang Z,Lee J,et al.A randomized,double-blind,multicenter,placebo-controlled clinical study on the efficacy and safety of Shenmai injection in patients with chronic heart failure[J].Journal of Ethnopharmacology,2016,186:136-142.
[5] Shi L,Xie Y,Liao X,et al.Shenmai injection as an adjuvant treatment for chronic cor pulmonale heart failure: a systematic review and meta-analysis of randomized controlled trials[J].BMC,2015,15(1):193-205.
[6] 熊萍,连捷,余小清.阿霉素为主化疗83例乳腺癌心电图分析[J].临床医药实践杂志,2006,15(4):263-264.
[7] 杨旭丽.参麦对新疆维吾尔族乳腺癌CAF化疗致心肌毒性的疗效观察[D].乌鲁木齐:新疆医科大学,2008.
[8] 王翠英,宋春燕,沈凤梅.参麦注射液对阿霉素心脏毒性保护作用的研究[J].临床荟萃,2012,27(13):1169-1170.
[9] 郝文.参麦注射液对阿霉素心脏毒性反应的防治作用[J].中医药临床杂志,2007,19(1):5-6.
[10] 李秋云,利明,李永宝,等.参麦注射液对乳腺癌吡柔比星化疗的心肌保护作用[J].右江医学,2012,42(6):669-671.
[11] 粟玉旺.参麦注射液防治表柔比星心脏毒性的临床观察[J].世界最新医学信息文摘,2013,13(5):189-190.
[12] 王昌俊,陈庆强,邓力,等.参麦注射液防治蒽环类化疗药物心脏毒性的临床观察[J].中国中医药科技,2003,10(2):111-112.
[13] 任红军,崔秀洁.参麦注射液防治蒽环类药物所致心脏毒性的临床观察[J].中外医疗,2012,31(15):106-108.
[14] 孙长勇,杨淑莲,侯伟,等.参麦注射液防治急性髓细胞白血病患者柔红霉素心肌毒性临床观察[J].上海中医药杂志,2012,46(8):47-49.
[15] 刘晓燕,邹青峰,陈文晟,等.参麦注射液预防恶性肿瘤化疗所致心脏毒性及骨髓反应的临床观察[J].广西医学,2012,34(11):1578-1579.
[16] 马廷行,姜春壮,钟伟,等.参麦注射液治疗阿霉素所致心脏毒性临床观察[J].临床肿瘤学杂志,2000,5(1):57-58.
[17] 李燕妃,许德明,赵小琼,等.参麦注射液治疗蒽环类药物所致毒性的临床研究[J].现代肿瘤医学,2006,14(10):1277-1279.
[18] 马福春.参麦注射液对接受表柔比星化疗的恶性肿瘤患者心肌酶水平的影响[J].肿瘤基础与临床,2014,27(1):66-67.
[19] 张小风,蔡元训.参麦注射液联合化疗治疗恶性肿瘤疗效观察[J].浙江中西医结合杂志,2006,16(12):741-742.
[20] 李翠兵,周晓峰,宋欣颖.中药注射剂对蒽环类药物所致心脏毒性的保护作用[J].肿瘤药学,2013(5):385-388.
[21] 孙燕,周际昌.临床肿瘤内科手册[M].第3版.北京:人民卫生出版社,1997:30-45.
[22] Kalam K,Marwick TH.Role of cardioprotective therapy for prevention of cardiotoxicity with chemotherapy:a systematic review and meta-analysis[J].Eur J Cancer,2013,49(13):2900-2909.
[23] Tebbi CK,London WB,Friedman D,et al.Dexrazoxane-associated risk for acute myeloid leukemia/myelodysplastic syndrome and other secondary malignancies in pediatric Hodgkin's disease[J].Journal of Clinical Oncology,2007,25(5):493-500.
[24] Seif AE,Walker DM,Li Y,et al.Dexrazoxane exposure and risk of secondary acute myeloid leukemia in pediatric oncology patients[J].Pediatric Blood & Cancer,2014,62(4):704-709.
[25] Shaikh F,Dupuis LL,Alexander S,et al.Cardioprotection and second malignant neoplasms associated with dexrazoxane in children receiving anthracycline chemotherapy:a systematic review and meta-analysis[J].JNCI,2016,108 (4): djv357.
[26] 刘晓健,刘义,胡长宏,等.参脉注射液对阿霉素所致心肌细胞毒性的影响[J].中国现代药物应用,2008,7(2):11-13.
[27] Wang LX,Xie YM,Ai QH,et al.Post-marketing clinical safety assessment of Shenmai injection based on active monitoring and passive monitoring in large data background[J].China Journal of Chinese Materia Medica,2015,40(24):4752-4756.
[28] Schulz KF,Altman DG,Moher D.CONSORT 2010 Statement: updated guidelines for reporting parallel group randomised trials[S].Int J Surg,2011,9(8):672-677.
(本文编辑薛妮)
国家中医药管理局“十二五”重点专科建设项目,编号:国中医药医政发[2012]2号;国家中医药管理局中医药重点学科建设项目,编号:国中医药人教发[2012]32号
上海中医药大学附属普陀医院(上海 200062)
刘丽丽,E-mail:et5709394@163.com
R542 R289.5
A
10.3969/j.issn.1672-1349.2017.08.03
1672-1349(2017)08-0904-07
2017-01-22)
引用信息:万光升,刘丽丽,李敬瑜,等.参麦注射液预防化疗所致心脏毒性的系统评价[J].中西医结合心脑血管病杂志,2017,15(8):904-910.

