蒙药草乌及其炮制品的六种生物碱类成分血浆中含量测定△
策力木格 聂颖兰 梁 慧 张小峰 松 林* 图 雅
(1.内蒙古医科大学蒙医药学院,内蒙古 呼和浩特 010110;2.中国中医科学院医学实验中心,北京 100700;3.中国中医科学院数据中心,北京 100700)
蒙药草乌及其炮制品的六种生物碱类成分血浆中含量测定△
策力木格1聂颖兰2梁 慧1张小峰1松 林1*图 雅3
(1.内蒙古医科大学蒙医药学院,内蒙古 呼和浩特 010110;2.中国中医科学院医学实验中心,北京 100700;3.中国中医科学院数据中心,北京 100700)
目的:建立血浆中,草乌及其诃子汤炮制品的6种生物碱类成分LC-MS含量测定的方法。方法:血浆样品用加25%氨水、乙醚萃取后,采用ZORbax-Extend-C18 4.6×250mm 5-Micron 80A柱子检测,流动相水相为10mmol醋酸铵水溶液(氨水调ph=9.0)有机相为乙腈,选择离子检测m/z 604(苯甲酰乌头原碱)、m/z 590(苯甲酰新乌头原碱)、m/z 574(苯甲酰次乌头原碱)m/z 632(新乌头碱)、m/z 646(乌头碱)、m/z 616(次乌头碱)。结果:本方法6种成分线性关系均良好,精密度、稳定性、基质效应RSD都低于10%,加样回收率为59.11%~96.57%。结论:此样品处理快速简便、检测方法精密度高,适用于血浆中新乌头碱、次乌头碱、乌头碱、苯甲酰新乌头原碱、苯甲酰次乌头原碱、苯甲酰乌头原碱检测,以其为草乌及诃子汤炮制草乌的进一步药代毒代动力学研究提供参考。
草乌;炮制;诃子制草乌;含量测定
草乌为毛茛科多年生草本植物北乌头Aconitum kusnezoffii Reichb.的干燥块根[1]。是中医、蒙医常用药。蒙医主要用于杀“粘(nian)”,止痛,燥“协日乌素”。草乌含有生物碱、糖类、挥发性成分,但在这些成分中起主要治疗作用的是乌头类生物碱,并且草乌的有毒成分也恰恰是起主要治疗作用的乌头类生物碱[2],主要有乌头碱、新乌头碱和次乌头碱,而且其治疗量和中毒量非常相近,安全范围小[3]因服用含乌头碱类毒性成分的药而致中毒的事故每年都有大量发生。为了降低草乌的毒性有多种炮制方法被采用,草乌经炮制后,毒性大大减低,可内服入药。草乌蒙医特色炮制法,即诃子汤炮制草乌方法广泛收到认可。本研究通过检测草乌生药及其诃子汤炮制品口服给药动物血浆中新乌头碱、次乌头碱、乌头碱及苯甲酰新乌头原碱、苯甲酰次乌头原碱、苯甲酰乌头原碱的含量,以其为草乌及诃子汤炮制草乌的进一步药代毒代动力学研究提供参考。
1 仪器与试剂
液-质联用仪 :Agilent 1200高效液相色谱仪;h-ALS-SL;MS QQQ;1260 DAD;Column-SL;1260 BinPump1200Series Rapid Resolution LC System; pH值计;离心机(TGL-16G);
试剂:乌头碱( 批号:MUST-15013008) 、次乌头碱( 批号:MUST-15090918) 和新乌头碱( 批号: MUST-15091504) 苯甲酰乌头原碱(MUST-15012215)苯甲酰次乌头原碱(MUST-150108006)苯甲酰新乌头原碱(MUST-16012816)对照品购自北京凯瑞恩科贸中心。诃子(批号:20140101,执行标准:《中国药典》2010年版一部),生草乌(批号:141001,执行标准:《中国药典》2010年版一部), 乙腈(色谱纯,DikmaPure公司),氨水(色谱纯,FluKa公司),醋酸铵(色谱纯,DikmaPure公司),乙醚(分析纯,国药集团化学试剂公司)三氯甲烷(分析纯,国药集团化学试剂公司)异丙醇(色谱纯,DikmaPure公司)超纯水(自制)。
2 实验方法
2.1 含药血浆的制备:称取草乌及诃子汤炮制草乌干燥粉末加适量0.5%CMC,混匀,15只SD大鼠,随机分为3组,每组5只,一组为空白组,其余2组为给药组,所有大鼠实验前禁食12h(自由饮水)。给药组大鼠称重后,1mL/100g的体积灌胃给药,给药后1h腹腔注射水合氯醛麻醉,腹主动脉采血后放入肝素化采血管中,静置30min,4℃,3000rpm离心15min,取上清液,合并同一组不同大鼠血浆备用。空白组同法灌胃给0.5%CMC溶液后采血,合并大鼠血浆作为空白血浆备用。
2.2 血浆中6 种生物碱的含量测定
2.2.1 色谱条件:色谱柱选择ZORbax-Extend-C18 4.6×250mm 5-Micron 80A柱子分离,流动相为10mmol醋酸铵水溶液(氨水调pH=9.0):乙腈,流速为1mL/min,柱温30℃,进样量2μL。
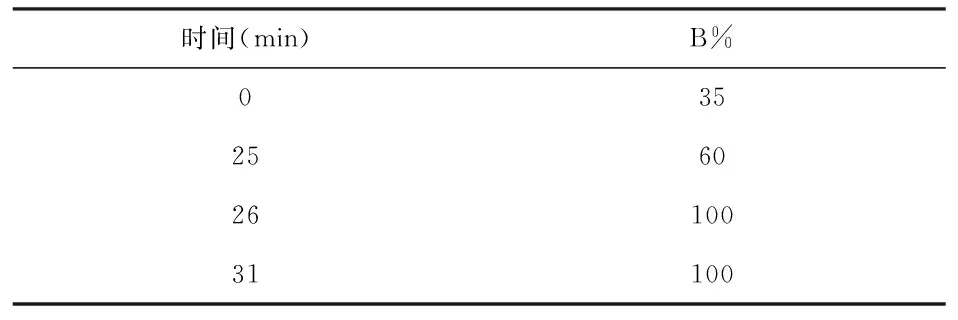
表1 时间梯度
2.2.2 质谱条件:离子源为电喷雾离子化源(ESI):正离子检测;毛细管出口电压(v):135;碰撞电压(v):40;Gas Temp (°C): 300;Nebulizer (psi) :45 ;Gas Flow (l/min): 12 ;选择离子检测m/z 604(苯甲酰乌头原碱)、m/z 590(苯甲酰新乌头原碱)、m/z 574(苯甲酰次乌头原碱)m/z 632(新乌头碱)、m/z 646(乌头碱)、m/z 616(次乌头碱)。
2.2.3 对照品溶液的制备:取新乌头碱对照品、次乌头碱对照品、乌头碱对照品、苯甲酰乌头原碱对照品、苯甲酰次乌头原碱对照品、苯甲酰新乌头原碱对照品适量,精密称定 ,加异丙醇-三氯甲烷(1 : 1)混合溶液分别制成每lmL含1mg对照品的混合溶液,即得母液。
2.2.4 血浆样品处理:取血浆样品200μL,加25%的氨水混旋振荡1min,再加乙醚1mL,混旋振荡5min,10000rmp离心10 min,取上清液,氮气吹干,用40μL异丙醇-三氯甲烷(1 : 1)混合溶液复溶。取40μL于自动进样器样品瓶中,设定2μL进样检测。
3 检测结果及方法学考查
3.1 专属性研究:取空白血浆、含药血浆各200μL,采用2.2.4项下处理方法处理记录色谱图(图1)。由图可知在此色谱-质谱条件下,新乌头碱、乌头碱、次乌头碱和苯甲酰新乌头原碱、苯甲酰次乌头原碱、苯甲酰乌头原碱峰形良好,血浆内杂质不干扰样品测定。本实验中建立的方法测定草乌及其诃子汤炮制品中6种生物碱的含量结果见表2。

表2 样品含量测定结果(ng/mL)
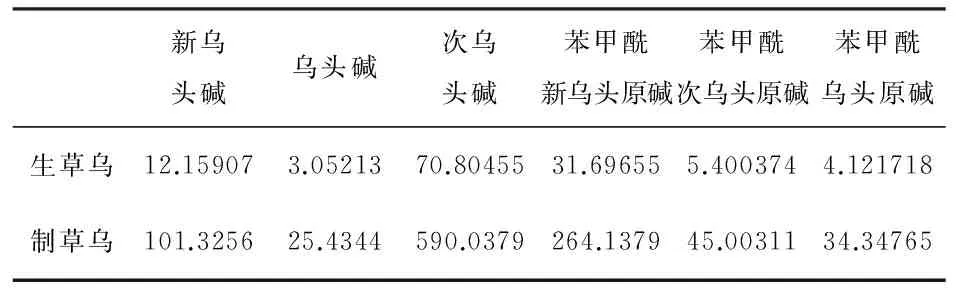
新乌头碱乌头碱次乌头碱苯甲酰新乌头原碱苯甲酰次乌头原碱苯甲酰乌头原碱生草乌12.159073.0521370.8045531.696555.4003744.121718制草乌101.325625.4344590.0379264.137945.0031134.34765
3.2 线性范围研究及定量下线:取对照品混合溶液母液,配制成不同浓度的系列对照品溶液分别放入9支EP管中,氮气吹干,再各管中加入空白血浆200μL,使各管标准品的最终浓度达到0.078、0.15625、0.3125 、0.625 、1.25、2.5、5、10、20ng/mL水平,按上述2.2.4方法处理后进行HPLC—MS检测,分别记录新乌头碱、乌头碱、次乌头碱、苯甲酰新乌头原碱、苯甲酰次乌头原碱、苯甲酰乌头原碱的峰面积,以峰面积之比为纵坐标,以相对应各点浓度为横坐标绘制标准曲线。取标准曲线的下限为定量下限,新乌头碱、乌头碱、次乌头碱、苯甲酰新乌头原碱、苯甲酰次乌头原碱、苯甲酰乌头原碱的定量下限分别为0.078ng/mL。结果图2表3。

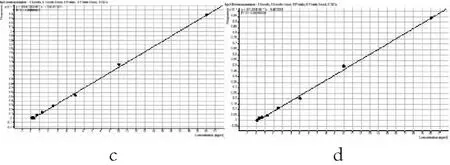
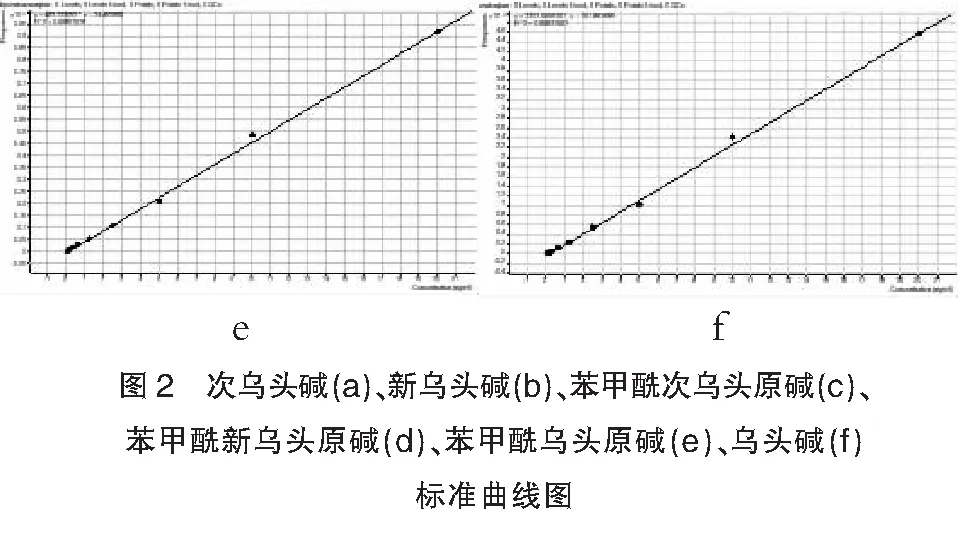
表3 6种检测成分的加样最终浓度及血浆标准曲线回归方程
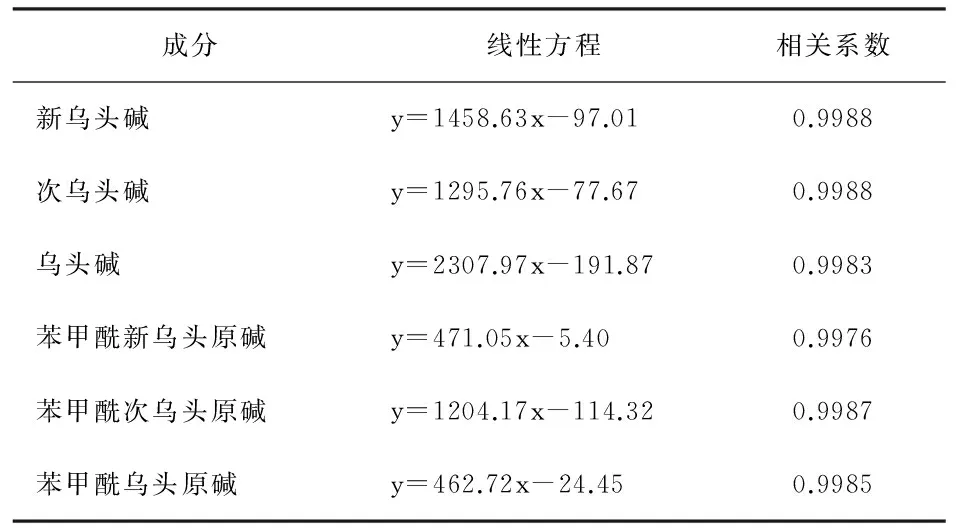
成分线性方程相关系数新乌头碱y=1458.63x-97.010.9988次乌头碱y=1295.76x-77.670.9988乌头碱y=2307.97x-191.870.9983苯甲酰新乌头原碱y=471.05x-5.400.9976苯甲酰次乌头原碱y=1204.17x-114.320.9987苯甲酰乌头原碱y=462.72x-24.450.9985
3.3 精密度研究:取新乌头碱、乌头碱、次乌头碱、苯甲酰新乌头原碱、苯甲酰次乌头原碱、苯甲酰乌头原碱混标溶液吹干,各加空白兔血浆200μL,按配制成最终3种浓度血浆标准溶液,每个浓度各5管。按血浆样品处理方法处理后,同一日内测定5次,计算日内精密度;连续测定5 d,计算日间精密度结果见表4。
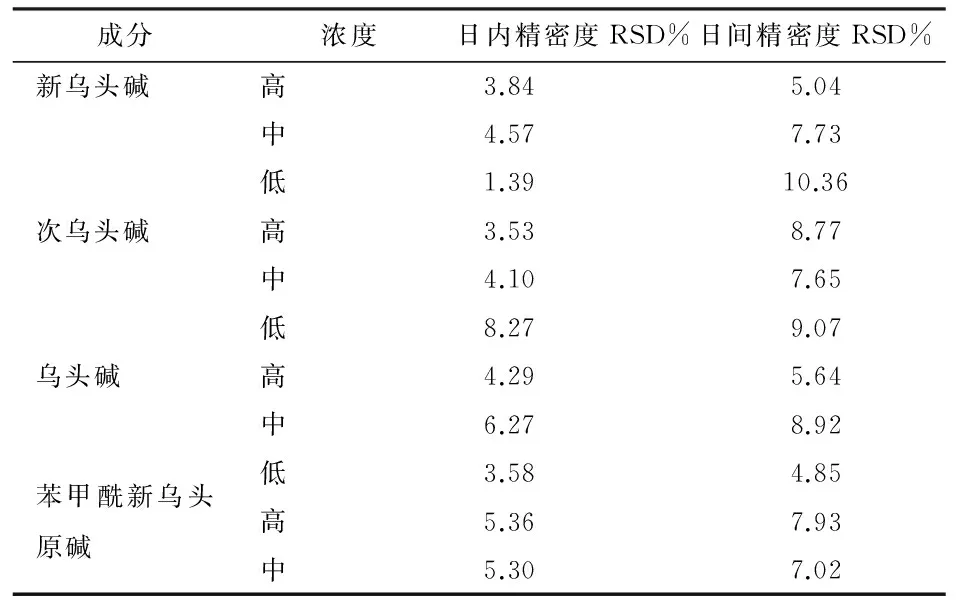
表4 各成分精密度
3.4 萃取回收率与基质效应考查:配制混标溶液高、中、低3个浓度,氮气吹干后加入200μL异丙醇-三氯甲烷(1:1)溶液复溶。测得响应值为A;将高、中、低3个不同浓度的混标吹干物上加入已经处理好的空白血浆提取物混合制备,测得响应值为B;将高、中、低3个不同浓度的混标吹干物上加入空白血浆,提取制备,测得的响应值为C。计算出基质效应(B/A),回收率(C/B)。结果如表5。
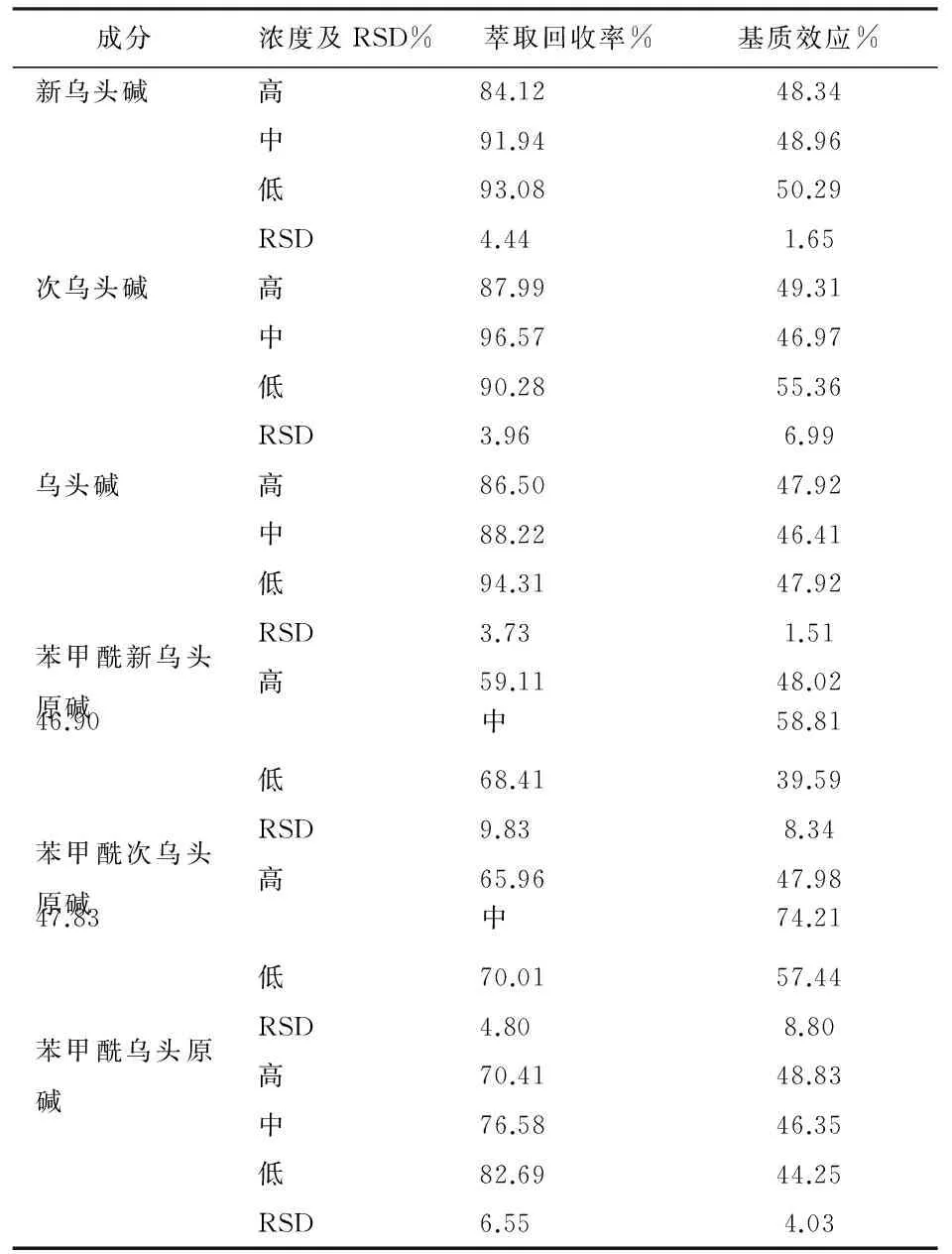
表5 各成分萃取回收率和基质效应
3.5 稳定性研究:精密量取混标溶液高、中、低3个浓度溶液氮气吹干,取空白血浆200μL加入吹干物中,按照血浆样品处理方法处理,于室温下放置0、2、4、8、12、24测定样品,运用其峰面积计算RSD,新乌头碱、乌头碱、次乌头碱、苯甲酰新乌头原碱、苯甲酰乌头原碱、苯甲酰次乌头原碱RSD分别为1.24%、1.97%、2.10%、4.47%、3.95%、3.69%。
4 讨论
本实验中建立了动物血浆中草乌及其诃子汤炮制品新乌头碱、乌头碱、次乌头碱、苯甲酰新乌头原碱、苯甲酰乌头原碱、苯甲酰次乌头原碱同时检测的HPLC-MS测定方法,具有准确、灵敏、简便、测得数据可靠的优点,对目标化合物进行选择性离子检测,空白血浆无杂质干扰。线性关系良好,血浆的萃取回收率高,6种物质的日内、日间精密度RSD均小于10%,适用于草乌的浓度监控、药代动力学和毒代动力学研究。
[1]罗布桑.蒙药学[M].呼和浩特:内蒙古人民出版社,2006:185.
[2] 张小峰,松林,图雅,等. 三种不同产地蒙药草乌炮制前后三种乌头碱含量的比较研究[J]. 中国民族医药杂志, 2016, 卷缺失(2): 42-43.
[3] Aimin Sun, Bo Gao,?Xueqing Ding et al.? Quantitative and Qualitative Analysis of Aconitum Alkaloids in Raw and Processed Chuanwu and Caowu by HPLC in Combination with Automated Analytical System and ESI/MS/MS[J]. ?Analytical Methods in Chemistry.2012,doi:10.1155/2012/936131.
[4] 邱俏檬,刘刚,梁欢,等. 高效液相色谱-质谱法同时检测兔血浆中3种草乌成分[J]. 中国中西医结合急救杂志, 2009, 16(2): 106-108.
[5]韩志强,巴图德力根. 烘制法对不同质地蒙药草乌炮制效果的比较研究[J]. 中国临床药理学杂志, 2015, 31(1): 67-69.
[6]晓华,张思远,海平,等. 草乌中二萜生物碱的提取工艺及化学成分研究[J]. 安徽农业科学, 2015, 43(2): 113-114.
2016年10月10日收稿
Content determination of six alkaloid compositions from Caowu and its Hezi decoction processed products in the plasma
Celi muge NIE Yin-lan LIANG Hui ZHANG Xiao-feng, Songlin Tuya
Mongolia medicine college in inner Mongolia medicine university huhhot 010110
Objective: A quantitative analysis method for simultaneous determination of six Alkaloid compositions from Cao Wu and its He Zi decoction processed products in the plasma was established by applying LC-MS. Methods: After ether extraction, the column was ZORbax-Extend-C18(4.6×250mm,5-Micron 80A); the mobile phase was acetonitrile - a buffer solution consisting of 10mmol/L ammonium acetate (ammonia pH=9.0?Regulation); m/z 604 (benzoyl aconite original base), m/z 590 (benzoyl new aconite original base), m/z 574 (benzoyl aconite original base) m/z 632 (new aconitine), m/z 646 (Aconitum alkaloids) and m/z 616 (Aconitum alkaloids) was selected by ion detection. Results: The linear correlation coefficients of six components were good, and the RSD of their precision, stability and matrix effects were all less than 10%; the average recovery was between 59.11% and 96.57%. Conclusion: The method is simple, rapid, accurate,and can be applied to the determination of new aconitine, hypaconitine and aconitine, benzoyl new aconite original base, benzoyl aconite original base, aconite original base from the plasma which was provided further reference of study on pharmacokinetics and toxicokinetics of Cao Wu and its He Zi decoction processed products.
Aconiti kusnezoffii Radix; processed; processed with Chebulae Fructus; content determination
国家自然科学基金项目(No.81360677;No.81274192)
策力木格,硕士研究生,研究方向:蒙药配伍规律研究,电话:15647135811,E-mail:875061667@qq.com
*通信作者:松林,教授,硕士生导师,研究方向:蒙药配伍规律研究,炮制规范化研究,电话:0471-6657613 ,E-mail: songlinwps@163.com
R291.2
B
1006-6810(2017)01-0042-04

