微生物胞外电子传递效率的合成生物学强化
李锋,宋浩
微生物胞外电子传递效率的合成生物学强化
李锋1,2,宋浩1,2
1 天津大学化工学院系统生物工程教育部重点实验室,天津 300072 2 天津大学天津化学化工协同创新中心合成生物学研究平台,天津 300072

李锋, 宋浩. 微生物胞外电子传递效率的合成生物学强化. 生物工程学报, 2017, 33(3): 516–534.Li F, Song H. Promoting efficiency of microbial extracellular electron transfer by synthetic biology. Chin J Biotech, 2017, 33(3): 516–534.
电活性微生物 (产电微生物和亲电微生物) 通过与外界环境进行双向电子和能量传递来实现多种微生物电催化过程 (包括微生物燃料电池、微生物电解电池、微生物电催化等),从而实现在环境、能源领域的广泛应用,并为开发有效且可持续性生产新能源或大宗精细化学品的工艺提供了新机会。但是,电活性微生物的胞外电子传递效率比较低,这已经成为限制微生物电催化系统在工业应用中的主要瓶颈。以下综述了近年来利用合成生物学改造电活性微生物的相关研究成果,阐明了合成生物学如何用于打破电活性微生物胞外电子传递途径低效率的瓶颈,从而实现电活性微生物与环境的高效电子传递和能量交换,推动电活性微生物电催化系统的实用化进程。
电活性微生物,合成生物学,微生物电催化,微生物燃料电池,微生物电合成
环境污染和能源短缺已经成为世界上的两大难题。绿色可再生新能源是替代化石燃料,解决未来保护环境和能源短缺的可持续发展的必经之路。以电活性微生物为主导的微生物电催化系统,包括微生物产电[1-2]、微生物电合成[3]、微生物非平衡电发酵[4-5]等),作为一种新型的绿色新能源生产方式正崭露头角。微生物电催化过程是通过电活性微生物与外界环境进行双向电子和能量交换,实现环境、能源领域的广泛应用,如促使有机废弃物降解和电能回收的微生物燃料电池 (Microbial fuel cells, MFC)[6-7]、用于生物制氢的微生物电解池 (Microbial electrolysis cells, MEC)[8-9]、用于实现CO2固定[10]和大宗精细化学品合成的非平衡电发酵和微生物电合成 (Microbial electrosynthesis, MES)[11-13],以及微生物冶金[14]、生物传感器[15-16]和生物电子 学等[17]。
双向电子传递指电活性微生物与外界环境进行“双向”电子和能量交换,即微生物向外界环境释放和从外界环境获取电子的过程。目前发现电活性微生物近上百种[18],主要可分为可释放电子的产电微生物 (Exoelectrogens)和可直接从电极获取电子并转化为胞内还原力的亲电微生物 (Electroautotrophic bacteria) 两大类。由于电活性微生物的胞外电子传递效率低,这些微生物电催化系统普遍存在效率低下的缺点,距离实际应用对电催化效率的要求相去较远,已成为限制其应用的主要瓶颈。随着合成生物学技术的引入,设计重构与功能强化电活性微生物,以突破胞外电子传递效率低这个关键技术瓶颈,将加速微生物电催化系统的产业化发展进程。
本综述围绕利用合成生物学改造非电活性细胞为电活性微生物、拓宽电活性微生物可利用的碳源谱、强化电活性微生物代谢活性、合成可溶性电子传递载体、提高胞内还原当量 (可释放的电子源泉),以及构建介观多细胞自更新活性生物膜提高“电极-细胞”间的电子跨膜传递速率,系统综述了近5年左右国际上在改造双向电子传递途径方面的进展。
1 电活性微生物的双向电子传递的分子机制
目前为止,电活性微生物和电极间的3种电子传递机制获得人们的广泛认可 (图1A):即直接的电子传递 (微生物在形成厚实的生物膜后,通过自身的细胞色素或导电鞭毛实现与电极间的直接接触导电)、电子传递介质介导的电子传递 (微生物通过自身分泌的氧化还原电子传递介质实现和电极间的电子交换) 和间接的电子传递机制 (微生物通过自身代谢物如氢气、甲酸实现和电极间的电子交换)[19-21]。在产电微生物的“放电”过程中,由底物氧化释放的电子,按照电子传递链中血红素蛋白氧化还原电位由低到高的顺序,跨膜传递到胞外电子受体上。一系列串联的血红素蛋白,所表现出的重叠电势确保了电子能顺利地传递到胞外[20]。在模式产电微生物,如希瓦氏菌和泥菌中,主要通过生物膜 (厚达100 μm) 上的型-细胞色素 (由多种不同电势血红素蛋白组成) 进行直接电子传递,并通过自身合成的核黄素等氧化还原导电介质进行电子传递[22]。此外,和还可以利用自身的细胞附属物“纳米天线”——导电鞭毛进行远距离电子传递[23-25]。在生物电化学系统中,生物膜形成的速度、厚度和形态决定了直接电子传递的效率[26-27]。然而,在电子传递介质介导的电子传递中,产电微生物自身分泌的可溶性的氧化还原性分子或可溶性离子,可以通过自身的氧化还原再生来完成胞外远距离的电子传递。产电微生物可以分泌多种可溶性的氧化还原性分子,如奥奈达希瓦氏菌分泌的黄素 (核黄素和黄素单核苷酸)[28]、绿脓假单胞菌分泌的吩嗪[29]、枯草芽孢杆菌分泌的核黄素和克雷伯氏菌分泌的醌类[30]等。而间接的电子传递指产电微生物利用自身代谢物 (氢气、甲酸等) 来完成的胞外电子传递过程[3]。
相对于产电微生物的胞外电子传递机制被科学家们研究得较透彻,人们对亲电微生物的“充电”过程,即细胞从电极直接摄入电子的机制则研究得非常有限。亲电微生物从外界电极获取电子的机制主要也包括通过自身的细胞色素或导电鞭毛实现与电极间的直接摄取电子、通过自身分泌的氧化还原完成的电子介质介导传递和微生物通过胞外的氢气、甲酸、Fe2+或 NH3等完成的间接电子传递3种方式[19](图1B)。电子的流出和进入是否经由相同的途径进行传递完成电子由胞外跨膜传递到胞内的过程,还没有被系统阐明。进入细胞的电子被进一步转化为胞内还原力 (NADH或NADPH),可以用于固定CO2或催化产物合成[21]。
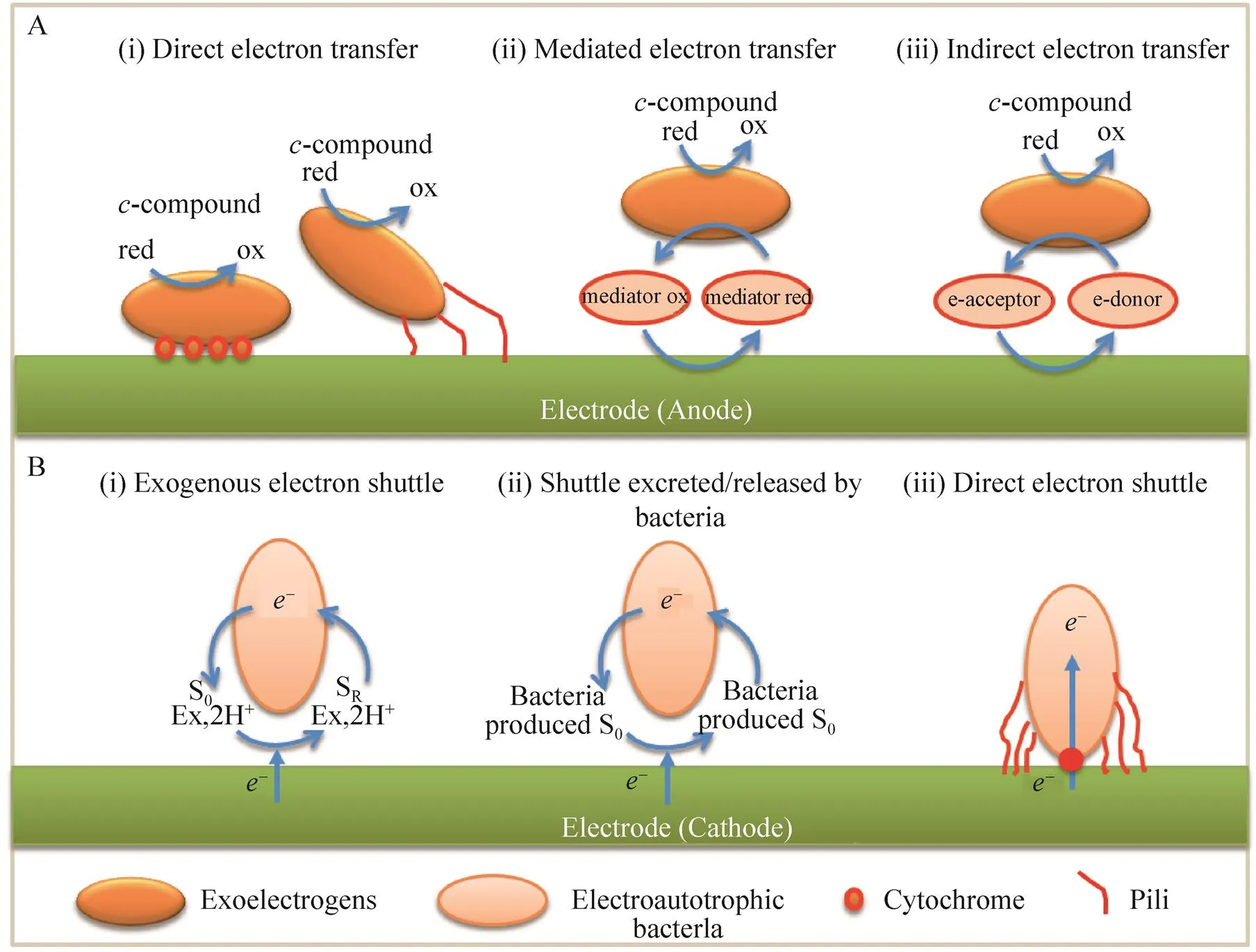
图1 电活性微生物的双向电子传递机制[19,21]
2 利用合成生物学改造电活性微生物
2.1 利用合成生物学改造非产电微生物为产电微生物
作为创造新生命的工具,合成生物学已经被用来构建新的产电微生物。加州大学劳伦斯伯克利国家实验室的Ajo-Franklin课题组在埃希氏大肠杆菌中,异源表达了的胞外电子传递色素蛋白 (CymA、MtrA、MtrB、MtrC),重构了胞外电子传递路径 (CymA-MtrCAB)[31],成功地将改造成产电微生物。所构建的产电可还原可溶的的金属Fe3+离子和无机固体氧化物α-Fe2O3,其还原速度较原菌分别提高了8倍和4倍。其后期研究结果显示,在表达有MtrCAB色素系统的大肠杆菌中继续表达CymA蛋白或添加核黄素可促进大肠杆菌的胞外电子传递和细胞生长[32]。导入MtrCAB-CymA色素系统的大肠杆菌输出电流提高了8倍,电流的输出虽然没有影响到细胞生长和底物消耗,但对代谢流的分布产生影响,更有利于氧化型产物的生成[33]。
Yong等[34]也在改造大肠杆菌产电方面进行了研究,在大肠杆菌中异源表达的合成“孔蛋白”基因,显著增加了大肠杆菌的细胞膜通透性 (图2A),减少了电子传递介质的传递的阻力,使电子传递介质能自由穿梭细胞膜,从而使每个细胞的电催化性能获得有效提升,提高了胞间电子跨膜传递速率,成功地将非产电微生物改造为产电微生物,揭示了电子传递介质在电活性细胞内外的传递阻力是限制胞外电子传递速率的重要步骤。同时,Yong等[35]通过敲除大肠杆菌中合成乳酸的乳酸脱氢酶基因,重定向胞内可释放电子,释放了存储在乳酸等中间代谢物中的电子 (图2B);通过敲除三羧酸循环 (TCA) 的抑制基因,解除了Arc系统对TCA代谢通量的抑制调控,增加了TCA循环中多个核心酶的表达量,加快了TCA的代谢流,提高了胞内释放电子池 (NADH) 浓度,增加胞内可释放电子总量 (图2C)[36]。从而显著提高了大肠杆菌的胞外电子传递能力,成功将非产电的大肠杆菌理性改造成为有一定胞外电子传递能力的产电微生物。
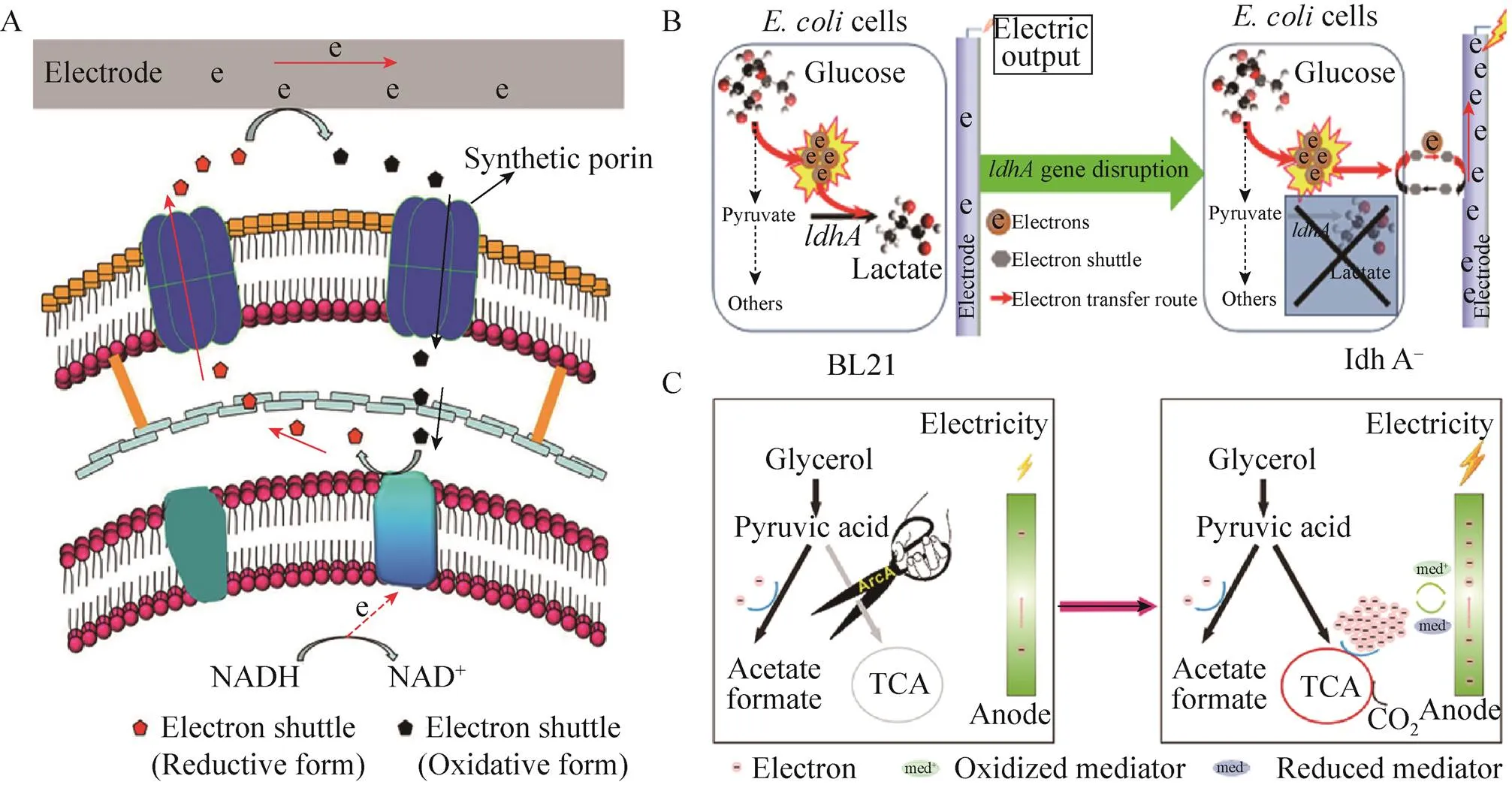
图2 合成生物学改造非产电微生物为产电微生物[34-36]
Schmitz等[37]在恶臭假单胞菌中导入合成绿脓菌素的全部基因簇,使得严格耗氧的恶臭假单胞菌在低溶氧条件下能够合成吩嗪,并利用吩嗪作为电子介质和电极进行电子传递和能量交换,将严格好氧且不能进行胞外电子传递的恶臭假单胞菌成功改造成可以利用电极进行厌氧呼吸的产电菌。有效地解决了恶臭假单胞菌在工业上进行大规模发酵时,因加大溶氧而导致的发酵罐起泡问题。这些通过合成生物学成功将非电活性微生物改造为电活性微生物的手段有可能推动微生物电催化技术的工业化发展。
2.2 利用合成生物学改造产电微生物
结合合成生物学的多基因表达调控策略,近几年在强化产电微生物的底物摄取范围和速度、提高胞内可释放电子池浓度、增强细胞间电子传递介质的合成和构建导电活性生物膜等方面的改造取得了重要进展。不仅阐明了合成生物学如何打破产电微生物胞外电子传递途径的瓶颈,实现产电微生物与环境的高效电子传递和能量交换,也推进电活性微生物电催化系统的实用化进程。
2.2.1 利用合成生物学提高底物摄取范围和速度
产电微生物的底物 (电子供体) 摄取范围和利用能力是限制其胞外电子传递能力的重要因素。底物的氧化摄取速度受到可用于运输底物的蛋白种类、运输需要的能量ATP和可用的酶种类等生物因素控制。研究人员利用自适应性进化和重定向筛选等非合成生物学策略成功地拓宽了产电微生物的底物摄取范围;如Sekar等通过一年多的自适应进化策略,激活了希瓦氏菌的木糖利用能力,使得可以利用木糖生长产电[38]。而理性定向的合成生物学策略不仅可以特定地拓宽产电微生物的底物利用范围还能加快其底物摄取速度。如在中表达负责甘油和葡萄糖摄取的蛋白和相应代谢酶类来拓宽底物的摄取范围,使得希瓦氏菌在厌氧和有氧条件下能够利用甘油或葡萄糖作为唯一的碳源和电子供体[39-40]。此外,由于厌氧条件下胞内的乳酸一直受限于缺少足够质子动力势的推动而吸入缓慢,Johnson等在中异源引入藻类的光合质子泵系统[41],加快了ATP的合成及底物乳酸的吸收速度,提高了电流输出,加快了细胞生长。这些研究显示了通过增加底物的摄取范围或速度可以有效地提高电子传递通量。
另一方面,为了克服产电菌可用的碳源谱过窄的限制 (如仅能利用乳酸为碳源),Yang等[42]利用合成生物学改造和混菌互利共生来实现混菌共培养,构建了以木糖为底物的“发酵菌-产电菌”混菌产电生态系统 (图3A)。在大肠杆菌 (发酵菌) 中导入合成核黄素的代谢模块,使其可以以木糖为碳源高产电子传递介质 (核黄素),提高了希瓦氏菌 (产电菌) 的胞外电子传递效率,同时大肠杆菌的代谢副产物 (乳酸、甲酸等) 可以进一步作为希瓦氏菌的电子供体和碳源;同时进一步改造希瓦氏菌的细胞壁极性,增强产电菌和电极的疏水性作用,显著增强-型细胞色素介导的直接接触胞外电子传递的能力。而最近Lin等[43]通过敲除酿酒酵母(发酵菌) 乙醇合成途径,使前体物更多流向乳酸生成方向来促进乳酸的生成。利用酿酒酵母降解葡萄糖高产乳酸,间接地为希瓦氏菌提供碳源和电子供体。此外,进一步改造希瓦氏菌,提高其细胞膜的电子传递介质通透性和细胞疏水性,促进产电细胞和电极间的紧密结合。成功构建了以葡萄糖为底物的混菌产电生态系统 (图3B)。所构建的“发酵菌-产电菌”混菌产电生态系统,不仅解决了单一产电菌仅能利用非常有限的碳源 (乳酸和乙酸) 这一限制微生物电催化系统使用范围的重要问题,同时也进一步解释了现实生态环境中不同电活性微生物互相分享彼此的电子传递介质,提供自身产物作为其他电活性细胞底物的种群互利现象。
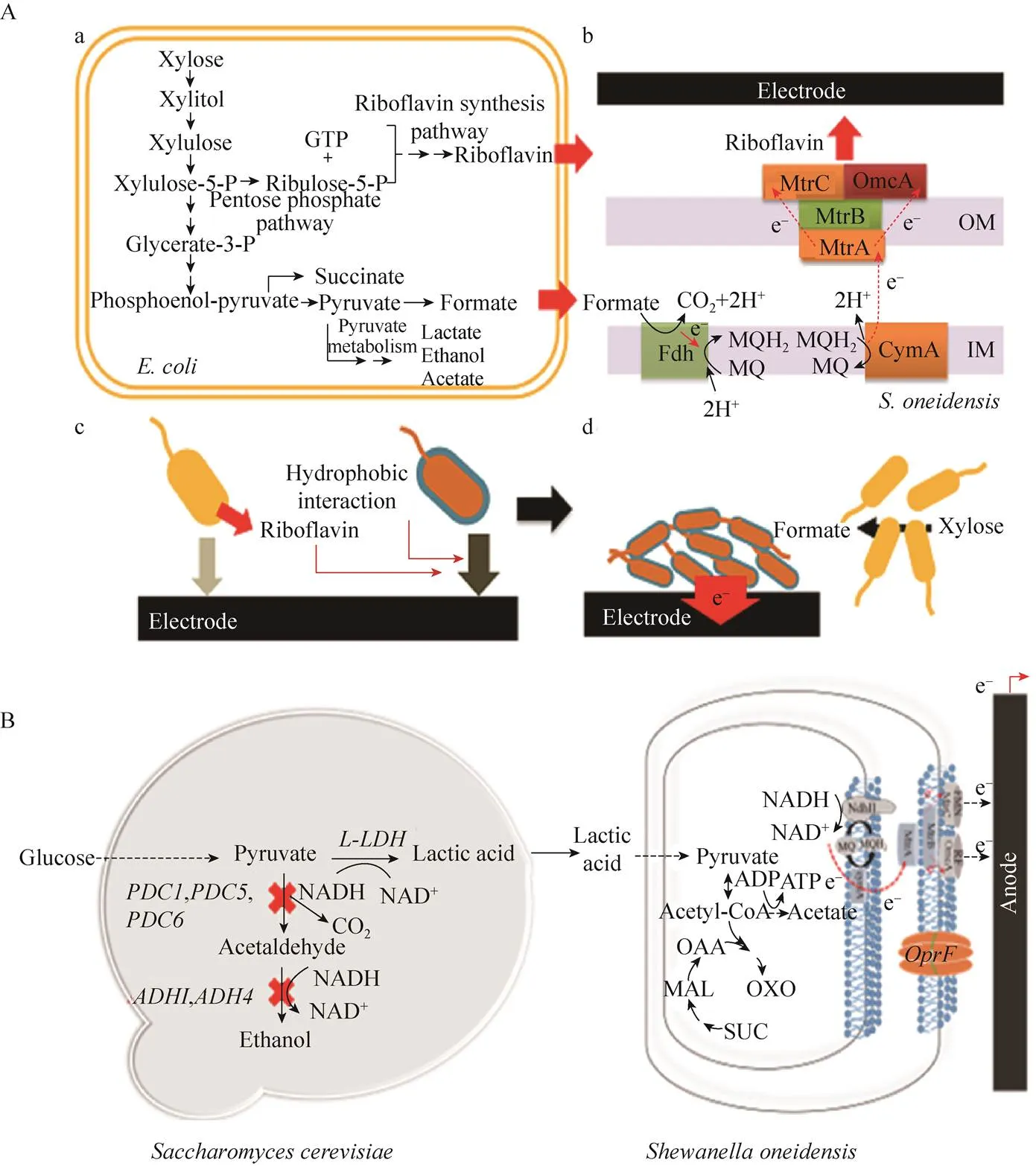
图3 合成生物学改造产电微生物的底物利用范围[42-43]
2.2.2 利用合成生物学提高胞内可释放电子池浓度
产电微生物的胞内电子池容量大小 (即电子载体NAD(H/+)总量和NADH/NAD+的比例) 是决定其所能释放电流大小的根本因素。NADH/NAD+的比例受到胞内辅因子合成模块的代谢通量和胞内氧化还原状态的直接影响。在提高产电微生物的胞内电子池,Yong等[44]通过表达中NAD+合成酶基因,提高了胞内的电子池NAD(H/+)总量的同时也促进胞内电子传递介质绿脓菌素的合成,二者协同作用提高了单个细胞的电催化活性,促进了的胞外电子传递效率;Han等[45]通过在梭状芽孢杆菌中异源表达甲酸脱氢酶基因,改变了胞内的氧化还原状态,促进了胞内还原力的生成,提高了内NAD(H/+)总量和NADH/NAD+的比值,拓宽了胞内可释放电子池的同时提高了胞内还原当量,在单细胞水平上揭示了胞内可释放电子池的形成和积累是决定细胞胞外电子传递通量的速控步骤,阐明了胞内代谢决定了胞外电子传递能力的分子机制。这些电活性微生物改造策略直接导致了胞外电子传递通量和单细胞产电能力的大幅提高,揭示了胞内可释放电子池的浓度与胞外电子传递速率存在正相关关系。
2.2.3 利用合成生物学改造胞间电子传递介质
产电微生物通过自身特有的胞外电子传递链将胞内代谢释放的电子传到细胞外,然后通过直接接触导电或自身分泌的电子传递介质间接将电子传递到胞外电子受体上。据统计,在可以分泌电子传递介质的产电微生物体内,以可溶性的氧化还原性分子或电容性粒子介导的电子传递是最主要的胞外电子传递方式,其输送的电量占总电量的70%−90%[46]。因此,电子传递介质的合成与传递是决定胞外电子传递速率的根本因素。利用合成生物学改造产电微生物胞内可溶性电子传递介质 (核黄素、吩嗪和醌类) 的合成和传递,可以较大地提高产电微生物的胞外电子传递速率。
众所周知,主要依赖于核黄素进行远距离胞外电子传递,而其自身所能合成的核黄素量又极低。为解决这一限制胞外电子传递的主要因素,Yang等[47]通过合成生物学的多基因表达策略,将枯草芽孢杆菌中编码核黄素合成的核心基因簇 () 引入希瓦氏菌中,改造后的经IPTG诱导表达后,黄素 (核黄素和黄素腺嘌呤二核苷酸) 产量获得显著提高 (25.7倍),直接提高了电子传递介质介导胞外电子传递效率。核黄素含量的提高又进一步促进了希瓦氏菌在电极表面生物膜的形成,间接地提高了-细胞色素和纳米天线直接介导的电子传递效率。生物电化学实验结果显示,核黄素合成模块的成功引入,分别从单个细胞导电水平的提升和电极上附着的生物量增多两个角度来显著提高产电细胞的双向电子传递性能,使得电子进入细胞和传出细胞的速度各自提高13.2和15.5倍 (图4),成功揭示了可以通过合成生物学手段来改造用于电合成的亲电极微生物,提高亲电微生物的电子摄取速率,为电合成的菌株开发指明方向。Yong等[48]通过精确调控“群体感应系统”中的关键调控基因和的表达,促进了中吩嗪-1-羧酸和绿脓菌素等电子介质的合成,促进了电子传递介质介导的胞外电子传递,使得的胞外电子传递效率提高了1.6倍。为进一步提高的电子传递效率,Yong等[29]又通过直接表达绿脓菌素合成相关的甲基转移酶基因,显著提升了绿脓菌素的合成量,进一步促进了胞外电子传递效率的提高[27,44],上述实验结果表明电子传递介质在电活性细胞内外的传递阻力是限制胞外电子传递速率的重要步骤。
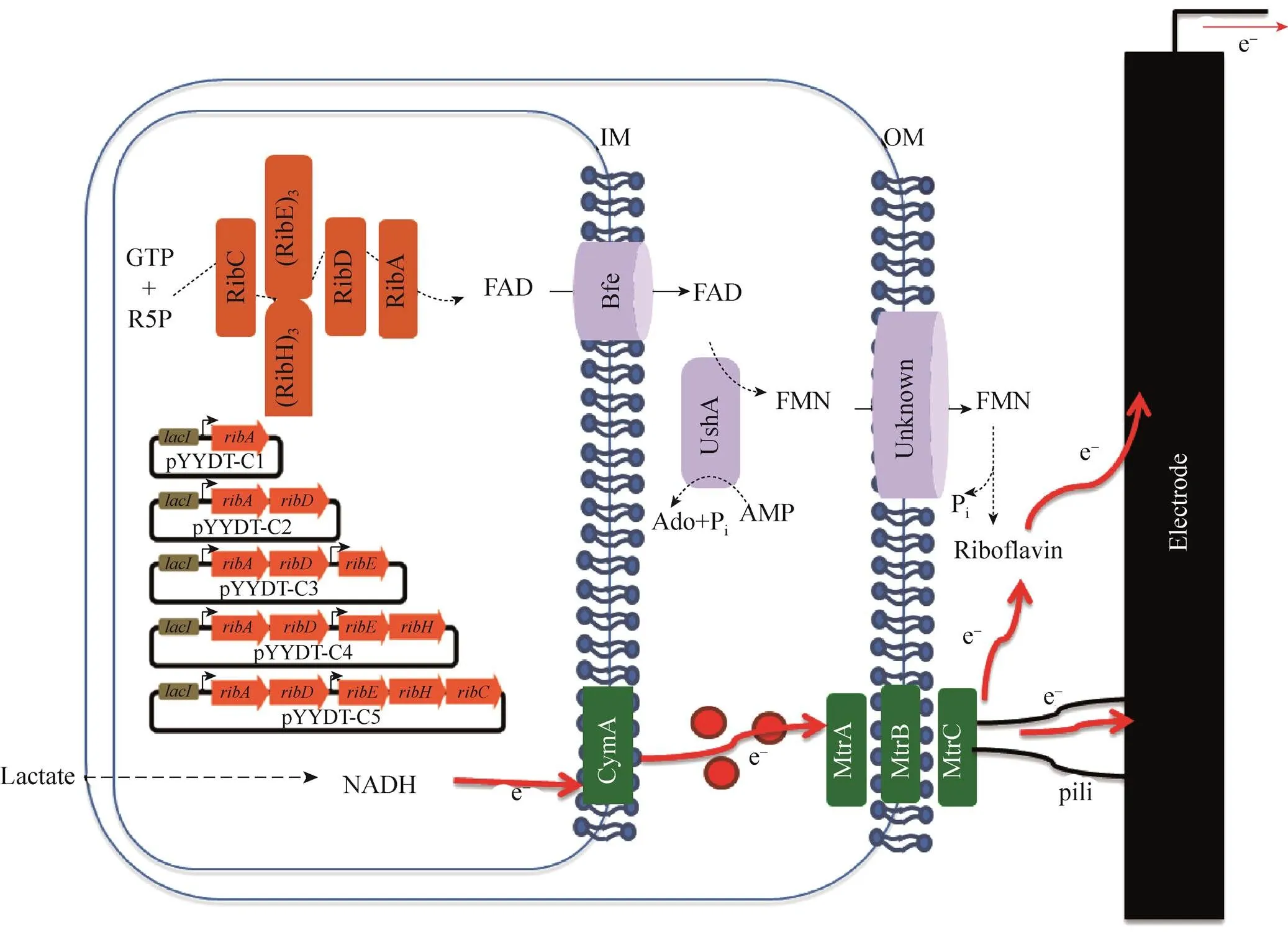
图4 改造产电微生物的胞间电子传递介质
2.2.4 利用合成生物学改造电活性生物膜
微生物分泌的黏附素、多糖、蛋白和DNA等聚合物导致细胞间相互交联形成的导电细胞群体,即生物膜[49]。微观研究表明,生物膜的形成是一个包括初始期、形成期、成熟期、稳定期和分解期的稳定循环过程[27]。产电性微生物生物膜的形成受电极材料、环境条件和生物膜自身的厚度影响。此外,外膜型细胞色素系统和群体感应系统也在产电微生物 (、和) 的生物膜形成中也起着重要的作用。在电催化系统中,高活性的生物膜往往更有利于电子的传递。而野生型产电微生物的生物膜普遍厚度较薄,包含的细胞量较小,不利于电子的传递。因此,生物膜的形成是限制胞外电子传递效率的重大挑战。
Liu等[51]在中分别通过诱导和组成型两套方案异源表达了大肠杆菌中用于合成第二信使分子 (c-di-GMP) 的二鸟苷环化酶基因,改造后的细胞生长状况和野生型相当,但在有氧和厌氧条件下,经电镜观察,极易在电极表面形成更加致密的电活性生物膜。致密的生物膜显著地增强了以型细胞色素介导的直接胞外电子传递效率,同时也促进了以核黄素为电子介质的间接胞外电子传递效率。首次揭示生物膜的细胞量与产电效率呈线性关系,为采用合成生物学方法与纳米生物技术方法提高电催化效率的设计策略奠定了理论基础。Nguyen等[50]开发的自组装生物功能材料平台,可用于改造电活性微生物的生物膜结构,让细胞的表面布满“导电鳞甲”,为整体提高产电微生物胞外电子的传递性能,甚至亲电微生物的电子摄取能力提供理论可能。生物膜的形成不仅有助于电活性微生物与电极之间的电子传递,也将较大地推动双向电子传递 (即电子进、出细胞) 效率,这一限制微生物燃料电池和微生物电合成关键科学问题的解决。
2.3 工程化产电微生物的应用
以产电微生物为主导的微生物电催化系统,作为一种新型的绿色新能源生产方式在环境、能源领域方面获得广泛应用,如用于废水处理、生物冶金、土壤修复、环境监测、生物计算和生物传感器方面的微生物燃料电池 (MFC),用于生物制氢、海水淡化和卤素还原的微生物电解电池 (MEC)。而最近产电微生物在非平衡发酵产高附加值化学品、生物计算和生物传感器等方面也扮演越来越重要的角色。
2.3.1 非平衡电发酵应用
非平衡电发酵[4,39,52-53]是一种由产电微生物的胞外电子传递特性——依靠胞外电极 (阳极) 进行无氧呼吸演变而来的全新发酵模式,实现了利用胞外能量代谢“拉动”胞内物质代谢的发酵过程,在厌氧条件下,通过将胞内过剩的还原力转化成电子释放到胞外电极来调控胞内的氧化还原平衡,提升底物降解速度的同时减少副产物的生成,提高产物产率的同时也回收部分电能。为加快厌氧条件下利用甘油产乙醇的速率和产率,Flynn等[39]在体内引入来自大肠杆菌的甘油代谢模块和运动假单胞菌乙醇生成模块,结合自身的胞外电子传递机制,将胞内过剩的还原力释放到胞外电极上,调节了胞内氧化还原平衡,较大地提升了底物甘油的降解速度,缩短发酵周期;同时降低副产物乙酸的生成量,提高产物乙醇的产率和纯度,实现产电微生物利用甘油产高纯度乙醇的非平衡电发酵模式。
Sturm-Richter等[52]利用改造的大肠杆菌和甲烷杆菌构建出混菌共培养的非平衡电发酵模式。首先在大肠杆菌中引入的胞外电子传递路径,将大肠杆菌改造成可进行胞外电子传递的模式发酵菌;然后结合甲烷杆菌共发酵来降解副产物甲酸产甲烷和CO2,减弱底物抑制,加快底物降解。所构建的混菌非平衡发酵模式有效地提高了厌氧条件下甘油产乙醇的发酵速率和产率。Speers等[54]则利用同为严格厌氧的电活性微生物和进行混菌共培养,非平衡发酵甘油产乙醇,的代谢副产物乙酸可以作为的电子供体和碳源,由此来降解副产物抑制,拉动底物降解。由于电活性微生物罗尔斯通真氧产碱菌在氮饥饿、TCA循环或有氧呼吸受抑制等生长受抑制的状态下能合成聚羟基丁酸酯 (PHB),为维持菌株处于氮饥饿的生长抑制状态,Nishio等[53]利用胞外电极替代可以引起氮饥饿解除的硝酸盐作为电子受体,加速了果糖非平衡发酵产PHA的速率。此外,Zhu等[55]通过添加胞外电极和胞间电子传递介质,将丙酸梭菌胞内过剩的NADH变成电子释放到胞外,抑制了丙酰辅酶A脱氢酶的活性,阻断了丙酰辅酶A向丙酸合成的方向转化,促使大量积累的丙酰辅酶A向附加值更高的丙烯酸转化,减少了副产物丙酸的生产,提高了l利用乳酸产丙烯酸的产率。
2.3.2 生物计算和生物传感器应用
合成生物学改造胞外电子传递链的工作主要在生物传感器和生物计算中获得重要应用。Hu 等[17]通过理性重构细胞内的“基因电路”,选择和优化启动子和核糖体结合位点,实现转录、翻译水平上对希瓦氏菌的胞外电子传递基因的精准调控,构建了AND“逻辑门”控制的智能可控型MFC,这种生物电信号输出可能成为设计生物电化学传感器和生物智能计算的有效输出信号 (图5A)。同上,Li等[56]以lasI/rhlI 突变的为底盘,构建了基于QS系统双信号分子控制的AND “逻辑门”智能型MFC (图5B)。Webster等[15]通过利用氧化砷敏感型启动子控制希瓦氏菌胞外电子传递链的表达,构建了可以检测到环境中浓度极低的氧化砷智能微生物传感器,其在环境监测和污染物防控中获得重要推广。Franks等[16]基于合成生物学方法,提出将可以进行光和电等可视化胞外输出的微生物和可以还原重金属离子的微生物传感器结合,构建出可以快速、高效检测环境中重金属离子的微生物传感器。因此利用合成生物学改造电活性微生物的电子传递链可以用于环境生物传感器开发,尤其在有毒污染物高度特异性检测方面的潜在应用。
2.4 利用合成生物学改造亲电微生物
近几年,电合成因具有直接以CO2为原料、能量转换较光合作用效率更高 (10−100倍以上)、电能来源多样 (如风电、光伏发电) 等优势,微生物电合成的出现使得利用亲电微生物合成高附加值化学品成为目前研究的热点。微生物电合成指亲电微生物利用难并网的电能来固定还原CO2或者低还原度的化合物生产高附加值电燃料和化学品的生物催化过程。然而,由于不同亲电微生物的具体电子进入机制目前尚未研究清楚,按照电子进入细胞的方式不同,大致可将电合成分为直接摄取电子电合成、电子介质介导摄取电子的电合成和间接摄取电子电合成。相对于产电微生物的被广泛改造,利用合成生物学改造亲电微生物的只有[57-58]和MR-1[59]两种。
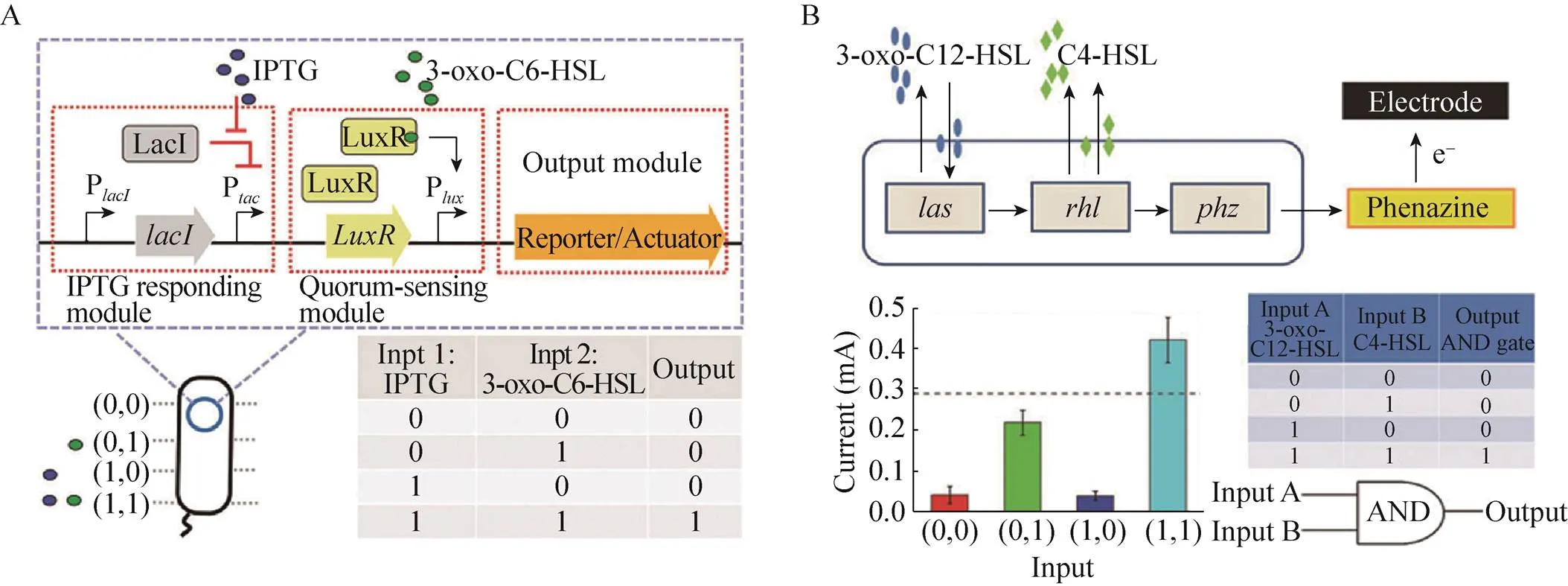
图5 产电微生物在生物计算和生物传感器应用[17,56]
2.4.1 基于直接摄取电子的微生物电合成
虽然产电微生物和因特有的“异化金属还原路径”能够还原固体金属氧化物而被人类广泛研究,但最近研究表明它们也可以通过自身的型细胞色素系统从电极上直接摄取电子。为了扭转和的胞外电子链的传递方向,使其能够用于电合成高附加值化合物,Bond等[60]给MR-1施加–0.36 V电压,电子可以直接通过MtrCAB路径跨过细胞外膜和周质空间逆流到细胞内膜的甲基萘醌池内,并进一步返流到细胞周质空间还原延胡索酸合成琥珀酸。最近,Jeon等[59]在MR-1中异源表达了异丁醇合成路径 (Ehrlich pathway) 的酮基异戊酸脱羧酶基因和乙醇脱氢酶基因,直接以电极为电子供体,促进了异丁醇产量的提高 (19.3 mg/L)。Soussan等[61]发现可以通过自身的型细胞色素介导,直接从阴极表面摄取电子还原CO2和琥珀酸生产甘油。
目前发现的亲电微生物,大多数都以直接摄取电子的方式从电极上获得电子。Nevin等[65]发现一些自养型的亲电微生物 (梭菌、鼠孢菌和热醋穆尔氏菌等产乙酸菌) 因具有高效还原CO2的Wood–Ljungdahl路径和直接从电极获得电子的能力,可以直接利用电子还原CO2产乙酸、甲酸和2-羰基丁酸等高附加值化合物。其中,Choi等[66]发现巴氏梭菌可以直接从电极上摄取电子来促进丁醇和1,3-丙二醇的产量。Nevin等[62]利用太阳能电池板接受太阳能转化来的电能,让直接利用电子固定CO2为乙酸。在此基础上,近两年UC-Berkeley的杨培东课题组通过构建亲电微生物与无机催化剂相结合 (–CdS)的“人工光合叶片”系统,直接将光能转化为电能来固定CO2合成高附加值化学品[63,67-68]。Valdes等[69]发现嗜酸氧化亚铁硫杆菌可以直接依靠氧化Fe2+和S2–释放的电子固定CO2和N2。此外,Gong等[64]发现产甲烷菌可以直接从电极上获得电子还原CO2产甲烷。Gong等构建的混菌电合成体系,利用阳极的H2S作为电子供体 (降解H2S为SO42–释放出8个电子),来给阴极的提供还原力,从而固定CO2合成有机物。其在阳极处理含硫废水的同时完成了阴极CO2还原,120 h内库伦效率达90%,展示了一定工业应用前景。
2.4.2 基于电子载体介导的摄取电子微生物电合成
大量的研究工作显示,一些人工的氧化还原电子传递介质 (甲基紫 (MV)、中性红 (NR)、二磺酸蒽醌 (AQDS)) 具有很强的氧化还原活性,可以促进微生物从电极上摄取电子,提高电合成的效率[22]。其中MV因进不去细胞内膜只能在周质空间发生电化学反应。其标准化学电动势和H2接近,可以作为氢化酶的氧化还原伴侣,用于H2的生产和氧化研究[70-72]。最近的研究显示,还原型的AQDS也可以用于提高拜氏梭菌的H2产量[73]。不同于MV的作用机制,中性红 (NR) 通过紧贴到微生物细胞膜上,和胞内的NAD+或延胡索酸还原酶发生氧化还原反应来加快电子的摄取速度[74-75]。Choi等[76]发现MV和NR可以促进酪丁酸梭菌的丁酸产率提高,并进一步揭示了MV是通过间接提高电子从铁氧还原蛋白池到NADH池的速度,而NR是通过直接加快电极上电子到NADH池的流速,来改变胞内可用NADH的浓度来提高丁酸的合成。此外,一些亲电微生物自身分泌的电子氧化还原传递介质 (如spp. 合成的吩嗪和合成的核黄素) 也可以加快电子的摄取效率。这些自身合成电子传递介质优点在于:同一种电子传递介质可以被多种亲电微生物使用;它们可以在周质的多个位点 (细胞周质空间和细胞质内) 进行电子传递反应。Aulenta等[77]发现脱卤拟球菌spp. 可以分泌一种类似氰钴胺素 (维生素B12) 的导电介质,来提高细菌从阴极摄取电子和自身生长的速度,促进三氯乙烯的脱氯过程。Boussicault等[78]发现来自细胞裂解或者胞外DNA降解的单个嘌呤和嘧啶碱基也可作为电子介质促进阴极电子的摄取。总之,上述例子不仅有助于解释亲电微生物摄取电子传递机理,更提供了一种新的调控亲电微生物的生长、代谢和电合成的策略。
2.4.3 基于间接摄取电子的微生物电合成
作为首个被用来工程化的亲电微生物,已被广泛用于电合成研究。因其不能直接从电极上摄取电子,UCLA的Liao[58]和Harvard的Nocera等[57]分别将电子转换成甲酸和氢气等可接受的电子供体形式,然后再利用工程化的来固定CO2电合成生物燃料。其中,Liao等[58]分三步完成系统设计:1) 首先改造:在敲除的PHB合成路径相关基因 (、、、和) 的基础上,继续在缬氨酸合成路径上异源表达的乙酰醇酸合成酶基因,的酮醇酸还原异构酶基因和二羟酸脱水酶基因,在异丁醇合成路径上表达中的酮基脱羧酶基因和中的乙醇脱氢酶基因,改造获得1株可以单独利用氢气或甲酸作唯一能源发酵产生物燃料的工程菌LH74D。 2) 通过电化学系统将电子和CO2转化兼具碳源和电子供体属性的甲酸。3) 工程菌LH74D在100 h内可以利用阴极生产的甲酸为唯一的碳源和能源进行生长,合成浓度为140 mg/L的生物燃料。同上,Nocera等[57]在敲除的PHB合成路径关键基因和的基础上,同源表达编码酮基硫解酶基因和乙酰乙酰基辅酶A转移酶基因,异源表达来自sp. 的基因乙酰乙酸脱羧酶和乙醇脱氢酶,使得乙酰辅酶A重定向于合成异丙醇,构建得到可以成功利用CO2和H2进行生长的工程菌Re2133-pEG12。然后利用无机催化剂磷酸钴电解水产生的H2为其提供还原力固定CO2,合成的异丙醇浓度高达216 mg/L。以上这些将合成生物学成功应用于开发高效亲电微生物的案例表明,工程化的高效电活性微生物已经成为微生物电催化技术的核心部件,将为未来电合成微生物的改造起到重要参考作用。
3 基因组工具箱开发
基因组工具箱是未来研究电活性微生物怎样和环境进行电子交换,以及设计优化电活性微生物为人类服务的基础。过去十年,人类已经完成了电催化模式细胞和的测序工作,极大方便了人们对电子传递分子机制的理解和相关代谢模块的设计和研究。例如,Fredrickson[79]总结了的传感、调控、代谢系统,并用动力学模型对其生长、底物消耗和产物的分泌进行了详细描述。但相关基因工具箱的缺乏仍旧限制了人类对电活性微生物的开发和探索速度。相对于模式产电菌和,其他的电活性微生物可用的基因工具则更少。如[80]虽然已经可以利用其基于基因测序获得的代谢模块,但有关其合成生物学改造的文献却很少。最近,的遗传转化和异源表达系统开发成功[81],其基因组序列的进一步公开加快了其工程化的可能性。此外,由于受限于可操作的基因工具数量(双质粒系统的开发),关于只有相关基因组序列可知。可用的基因工具是深入研究细胞代谢和胞外电子传递的基础。然而,大多已描述的胞外电子传递路径并未被详细阐明,尤其是关于电子如何进入电活性微生物进行电合成的机制仍存有异议。因此,作为限制进一步探索和挖掘电活性微生物的瓶颈,在电活性微生物中开发高效的基因组编辑工具 (如CRISPR-Cas9[82]、sRNA[83])、新的DNA组装方法 (Gibison大片段重组[84])、快捷准确的DNA从头合成方法来丰富合成生物学基因组编辑工具箱,是突破现状和进一步深入研究和改造电活性微生物为人类服务的重要手段。
4 前景展望
过去几年中,随着人类对胞外电子传递机制理解的不断加深,以及电活性微生物在生物产电、生物产氢、CO2固定和化学品生物电合成等领域的不断应用,使得微生物电催化逐渐发展成为一个新兴的生物技术。但如下几个主要科学及技术瓶颈仍极大限制着微生物电催化系统的产业化应用:1) 电活性微生物较低的电子传递效率和电催化活性 (细胞摄取和利用电子的能力较低、CO2固定和转化效率低、过电势高) 仍然难以满足工业需求。比如,虽然由于测序的完成以及基因工具的不断开发,推进了sp. 在合成气发酵中的研究[85-86],但对电合成时sp.电生理、电催化的分子机制尚缺乏深入研究。2) 对大多数电活性微生物在产电和电合成过程中,胞外电子传递和摄取的机制仍旧不清晰[87-88],比如,对导电菌毛蛋白纳米线和生物膜的电子传递机制仍存在较大争议[24,89-91],从而较难实现提高电子传递效率的理性设计。3) 针对非模式的电活性微生物不断被发现,但对其电活性生理及物质、能量代谢的分子机制缺乏系统理解,同时能用的代谢工程和合成生物学工具仍然非常有限,急需系统开发改造这些电活性微生物基因组水平的调控和编辑工具。
展望未来,要创造出工业可用的高效电活性微生物,促进电活性微生物的产业化应用获得更快的发展,我们将在以下几个方面进行深入研究:1) 深入研究电活性微生物的电子传递路径及其调控、组装分子机制,从而不断提高电活性微生物的胞外电子传递通量和效率。2) 研究电活性微生物的物质和能量代谢的耦合关系,使电子能定向高效合成特定产物。3) 不断扩充现有的合成生物学工具箱、寻找新的可进行基因组编辑的电活性微生物。
[1] Logan BE. Exoelectrogenic bacteria that power microbial fuel cells. Nat Rev Microbiol, 2009, 7(5): 375–381.
[2] Lovley DR. Bug juice: harvesting electricity with microorganisms. Nat Rev Microbiol, 2006, 4(7): 497–508.
[3] Rabaey K, Rozendal RA. Microbial electrosynthesis —revisiting the electrical route for microbial production. Nat Rev Microbiol, 2010, 8(10): 706–716.
[4] Moscoviz R, Toledo-Alarcón J, Trably E, et al. Electro-fermentation: how to drive fermentation using electrochemical systems. Trends Biotechnol, 2016, 34(11): 856–865.
[5] Schievano A, Sciarria TP, Vanbroekhoven K, et al. Electro-fermentation—merging electrochemistry with fermentation in industrial applications. Trends Biotechnol, 2016, 34(11): 866–878.
[6] Xie X, Ye M, Hsu PC, et al. Microbial battery for efficient energy recovery. Proc Natl Acad Sci USA, 2013, 110(40): 15925–15930.
[7] Liu XW, Li WW, Yu HQ. Cathodic catalysts in bioelectrochemical systems for energy recovery from wastewater. Chem Soc Rev, 2013, 43(22): 7718–7745.
[8] Mehanna M, Kiely PD, Call DF, et al. Microbial electrodialysis cell for simultaneous water desalination and hydrogen gas production. Environ Sci Technol, 2010, 44(24): 9578–9583.
[9] Luo HP, Jenkins PE, Ren ZY. Concurrent desalination and hydrogen generation using microbial electrolysis and desalination cells. Environ Sci Technol, 2011, 45(1): 340–344.
[10] Lovley DR, Nevin KP. Electrobiocommodities: powering microbial production of fuels and commodity chemicals from carbon dioxide with electricity. Curr Opin Biotechnol, 2013, 24(3): 385–390.
[11] Choi O, Sang BI. Extracellular electron transfer from cathode to microbes: application for biofuel production. Biotechnol Biofuels, 2016, 9: 11.
[12] Li H, Liao JC. Biological conversion of carbon dioxide to photosynthetic fuels and electrofuels. Energy Environ Sci, 2013, 6(10): 2892–2899.
[13] Sadhukhan J, Lloyd JR, Scott K, et al. A critical review of integration analysis of microbial electrosynthesis (MES) systems with waste biorefineries for the production of biofuel and chemical from reuse of CO2. Renew Sust Energ Rev, 2016, 56: 116–132.
[14] Heijne AT, Liu F, van der Weijden R, et al. Copper recovery combined with electricity production in a microbial fuel cell. Environ Sci Technol, 2010, 44(11): 4376–4381.
[15] Webster DP, TerAvest MA, Doud DFR, et al. An arsenic-specific biosensor with genetically engineeredin a bioelectrochemical system. Biosens Bioelectron, 2014, 62: 320–324.
[16] Bereza-Malcolm LT, Mann G, Franks AE. Environmental sensing of heavy metals through whole cell microbial biosensors: a synthetic biology approach. ACS Synth Biol, 2015, 4(5): 535–546.
[17] Hu YD, Yang Y, Katz E, et al. Programming the quorum sensing-based AND gate infor logic gated-microbial fuel cells. Chem Commun, 2015, 51(20): 4184–4187.
[18] Koch C, Harnisch F. Is there a specific ecological niche for electroactive microorganisms? Chemelectrochem, 2016, 3: 1–15.
[19] Sydow A, Krieg T, Mayer F, et al. Electroactive bacteria—molecular mechanisms and genetic tools. Appl Microbiol Biotechnol, 2014, 98(20): 8481–8495.
[20] Firer-Sherwood M, Pulcu GS, Elliott SJ. Electrochemical interrogations of the Mtr cytochromes from: opening a potential window. JBIC J Biol Inorg Chem, 2008, 13(6): 849–854.
[21] Tremblay PL, Zhang T. Electrifying microbes for the production of chemicals. Front Microbiol, 2015, 6: 201.
[22] Rosenbaum M, Aulenta F, Villano M, et al. Cathodes as electron donors for microbial metabolism: which extracellular electron transfer mechanisms are involved? Bioresource Technol, 2011, 102: 324–333.
[23] Gorby YA, Yanina S, McLean JS, et al. Electrically conductive bacterial nanowires produced bystrain MR-1 and other microorganisms. Proc Natl Acad Sci USA, 2006, 103(30): 11358–11363.
[24] Malvankar MS, Vargas M, Nevin KP, etal. Tunable metallic-like conductivity in microbial nanowire networks. Nat Nanotechnol, 2011, 6(9): 573–579.
[25] Reguera G, McCarthy KD, Mehta T, et al. Extracellular electron transfermicrobial nanowires. Nature, 2005, 435(7045): 1098–1101.
[26] Thormann KM, Saville RM, Shukla S, et al. Initial phases of biofilm formation inMR-1. J Bacteriol, 2004, 186(23): 8096–8104.
[27] Thormann KM, Saville RM, Shukla S, et al. Induction of rapid detachment inMR-1 biofilms. J Bacteriol, 2005, 187(3): 1014–1021.
[28] Kotloski NJ, Gralnick JA. Flavin electron shuttles dominate extracellular electron transfer by. mBio, 2013, 4(1): e00553–12.
[29] Yong XY, Shi DY, Chen YL, et al. Enhancement of bioelectricity generation by manipulation of the electron shuttles synthesis pathway in microbial fuel cells. Bioresour Technol, 2014, 152: 220–224.
[30] Xia X, Cao XX, Liang P, et al. Electricity generation from glucose by asp. in microbial fuel cells. Appl Microbiol Biotechnol, 2010, 87(1): 383–390.
[31] Jensen HM, Albersc AE, Malley KR, et al. Engineering of a synthetic electron conduit in living cells. Proc Natl Acad Sci USA, 2010, 107(45): 19213–19218.
[32] Jensen HM, TerAvest MA, Kokish MG, et al. CymA and exogenous flavins improve extracellular electron transfer and couple it to cell growth in Mtr-expressing. ACS Synth Biol, 2016, 5(7): 679–688.
[33] TerAvest MA, Zajdel TJ, Ajo-Franklin CM. The Mtr pathway ofMR-1 couples substrate utilization to current production in. Chemelectrochem, 2014, 1(11): 1874–1879.
[34] Yong YC, Yu YY, Yang Y, et al. Enhancement of extracellular electron transfer and bioelectricity output by synthetic porin. Biotechnol Bioeng, 2013, 110(2): 408–416.
[35] Yong YC, Yu YY, Yang Y, et al. Increasing intracellular releasable electrons dramatically enhances bioelectricity output in microbial fuel cells. Electrochem Commun, 2012, 19: 13–16.
[36] Liu J, Yong YC, Song H, et al. Activation enhancement of citric acid cycle to promote bioelectrocatalytic activity of arca knockouttoward high-performance microbial fuel cell. ACS Catal, 2012, 2(8): 1749–1752.
[37] Schmitz S, Nies S, Wierckx N, et al. Engineering mediator-based electroactivity in the obligate aerobic bacteriumKT2440. Front Microbiol, 2015, 6: 284.
[38] Sekar R, Shin HD, DiChristina TJ. Activation of an otherwise silent xylose metabolic pathway in. Appl Environ Microbiol, 2016, 82(13): 3996–4005.
[39] Flynn JM, Ross DE, Hunt KA, et al. Enabling unbalanced fermentations by using engineered electrode-interfaced bacteria. mBio, 2010, 1(5): e00190–10.
[40] Choi D, Lee SB, Kim S, et al. Metabolically engineered glucose-utilizingstrains under anaerobic conditions. Bioresour Technol, 2014, 154: 59–66.
[41] Johnson ET, Baron DB, Naranjo B, et al. Enhancement of survival and electricity production in an engineered bacterium by light-driven proton pumping. Appl Environ Microbiol, 2010, 76(13): 4123–4129.
[42] Yang Y, Wu YC, Hu YD, et al. Engineering electrode-attached microbial consortia for high-performance xylose-fed microbial fuel cell. ACS Catal, 2015, 5(11): 6937–6945.
[43] Lin T, Bai X, Yang Y, et al. Syntheticconsortium enables glucose-fed high-performance microbial fuel cell. AIChE J, 2016.
[44] Yong XY, Feng J, Chen YL, et al. Enhancement of bioelectricity generation by cofactor manipulation in microbial fuel cell. Biosens Bioelectron, 2014, 56: 19–25.
[45] Han S, Gao XY, Ying HJ, et al. NADH gene manipulation for advancing bioelectricity inmicrobial fuel cells. Green Chem, 2016, 18: 2473–2478.
[46] Baron D, LaBelle E, Coursolle D, et al. Electrochemical measurement of electron transfer kinetics byMR-1. J Biol Chem, 2009, 284(42): 28865–28873.
[47] Yang Y, Ding YZ, Hu YD, et al. Enhancing bidirectional electron transfer ofby a synthetic flavin pathway. ACS Synth Biol, 2015, 4(7): 815–823.
[48] Yong YC, Yu YY, Li CM, et al. Bioelectricity enhancementoverexpression of quorum sensing system in-inoculated microbial fuel cells. Biosens Bioelectron, 2011, 30(1): 87–92.
[49] WatnickP, Kolter R. Biofilm, city of microbes. J Bacteriol, 2000, 182(10): 2675–2679.
[50] Nguyen PQ, Botyanszki Z, Tay PKR, et al. Programmable biofilm-based materials from engineered curli nanofibres. Nat Commun, 2014, 5: 4945.
[51] Liu T, Yu YY, Deng XP, et al. Enhancedbiofilm promotes bioelectricity generation. Biotechnol Bioeng, 2015, 112(10): 2051–2059.
[52] Sturm-Richter K, Golitsch F, Sturm G, et al. Unbalanced fermentation of glycerol inheterologous production of an electron transport chain and electrode interaction in microbial electrochemical cells. Bioresour Technol, 2015, 186: 89–96.
[53] Nishio K, Kimoto Y, Song J, et al. Extracellular electron transfer enhances polyhydroxybutyrate productivity in. Environ Sci Technol Lett, 2014, 1(1): 40–43.
[54] Speers AM, Young JM, Reguera G. Fermentation of glycerol into ethanol in a microbial electrolysis cell driven by a customized consortium. Environ Sci Technol, 2014, 48(11): 6350–6358.
[55] Zhu L, Chen H, Huang L, et al. Electrochemical analysis ofand its acrylic acid production in microbial fuel cells. Eng Life Sci, 2011, 11: 238–244.
[56] Li Z, Rosenbaum MA, Venkataraman A, et al. Bacteria-based AND logic gate: a decision-making and self-powered biosensor. Chem Commun, 2011, 47: 3060–3062.
[57] Torella JP, Gagliardi CJ, Chen JS, et al. Efficient solar-to-fuels production from a hybrid microbial- water-splitting catalyst system. Proc Natl Acad Sci USA, 2015, 112(8): 2337–2342.
[58] Li H, Opgenorth PH, Wernick DG, et al. Integrated electromicrobial conversion of CO2to higher alcohols. Science, 2012, 335(6076): 1596.
[59] Jeon JM; Park H; Seo HM, et al. Isobutanol production from an engineeredMR-1. Bioproc Biosyst Eng, 2015, 38: 2147–2154.
[60] Ross DE, Flynn JM, Baron DB, et al. Towards electrosynthesis in: energetics of reversing the mtr pathway for reductive metabolism. PLoS ONE, 2011, 6: e16649.
[61] Soussan L, Riess J, Erable B, et al. Electrochemical reduction of CO2catalysed bygrown on polarized stainless steel cathodes. Electrochem Commun, 2013, 28: 27–30.
[62] Nevin KP, Woodard TL, Franks AE, et al. Microbial electrosynthesis: feeding microbes electricity to convert carbon dioxide and water to multicarbon extracellular organic compounds. mBio, 2010, 1(2): e00203–10.
[63] Sakimoto KK, Wong AB, Yang PD. Self- photosensitization of nonphotosynthetic bacteria for solar-to-chemical production. Science, 2016, 351(6268): 74–77.
[64] Gong Y, Ebrahim A, Feist AM, et al. Sulfide-driven microbial electrosynthesis. Environ Sci Technol, 2013, 47: 568–573.
[65] Nevin KP, Hensley SA, Franks AE, et al. Electrosynthesis of organic compounds from carbon dioxide is catalyzed by a diversity of acetogenic microorganisms. Appl Environ Microbiol, 2011, 77: 2882–2886.
[66] Choi O, Kim T, Woo HM, et al. Electricity-driven metabolic shift through direct electron uptake by electroactive heterotroph. Sci Rep-Uk, 2014, 4: 6961.
[67] Liu C, Gallagher JJ, Sakimoto KK, et al. Nanowire-bacteria hybrids for unassisted solar carbon dioxide fixation to value-added chemicals. Nano Lett, 2015, 15(5): 3634–3639.
[68] Kornienko N, Sakimoto KK, Herlihy DM, et al. Spectroscopic elucidation of energy transfer in hybrid inorganic-biological organisms for solar-to-chemical production. Proc Natl Acad Sci USA, 2016, 113(42): 11750–11755.
[69] Valdes J, Pedroso I, Quatrini R, et al.metabolism: from genome sequence to industrial applications. BMC Genomics, 2008, 9: 597.
[70] Aulenta F, Catervi A, Majone M, et al. Electron transfer from a solid-state electrode assisted by methyl viologen sustains efficient microbial reductive dechlorination of TCE. Environ Sci Technol., 2007, 41: 2554–5259.
[71] Lojou E, Durand MC, Dolla A, et al. Hydrogenase activity control atcell-coated carbon electrodes: biochemical and chemical factors influencing the mediated bioelectrocatalysis. Electroanalysis, 2002, 14: 913–922.
[72] Steinbusch KJ, HamelersHV, Schaap JD, et al. Bioelectrochemical ethanol production through mediated acetate reduction by mixed cultures. Environ Sci Technol, 2010, 44: 513–517.
[73] Hatch JL, Finneran KT. Influence of reduced electron shuttling compounds on biological H2production in the fermentative pure culture. Curr Microbiol, 2008, 56: 268–273.
[74] Park DH, Zeikus JG. Utilization of electrically reduced neutral red by: physiological function of neutral red in membranedriven fumarate reduction and energy conservation. J. Bacteriol, 1999, 181: 2403–2410.
[75] Park, DH, Laivenieks M, Guettler MV,et al. Microbial utilization of electrically reduced neutral red as the sole electron donor for growth and metabolite production. Appl Environ Microbiol, 1999, 65: 2912–2917.
[76] Choi O, Um Y, Sang BI. Butyrate production enhancement byusing electron mediators and a cathodic electron donor. Biotechnol Bioeng, 2012, 109: 2494–2502.
[77] Aulenta F, Canosa A, Reale P, et al. Microbial reductive dechlorination of trichloroethene to ethene with electrodes serving as electron donors without the external addition of redox mediators. Biotechnol Bioeng, 2009, 103: 85–91.
[78] Boussicault F, Robert M. Electron transfer in DNA and in DNA-related biological processes. Electrochemical insights. Chem Rev, 2008, 108: 2622–2645.
[79] Fredrickson JK, Romine MF, Beliaev AS, et al. Towards environmental systems biology of. Nat Rev Microbiol, 2008, 6(8): 592–603.
[80] Ishii T, Kawaichi S, Nakagawa H, et al. From chemolithoautotrophs to electrolithoautotrophs: CO2fixation by Fe(II)-oxidizing bacteria coupled with direct uptake of electrons from solid electron sources. Front Microbiol, 2015, 6: 994.
[81] Kita A, Iwasaki Y, Sakai S,et al. Development of genetic transformation and heterologous expression system in carboxydotrophic thermophilic acetogen. J Biosci Bioeng, 2013, 115: 347–352.
[82] DiCarlo JE, Norville JE, Mali P, et al. Genome engineering inusing CRISPR-Cas systems. Nucleic Acids Res, 2013, 41(7): 4336–4343.
[83] Na D, Yoo SM, Chung H, et al. Metabolic engineering ofusing synthetic small regulatory RNAs. Nat Biotechnol, 2013, 31(2): 170–174.
[84] Gibson DG, Young L, Chuang RY, et al. Enzymatic assembly of DNA molecules up to several hundred kilobases. Nat Methods, 2009, 6(5): 343–345.
[85] Leang C, Ueki T, Nevin KP, et al. A genetic system for: a chassis for autotrophic production of biocommodities and a model homoacetogen. Appl Environ Microbiol, 2013, 79: 1102–1109.
[86] Köpke M, Held C, Hujer S, et al.represents a microbial production platform based on syngas. Proc Natl Acad Sci USA, 2010, 107(29): 13087–13092.
[87] Kracke F, Vassilev I, Kromer JO. Microbial electron transport and energy conservation-the foundation for optimizing bioelectrochemical systems. Front Microbiol, 2015, 6: 575.
[88] Nealson KH, Rowe AR. Electromicrobiology: realities, grand challenges, goals and predictions. Microb Biotechnol, 2016, 9: 595–600.
[89] Malvankar NS, Lovley DR. Microbial nanowires: a new paradigm for biological electron transfer and bioelectronics. Chemsuschem, 2012, 5: 1039–1046.
[90] Strycharz SM, Malanoski AP, Snider RM, et al. Application of cyclic voltammetry to investigate enhanced catalytic current generation by biofilm- modified anodes ofstrain DL1vs. variant strain KN400. Energy Environ Sci, 2011, 4: 896–913.
[91] Strycharz-Glaven SM, Tender LM. Study of the mechanism of catalytic activity ofbiofilm anodes during biofilm growth. Chemsuschem, 2012, 5: 1106–1118.
(本文责编 陈宏宇)
宋浩 天津大学化工学院教授 (制药工程、生物工程方向)、博士生导师。2004年获得美国休斯顿大学化学工程博士学位。2004−2009年在美国得克萨斯大学和杜克大学从事合成生物学博士后研究,2009−2013年在新加坡南洋理工大学做助理教授。2013年入选国家“青年千人”计划,并加入天津大学化工学院、系统生物技术教育部重点实验室。研究兴趣为合成生物学与代谢工程,主要侧重在微生物电催化过程 (微生物电合成、微生物-多酶燃料电池等)、微生物生态系统和生物制药。承担多项国家课题,包括重大863项目、973子课题、国家自然科学基金和多项公司横向课题等。发表了近70篇SCI文章,包括、、、等。

Promoting efficiency of microbial extracellular electron transfer by synthetic biology
Feng Li1,2, and Hao Song1,2
1 Key Laboratory of Systems Bioengineering (Ministry of Education), School of Chemical Engineering and Technology, Tianjin University, Tianjin 300072, China 2 SynBio Research Platform, Collaborative Innovation Centre of Chemical Science and Engineering, Tianjin University, Tianjin 300072, China
Electroactive bacteria, including electrigenic bacteria (exoelectrogens) and electroautotrophic bacteria, implement microbial bioelectrocatalysis processesbi-directional exchange of electrons and energy with environments, enabling a wide array of applications in environmental and energy fields, including microbial fuel cells (MFC), microbial electrolysis cells (MEC), microbial electrosynthesis (MES) to produce electricity and bulk fine chemicals. However, the low efficiency in the extracellular electron transfer (EET) of exoelectrogens and electrotrophic microbes limited their industrial applications. Here, we reviewed synthetic biology approaches to engineer electroactive microorganisms to break the bottleneck of their EET pathways, to achieve higher efficiency of EET of a number of electroactive microorganisms. Such efforts will lead to a breakthrough in the applications of these electroactive microorganisms and microbial electrocatalysis systems.
electroactive bacteria, synthetic biology, microbial electrocatalysis, microbial fuel cells, microbial electrosynthesis
November 1, 2016; Accepted:January 13, 2017
Hao Song. Tel: +86-22-60977327; E-mail: hsong@tju.edu.cn
Supported by: National Natural Science Foundation of China (Nos. 21376174, 21621004), National Basic Research Program of China (973 Program) (No. 2014CB745103), Tianjin Science & Technology Council (No. 13JCYBJC40700).
国家自然科学基金 (Nos. 21376174, 21621004),国家重点基础研究发展计划(973计划) (No. 2014CB745103) ,天津市科委 (No. 13JCYBJC40700) 资助。
2017-01-23
http://www.cnki.net/kcms/detail/11.1998.Q.20170123.1554.001.html

