儿童患者应用静注人免疫球蛋白的情况及合理性评价
温爱萍,王维娜,陈佳帅,李 佳(.首都医科大学附属北京友谊医院药剂科,北京 00050;.北京市密云区中医医院,北京0500;.首都儿科研究所附属儿童医院,北京 0000)
儿童患者应用静注人免疫球蛋白的情况及合理性评价
温爱萍1,王维娜1,陈佳帅2,李 佳3(1.首都医科大学附属北京友谊医院药剂科,北京 100050;2.北京市密云区中医医院,北京101500;3.首都儿科研究所附属儿童医院,北京 100020)
目的:考察我院儿童患者应用静注人免疫球蛋白的情况,并评价其合理性。方法:回顾2014年9月 – 2016年4月我院儿童患者应用静注人免疫球蛋白的情况,评价临床诊断与我国说明书和《临床用药须知》适应证的相符性,同时根据相关指南对超说明书应用静注人免疫球蛋白的获益情况进行评分,根据平均分确定获益等级,并评价给药方案的合理性。结果:160例应用静注人免疫球蛋白的儿童患者的主要诊断为重症感染、肝移植和新生儿ABO溶血等,其中有53.74%的病例存在超说明书用药。在超说明书用法中,肝移植、新生儿ABO溶血病、噬血细胞综合征、造血干细胞移植、急性移植物抗宿主病和新生儿溶血性贫血可能获益。仅68例患儿应用静注人免疫球蛋白的给药方案符合说明书或指南推荐。结论:部分儿童患者应用静注人免疫球蛋白的合理性还有待进一步验证,且给药方案仍需进一步优化。
静注人免疫球蛋白;儿童患者;合理性
静注人免疫球蛋白(Intravenous immunoglobulin,IVIg)是从健康人血浆中分离制备而成的生物制剂,主要成分为IgG,它具有免疫替代、免疫调节、抗感染和抗炎等治疗作用[1]。IVIg最初仅用于治疗原发性和继发性免疫球蛋白缺陷及自身免疫性疾病,现已逐渐扩展到神经病学、血液和血液肿瘤学以及皮肤病学等多个领域的疾病治疗[2]。临床应用IVIg领域的扩展和我国生产厂家说明书更新的滞后,使得我国超说明书应用甚至滥用IVIg的情况日益严重。但IVIg严格的生产过程和紧缺的血浆来源,使其供给难以满足临床需求。如何将高需求量、低供给量且具有应用风险的IVIg合理地分配和应用于儿童患者,应引起广泛重视。本文拟通过分析我院儿童患者应用IVIg的情况,参考现有的循证医学证据评价其用药合理性,为促进IVIg在儿童患者中的合理应用提供参考依据。
1 资料与方法
1.1 资料来源
采用回顾性方法,对我院2014年9月 ~ 2016年4月应用IVIg的儿童患者病历进行检索,共计160例。利用电子病历系统,对患儿的病历资料进行查阅,详细记录患儿的一般情况、住院科室、出院诊断、IVIg给药方案和疗程等信息。
1.2 适应证相符性评价
将我国IVIg药品说明书(成都蓉生药业有限责任公司)和2010年版《临床用药须知》[3]的适应证视为核准适应证,包括:原发性免疫球蛋白G缺陷病,继发性免疫球蛋白缺陷病(如重症感染、新生儿脓毒症和艾滋病等),自身免疫性疾病(如原发性血小板减少性紫癜和川崎病)及其他用途(如婴幼儿毛细支气管炎、重症系统性红斑狼疮、原发和继发抗磷脂综合征等)。除此之外的用法视为超说明书用法。
1.3 超说明书用法获益性评价
根据2006年美国变态反应哮喘和免疫学会IVIg使用指南(A)[4]、2011年英国IVIg临床使用指南(B)[5]、2012年澳大利亚IVIg临床使用标准(C)[6]和2007年加拿大国家血液和血液制品咨询委员会静脉注射免疫球蛋白治疗血液病指南(D)[7],制定IVIg的获益评分标准(见表1)。根据上述指南的评分标准对我院IVIg超说明书用法的获益情况进行评分,根据平均分确定获益等级(3分,肯定获益;<3且≥2分,很可能获益;<2且≥1分,可能获益;<1分,不可能获益)[8]。

表1 IVIg的获益评分标准及说明Tab 1 Grading standards and descriptions of the benefits of IVIg
1.4 给药方案及疗程合理性评价
对我国说明书、2010年版《临床用药须知》[3]及相关指南[4-7]推荐的IVIg给药方案及疗程进行归纳总结,对我院患儿应用IVIg的给药方案进行评价,无相关推荐者不作评价。
2 结果
2.1 一般情况
160例患儿中男性77例(48.13%),女性83例(51.87%)。年龄0岁 ~ 17岁,平均年龄(1.45 ± 3.37)岁,体重1.15 kg ~ 55 kg,平均体重(7.95 ± 10.45)kg。
2.2 适应证相符性及超说明书用法获益情况
160例患儿的主要诊断与IVIg核准适应证的相符性及获益评分见表2。结合患者的临床情况,将新生儿肺炎、新生儿脓毒症、支气管肺炎、化脓性脑膜炎、泌尿系感染、重症脓毒症和病毒性脑膜炎判定为“重症感染”。结果显示,我院患儿应用IVIg的主要诊断为“重症感染”(41.88%),其次为肝移植(21.25%)和新生儿ABO溶血(14.38%)等,其中超说明书用法占53.74%。在超说明书用法中,肝移植、新生儿ABO溶血病、噬血细胞综合征、造血干细胞移植、急性移植物抗宿主病和新生儿溶血性贫血可能获益。
2.3 给药方案及疗程合理性
结果表明,仅68例患儿给药方案符合说明书或指南推荐。所有川崎病(n = 7)和新生儿溶血性贫血(n = 1)患儿应用IVIg的给药方案均与说明书或指南推荐相符;所有化脓性脑膜炎、泌尿系感染、重症脓毒症和急性移植物抗宿主病患儿应用IVIg的给药方案与说明书或指南推荐均不符。详见表3。
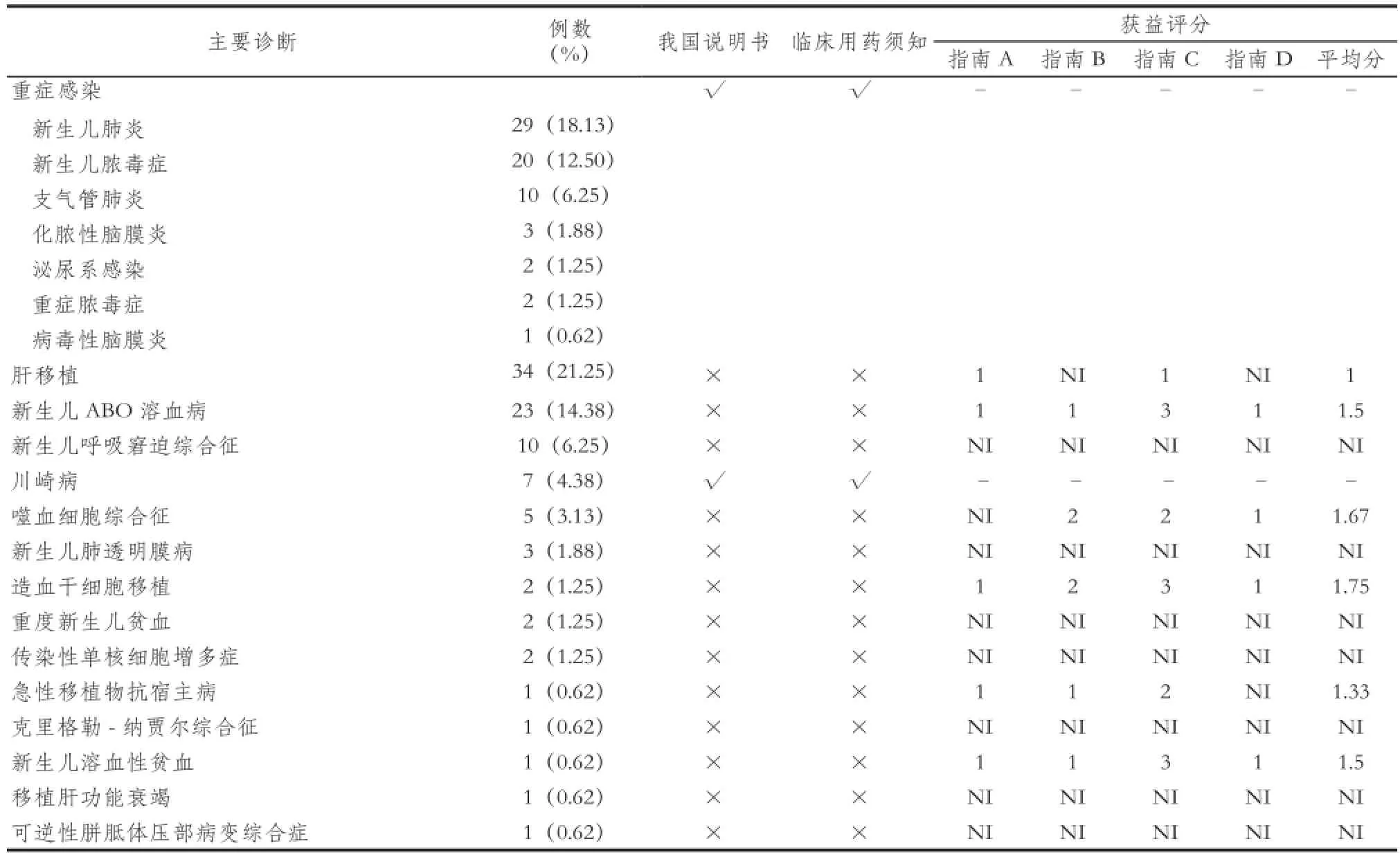
表2 患儿的主要诊断与IVIg核准适应证相符性和超说明书用法获益评分Tab 2 Compliance of the patients' primary diagnoses with the IVIg indications and benefits of the off-label uses

表3 IVIg给药方案的相关推荐及患儿给药方案合理性评价Tab 3 Recommendations of the dosing regimen of IVIg and the rationality evaluation
3 讨论
3.1 IVIg的超说明书应用情况
从诊断角度评价,我院超半数儿童患者为超说明书应用IVIg(占53.74%),这一结果与蔡志波等[8]的研究结果(75.9%)相比较低。蔡志波等[8]的研究是以美国食品药品监督管理局(FDA)批准的适应证作为IVIg的核准适应证,包括:①治疗原发性免疫缺陷病;②预防低免疫球蛋白血症患者细菌感染和慢性淋巴细胞白血病患者反复细菌感染;③预防川崎病患者冠状动脉瘤;④预防骨髓移植后感染、肺炎以及移植物抗宿主病;⑤减少人类免疫缺陷病毒(HIV)感染儿童的严重感染;⑥增加特发性血小板减少性紫癜(ITP)患者的血小板计数预防和控制出血;⑦慢性炎症性脱髓鞘性多发性神经病(CIDP)。而本研究是以我国说明书及《临床用药须知》中IVIg的适应证作为核准适应证。
另外,我国的IVIg核准适应证中包括“重症感染”,这一诊断的界定较为模糊,缺乏统一的判定标准,可能导致临床判断的主观性。本研究中,结合患者的临床情况,将新生儿肺炎、新生儿脓毒症、支气管肺炎、化脓性脑膜炎、泌尿系感染、重症脓毒症和病毒性脑膜炎判定为“重症感染”(占41.88%),这一结果不可避免地存在主观性。如何及时准确判断有无细菌性感染及感染的严重程度仍是儿科医生面临的问题,目前临床上常用的感染指标,如白细胞、中性粒细胞百分比、C-反应蛋白和血沉等缺乏特异性。有研究表明,降钙素原可能可以在一定程度上预测感染及其严重程度,但其临床应用也存在一定的局限性[9-10]。而且需注意本研究考察的指南中仅提及了新生儿脓毒症,且其获益平均分为1(可能获益,结果未显示),并未提及其他感染性疾病,可见IVIg用于重症感染治疗的效果仍存在争议。建议药品说明书在临床试验或充分循证的基础上指出明确的适应证,这样才能避免临床的盲目应用。
3.2 IVIg超说明书用法的获益情况
本研究表明,在超说明书用法中,仅肝移植、新生儿ABO溶血病和噬血细胞综合征等可能获益,而其他用法在指南中并无相关推荐,缺乏证据支持。
术后感染和免疫并发症是肝移植术后面对的主要问题,肝移植术后需常规应用免疫抑制剂,然而其免疫抑制作用导致感染发生风险的增加,且目前并没有确切的临床指标用来预测最低的抗排异药物剂量[11],因此有研究推荐用IVIg平衡调节移植术后患者的免疫功能[12-13]。目前尚不清楚IVIg的作用机制,然而越来越多的研究证据表明,IVIg可能发挥长期的细胞免疫调控作用,提示肝移植术后早期应用IVIg可能获益[13-14]。有研究显示,IVIg对提高淋巴细胞毒交叉配合试验阳性的肝移植患者的存活率有重要意义[15-17];还有研究显示,IVIg有助于提高ABO血型不相容性肝移植患者的存活率,降低移植后抗体介导的排斥反应和急性细胞排斥反应的发生率[18-20]。目前,IVIg用于肝移植患者的文献报道有限,且笔者没有检索到IVIg用于儿童肝移植患者的临床研究,在我国2015版《中国儿童肝移植临床诊疗指南》[21]和2014年版《美国小儿肝移植患者实践指南》[22]中也未提及IVIg,可见IVIg用于儿童肝移植患者的合理性还有待进一步探讨。
IVIg可阻断网状内皮细胞的Fc受体,从而阻止新生儿红细胞的溶解,这一竞争性抑制作用提示对于新生儿免疫性溶血性疾病,有必要早期应用IVIg[23]。Gottstein等[24]的Meta分析表明IVIg可以显著降低高风险换血疗法在新生儿ABO溶血症患者中的使用率。英国指南[5]建议,对于新生儿ABO溶血病,若密集光疗下高胆红素血症依然逐渐恶化,可以使用IVIg。美国儿科学会也推荐大剂量IVIg(1 g·kg-1)可用于ABO溶血病的治疗,然而其作为ABO溶血病的常规治疗还未达成共识[25]。
嗜血细胞综合症(H e m o p h a g o c y t i c lymphohistiocytosis,HLH)是罕见、危及生命的疾病,主要影响患儿的单核巨噬细胞系统,可为原发,也可继发于其他疾病(主要为感染)。尽管包含依托泊苷的化疗方案目前是HLH的推荐疗法,然而由于HLH患者处于免疫过度激活状态,糖皮质激素、IVIg或联合免疫调节治疗仍被广泛应用。IVIg在其中的免疫调节机制不明,可能改变T细胞的激活和细胞因子的产生过程。有研究表明,在HLH的治疗方面,IVIg与包含依托泊苷的化疗方案相比同样有效,且初始治疗应用IVIg可能避免由依托泊苷导致的继发恶性肿瘤[26],但此结论源自1篇回顾性研究,其结果仍需进一步验证。
综上,本研究在检索IVIg临床证据的基础上,系统总结了IVIg在我国应用的适应证和相关指南的推荐情况,同时分析了我院IVIg的临床应用情况。研究发现,我国IVIg说明书的适应证内容有待明确化、具体化,部分儿童患者应用IVIg的合理性还有待进一步验证,且给药方案仍需进一步优化。
[1] Garcia-Lloret M, McGhee S, Chatila T. Immunoglobulin replacement therapy in children[J]. Immunol Allergy Clin North Am, 2008, 28(4): 833-849.
[2] Hartung HP, Mouthon L, Ahmed R,et al. Clinical applications of intravenous immunoglobulins (IVIg)—beyond immunodeficiencies and neurology[J]. Clin Exp Immunol, 2009, 158(Suppl 1): 23-33.
[3] 国家药典委员会.中华人民共和国药典临床用药须知[M].2010年版.北京:中国医药科技出版社,2010:1158-1159.
[4] Orange JS, Hossny EM, Weiler CR,et al. Use of intravenous immunoglobulin in human disease: a review of evidence by members of the Primary Immunodeficiency Committee of the American Academy of Allergy, Asthma and Immunology[J]. J Allergy Clin Immunol, 2006, 117(4 Suppl): S525-S553.
[5] Department of Health. Clinical guidelines for immunoglobulin use: update to second edition[EB/OL].(2011-08-01)[2016-06-27]. https://www.gov.uk/government/uploads/system/uploads/ attachment_data/file/216671/dh_131107.pdf.
[6] National Blood Authority. Criteria for the clinical use of intravenous immunoglobulin in Australia[EB/OL]. (2012-07-01)[2016-06-27]. https://www.blood.gov.au/system/files/documents/NBA_ IVIgCriteria_SecondEdition_Internals-WEB_updated_ref.pdf .
[7] Anderson D, Ali K, Blanchette V,et al. Guidelines on the use of intravenous immune globulin for hematologic conditions[J]. Transfus Med Rev, 2007, 21(2 Suppl 1): S9-S56.
[8] 蔡志波,林艳,王珏.儿童使用静注人免疫球蛋白情况及合理性分析[J].中国药学杂志,2012,47(10):781-784.
[9] 何建平,申昆玲,林影,等.前降钙素对新生儿重症感染的诊断价值[J].首都医科大学学报,2005,26(5):545-548.
[10] 赵劭懂,陈俊,葛许华,等.降钙素原在儿科重症感染中的诊断价值[J].实用医学杂志,2016,32(2):300-303.
[11] Kornberg A. Intravenous immunoglobulins in liver transplant patients: perspectives of clinical immune modulation[J]. World J Hepatol, 2015, 7(11): 1494-1508.
[12] Sewell WA, Kerr J, Behr-Gross ME,et al. European consensus proposal for immunoglobulin therapies[J]. Eur J Immunol, 2014, 44(8): 2207-2214.
[13] Boros P, Gondolesi G, Bromberg JS. High dose intravenous immunoglobulin treatment: mechanisms of action[J]. Liver Transpl, 2005, 11(12): 1469-1480.
[14] Gelfand EW. Intravenous immune globulin in autoimmune and inf l ammatory diseases[J]. N Engl J Med, 2013, 368(8): 776-777.
[15] Leonard GR, Shike H, Uemura T,et al. Liver transplantation with a strongly positive crossmatch: case study and literature review[J]. Liver Transpl, 2013, 19(9): 1001-1010.
[16] Shindoh J, Sugawara Y, Tamura S,et al. Living donor liver transplantation for patients immunized against human leukocyte antigen[J]. J Hepatobiliary Pancreat Sci, 2013, 20(3): 279-285.
[17] Hong G, Yi NJ, Suh SW,et al. Preoperative selective desensitization of live donor liver transplant recipients considering the degree of T lymphocyte cross-match titer, model for end-stage liver disease score, and graft liver volume[J]. J Korean Med Sci, 2014, 29(5): 640-647.
[18] Kim JD, Choi DL, Han YS. Fourteen successful consecutive cases of ABO-incompatible living donor liver transplantation: new simplified intravenous immunoglobulin protocol without local infusion therapy[J]. Transplant Proc, 2014, 46(3): 754-757.
[19] Lee SD, Kim SH, Kong SY,et al. ABO-incompatible living donor liver transplantation without graft local infusion and splenectomy[J]. HPB (Oxford), 2014, 16(9): 807-813.
[20] Shen T, Lin BY, Jia JJ,et al. A modified protocol with rituximab and intravenous immunoglobulin in emergent ABO-incompatible liver transplantation for acute liver failure[J]. Hepatobiliary Pancreat Dis Int, 2014, 13(4): 395-401.
[21] 夏强.中国儿童肝移植临床诊疗指南(2015版)[J].中华移植杂志(电子版),2016,10(1):2-11.
[22] 高伟.美国小儿肝移植患者实践指南(2014年版)[J].实用器官移植电子杂志,2014,2(5):257-261.
[23] Beken S, Hirfanoglu I, Turkyilmaz C,et al. Intravenous immunoglobulin G treatment in ABO hemolytic disease of the newborn, is it myth or real?[J]. Indian J Hematol Blood Transfus, 2014, 30(1): 12-15.
[24] Gottstein R, Cooke RW. Systematic review of intravenous immunoglobulin in haemolytic disease of the newborn[J]. Arch Dis Child Fetal Neonatal Ed, 2003, 88(1): F6-F10.
[25] American academy of pediatrics subcommittee on hyperbilirubinemia. Management of hyperbilirubinemia in the newborn infant 35 or more weeks of gestation[J]. Pediatrics, 2004, 114(1): 297-316.
[26] Rajajee S, Ashok I, Manwani N,et al. Profile of hemophagocytic lymphohistiocytosis; efficacy of intravenous immunoglobulin therapy[J]. Indian J Pediatr, 2014, 81(12): 1337-1341.
Evaluation of the clinical use of intravenous immunoglobulin in pediatric patients
WEN Ai-ping1, WANG Wei-na1, CHEN Jia-shuai2, LI Jia3(1. Department of Pharmacy, Beijing Friendship Hospital Affiliated to Capital Medical University, Beijing 100050, China; 2. Department of Pharmacy, Miyun District Hospital of Traditional Chinese Medicine, Beijing 101500, China; 3. Department of Pharmacy, Children's Hospital Affiliated to Capital Institute of Pediatrics, Beijing 100020, China)
Objective: To review and evaluate the clinical application of intravenous immunoglobulin in pediatric patients. Methods: The data of intravenous immunoglobulin used in pediatric patients were collected from September 2014 to April 2016 retrospectively. The consistency between the primary diagnoses and the label information or pharmacopoeia was evaluated. The benefits of the off-label use of intravenous immunoglobulin were scored and graded based on the guidelines. The rationality of dosing regimen was evaluated according to the label information, pharmacopoeia and guidelines. Results: A total of 160 pediatric patients were included, and the primary diagnoses of the patients were severe infections, liver transplantation and ABO hemolytic disease of the newborn, 53.74% of which were off-label use. Among the off-label use, intravenous immunoglobulin was probably beneficial for the patients with liver transplantation, ABO hemolytic disease of the newborn, hemophagocytic lymphohistiocytosis, hematopoietic stem cell transplantation, acute graft-versus-host disease and hemolytic anemia of the newborn. Only 68 patients' dosing regimens were judged as rational according to the label information or guidelines. Conclusion: The rationality of the clinical use of intravenous immunoglobulin in pediatric patients demands to be further verified, and the dosing regimen needs to be standardized.
R969.3
A
1672 – 8157(2017)01 – 0051 –05
2016-08-28
2016-11-17)
温爱萍,女,主管药师;研究方向:临床药学。E-mail:wenaiping@126.com

