星点设计-效应面法优化柚皮素包合物自微乳给药系统
王章姐, 施伶俐, 华 芳, 杨梦凡
(安徽新华学院 药学院,安徽 合肥230088)
星点设计-效应面法优化柚皮素包合物自微乳给药系统
王章姐, 施伶俐, 华 芳, 杨梦凡
(安徽新华学院 药学院,安徽 合肥230088)
研究星点设计-效应面法优化柚皮素包合物自微乳化给药系统最佳处方。通过测定柚皮素包合物在各介质中的溶解度,利用伪三元相图初步筛选柚皮素包合物自微乳给药系统组分;以柚皮素在不同自微乳处方中的载药量和粒径为指标,采用星点设计-效应面优化法,确定最佳处方。柚皮素包合物自微乳最佳处方选择油酸乙酯为油相,聚山梨酯80为乳化剂,PEG 400为助乳化剂,油相比例为14.39%,Km值为2.05,最佳处方中载药量为159.435 mg/g,粒径为28.35 nm。关键词:柚皮素包合物;自微乳;星点设计;效应面法
柚皮素(naringenin,NAR)是一种二氢黄酮类化合物,有研究报道,柚皮素具有抗癌、抗炎、抗菌、抗氧化、解痉利胆等多方面药理作用[1-3],但NAR水溶性和脂溶性均较差、口服生物利用度低,故其口服制剂在临床上应用受到了限制。前期对柚皮素包合物进行研究,结果显示,将NAR用β-CD包合后,其溶出度有所增加。
在处方和工艺优化时,通常需要考察多个自变量对因变量的影响,国内常用正交设计或者均匀设计对结果进行优化,但这两种方法实验精度低。星点设计-效应面法实验精度高,实验次数少,所建立的数学模型预测性较好[4-5]。自微乳给药系统(self micro-emulsifying drug delivery system,SMEDDS)由油相、表面活性剂和助表面活性剂构成的均一、澄清的液体,该系统在胃肠道内通过胃肠道蠕动自发形成粒径小于100 nm的O/W型乳剂,SMEDDS可作为疏水性、难吸收等药物的优良载体,可增加药物的表面积和溶解度[6]。作者采用星点设计-效应面法优化NAR包合物自微乳给药系统,为制备临床应用新剂型奠定基础。
1 材料与方法
1.1 材料与试剂
NAR原料药:批号HK20131222,质量分数98%,陕西慧科植物开发有限公司;NAR对照品:中国药品生物制品检定所,批号110722-201018;β-环糊精:上海源叶生物科技有限公司;聚氧乙烯氢化蓖麻油:Cremophor RH40,北京凤礼精求商贸有限责任公司;聚山梨酯80:天津市光复精细化工研究所;辛酸葵酸三甘油脂:GTCC,英国Croda公司;油酸乙酯:上海源叶生物科技有限公司;1,2丙二醇:北京凤礼精求商贸有限责任公司;聚乙二醇400:PEG 400,上海源叶生物科技有限公司;油酸、异丙醇:国药集团化学试剂有限公司;聚氧乙烯辛基苯基醚:OP乳化剂,上海玖意化学试剂有限公司;乙醇等其余试剂均为分析纯。
1.2 仪器
DF-101S型智能集热式恒温加热磁力搅拌器:河南省予华仪器有限公司;SHZ-DI-Ⅱ型循环水式真空泵:浙江黄岩求精真空泵厂;Zetasizer Nano ZS纳米粒电位分析仪:马尔文仪器有限公司;Autoscience AS3120超声波清洗机:奥特赛恩斯仪器有限公司;UV-2550紫外-可见分光光度仪:日本岛津公司;BT125D电子分析天平:赛多利斯科学仪器(北京)有限公司;DZF1.0型真空干燥箱:上海长源仪器设备厂;CP2115D电子天平:Satorius公司。
1.3 方法
1.3.1 NAR-β-CD包合物的制备 在前期研究基础上,称取100 g β-CD溶于水中,加热溶解制成β-CD饱和水溶液,备用。称取20 g NAR原料药,加入适量70%乙醇,置于48.11℃恒温磁力搅拌中,加入β-CD饱和水溶液,磁力加热搅拌84.72 min,静置,放入冰箱中冷藏24 h,真空抽滤,用无水乙醇多次洗涤滤饼,干燥,得到橙黄色固体即为NAR-β-CD包合物[7]。
1.3.2 NAR-β-CD包合物在不同介质中溶解度的测定 分别称取约2 g不同油相、乳化剂和助乳化剂置于带塞西林瓶中,加入过量的NAR-β-CD包合物,搅拌后密封超声30 min,以促进其溶解,然后在 37℃水浴中平衡 48 h,10 000 r/min离心 10 min,取上清液,用0.45 μm的微孔滤膜滤过,取续滤液用甲醇稀释至适宜倍数,作为供试品溶液。分别精密吸取供试品20 μL,以HPLC法测定,记录峰面积,计算相应成分在不同介质中的溶解度。
1.3.3 NAR-β-CD包合物自微乳的制备 取NAR-β-CD包合物、乳化剂、助乳化剂,精密称定,依次加入具塞锥形瓶中,置37℃水浴中溶解,混匀。再取油相,精密称定,加入上述锥形瓶中,同样条件下混匀,得到NAR-β-CD包合物自微乳。
1.3.4 自微乳粒径的测定 取NAR-β-CD包合物自微乳适量,加水稀释50倍,用纳米粒分析仪测定自微乳乳滴的粒径。
1.3.5 饱和载药量的测定 将过量的NAR-β-CD包合物加入到空白自微乳中,于60℃水浴中涡旋搅拌,以促进其溶解,然后在37℃水浴中平衡48 h,10 000 r/min离心10 min,上清液用0.45 μm的微孔滤膜滤过,取续滤液用甲醇稀释至适宜倍数,采用HPLC测定NAR含量,计算饱和载药量。
1.3.6 伪三元相图初步筛选 将不同质量比的乳化剂与助乳化剂Km值 (3∶1、2∶1、1∶1、1∶2、1∶3)混匀后,与油相按9∶1、8∶2、7∶3、6∶4、5∶5、4∶6、3∶7、2∶8、1∶9的比例混合,滴加水相中并观察,直至形成带有蓝色乳光溶液或澄清透明溶液,采用origin 9.0程序绘制伪三元相图,以相图中自微乳存在区域的大小来筛选乳化剂和助乳化剂。
1.3.7 星点设计-效应面法优化处方 在前期伪三元相图筛选处方的基础上,选择对自微乳性质影响较大的两个因素油相质量分数(X1)及Km(X2)为考察因素,运用伪三元相图对Km值进行试验,结果发现Km为4时,出现较大面积凝胶区域,故Km的范围为1~3;油相质量分数越低越有利于自微乳体系的形成和稳定,故将油相质量分数的范围为10%~40%。以载药量、粒径为评价指标,采用星点设计-效应面法对处方进行优化,因素水平见表1,试验设计及结果见表2[8]。
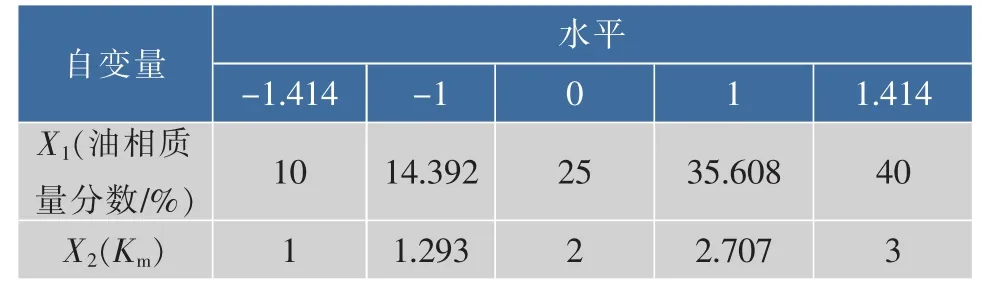
表1 星点设计因素水平表Table 1 Factors and levels of central composite design

表2 星点设计及结果Table 2 Central composite design and response
2 结果与分析
2.1 NAR-β-CD包合物在不同介质中溶解度的测定
由表3可知,NAR-β-CD包合物在不同油相中的溶解度顺序依次为油酸乙酯>GTCC>油酸,且NAR-β-CD包合物在油酸乙酯中的溶解度明显大于油酸和GTCC,故油相确定为油酸乙酯。NAR-β-CD包合物在不同乳化剂中的溶解度顺序依次为OP乳化剂>聚山梨酯80>Cremophor RH40,NAR-β-CD包合物在不同助乳化剂中的溶解度顺序依次为PEG 400>异丙醇>1,2-丙二醇,故乳化剂初步确定为OP乳化剂或聚山梨酯80,助乳化剂初步确定为异丙醇或PEG 400。

表3 NAR-β-CD包合物在不同介质中的溶解度Table 3 Solubility of NAR-β-CD inclusion complex in different media
2.2 伪三元相图初步筛选处方
在Km值(1∶1)相同的条件下,自微乳区域的面积见图1。即当油相为油酸乙酯,乳化剂为聚山梨酯80,助乳化剂为PEG400时的所形成的自微乳区域最大。因此初步选定该处方为后续待优化处方。
2.3 星点-设计效应面法优化处方
2.3.1 模型拟合 采用Design Expert 8.0.6软件,分别对各因素水平进行多元线性回归和非线性回归(二项式公式拟合),多元线性回归方程:载药量(Y1)=131.21-6.04A-2.17 B,r=0.254;粒径 (Y2)=42.79-3.03A+1.13 B,r=0.158;通过多元线性回归方程可以看出,相关系数均较低,表示自变量与因变量之间线性相关性较差,多元线性回归拟合度不佳,预测性较差,故采用二项式拟合。二项式拟合模型为载药量 (Y1)=149.30-6.04A-2.17B-4.38AB-6.51A2-22.89B2,r=0.9;粒径 (Y2)=29.52-3.03A+1.13B-3.68AB+1.56A2+20.01B2,r=0.934。两个二项式拟合方程的相关系数分别是0.9和0.934,表明此设计模型拟合程度良好,可以用此模型对NAR包合物自微乳处方进行预测和分析。
2.3.2 效应面优化 由Design Expert 8.0.6软件绘制不同影响因素对于响应值的三维曲线,载药量的效应曲面见图2。根据方程和响应面图确定NAR包合物自微乳的最优处方为:油相比例为14.39%,Km值为2.05;载药量理论值为159.435 mg/g,粒径理论值为28.35 nm。

图1 不同乳化剂及助乳化剂的伪三元相图Fig.1 Different surfactants and cosurfactants on pscudo-ternary phase diagram
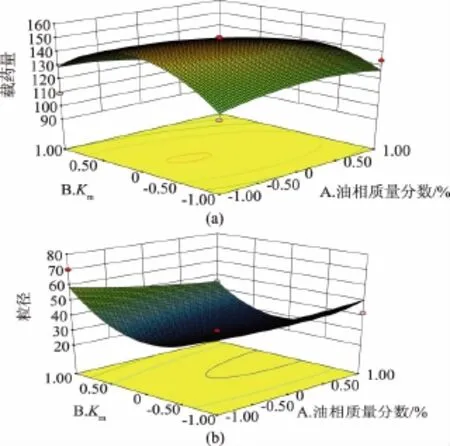
图2 载药量、粒径的效应面的三维图Fig.2 Response surface plot (3D)of drug loading capacity and particle size
2.4 验证试验
根据优化的最佳处方,制备NAR包合物自微乳验证试验,并对载药量和粒径进行测定,结果见表4。其中偏差=(预测值-实测值)/预测值。通过验证实验可知,最优处方粒径和载药量的真实值与预测值之间为显著性差异,说明星点设计-效应面法所建立的模型预测性良好,可较好地应用于NAR包合物自微乳的处方优化。
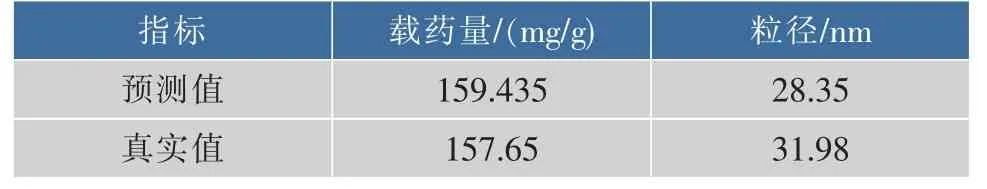
表4 星点设计-效应面优化法验证Table 4 Verification of the central composite designresponse surface methodology
其中,载药量偏差为1.12%,粒径偏差为1.28%。
3 结语
自微乳的基本组成包括油相、乳化剂和助乳化剂,本处方油相筛选时,选用半合成中链甘油三酯衍生物,因其具有不同的饱和度或水解基团,可增加药物的溶解度并具有一定的乳化能力。本研究中乳化剂的选择一般采用高亲水亲油平衡 (HLB11-15)值的非离子型乳化剂,如较为常用的聚山梨酯80、Cremophor RH40等,可改变小肠上皮细胞膜的流动性和细胞间紧密连接,增加药物的膜渗透性,改善药物的吸收。处方中助乳化剂选择能与乳化剂相溶的低相对分子质量的醇类如PEG400、异丙醇等可辅助溶解药物,主要用于提高膜的牢固性和界面膜的柔顺性流动性,调节助乳化剂的HLB值,同时又减少乳化剂的用量,降低其潜在毒性。
在自微乳处方筛选中,通过测定NAR-β-CD包合物溶解度,可以看出NAR-β-CD包合物在各介质中溶解度明显大于NAR在各介质中的溶解度,但NAR在油酸乙酯中溶解度仍然最大,且明显大于其他油相[9]。NAR在乳化剂聚山梨酯80和OP乳化剂中溶解度均较好;在助乳化剂PEG 400中溶解度最大,异丙醇次之,但溶解度相差不是太大,均可考虑作为处方成分使用。
β-CD包合和制成自微乳都是增加难溶性药物溶解度和提高难溶性药物口服生物利用度的常用方法,本研究首次将包合技术和自微乳化技术相结合,先将NAR制成包合物,增加了NAR的溶解度和稳定性,再将NAR-β-CD包合物制成自微乳,进一步增加NAR的溶解度,此方法拓展了包合技术的应用范畴,创新了自微乳化技术的形式。
作者在测定溶解度的基础上采用伪三元相图所形成微乳区的大小初步筛选乳化剂和助乳化剂,在相同Km时,乳化剂为聚山梨酯80,助乳化剂为PEG400时所形成的区域最大。
运用星点设计-效应面法进一步优化NAR-β-CD包合物自微乳处方时,以载药量和粒径为考察指标,粒径越小,油水界面积越大,稳定性、吸收越好,生物利用度越高;载药量愈大,越有利于灵活调整临床用药剂量,愈易满足临床需要。
前期实验将NAR制成NAR-β-CD包合物,并比较了两者在人工胃液中90 min的累积溶出率,结果表明,NAR制成NAR-β-CD包合物后溶出度显著提高。将NAR-β-CD包合物制成自微乳后,其溶出度是否比NAR-β-CD包合物高,在后续工作中有待进一步研究。
[1]ZHANG Fayun,DU Gangjun,ZHANG Ling,et al.Naringenin enhances the anti-tumor effect of doxorubicin through selectively inhibiting the activity of multidrug resistance-associated proteins but not P-glycoprotein[J].Pharmaceutical Research,2009,26(4):914-925.
[2]Fenglin Yen,Tzu-Hui Wu,Liang-Tzung Lin,et al.Naringenin-loaded nanoparticles improve the physicochemical propertie and the hepatoprotective effects of naringenin in orally-administered rats with CCl4-induced acute liver failure life[J]. Pharmaceutical Research,2009,26(4):893-902.
[3]YANG Hongliang,TIAN Heng,LI Peibo,et al.Investigate on the biological activities of Naringin and Naringenin[J].Journal of Chinese Medicinal Materials,2007,30(6):752-754.(in Chinese)
[4]LIU Yanjie,XIANG Rongwu.Application of central composite design/response surface methodology in pharmacy experiment design[J].Chinese Journal of Modern Applied Pharmacy,2007,24(6):455-457.(in Chinese)
[5]EHAB H,ADEL S.Application of multiple response optimization technique to extended release formulations design[J].J Control Release,2001,73(2-3):329-338.
[6]LV Juanli,LI Yan,SHEN Dan,et al.Microemulsion promote a summary of the mechanism of drug oral absorption and application[J].China Pharmacist,2008,11(5):575-578.(in Chinese)
[7]XU Xinrong,YU Haitao,HANG Li,et al.Preparation of inclusion complex of naringenin and β-cyclodextrin and inhibitory effects of it on choroidal neovascularization in model rats[J].China Pharmacy,2014,25(11):981-984.(in Chinese)
[8]YE Lei,HU Rongfeng,WANG Xiaohua,et al.Optimization of puerarin self-microemulsifying system using central composite design-resonse surface methodology[J].Chinese Traditional Patent Medicine,2014,36(3):514-519.
[9]WANG Zhangjie,HU Rongfeng,WANG Guokai,et al.Optimization of self-microemulsifying drug delivery system of naringenin by box-behnken design and response surface method[J].Chinese Traditional and Herbal Drugs,2014,45(17):2461-2466.
Optimization of Self-Microemulsifying Drug Delivery System for Naringenin-β-Cyclodextrin Inclusion Complex by Central Composite Design and Response Surface Method
WANG Zhangjie, SHI Lingli, HUA Fang, YANG Mengfan
(School of Pharmaceutical Sciences,Anhui Xinhua College,Hefei 230088,China)
This study was aim to investigate the formula of self-microemulsifying drug delivery system for naringenin naringenin-β-cyclodextrin (NAR-β-CD)inclusion complex by central composite design-response surface method.The solubility test of NAR-β-CD inclusion complex in different secondary solvents and pseudotemary phase diagam were utilized to select components of NAR-β-CD inclusion complex self-microemulsifying drug delivery system.According to the drug loading and particle size of naringenin in different self-microemulsifying drug prescriptions,the optimal prescription was determined using the central composite design and response surface method.The optimal prescription of NAR-β-CD inclusion complex self-microemulsifying drug delivery system was composed of Ethyloleate(oil),Polysorbate 80 (surfactant),and PEG 400(co-surfactant),with oil ratio of 14.39%,and the Kmat 2.05.The drug loading of naringenin was 159.435 mg/g,and particle size was 28.35 nm.
NAR-β-CD inclusion complex,self-microemulsifying;centralcompositedesign,response surface
TS 23
A
1673—1689(2017)03—0310—05
2015-03-18
国家级大学生创新创业训练计划项目(201312216024);安徽高校自然科学研究项目(KJ2016A312);安徽新华学院校级质量工程项目(2013jgkcx02);安徽新华学院校级科研项目(2013zr008)。
王章姐(1982—),女,安徽枞阳人,医学硕士,副教授,主要从事药物新剂型方面的研究。E-mail:40462634@qq.com
王章姐,施伶俐,华芳,等.星点设计-效应面法优化柚皮素包合物自微乳给药系统[J].食品与生物技术学报,2017,36(03):310-314.

