二(2,2-二硝基丙基)硝胺的合成及热性能
刘卫孝,姬月萍,2,陈 斌,高福磊,汪营磊,刘亚静,潘永飞,闫峥峰
(1.西安近代化学研究所,西安 710065;2.氟氮化工资源高效开发与利用国家重点实验室,西安 710065)
二(2,2-二硝基丙基)硝胺的合成及热性能
刘卫孝1,姬月萍1,2,陈 斌1,高福磊1,汪营磊1,刘亚静1,潘永飞1,闫峥峰1
(1.西安近代化学研究所,西安 710065;2.氟氮化工资源高效开发与利用国家重点实验室,西安 710065)
以2,2-二硝基丙醇为原料,经缩合、硝化反应合成了二(2,2-二硝基丙基)硝胺(BDNPN)。用红外光谱、核磁共振、元素分析对中间体及目标化合物的结构进行了表征。优化了反应条件,硝化反应的最佳条件为nBDNPA:nHNO3=1∶30,反应温度为50 ℃,反应时间为1 h,收率92.1%。用DSC和TG-DTG考察了目标化合物的热性能。结果表明, BDNPN的热分解峰温为212.3 ℃,具有较好的热稳定性。
有机化学;二(2,2-二硝基丙基)硝胺;BDNPN;合成;表征;热性能
0 引言
偕二硝基类含能化合物具有能量适中、安定性好等特点,被广泛用于推进剂及炸药中[1-6]。二(偕二硝基丙基)硝胺(BDNPN)是偕二硝基类含能化合物的一个典型代表,其热稳定性好,与硝化棉等大多数材料的相容性好,其能量与RDX相当,非常有望作为RDX替代物,用于推进剂、发射药配方中[7]。 2010年,美国陆军军备研究、开发与工程中心以BDNPN取代RDX,用于改性单基发射药中,弹药钝感性能明显提升,且不会过多损失能量,相关配方在60 mm火炮中进行了演示验证,各项指标非常优异[8]。然而,在上述研究前,国内外关于BDNPN合成和热性能的相关研究未见公开报道。2012年,Saikia A[9]等以BDNPA为起始原料,利用微波辅助合成手段,成功制备了BDNPN,收率达到85%,但文中未提及二(2,2-二硝基丙基)胺(BDNPA)的制备方法。
本研究以2,2-二硝基丙醇(DNPOH)为起始原料,与氨经mannich缩合,得到中间体BDNPA,并参考文献[9]合成路线,利用常规加热方式,以硝酸为硝化剂对BDNPA进行硝化,得到目标化合物BDNPN;通过对合成反应条件进行优化,降低了硝化反应温度(文献值65 ℃[9]),提高了反应收率;采用DSC、TG-DTG热分析方法,对中间体和目标化合物的热分解性能进行了研究,为应用研究提供参考。
1 实验
1.1 试剂及仪器
2,2-二硝基丙醇,纯度≥98%(HPLC),自制;乙酸铵,乙酸酐、浓硫酸等均为分析纯;硝酸(质量分数≥98%)为工业品。
NEXUS 807型傅里叶变换红外光谱仪,美国热电尼高力公司;AV 500型(500 MHz)超导核磁共振仪,瑞士BRUKER公司;VARIO-EL-3型元素分析仪,德国EXEMENTAR公司;LC-2010A型高效液相色谱仪(归一化法),日本岛津公司;Q-200型差示扫描量热仪,美国TA公司;TA 2950热重仪,美国Nicolet公司;X-6型显微熔点仪,北京泰克仪器有限公司。
1.2 合成路线
以2,2-二硝基丙醇为原料,经缩合反应生成中间体二(2,2-二硝基丙基)胺(BDNPA),再经过硝化反应得到目标化合物二(2,2-二硝基丙基)硝胺(BDNPN),合成路线如图1所示。
1.3 化合物的合成
1.3.1 二(2,2-二硝基丙基)胺(BDNPA)的合成
将DNPOH(11.3 g,0.075 mol)和20 ml水加入反应瓶中,溶解后,加热升温至60 ℃,搅拌下分批加入乙酸铵(2.3 g,0.03 mol),保温20 min后,降至室温,析出大量白色固体,经过滤、水洗、干燥得二(2,2-二硝基丙基)胺(BDNPA)6.8 g,收率80.1%,纯度98.5%,熔点66~69 ℃。
1H NMR(DMSO-d6,500 MHz),δ:2.08(s,6 H,CH3),3.23(m,1 H,NH),3.72(m,4 H,CH2);IR(KBr),υ(cm-1):3 383(N—H);2 932(—CH3):1 336,1 576(—NO2);元素分析(C6H11O8N5,%):计算值,C25.31,H3.92,N23.75;实验值,C25.62,H3.92,N24.91。
1.3.2 二(2,2-二硝基丙基)硝胺(BDNPN)的合成
在反应瓶中加入20 ml浓硝酸,搅拌下加热升温至50 ℃,分批加入BDNPA(5 g,0.018 mol),反应过程放热明显,加完后保温1 h,迅速倒入冰水中搅拌,出现大量白色沉淀,过滤、水洗至洗涤液呈中性,干燥得白色固体6.04 g,收率92.1%,纯度98.7%,熔点189.3 ℃(DSC,10 ℃/min)。
1H NMR(DMSO-d6,500 MHz),δ:2.36(s,6 H,CH3),5.39(s,4 H,CH2);IR(KBr),υ(cm-1):2 940(—CH3):1 342,1 603(—NO2);元素分析(C6H10O10N6,%):计算值,C22.08,H3.07,N25.76;实验值,C22.22,H3.01,N24.18。
1.4 BDNPA和BDNPN的热性能
采用差示扫描量热(DSC)、热失重(TG-DTG)热分析方法,研究了BDNPA和BDNPN的热分解性能。
2 结果与讨论
2.1 缩合反应条件优化
2.1.1 反应物料摩尔比对BDNPA收率的影响
考察了在反应温度为60 ℃、反应时间为20 min的情况下,不同反应物料摩尔比对BDNPA收率(η)的影响,结果如表1所示。
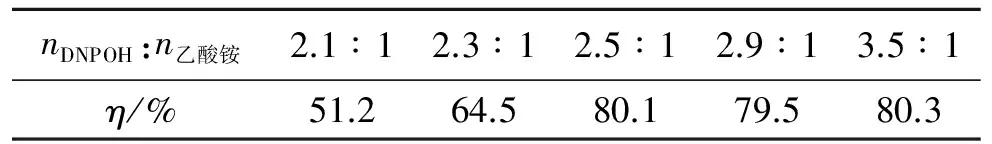
表1 反应物料摩尔比对BDNPA收率的影响
由表1可看出,BDNPA的收率受反应料比的影响较大。随着DNPOH加入量的增加,反应收率明显提高,当DNPOH和乙酸铵的摩尔比为2.5∶1时,收率为80.1%,继续增加DNPOH的加入量收率变化不大。因此,综合考虑,最佳的反应料比为2.5∶1。
2.1.2 反应温度对BDNPA收率的影响
在nDNPOH:n乙酸铵为2.5∶1,反应时间为20 min的情况下,考察了反应温度(T)对BDNPA收率(η)的影响,结果如表2所示。

表2 反应温度对BDNPA收率的影响
由表2可看出,当反应温度低于30 ℃时,几乎不反应,随着温度的逐渐升高,反应收率明显提高,当反应温度为60 ℃时,收率为80.1%,之后继续升高,反应温度就会因为副反应的加强而影响收率。因此,60 ℃为反应的最佳温度。
2.2 硝化反应条件优化
2.2.1 硝化剂和反应物料摩尔比对BDNPN收率的影响
控制硝化反应温度在50 ℃,反应1 h,考察不同硝化体系和反应物料摩尔比对BDNPN收率(η)的影响,结果如表3所示。表3中,H2SO4和(CH3CO)2O均作为脱水剂。

表3 硝化剂和反应物料摩尔比对BDNPN收率的影响
在硝化反应中,硝化体系和用量对反应结果有很大的影响。本实验选用3种常用的硝化体系进行硝化反应。从表3中可看出,随着硝酸用量的增加,收率逐渐增加,当nBDNPA:nHNO3达到1∶30时,再增加硝酸用量,收率没有明显增加;此外,在硝酸用量相同的情况下,通过加入H2SO4和(CH3CO)2O作为脱水剂,收率依然没有明显提高。因此,综合考虑,选择HNO3作为硝化剂,HNO3与底物的最佳摩尔比为1∶30。
2.2.2 反应温度对BDNPN收率的影响
物料比nBDNPA:nHNO3=1∶30,反应时间为1 h,考察了不同反应温度(T)对BDNPN收率(η)的影响,结果如表4所示。
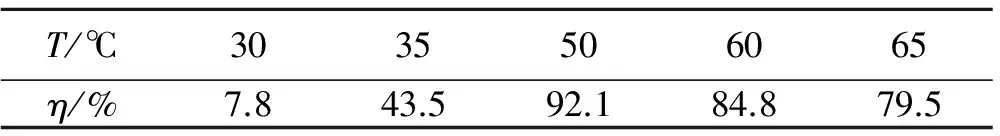
表4 反应温度对BDNPN收率的影响
在高温硝化时,需要外界提供一定的热量,以维持反应的进行,但温度过高,又会导致产物分解和促进副反应的发生,从而影响反应收率。表4中给出的结果表明,随着反应温度的升高,收率随之增加,当温度大于50 ℃时,反应的收率开始降低。因此,最适宜的硝化温度为50 ℃。
2.3 BDNPA和BDNPN的热性能
图2为升温速率为10 ℃/min时BDNPA的热分解DSC曲线。从图2可看出,曲线上存在1个强的吸热峰和1个放热峰,在65.5 ℃处较尖的吸热峰为BDNPN的熔点,与熔点仪测试的结果基本一致,173.7 ℃为BDNPA分解放热峰,放热峰出现一个台阶,说明样品的分解不是一步完成。
图3为BDNPA在常压下的TG-DTG曲线。从图3可看出,当温度低于110 ℃失重很小,累积失重仅0.4%,说明液态BDNPA在较大的温度范围内仍较稳定;在温度从120 ℃上升到200 ℃的过程中,该物质快速分解失重,累积失重达到95.1%,在失重峰曲线下行时,同样出现了一个台阶,从而进一步证实了该物质存在二次分解的观点。
图4为升温速率为10 ℃/min时BDNPN的热分解DSC曲线。从图4可看出,曲线上存在1个吸热峰和1个放热峰,在189.3 ℃处吸热峰为BDNPN的熔点,熔化完毕后,随即开始分解,这与通过熔点仪测试熔点时,当观察到样品即将熔化时,立刻变成棕黄色的现象一致,212.3 ℃为BDNPA分解放热峰。
图5为BDNPN在常压下的TG-DTG曲线。从图5可看出,当温度低于170 ℃时,热稳定性很好,累积失重仅0.7%; 171 ℃时,失重速率开始增加,当温度到达255 ℃时,分解后的残余仅2.5%。结合其DSC和TG-DTG热分析结果可看出, BDNPN热分解温度较高,分解后残留少,是一种热性能优异的含能材料。
通过对比图2和图4可看出,BDNPN的热分解温度明显高于BDNPA,主要因为BDNPA分子中亚氨基上活泼氢的酸性降低了化合物的热稳定性,活泼氢被硝基取代后,热稳定性大幅提高。
3 结论
(1)以2,2-二硝基丙醇为原料,经缩合、硝化反应合成了二(2,2-二硝基丙基)硝胺(BDNPN)。用红外光谱、核磁共振、元素分析,对中间体及目标化合物的结构进行了表征。
(2)缩合反应的最佳反应条件为nDNPOH:n乙酸铵=2.5∶1,反应温度为60 ℃,反应时间为20 min,收率80.1%,纯度98.5%;硝化反应的最佳反应条件为nBDNPA:n硝酸=1∶30,反应温度为50 ℃,反应时间为1 h,收率92.1%,纯度98.7%。
(3)BDNPA和BDNPN的热分解峰温分别为173.7 ℃和212.3 ℃,热稳定性均较好,有望在固体推进剂和发射药中得到应用。
[1] 姬月萍, 李普瑞, 汪伟, 等. 含能增塑剂的现状和发展[J]. 火炸药学报, 2005, 28(4):47-51.
[2] 刘亚静, 陈斌, 刘卫孝, 等. 绿色方法合成2,2-二硝基-1,3-丙二醇[J]. 含能材料, 2010, 18(6):623-626.
[3] 张丽洁, 姬月萍, 陈斌, 等. 1,3,5,5-四硝基六氢嘧啶的高收率合成[J]. 含能材料, 2012, 20(4):441-444.
[4] 张寿忠, 朱天兵, 冯晓晶, 等. 2, 2 -二硝基丁醇的合成及其应用[J]. 化学推进剂与高分子材料, 2012, 10(3):27-29.
[5] 陈斌, 张志忠, 姬月萍. 偕二硝基类含能增塑剂的合成及应用[J]. 火炸药学报, 2007, 30(2):67-70.
[6] 王文浩, 周集义. BDNPA/F增塑剂的合成及其发展[J]. 含能材料, 2007, 15(1):90-93.
[7] Rozumov E, Chiu D, Manning T G, et al. RDX and BDNPN as composite fillers for propellant formulations[C]//Proceedings of the 42nd JANNAF Combustion Subcommittee. Boston, Massachusetts, 2008.
[8] Eugene Rozumov, Thelma Manning, Duncan Park, et al. BDNPN as an energetic additive for propellant formulations[C]//41st International Annual Conference of ICT, 2010.
[9] Saikia A, Sivabalan R, Gore G M, et al. Microwave-assisted quick synthesis of some potential high explosives[J]. Propellants Explos. Pyrotech., 2012, 37(5):540-543.
(编辑:崔贤彬)
Synthesis and thermal performance of bis(2,2-dinitropropyl)nitramine
LIU Wei-xiao1, JI Yue-ping1,2, CHEN Bin1, GAO Fu-lei1, WANG Ying-lei1,LIU Ya-jing1, PAN Yong-fei1, YAN Zheng-feng1
(1.Xi'an Modern Chemistry Research Institute, Xi'an 710065, China;2.State Key Laboratory of Fluorine & Nitrogen Chemicals, Xi'an 710065, China)
Bis(2,2-Dinitropropyl)nitramine(BDNPN) was synthesized via condensation and nitration using 2,2-dinitropropanol as starting material.The structures of intermediate and target compound were characterized by IR,NMR,elemental analysis. The factors influencing the condensation and nitration were investigated.The optimized nitration conditions were determined that the molar ratio ofnBDNPN:nHNO3was 1∶30 for 1 hours at 50 ℃,the yield of BDNPN is 92.1%. The thermal performance of target compound was studied using DSC and TG-DTG.The result shows that the peak temperature of the exothermic decomposition reaction of BDNPN is 212.3 ℃, revealing that BDNPN has preferable thermal stability.
organic chemistry;bis(2,2-dinitropropyl)nitramine;BDNPN;synthesis;characterization;thermal performance
2016-11-12;
2016-12-26。
刘卫孝(1983—),男,工程师,研究方向为含能材料合成。E-mail:liuwx1983@126.com
V512
A
1006-2793(2017)02-0204-04
10.7673/j.issn.1006-2793.2017.02.013

