贝伐珠单抗或抗EGFR单抗联合FOLFOX方案治疗晚期转移性结直肠癌的临床研究
李伟 李威威 宋锐 张海萍
·论著·
贝伐珠单抗或抗EGFR单抗联合FOLFOX方案治疗晚期转移性结直肠癌的临床研究
李伟 李威威 宋锐 张海萍
目的 探讨贝伐珠单抗或抗表皮生长因子受体(epidermal growth factor receptor,EGFR)单抗联合FOLFOX方案(奥沙利铂85 mg/m2+5-氟尿嘧啶400 mg/m2+亚叶酸钙200 mg/m2)治疗晚期转移性结直肠癌(metastatic colorectal cancer,mCRC)的临床疗效。方法 选取2011年3月至2014年10月入院治疗的晚期mCRC患者67例作为研究对象,根据化疗方式的不同将其分为FOLFOX组22例、贝伐珠单抗+FOLFOX组22例、抗EGFR单抗+FOLFOX组23例。记录3组患者治疗期间疗效以及不良反应发生等情况并进行比较。结果 贝伐珠单抗+FOLFOX组、抗EGFR单抗+FOLFOX组晚期mCRC患者总缓解率9(40.91%)、8(34.78%)均显著高于FOLFOX组5(22.73%),差异有统计学意义(χ2值依次为3.617、2.963,均P<0.05),贝伐珠单抗+FOLFOX组总缓解率略高于抗EGFR单抗+FOLFOX组,差异无统计学意义(χ2=0.704,P>0.05);贝伐珠单抗+FOLFOX组、抗EGFR单抗+FOLFOX组晚期mCRC患者总控制率18(81.82%)、18(78.26%)均显著高于FOLFOX组13(59.09%),差异有统计学意义(χ2值依次为2.909、2.787,均P<0.05),贝伐珠单抗+FOLFOX组总控制率略高于抗EGFR单抗+FOLFOX组,差异无统计学意义(χ2=1.054,P>0.05)。贝伐珠单抗+FOLFOX组、抗EGFR单抗+FOLFOX组晚期mCRC患者中位无进展生存期(Medianprogressionfreesurvival,mPFS) 9.6个月、10.2个月均显著高于FOLFOX组7.5个月,差异有统计学意义(χ2值依次为2.714、3.157,均P<0.05),抗EGFR单抗+FOLFOX组mPFS略高于贝伐珠单抗+FOLFOX组,差异无统计学意义(χ2=0.935,P>0.05);贝伐珠单抗+FOLFOX组、抗EGFR单抗+FOLFOX组晚期mCRC患者中位总生存期(Medianoverallsurvival,mOS) 24.1个月、26.4个月均显著高于FOLFOX组18.3个月,差异有统计学意义(χ2值依次为2.909、3.371,均P<0.05),抗EGFR单抗+FOLFOX组mOS略高于贝伐珠单抗+FOLFOX组,差异无统计学意义(χ2=1.177,P>0.05)。3组患者不良反应发生情况比较差异无统计学意义(均P>0.05)。结论 贝伐珠单抗或抗EGFR单抗联合FOLFOX两种化疗方案对于晚期mCRC患者治疗均疗效显著,贝伐珠单抗+FOLFOX化疗方案总缓解率和总控制率稍高,抗EGFR单抗+FOLFOX化疗方案mPFS和mOS稍长,且不良反应发生情况均未见增加,该两种化疗方案均可在临床进行推广。
贝伐珠单抗;抗EGFR单抗;FOLFOX方案;转移性结直肠癌
CRC是消化系统常见的恶性肿瘤之一[1],据世界卫生组织(WorldHealthOrganization,WHO)最新统计结果显示CRC在所有恶性肿瘤中的发病率排第3位、死亡率排第4位,在国内其发病率呈逐年上升趋势,近年来备受关注[2,3]。目前针对mCRC的标准化疗方案是5-氟尿嘧啶、亚叶酸钙为基础联合伊立替康(FORFIRI方案)或奥沙利铂(FOLFOX方案)[4]。贝伐珠单抗、抗EGFR单抗作为两种不同类型的靶向药物在mCRC一线及二线治疗中得到了广泛应用,本研究选取2011年3月至2014年10月于本院入院治疗的晚期mCRC患者67例作为研究对象,探讨贝伐珠单抗或EGFR单抗联合FOLFOX方案治疗晚期mCRC的临床疗效,并对其不良反应发生情况进行详细比较,现作汇报如下。
1 资料与方法
1.1 一般资料 选取2011年3月至2014年10月于本院入院治疗的晚期mCRC患者67例作为研究对象,所有患者均经病理明确诊断并确诊[5]。其中男50例,女17例;年龄28~74岁,平均年龄(55.49±7.57)岁。其中结肠癌患者30例,直肠癌患者37例;高分化患者18例,中分化患者45例,低分化患者4例;肝转移患者46例,肺转移患者17例,盆腔转移患者4例。根据化疗方式的不同将其分为FOLFOX组22例、贝伐珠单抗+FOLFOX组22例、抗EGFR单抗+FOLFOX组23例。纳入标准[6]:(1)所有患者观察指标明确,病灶大小可经CT或MRI检测;(2)既往一线方案治疗失败至本次研究分组时间超过4周以上;(3)患者均无化疗禁忌证且肝肾功能白细胞血小板均正常;(4)患者ECOG评分超过70分;(5)所有患者无第二原发肿瘤。
1.2 药品 奥沙利铂(江苏奥赛康药业股份有限公司提供,批号:20100957,规格:50mg/支),5-氟尿嘧啶(上海旭东海普药业有限公司提供,批号:20101107,规格:250mg/支),亚叶酸钙(连云港金康医药科技有限公司提供,批号:20100911,规格:100mg/支),贝伐珠单抗(上海罗氏制药有限公司提供,批号:20110107,规格:100mg/支),抗EGFR单抗(百泰生物药业有限公司提供,批号:20110201,规格:50mg/支)。
1.3 方法
1.3.1FOLFOX组:于化疗第1天静脉滴注奥沙利铂85mg/m22h,第1~2天静脉滴注亚叶酸钙200mg/m22h,第1~2天静脉注射5-氟尿嘧啶400mg/m2,第1~2天持续46h静脉滴注5-氟尿嘧啶600mg/m2,以2周为1周期。
1.3.2 贝伐珠单抗+FOLFOX组:在FOLFOX组化疗方案的基础上于化疗当天使用贝伐珠单抗10mg/kg+0.9%氯化钠注射液100ml持续静脉滴注60min(第1次应用时长为90min),以2周为1周期。
1.3.3 抗EGFR单抗+FOLFOX组:在FOLFOX组化疗方案的基础上于化疗当天使用抗EGFR单抗100mg+0.9%氯化钠注射液250ml持续静脉滴注60min(第1次应用时长为90min),每周1次,以2周为1周期。3组患者化疗前后均常规予以止吐处理;本研究均采用易蒙停每2小时口服对症处理腹泻症状。本研究于4~6个化疗周期结束后7d对患者临床疗效进行评价,复查影像学评价疗效,治疗后对所有患者血常规、肝肾功能每周进行检查。
1.4 评价指标[7]本研究疗效评价依RICIST1.1实体瘤客观疗效评定标准,分为完全缓解(CR)、部分缓解(PR)、疾病稳定(SD)以及疾病进展(PD)四部分,其中总缓解=CR+PR,总控制=CR+PR+SD。本研究不良反应评价依美国国家癌症研究所常见不良反应事件术语评定标准(CTCAE)4.0.2版进行评定,分为0、Ⅰ、Ⅱ、Ⅲ、Ⅳ度[8]。
1.5 统计学分析 应用SPSS21.0统计软件,3组mCRC患者间平均年龄比较采用One-WayANOVO单因素方差分析、组内差异两两比较采用S-N-K检验,计数资料采用χ2检验,P<0.05为差异有统计学意义。
2 结果
2.1 3组晚期mCRC患者一般资料比较 3组患者性别比、平均年龄以及转移类型之间比较差异无统计学意义(均P>0.05),具有可比性。见表1。
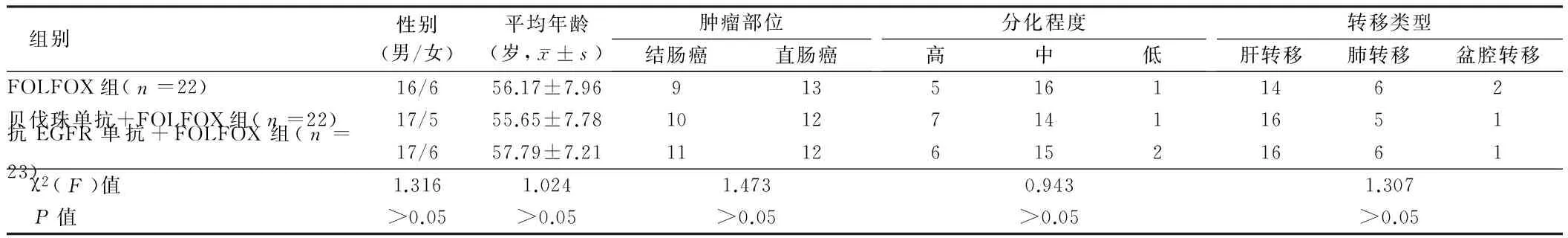
表1 3组晚期mCRC患者一般资料比较 例
2.2 3组晚期mCRC患者近期疗效比较 贝伐珠单抗+FOLFOX组、抗EGFR单抗+FOLFOX组晚期mCRC患者总缓解率(40.91%、34.78%)均显著高于FOLFOX组(22.73%),差异均有统计学意义(χ2值依次为3.617、2.963,均P<0.05),贝伐珠单抗+FOLFOX组总缓解率略高于抗EGFR单抗+FOLFOX组,差异无统计学意义(χ2=0.704,P>0.05);贝伐珠单抗+FOLFOX组、抗EGFR单抗+FOLFOX组晚期mCRC患者总控制率18(81.82%)、18(78.26%)均显著高于FOLFOX组13(59.09%),差异均有统计学意义(χ2值依次为2.909、2.787,均P<0.05),贝伐珠单抗+FOLFOX组总控制率略高于抗EGFR单抗+FOLFOX组,差异无统计学意义(χ2=1.054,P>0.05)。见表2。
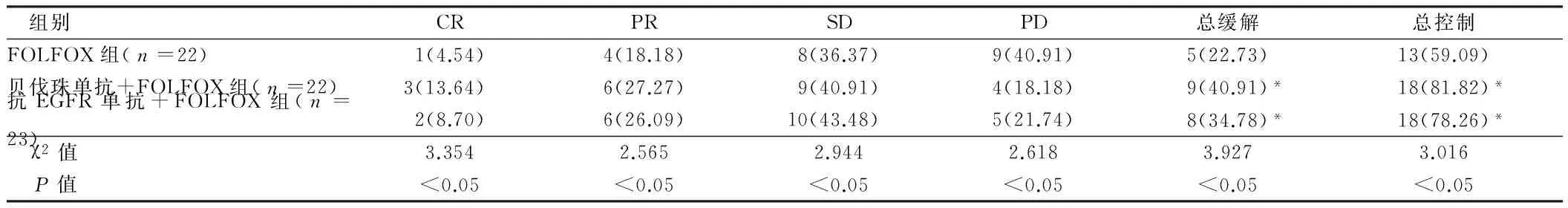
表2 3组晚期mCRC患者近期疗效比较 例(%)
注: 与FOLFOX组比较,*P<0.05
2.3 生存分析 对所有mCRC患者采用电话与门诊随访相结合的方式随访至2016年1月,所有患者总体mPFS9.2个月,总体mOS22.7个月。贝伐珠单抗+FOLFOX组、抗EGFR单抗+FOLFOX组晚期mCRC患者mPFS9.6个月、10.2个月均显著高于FOLFOX组7.5个月,差异均有统计学意义(χ2值依次为2.714、3.157,均P<0.05),抗EGFR单抗+FOLFOX组mPFS略高于贝伐珠单抗+FOLFOX组,不具有统计学差异(χ2=0.935,P>0.05);贝伐珠单抗+FOLFOX组、抗EGFR单抗+FOLFOX组晚期mCRC患者mOS24.1个月、26.4个月均显著高于FOLFOX组18.3 个月,差异均有统计学意义(χ2值依次为2.909、3.371,均P<0.05),抗EGFR单抗+FOLFOX组mOS略高于贝伐珠单抗+FOLFOX组,差异无统计学意义(χ2=1.177,P>0.05)。
2.4 3组晚期mCRC患者不良反应发生率比较 3组晚期mCRC患者治疗期间常见的不良反应为恶心呕吐、头晕、神经毒素、腹泻、肝肾功能损伤、白细胞下降以及血小板下降,主要为Ⅰ~Ⅱ度,经医护人员及时对症治疗后大部分患者均可耐受。3组晚期mCRC患者不良反应发生情况比较,差异无统计学意义(均P>0.05)。见表3。
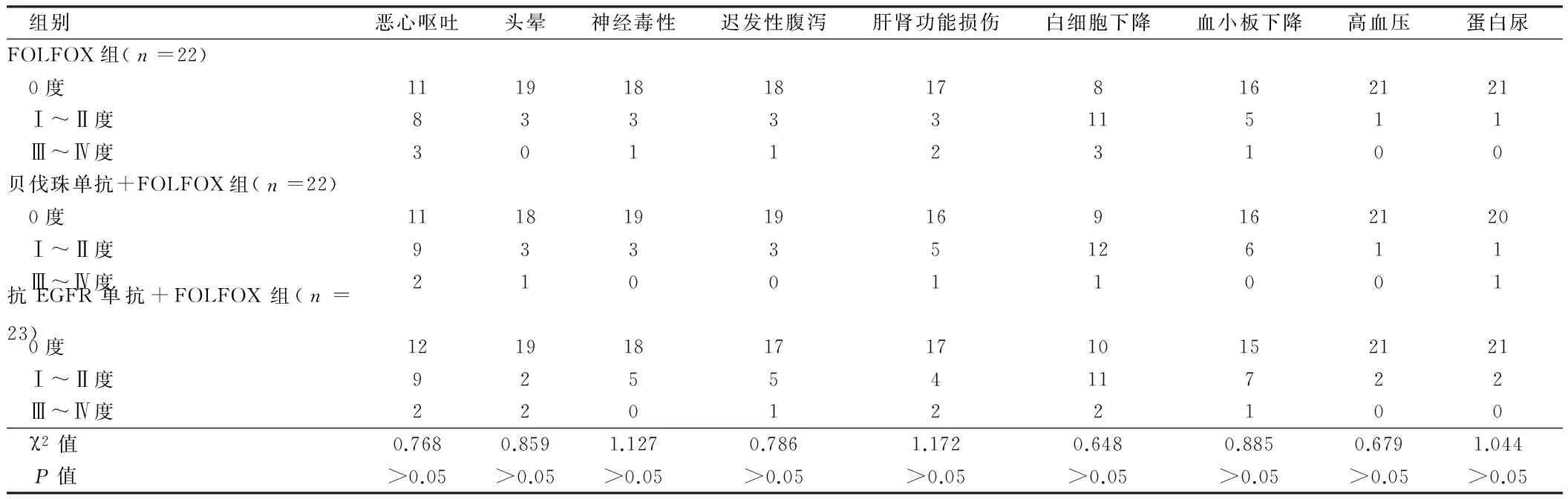
表3 3组晚期mCRC患者不良反应发生率比较 例
3 讨论
贝伐珠单抗、抗EGFR单抗作为两种不同类型的抗属肿瘤靶向治疗药物在mCRC一线及二线治疗中均得到了广泛应用[9]。贝伐珠单抗是一种重组的新型抗血管内皮生长因子的人源化IgG1单克隆抗体,其作用机制是通过选择性竞争血管内皮生长因子并与其受体相结合来阻断肿瘤细胞的增值与分裂。搜集国外研究资料表明5-氟尿嘧啶、亚叶酸钙为基础联合FOLFOX方案可显著提高患者的PFS以及OS,且不增加其不良反应的发生[10]。抗EGFR单抗主要用于CRC、非小细胞肺癌以及头颈癌等恶性实体瘤的治疗,搜集文献资料显示抗EGFR单抗不仅可以直接杀伤EGFR表达的肿瘤细胞,还具有通过增强细胞免疫功能来产生对肿瘤细胞的细胞免疫杀伤作用,这与Merck公司的抗体Erbitux具有类似的作用[11,12]。
谢永铮等[13]也对贝伐珠单抗联合FOLFOX治疗晚期mCRC的临床疗效及安全性评价进行了探讨,研究结果表明伐珠单抗+FOLFOX化疗方案在不增加不良反应的同时可显著提高临床疗效,值得推广应用;搜集文献资料显示有关抗EGFR单抗+FOLFOX化疗方案的报道较为少见。在总结上述经验与结合本院实际的基础上,本研究贝伐珠单抗+FOLFOX组、抗EGFR单抗+FOLFOX组晚期mCRC患者总缓解率9(40.91%)、8(34.78%)均显著高于FOLFOX组5(22.73%),与裴保香等[14]贝伐单抗联合不同化疗方案治疗mCRC中关于贝伐珠单抗+FOLFOX组的总有效率39.1%(9/23)相一致;贝伐珠单抗+FOLFOX组总缓解率略高于抗EGFR单抗+FOLFOX组,不具有统计学差异;贝伐珠单抗+FOLFOX组、抗EGFR单抗+FOLFOX组晚期mCRC患者总控制率18(81.82%)、18(78.26%)均显著高于FOLFOX组13(59.09%),略低于文献[14]中关于贝伐珠单抗+FOLFOX组总控制率82.6%(19/23),仍有待改善;贝伐珠单抗+FOLFOX组总控制率略高于抗EGFR单抗+FOLFOX组,不具有统计学差异。贝伐珠单抗+FOLFOX组、抗EGFR单抗+FOLFOX组晚期mCRC患者mPFS9.6个月、10.2个月均显著高于FOLFOX组7.5个月,略高于王巍等[15]贝伐珠单抗联合双周方案治疗45例mCRC患者中mPFS为9.0个月的报道;抗EGFR单抗+FOLFOX组mPFS略高于贝伐珠单抗+FOLFOX组,不具有统计学差异;贝伐珠单抗+FOLFOX组、抗EGFR单抗+FOLFOX组晚期mCRC患者mOS24.1个月、26.4个月均显著高于FOLFOX组18.3个月,但未见文献对OS的相关报道;抗EGFR单抗+FOLFOX组mOS略高于贝伐珠单抗+FOLFOX组。3组患者不良反应发生情况比较不具有统计学差异。是否将贝伐珠单抗+FOLFOX或抗EGFR单抗+FOLFOX分别交叉应用于mCRC患者的一线或二线治疗中可提高患者的疗效,有待于进一步探讨。
总之,贝伐珠单抗或抗EGFR单抗联合FOLFOX两种化疗方案对于晚期mCRC患者治疗均疗效显著,贝伐珠单抗+FOLFOX化疗方案总缓解率和总控制率稍高,抗EGFR单抗+FOLFOX化疗方案mPFS和mOS
稍长,且不良反应发生情况均未见增加,该两种化疗方案均可在临床进行推广。
1 张红梅,徐伶伶,安广宇.贝伐单抗联合FOLFIRI方案一线治疗转移性结直肠癌的临床评价.肿瘤防治研究,2012,39:1001-1004.
2PanCC,TsaiCM.Concomitantprimarylungcancerandmetastaticpulmonarycolorectalcancerthatrespondedtogemcitabine/cisplatin/bevacizumabcombinationtherapy.JournalofCancerResearchandPractice,2015,2:227-232.
3CollocaG,VenturinoA,GuarneriD.Analysisofclinicalendpointsofrandomisedtrialsincludingbevacizumabandchemotherapyversuschemotherapyasfirst-linetreatmentofmetastaticcolorectalcancer.ClinicalOncology,2016,25:128-135.
4 朱春荣,李大鹏,熊峰,等.贝伐珠单抗联合FOLFIRI方案治疗晚期转移性结直肠癌患者的临床观察.中国肿瘤临床,2012,39:1437-1439.
5 时淑珍,于韦韦,张捷,等.贝伐珠单抗联合FOLFIRI方案一线治疗转移性结直肠癌的临床研究.癌症进展,2013,11:461-464,479.
6 张秦,朱有才,鲍晋,等.贝伐珠单抗联合FOLFOX4化疗方案治疗晚期转移性结直肠癌的临床研究.中国临床药理学杂志,2015,31:345-347.
7 吴倩,石燕,陈丽,等.贝伐珠单抗联合FOLFOX或FOLFIRI方案治疗转移性结直肠癌的临床研究.临床肿瘤学杂志,2013,18:224-228.
8 孙艳坤,刘国恩,等.贝伐珠单抗治疗转移性结直肠癌的效果与成本研究综述.药物经济,2013,4:9-15.
9 蔡君,马红,朱涤潮,等.转移性结直肠癌贝伐单抗治疗中高血压的发生情况及客观有效率.肿瘤学杂志,2013,19:854-857.
10JeffreyRI,TonyRR,AllenLC,etal.Axitiniband/orbevacizumabwithmodifiedFOLFOX-6asfirst-linetherapyformetastaticcolorectalcancer:Arandomizedphase2study.Cancer,2013,119:435-441.
11 卢震海,王福龙,彭健宏,等.贝伐珠单抗联合术前化疗治疗结直肠癌肝转移临床研究.中华肝脏外科手术学电子杂志,2016,11:58-62.
12 曲颜丽,赛福丁·克尤木,唐勇.贝伐珠单抗联合化疗治疗转移性结直肠癌的疗效和安全性.世界华人消化杂志,2016,21:159-165.
13 谢永铮,任学群.贝伐珠单抗联合FOLFOX治疗晚期转移性结直肠癌的临床疗效及安全性评价.中国临床药理学杂志,2015,31:2208-2210.
14 裴保香,张子洋,徐艳萍.贝伐单抗联合不同化疗方案治疗转移性结直肠癌临床观察.中国药学杂志,2014,49:2039-2042.
10.3969/j.issn.1002-7386.2017.08.034
431700 湖北省天门市第一人民医院肿瘤科
R
A
1002-7386(2017)08-1237-04
2016-10-19)

