不同初始pH值下反硝化包埋颗粒的动力学特性
曾金平,陈光辉,李 军*,邓海亮,王秀杰
(1.北京工业大学建筑工程学院,北京市水质科学与水环境恢复工程北京市重点实验室,北京 100124;2.青岛大学环境科学与工程学院,山东 青岛 266071)
不同初始pH值下反硝化包埋颗粒的动力学特性
曾金平1,陈光辉2,李 军1*,邓海亮1,王秀杰1
(1.北京工业大学建筑工程学院,北京市水质科学与水环境恢复工程北京市重点实验室,北京 100124;2.青岛大学环境科学与工程学院,山东 青岛 266071)
采用批式实验研究了不同初始pH值下反硝化包埋颗粒在反应过程中、TN和pH值的变化规律,并探究了反硝化包埋颗粒的动力学特性.结果表明,在进水为30mg/L,反应温度控制在30℃,C/N比为6,反应周期为5h条件下,反硝化污泥经包埋后经过2周的适应性培养即表现出很好的反硝化性能,不同的初始pH值下,反硝化过程中的去除主要在0~1h内,的积累在1h时达到最大,同时pH值出现拐点,在1h达到最大后略有降低,这一拐点可以作为亚氮积累达到最大时的指示参数.动力学研究表明,反硝化最大比反硝化速率Kden出现在pH=7.5和8.0时,为2.9mg/(gM LVSS·h),表明最适宜反硝化包埋颗粒的pH值为7.5~8.0,TN去除率在91.7%以上.通过硝酸盐氮的比反硝化速率和亚硝酸盐氮的比反硝化速率的比较,可知在反硝化过程中硝酸盐氮的还原速率都大于亚硝酸盐氮的还原速率,是造成亚氮积累的原因.
反硝化;固定化;包埋菌;pH值;动力学
反硝化作为生物脱氮过程中的重要步骤,反硝化过程中的影响因素有很多,如微生物组成[1]、碳源种类[2]、pH值[3]、DO[4]和C/N[5]等.包埋固定化技术是现代生物工程领域中一项新兴的微生物固定技术,它是将微生物包埋在聚物膜或凝胶小格中,使微生物细胞被包埋在载体内部,载体的网格结构可以将微生物活细胞固定在特定的位置不至于渗漏,同时允许小分子底物及反应代谢产物自由扩散[6-7].
包埋固定化技术应用在污水处理中具有诸多优势,如:能使装置设备化,维持装置内生物量的高浓度和高活性;容易固液分离;能够对多种特殊菌种进行包埋;能增强微生物对环境和毒性物质的耐受能力[8].利用包埋固定化技术将反硝化污泥进行包埋固定化能有效提高反硝化污泥的抗负荷冲击能力,同时能够改善反应器中污泥上浮和污泥解体现象.袁林江[9]采用聚乙烯醇(PVA)对反硝化细菌进行包埋后发现反硝化细菌表现出明显的耐受性,尤其在低温情况(10℃)下仍表现出良好的脱氮性能;田晋红等[10]同样利用PVA将反硝化细菌进行包埋,在进水为150mg/L时,发现包埋后的反硝化细菌的最适温度未变,而且在10℃时包埋后的反硝化细菌仍表现出良好的脱氮性能,去除负荷接近未包埋的反硝化菌的3倍.
经包埋固定化的反硝化污泥具有许多优势,但在具体的实验过程中,如何确定实验条件下的反硝化动力学参数尤为重要.本文采用水性聚氨酯(WPU)作为包埋材料对反硝化污泥进行包埋固定化,采用Bicinchoninic Acid(BCA)法对反硝化包埋颗粒内的生物量进行测定,同时利用零级动力学模型在不同初始pH值条件下对反硝化包埋颗粒的动力学特性进行研究,进而为固定化反硝化系统奠定基础.
1 材料方法
1.1 反硝化反应器
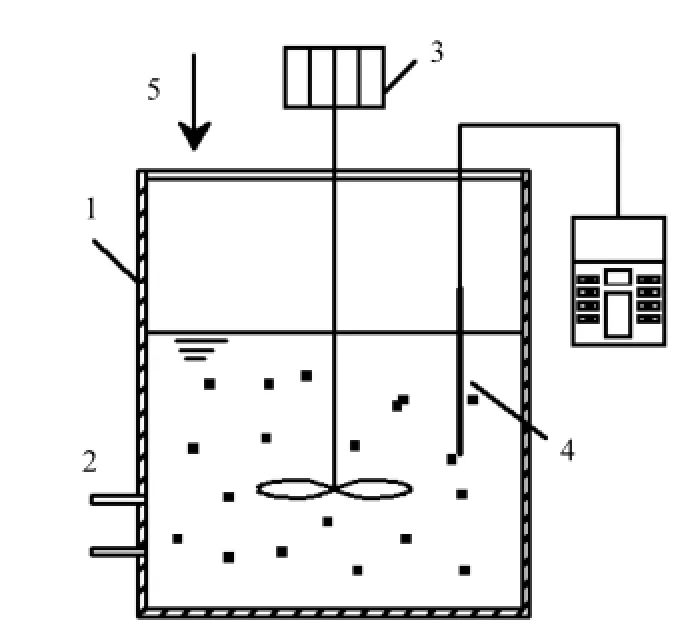
图1 反硝化SBR反应器Fig.1 The SBR of denitrification
反硝化反应器采用有机玻璃制造序批式反应器(SBR),如图1所示.反应器直径170mm,高245mm,有效容积2L,上部密封,只留一个排气口,为保证包埋颗粒在反应器内分布均匀,上部设有搅拌装置,外部设有水浴层,通过水浴加热保持反应器内温度维持在30℃.反应器的运行过程:反应器每天运行4个周期,每个运行周期t=5h,其中进水5min,反应285min,沉淀5min,出水5min,闲置60min.
1.2 包埋颗粒的制备
1.3 实验水质

表1 人工配水成分组成Table 1 The Compositions of artificial wastewater
1.4 批式实验
SBR反应器运行30d后,进行批式实验.将包埋颗粒按填充率15%投加到1L的血清瓶中,然后将血清瓶置于恒温磁力搅拌机上,设置转速为400r/min.实验装置如图2,实验采用瞬时进水,进水质量浓度为30mg/L,COD质量浓度为180mg/L(C/N=6)左右,并投加少量KH2PO4,HRT为5h.通过恒温磁力搅拌器控制温度在30℃,设置不同初始pH值:6.0、6.5、7.0、7.5、8.0、9.0进行试验,每小时取样检测反应器中、、COD和pH值变化.

图2 批式实验反应器Fig.2 The batch tests reactor
1.5 水质分析方法
1.6 包埋颗粒生物量测定
在包埋颗粒中,微生物被包埋在载体内或附着在载体表面,由于包埋材料的存在,因此直接测定MLSS或MLVSS的方式并不适合包埋颗粒.本研究采用测定蛋白质含量的方式,间接测得包埋颗粒内生物量,取用于包埋固定化的反硝化污泥,设置VSS梯度(以mg计)分别为:10、30、50、70、90、110、130、150,将取出的污泥经PBS缓冲液清洗后放入超声波细胞破碎仪内进行破碎处理,破碎功率为10%,破碎时间10min(设置破碎2s,间歇5s),之后采用BCA法[13]测定梯度污泥的蛋白质含量,得到蛋白质含量与VSS的线性关系.取20mL包埋颗粒,碾碎按处理污泥相同的方式测定蛋白质浓度,通过之前测得的蛋白质含量与VSS的线性关系图,得到包埋颗粒的MLVSS浓度.
1.7 反硝化速率的计算公式
采用CH3COO Na为碳源时,在不考虑细胞合成时,生物反硝化可用式(1)[14]和式(2)[15]表示:

将上述两式简化,根据文献[16-17],废水中硝酸盐氮反硝化过程可简化为式(3)表示:

反硝化过程中硝酸盐氮的转化速率和亚硝酸盐氮的转化速率计算公式,如式(4):

反硝化过程中硝酸盐氮的比反硝化速率计算如式(5):

式中:CX为反硝化包埋颗粒生物量,g/L.
当系统中还残余硝酸盐氮时 亚硝酸盐氮的比反硝化速率计算公式如式(6):

当系统中的硝酸盐氮全部消耗完毕时,亚硝酸盐氮的比反硝化速率计算公式如式(7):

反硝化脱氮模型采用零级模型[18]示:

式中:CN为t时刻(或)质量浓度,mg/L; CN0为t=0时刻的质量浓度,mg/L;CX为微生物质量浓度,g/L; Kden为最大比反硝化速率,mg/(gMLVSS·h).
2 结果与讨论
2.1 反硝化反应器的启动
反硝化污泥包埋后,在经过2周的适应后表现出良好的反硝化性能,实验所用水质见表1.在第15d对反硝化反应器进行沿程实验,实验结果如图3所示.
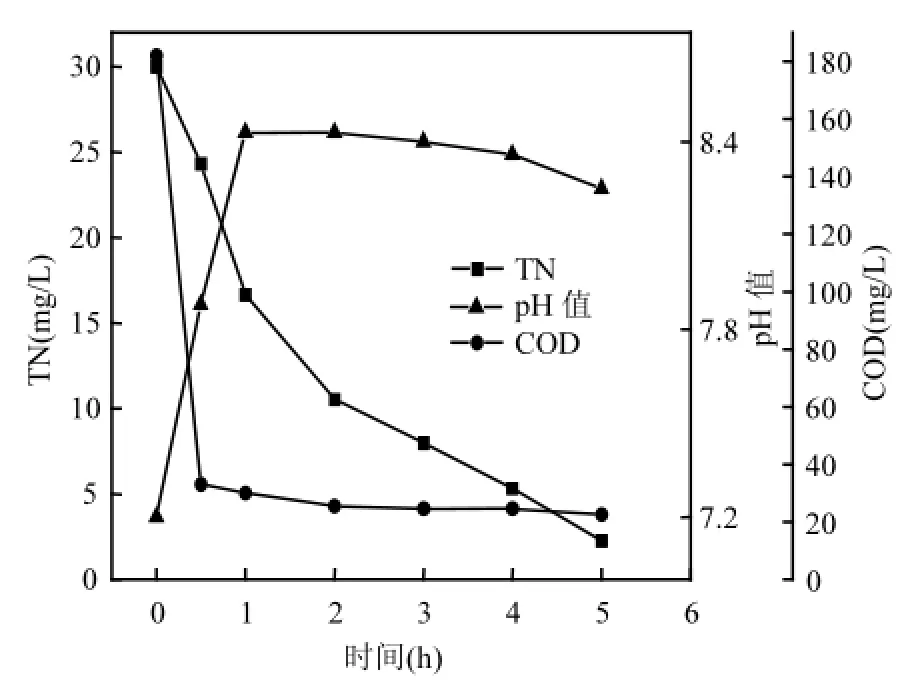
图3 反硝化包埋颗粒反应效果Fig.3 The denitrifying performance of immobilized granules
不同的pH值对硝酸盐氮还原酶、亚硝酸盐氮还原酶和微生物细胞活性的抑制程度不同,一般来说在反硝化系统中最佳pH值在7.5左右,pH=6.5、9.0时硝酸盐氮的去除率将为最佳去除率的70%左右,超过该范围时硝酸盐氮的去除率将急剧下降[20].本实验过程中反硝化的最佳pH是7.5和8.0,pH=6.5、7.0时硝酸盐氮去除率达到94.67%和96.10%;而pH=6.0、9.0时硝酸盐氮去除率虽然很高,达到99.7%和96.3%,但存在很明显的亚氮积累现象(图4b).
影响反硝化过程中NO2-N积累的因素主要有微生物种类[21]、pH值[3]、碳源种类[22-25]和C/N比[18,26].Van Rijn[27]利用施氏假单胞菌(Pseudomonas stutzeri)为单一的菌种对反硝化进行研究时发现以乙酸为碳源时,与其它碳源相比存在较高的亚氮积累现象;马娟等[28]在研究反硝化过程中的积累问题时发现:乙酸钠作为碳源,系统存在有大量的积累.袁怡等[16]利用乙酸钠为碳源,将C/N比控制在2.5和3.0时,积累率较高.本实验采用乙酸钠为碳源,也存在类似的积累问题.讨论反硝化过程中的积累问题时,可采用2步反硝化模型[29],即把看成反硝化过程中的唯一中间产物,表示为式(9).
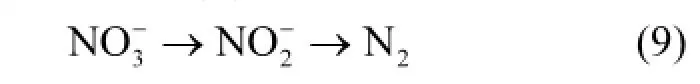
由于不同初始pH值下硝酸盐还原酶和亚硝酸盐还原酶的活性不同,导致反硝化过程中的积累量有所差异.由图4b可以看出:在前1h,不同的初始pH值下的亚氮积累达到最大.初始pH=6.0时,在1h时积累效果最为明显,达到19.2mg/L,积累率高达63.9%, pH=9.0时,积累率也很高,达到16.4mg/L,在反应5h后,残余量仍很高,分别为9.1和9.7mg/L,积累率还高达30.3%和32.2%,积累现象明显;在初始pH=6.5、7.0、7.5、8.0时,0~1h也存在较高的积累,分别为16.3、11.5、13.4、14.3mg/L,但是经过5h后,残余量都在2.0mg/L以下,可认为无的积累.
Glass等[30]在对高浓度硝酸盐废水反硝化过程的研究结果中发现,反硝化在不同的pH值范围内的反应机理有所不同:当pH<7时,硝酸盐氮可反硝化完全;pH值在7.5~9.0时,有明显的亚氮积累现象.宋佳强等[31]研究发现在酸性条件下,反硝化速率不高,而在中性和偏碱性条件下,反硝化速率明显提高,而且去除率也有提升,但是初始pH=8.0和9.0时,出现了亚氮积累现象.本实验在0~1h内产生较高的亚氮积累,但由于COD在此时仍有剩余,因此积累的亚氮会继续被还原,而5h之后仅在初始pH=6.0和9.0时出现亚氮积累,说明在偏酸性和偏碱性条件对亚硝酸盐还原酶的抑制作用较为明显.
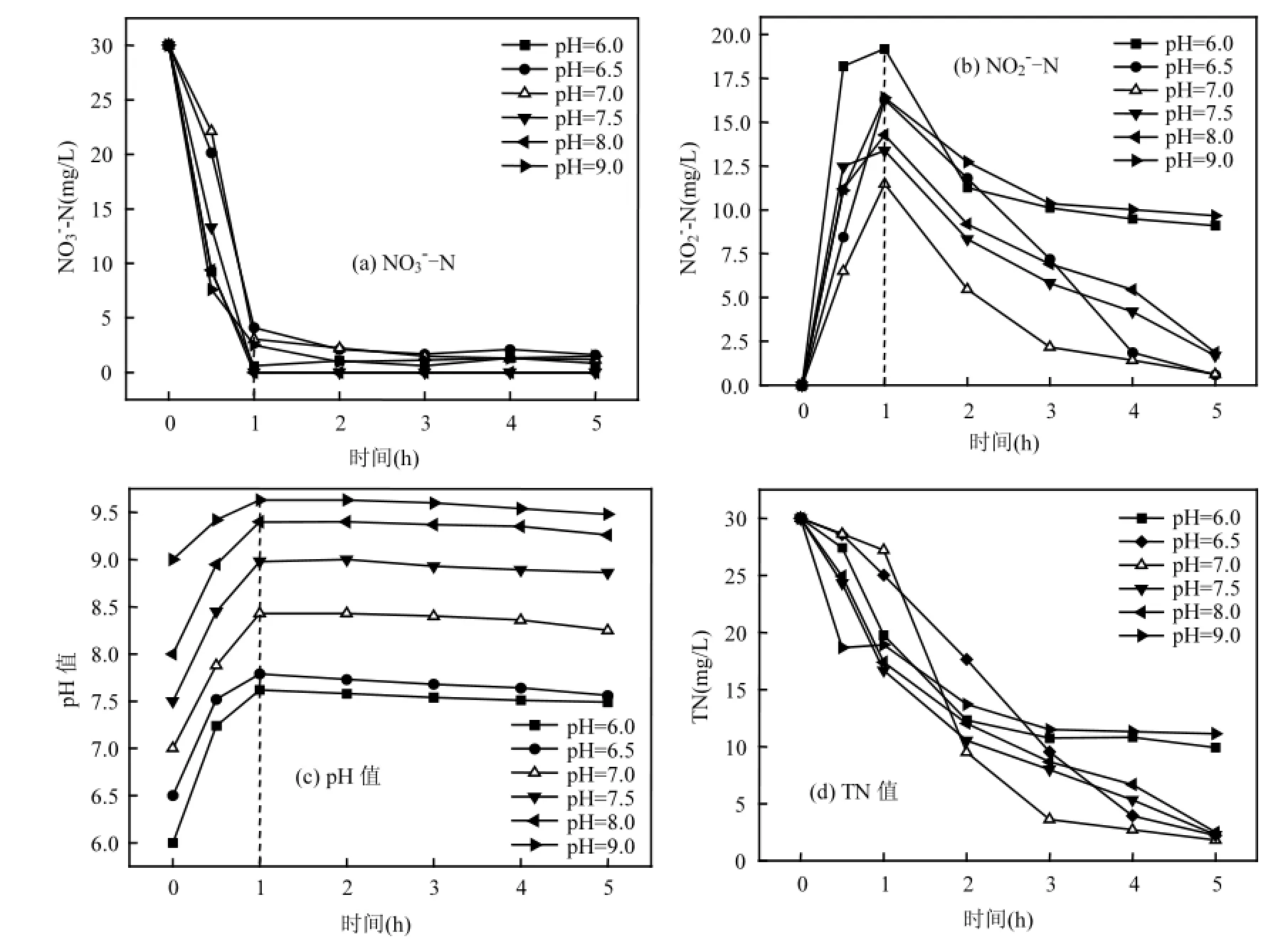
图4 反硝化过程中NO3-N、NO2-N、TN和pH值的变化规律Fig.4 The rule of NO3-N、NO2-N、TN and pH in the denitrification process under different initial pH
在反硝化过程会不断产生碱度,理论上每还原1.0g硝酸盐氮会产生3.6g碱度(以碳酸钙计).从图4c中可以看出,不同的初始pH值变化在前1h内增长很快,在1h时pH达到最大值,此时含量都低于5.0mg/L,而积累达到最大,之后pH略有降低;系统中pH有此变化的原因主要有以下几个:前0~1h内pH值大幅升高,是由于在被还原过程中产生的被不断的还原,而产生碱度;在之后的几个小时内,积累的亚氮继续被还原进而继续产生碱度,而实验采用乙酸钠作为碳源,乙酸根离子在水中会发生水解反应(式10)产生OH.

反硝化过程不断消耗系统中的乙酸根离子和产生碱度导致反应朝左边移动,使得OH离子的浓度不断下降,致使在反应的后4h内pH值略有下降.
由图4可以看出,反硝化包埋系统在不同的初始pH值下, NO3-N的去除主要发生在0~1h内,从进水30.0mg/L降解为5.0mg/L以下,平均去除速率达到25.0mg/(L·h);NO2-N在0~1h内增长迅速,在1h时积累达到最大,之后继续被还原,在此过程中,pH增长很快,pH=6.0、6.5、7.0、7.5、8.0、9.0增长速率分别为1.6,1.3,1.4,1.5,1.4,0.6/h.从图4b和图4c可以看出NO2-N积累达到最大的同时 pH值也达到最大值,之后则略有降低即出现pH值拐点,这一拐点值可作为反硝化包埋系统中NO2-N积累达到最大的指示性参数.
2.3 不同初始pH值下反硝化动力学特性
在批式实验阶段,认为反硝化包埋颗粒生物量变化不大,经BCA法测定出反硝化包埋颗粒的生物量平均为2.1gMLVSS/L.反硝化动力学特性用反硝化脱氮零级模型来表征,根据式(4)~(7)计算出硝酸盐氮和亚硝酸盐氮的转化速率以及比反硝化速率(表2).
由表2可以看出,反应结束时的硝酸盐氮比反硝化速率从pH=6.0时的2.7一直增加到pH=7.5和8.0时的2.9mgNO3-N/(gMLVSS·h);当pH值升到9.0时,硝酸盐氮比反硝化速率下降到2.8mgNO3-N/(gMLVSS·h).亚硝酸盐氮的比反硝化速率特有类似先升高后降低的规律,从pH=6.0时的1.2mg/(gMLVSS·h)缓慢增加到pH=8.0.时的1.5mg/(gMLVSS·h);pH值升高到9.0时,亚硝酸盐氮的比反硝化速率降到0.8m/(gMLVSS·h).硝酸盐氮比反硝化速率的最大值都出现在pH=7.5和8.0时,亚硝酸盐氮比反硝化速率的最大值出现在pH=8.0时;在pH=6.0和9.0时,硝酸盐氮和亚硝酸盐氮的比反硝化速率都不高,进一步说明在偏酸性(pH=6.0)和偏碱性(pH=9.0)下反硝化系统都受到了不同程度的抑制.表2中可看出硝酸盐氮的比反硝化速率都大于亚硝酸盐氮的比反硝化速率,硝酸盐氮的比反硝化速率几乎都在亚硝酸盐氮的比反硝化速率的1.9倍以上,正是硝酸盐的还原速率远大于亚硝酸盐的还原速率,从而导致亚氮的积累.

表2 不同初始pH值下的比反硝化速率[mgNOx-N/(gMLVSS·h)]Table 2 The specific denitrification rate under different initial pH value [mgNOx-N/(gMLVSS·h)]

图5 不同初始pH下CN-CN0随时间的变化规律Fig.5 The rule of CN-CN0with time under different initial pH
根据反硝化脱氮零级模型(式8),以时间t为横坐标,CN-CN0为纵坐标,绘制不同初始pH值下CN-CN0随时间t的变化曲线(图5).经过origin8.0软件线性拟合出不同初始pH值下的拟合方程(表3).

表3 不同初始pH值下的Kden值Table 3 The Kdenunder different initial pH value
徐亚同等[32]研究了反硝化污泥在驯化和未驯化时不同pH值对反硝化速率的影响,结果发现无论反硝化污泥是否经过了驯化,pH值在从6.0升高到9.5过程中,反硝化速率是先增加后降低的,最大反硝化速率出现在pH=7.5.本实验的结果与其有类似的变化规律,产生此变化规律的原因可能是由于在过酸或过碱条件下均会对系统反硝化过程造成了抑制作用.根据姜体胜等[33]的研究,反硝化在pH低于6.0时会受到强烈的抑制,当pH=4.7时,污泥就已经恶化,微生物酶的活性降低,导致细胞结构受到破坏,出现解絮现象,影响反硝化过程的正常进行.从表3可看出,在初始pH=6.0和 9.0时最大比反硝化速率最低,为2.1和1.9mg/(gMLVSS·h);系统反硝化过程中最大比反硝化速率出现在初始pH=7.5和8.0时,为2.9mg/(gMLVSS·h),是pH=6.0时的1.4倍,为pH=9.0时的1.5倍;初始pH=7.5时次之,为2.9mg/(gMLVSS·h),pH=6.5和pH=7.0时,最大比反硝化速率也比较高,都达到2.8mg/(gMLVSS·h).在pH=6.0和9.0下,反应结束时还有较高的亚氮积累(图4b),反硝化效果较差,可能是最大比反硝化速率低的原因;在pH=7.5和8.0时,反硝化效果最好,最大比反硝化速率也很高,因此认为反硝化包埋颗粒的最适pH值范围比反硝化活性污泥略高,为7.5~8.0.
3 结论
3.1 反硝化污泥经包埋后,在为期2周的适应性培养后,即表现出很好地反硝化性能,并能够维持稳定的运行.在进水为30mg/L,COD为180mg/L时,经过5h反应TN去除率达92.4%, COD去除率达到87.6%.
3.2 反硝化包埋颗粒对硝酸盐氮表现出良好的去除能力,仅1h对硝酸盐氮的去除率就已达到80.0%以上,在1h时亚硝酸盐氮积累达到最大,其中pH为6.0和9.0在反应结束时仍有较高的亚氮积累.反硝化最适宜pH值范围7.5~8.0,硝酸盐氮去除率都在98.0%以上,TN去除率分别为92.4%和91.7%.
3.3 在反硝化包埋系统中,pH值达到最大值时的拐点可作为积累达到最大的指示性参数.
3.4 反硝化脱氮零级模型能很好地表征反硝化动力学特性,在反硝化过程中,pH值从6.0升高到9.0,反硝化比反硝化速率呈现先升高后降低的趋势,硝酸盐氮比反硝化速率最大值出现在pH=7.5和8.0,为2.9mg/(g MLVSS·h),在不同的初始pH值下,所有硝酸盐氮的比反硝化速率都大于亚硝酸盐氮的比反硝化速率,从而导致亚氮的积累;反硝化过程中最大比反硝化速率出现在pH=7.5和8.0,为2.9mg/(g MLVSS·h)进一步表明反硝化包埋颗粒的最适pH值范围为7.5~8.0.
[1] Lee D Y, Ramos A, Macomber L, et al. Taxis response of various denitrifying bacteria to nitrate and nitrite [J]. Applied and Environmental Microbiology, 2002,68(5):2140-2147.
[2] 殷芳芳,王淑莹,昂雪野,等.碳源类型对低温条件下生物反硝化的影响 [J]. 环境科学, 2009,30(1):108-113.
[3] Thomsen J K, Geest T, Cox R P. Mass spectrometric studies of the effect of pH on the accumulation of intermediates in denitrification by Paracoccus denitrificans [J]. Applied and Environmental Micro -biology, 1994,60(2):536-541.
[4] Gomez MA, HontoriaE. Effect of dissolved oxygen concentration on nitrate removal fromground water using a denitrifying submenged filter [J]. Journal of Hazarsous Materials, 2002,90(3):267-278.
[5] 杨殿海,章非娟.碳源和碳氮比对焦化废水反硝化工艺的影响[J]. 同济大学学报:自然科学版, 1995,23(4):413-416.
[6] Chen Y, Zhou T, Yao S, et al. Ethanol production by repeated batch and continuous fermentations by Sacharomyces cerevisiae immobilized in a fibrous bed bioreactor [J]. Journal of Microbiology and Bioteshnology, 2013,23:511-517.
[7] Dong Y, Zhang Z, Jin Y, et al. Nitrification characteristics of nitrobacteria immobilized in waterborne polyurethane in waste -water of corn-based ethanol fule production [J]. Journal of Environment Science, 2012,24:999-1005.
[8] 李 军,曾金平,邓海亮,等.污水处理热点技术研发及产业化[J]. 建设科技, 2005,13:29-30.
[9] 袁林江.聚乙烯醇(PVA)固定化反硝化菌的脱氮性能 [J]. 中国环境科学, 1998,18(2):189-191.
[10] 田晋红,熊 平.固定化反硝化细菌脱氮的研究 [J]. 西南农业大学学报, 2004,26(3):318-321.
[11] Eaton A D, Franson M. Standard Methods for the Examination of Water & Wastewater [M]. Washington, DC: American Public Health Association (APHA), 2005:2001-3710.
[12] Cheng C K, Chang L S, Chi Chin S, et al. Simultaneous carbon-nitrogen removal in wastewater using phosphorylated PVA-immobilized microorganisms [J]. Enzyme and Microbial Technology, 1998,23(5):311-320.
[13] 张云贵,刘祥云,李天俊.生物化学实验指导 [M]. 天津:天津科学技术出版社, 2005.
[14] 马 娟,彭永臻,王 丽,等.温度对反硝化过程的影响以及pH值变化规律 [J]. 中国环境科学, 2008,28(11):1004-1008.
[15] Sawyer C N, McCarty P L, Parkin G F. Chemistry for environmental engineering [M]. fifth ed. NewYork, USA—McGraw-Hill Inc, 2003.
[16] 袁 怡,黄 勇,邓慧萍,等.C/N比对反硝化过程中亚硝酸盐积累的影响分析 [J]. 环境科学, 2013,34,(4):1416-1420.13.
[17] 赵 樑,倪伟敏,贾秀英,等.初始pH值对废水反硝化脱氮的影响[J]. 杭州师范大学学报:自然科学版, 2014,13(6):616-622.
[18] 叶剑锋.废水生物脱氮处理新技术 [M]. 北京:化学工业出版社, 2006:18-32.
[19] 付昆明,曹相生,孟雪征,等.污水反硝化过程中亚硝酸盐的积累规律 [J]. 环境科学, 2011,32(6):1660-1664.
[20] 沈耀良,王宝贞.废水生物脱氮处理新技术:理论与应用 [M].北京:中国华宁科学出版社, 1999:215-217.
[21] Lazarova V, Capdeville B, Nikolov L.Influence of seeding conditions on nitrite accumulation in a denitrifying fluidized bed reactor [J]. Water Research, 1994,28(5):1189-1197.
[22] Sun H W, Yang Q, Peng Y Z, et al. Nitrite accumulation during the denitrification process in SBR for the treatment of pre-treated landfill leachate [J]. Chinese Journal of Chemical Engineering, 2009,17(6):1027-1031.
[23] 孙洪伟,王淑莹,王希明,等.低温SBR反硝化过程亚硝酸盐氮积累实验研究 [J]. 环境科学, 2009,30(12):3620-3623.
[24] 孙洪伟,彭永臻,魏东洋,等.低温SBR反硝化过程亚硝酸盐氮积累的动力学研究 [J]. 中国给水排水, 2011,27(5):99-104.
[25] 田建强,李咏梅.以喹啉或吲哚为单一碳源时反硝化过程中亚硝酸盐的积累 [J]. 环境科学学报, 2009,29(1):68-74.
[26] 葛世建,王淑莹,杨岸明,等.反硝化过程中亚硝酸盐积累特性分析 [J]. 土木建筑与环境工程, 2011,33(1):140-146.
[27] 田建强.反硝化过程中亚硝酸盐积累的影响因素 [J]. 有色冶金设计与研究, 2008,29(3):42-44.
[28] 马 娟,宋相蕊,李 璐.碳源对反硝化过程NO2积累及出水pH值的影响 [J]. 中国环境科学, 2014,34(10):2556-2561.
[29] Ni B, Yu H. An approach for modeling two-step denitrification in activated sludge systems [J]. Chemical Engineering Science, 2008, 63(6):1449-1459.
[30] Glass C, Silverstein J. Denitrification kinetics of high nitrate concentration water: pH effect on inhibition and nitrite accumulation [J]. Water Research, 1998,32(3):831-839.
[31] 宋佳强.利用包埋固定化技术进行深度脱氮的研究 [D]. 北京:北京工业大学, 2014.
[32] 徐亚同.pH、温度对反硝化的影响 [J]. 中国环境科学, 1994, 14(4):308-313.
[33] 姜体胜,杨 琦,尚海涛,等.温度和pH值对活性污泥法脱氮除磷的影响 [J]. 环境工程学报, 2007,1(9):10-14.
Kinetic characteristics of immobilized denitrification granu lesunder different initial pH.
ZENG Jin-ping1, CHEN Guang-hui2, LI Jun1*, DENG Hai-liang1, WANG Xiu-jie1
(1.Key Laboratory of Beijing for Water Quality Science & Water Environment Recovery Engineering, College of Architecture and Civil Engineering, Beijing University of Technology, Beijing 100124, China;2.College of Environmental Science and Engineering, Qingdao University, Qingdao 266071, China).China Environmental Science, 2017,37(2):526~533
The rule of、、TN and pH during denitrification process was studied by using different initial pH in a bath-scale sequencing batch reactor with synthetic wastewater. The kinetic characteristics of immobilized granules also were investigated by batch tests. Under the condition of temperature 30℃,C/N 6and HRT 5h, the immobilized denitrification granules showed good performance during two weeks. Under the different initial pH, the nitrate removal occurs mainly in the 0~1h, and the nitrite accumulation attain its maximumat 1h, meanwhile the pH attained its maximumthen slightly reduced, formed a breakpoint of pH curve. Therefore, the breakpoint of pH curve could be used as an indicator to showthe maximumaccumulation of nitrite. K inetics study showed the maximumspecific denitrification rate occurred at pH=8.0, the pH=7.5was the next. It showed the most suitable denitrifying pH range was 7.5~8.0, and the removal of TN was 91.74%. Compared with nitrate and nitrite specific denitrification rate, the reason for nitrite accumulation is that the reductive rate of nitrate was more than nitrite during denitrification process.
denitrification;immobilization;immobilize granules;pH;kinetic
X703.1
A
1000-6923(2017)02-0526-08
曾金平(1991-),男,江西省赣州人,北京工业大学硕士研究生,主要从事污水处理及资源化方面研究.
2016-05-10
水体污染控制与治理科技重大专项(2015ZX07202-013);16人才培养质量建设-双培养计划新兴专业建设(004000542216031)
* 责任作者, 教授, jglijun@bjut.edu.cn

