两性霉素B前体脂质体的制备工艺研究
隋 琳,田 野,王永利,王立华,庚丽丽,赵 瑶,王璐璐
(1.内蒙古医科大学,内蒙古 呼和浩特 010100;2.河北北方学院理学院,河北 张家口 075000; 3.河北北方学院应用化学研究所,河北 张家口 075000)
两性霉素B前体脂质体的制备工艺研究
隋 琳1,3,田 野2,王永利3,王立华3,庚丽丽3,赵 瑶2,王璐璐2
(1.内蒙古医科大学,内蒙古 呼和浩特 010100;2.河北北方学院理学院,河北 张家口 075000; 3.河北北方学院应用化学研究所,河北 张家口 075000)
目的 研究两性霉素B前体脂质体制备工艺。方法 采用载体沉积法制备两性霉素B前体脂质体,以包封率为评价指标,采用单因素试验和正交试验优化处方,并观察其重现性和稳定性。结果 两性霉素B的最优处方工艺条件是膜材比为1∶2、载脂比为5∶1、药脂比1∶8。载体为甘露醇,最优处方下平均包封率(63.4±1.5)%。结论 由最佳处方工艺条件制备的两性霉素B前体脂质体的包封率和稳定性高,重现性好。
两性霉素B;前体脂质体;载体沉积法;低速离心法;包封率
两性霉素B(amphotericin B,AmB)是治疗隐球菌性脑膜炎应用最多也是最有效的一种药物,它属于大环多烯类抗真菌抗生素,主要作用于细胞膜的甾醇使菌体溶解破坏[1]。近年来,随着肿瘤和需要化疗的患者增多、广谱抗生素和糖皮质激素的广泛使用,以及插管和介入治疗患者的增加,深部真菌感染呈明显增多趋势,两性霉素B迄今仍然是作用最强的抗真菌药,但该药在治疗剂量下产生的严重的毒副作用限制了在临床上的使用[2,3]。前体脂质体是将药品吸附于极细的载体上,通常为具有良好流动性的粉末,使用前与水溶合可得脂质体混悬液,从而解决普通脂质体的聚集、沉降、融合、渗透和高温灭菌等稳定性的问题,降低药品的毒副作用。药品制成前体脂质体,可适用于静脉注射和其他的给药途径,提高药品的使用度[4,5]。
本文采用载体沉积法制备前体脂质体,是将药品、膜材和支撑剂用适量溶液溶解后制成类脂质溶液后吸附于载体上,形成前体脂质体,由于前体脂质体没有形成脂质体的完整结构,故不存在聚集、沉降等问题,同时制备工艺简单,增强了应用价值,提高了药品利用率[6]。
1 仪器与药品
722N型可见分光光度计(上海精密科学仪器有限公司),ZFQ-3型旋转蒸发仪(天津市第一玻工厂),SHZ-D(Ⅲ)循环水式真空泵(巩义市予华仪器有限责任公司),800型离心沉淀器(上海手术器械厂),TG328A型光学读数分析天平(湘仪天平仪器厂),CX-250超声波清洗器(北京医疗设备工厂)。实验所用试剂均为市售分析纯。
2 试验方法
2.1 两性霉素B前体脂质体的制备工艺
称取处方量的大豆卵磷脂、胆固醇、维生素E和PEG2000,溶于氯仿中,另取处方量两性霉素B溶于适量甲醇溶液中,超声溶解后,将两种溶液混匀,预热,制备类脂质溶液。再取适量过80目筛的载体于茄形瓶中,预热后,分次加入类脂质溶液,于恒温水浴上缓慢减压旋转蒸发出有机溶剂,类脂质膜材附着于载体粉末上。将制得品置于真空干燥器中干燥过夜,过40目筛,密闭于西林瓶中,冰箱4 ℃保存。使用前,取该前体脂质体粉末加入注射水溶合,超声溶解,即得脂质体混悬液[7]。
2.2 包封率的测定
2.2.1 检测波长的选择
分别精密量取两性霉素B、空白脂质体10 mg到100 mL容量瓶中,用二甲基亚砜甲醇混合液定容,以混合液做参比,在200~700 nm波长范围内进行全波长扫描,膜材、载体、辅料对两性霉素B的测定无干扰,因此选择408 nm为检测波长。
2.2.2 标准曲线的绘制
精密称取两性霉素B精制品10 mg于100 mL容量瓶中,甲醇和二甲亚砜的混合溶液定容,配制得100 μg·mL-1的标准液。准确移取2、4、6、8、10、12、14 mL标准液于100 mL容量瓶中,用甲醇和二甲亚砜的混合溶液稀释成2、4、6、8、10、12、14 μg·mL-1溶液,以混合溶液做空白对照,用722S可见分光光度计在408 nm波长处分别测定吸光度,用浓度(C)对吸光度(A)作线性回归,即得线性回归方程为A=0.1174C-0.0075(R2=0.999 9),结果表明,在2~14 μg·m-1范围内溶液吸光度与两性霉素B溶液浓度线性关系良好。
2.2.3 测定包封率的方法
将制得的两性霉素B前体脂质体粉末,加注射用水溶合,超声波溶解后,转移至25 mL容量瓶中定容,混合均匀。精密量取2.0 mL溶液置离心管中,在2 000 r·min-1、每次20 s的条件下离心10 min,弃去上层清液。精密移取5.0 mL甲醇和二甲基亚砜混合液溶解沉淀,以混合液做参比测定吸光度,计算两性霉素B的量。采用如下公式,计算大黄酚前体脂质体包封率[8]。
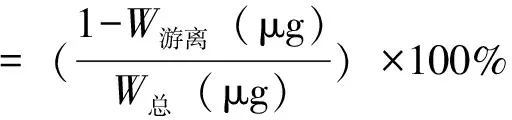
(W总为两性霉素B的总量;(1-W游离)为离心后上清液中两性霉素B的量)
2.3 单因素试验
2.3.1 载脂比对包封率的影响
固定其他因素,使处方中载体与卵磷脂的比例分别为3∶1、4∶1、5∶1、6∶1,制备两性霉素B前体脂质体,测得包封率(见图1)。结果表明,载脂比为5∶1时,包封率较高。
2.3.2 胆固醇用量对包封率的影响
固定其他因素,使处方中胆固醇∶卵磷脂的比例分别为1∶1、1∶2、1∶3、1∶4,制备两性霉素B前体脂质体,测定包封率(见图2)。结果表明,胆固醇卵磷脂比为1∶2时,包封率较高。
2.3.3 药脂比对包封率的影响
固定其他因素,使处方中药∶卵磷脂的比例分别为1∶4、1∶6、1∶8、1∶10,制备两性霉素B前体脂质体,测定包封率(见图3)。结果表明,药脂比为1∶8时,包封率较高。

图1 载体与卵磷脂的比的影响 图2 胆固醇与卵磷脂的比例的影响
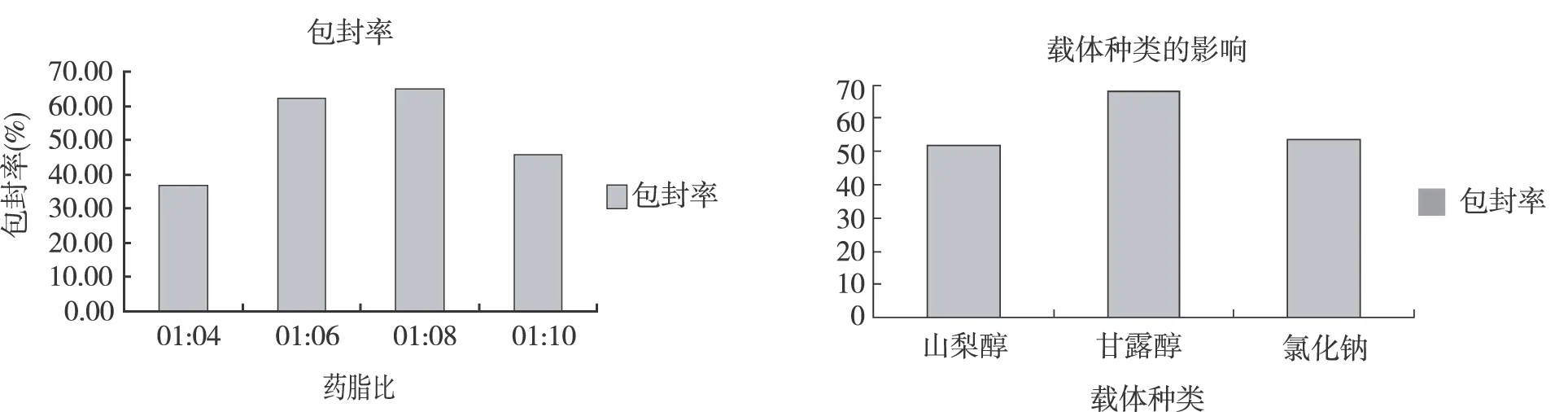
图3 药物与卵磷脂的比例的影响 图4 载体种类的影响
2.3.4 不同载体对包封率的影响
固定处方及工艺中的其他因素,分别选用山梨醇、甘露醇、氯化钠为载体,制备两性霉素B前体脂质体,测定包封率(见图4)。结果表明,选用甘露醇为载体时,包封率较高。
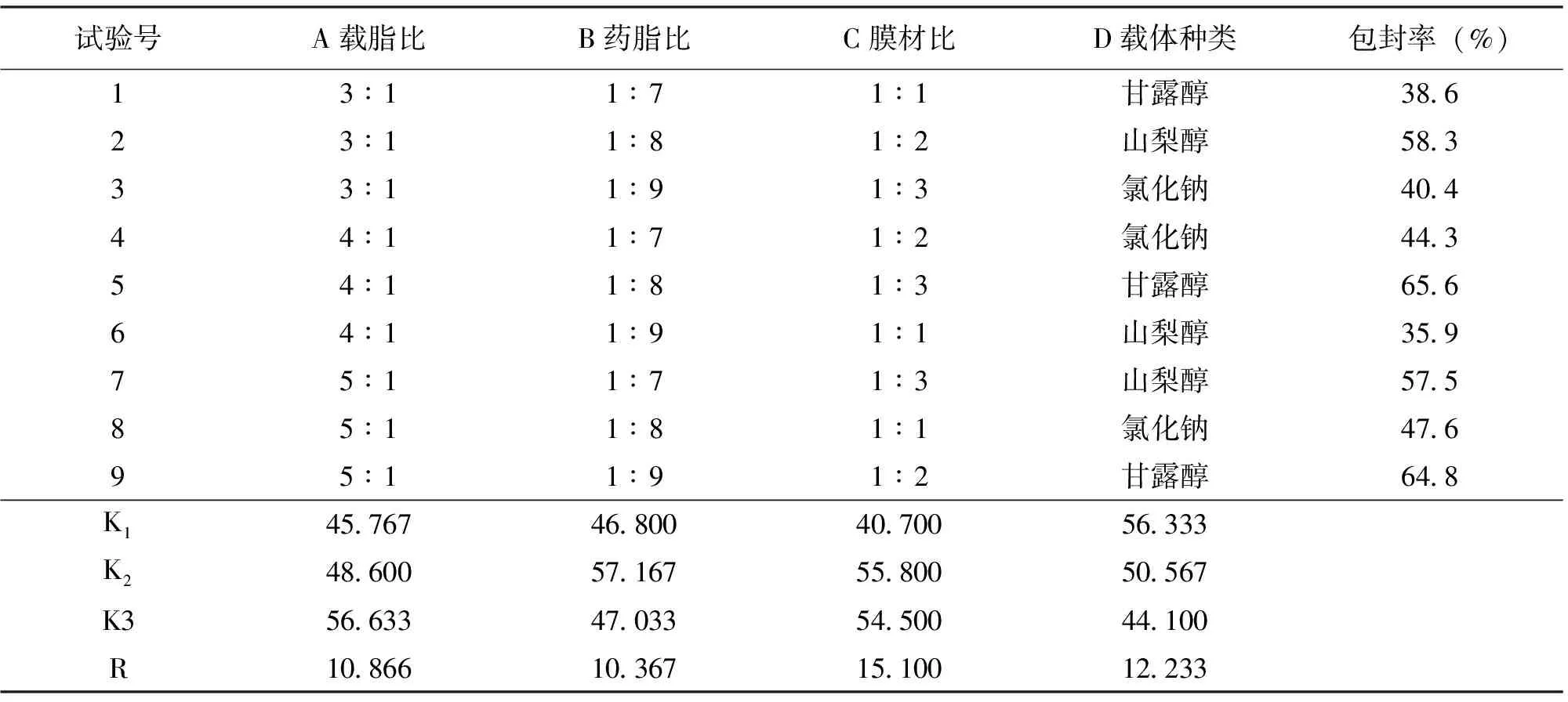
表1 正交试验设计与结果
2.4 正交优化试验
在单因素考察试验基础上,以包封率为指标,对处方中载脂比(A)、药脂比(B)、胆固醇卵磷脂比(C)、载体种类(D)4个因素进行优选,以期得到稳定性好、包封率较高的前体脂质体处方。选用L9(34)正交表安排试验,制备前体脂质体,测定包封率。试验设计及结果见表1。由表1分析可知胆固醇卵磷脂比是影响两性霉素B前体脂质体包封率的第一因素,载体种类次之,载脂比较小,药脂比最小,且无显著差异。最佳处方为A2B2C3D1,即胆固醇卵磷脂比为1∶3,载脂比为4∶1,载体为甘露醇,药脂比为1∶8。

表2 两性霉素B前体脂质体验证性实验

表3 Zeta电位与体系稳定性的关系
2.5 验证性试验
按最优工艺处方量重复制备3份两性霉素B前体脂质体,取适量加注射水溶合后,制得3份脂质体悬浊液,测其包封率(见表2)。证明该制备工艺制得的前体脂质体包封率较高,重现性良好。
2.6 稳定性考察
Zeta电位是表征胶体分散系稳定性的重要指标,它的重要意义在于数值与胶态分散的稳定性相关,是对颗粒之间相互排斥或吸引力的强度的度量。分子或分散粒子越小,Zeta电位(正或负)越高,体系越稳定,即溶解或分散可以抵抗聚集。反之,Zeta电位(正或负)越低,越倾向于凝结或凝聚,即吸引力超过了排斥力,分散被破坏而发生凝结或凝聚[9]。Zeta电位与体系稳定性的大致关系如表3所示。
3 讨论与结论
前体脂质体可预防脂质体之间相互聚集,且更适合包封脂溶性药物[10]。本实验对其载体山梨醇、甘露醇、氯化钠进行了考察,实验结果表明,甘露醇表面结构多孔,比表面积大,对于两性霉素B和磷脂的吸附性好,包封效果较好;通过正交试验优化制备工艺得到最优制备条件为胆固醇卵磷脂比为1∶3,载脂比为4∶1,载体为甘露醇,药脂比为1∶8;由Zeta电位测量实验实际测得两性霉素B脂质体混悬液的电位为-45 mV,制得的前体脂质体有较好的稳定性。
载体沉积法制备的两性霉素B前体脂质体为淡黄色,流动性良好的干燥颗粒,包封率(63.4±1.5)%,稳定性较好,其制备方法简单,易于规模化生产,质量可控,并且前体脂质体可压片和制备成胶囊药剂,便于贮存,具有很好的发展前景。
[1]陈裕充,温海.两性霉素B及其脂质体的抗真菌机制[J].中国真菌学杂志,2006,(05):312-314,307.
[2]仲跻云,陈梁,肖斌.口服用前体脂质体研究进展[J].药学与临床研究,2012,20(01):56-59.
[3]杨绮华.药物载体系统的研究进展[J].中国新药杂志,2002,11(08):593-596.
[4]郑稳生,王璐璐,张宇佳.多柔比星前体脂质体制备工艺筛选及质量考察[J].中国药师,2012,15(08):1130-1134.
[5]王健,李明轩.前体脂质体研究进展[J].中国医药工业杂志,2005,(11):58-62.
[6]杨鹏波,张华.脂质体的研究新进展[J].浙江中医药大学学报,2013,37(07):936-939.
[7]王立华,毛微曦,黄慧婷,等.大黄酚前体脂质体的制备及其质量评价[J].中草药,2014,45(14):2014-2017.
[8]李琅琅,王文喜,朱泱平.低速离心法测定荧光红GG脂质体包封率[J].浙江工业大学学报,2009,37(05):536-537.
[9]白春清.羧基壳聚糖包覆着核仁油前体脂质体的制备、表征、稳定性及体外释放研究[D].南昌:南昌大学,2011.
[10]郭慧丽,李高梅,兴国.两性霉素B脂质体的研究[D].武汉:华中科技大学,2008.
[责任编辑:毛微曦 英文编辑:刘彦哲]
Preparation Technology of Amphotericin B Proliposomes
SUI Lin1,3,TIAN Ye2,WANG Yong-li3, WANG Li-hua3,GENG Li-li3,ZHAO Yao2,WANG Lu-lu2
(1.Inner Mongolia Medical University,Hohhot,Inner Mongolia 010100,China; 2.School of Sciences,Hebei North Univesity,Zhangjiakou,Hebei 075000,China; 3.Institute of Applied Chemistry,Hebei North University,Zhangjiakou,Hebei 075000,China)
Objective To study preparation technology of amphotericin B proliposomes.Methods Amphotericin B proliposomes were prepared by carrier aggradation method.A single-factor investigation and orthogonal design were used to select the optimum formulation.And the repeatability and stability were observed.Results The best prescription of chrysophanol proliposomes was as follows:the ratio of cholesterol to phospholipid was 1∶2,the ratio of carrier to phospholipid was 5∶1,and the ratio of drug to phospholipid was 1∶8.The best carrier was mannnitol.The average encapsulation efficiency of the optimal prescription was:(63.4±1.5)%.Conclusion By using the best prescription amphotericin B was highly entrapped into proliposomes with good reproducibility and stability.
amphotericin B;proliposome;carrier aggradation method;low-speed centrifugation;entrapment efficiency
河北省科学技术研究与发展计划项目(12276104D-94);河北省高等学校科学研究计划项目(QN2015221);河北省高等学校科学技术研究青年基金项目(QN2015148)
隋琳(1993-),女,辽宁本溪人,内蒙古医科大学在读硕士研究生,研究方向:药物新剂型与新技术。
田野(1976-),女,内蒙赤峰人,副教授,硕士,研究方向:纳米材料。
R 943
A
10.3969/j.issn.1673-1492.2017.01.007
来稿日期:2016.11.15

