2016年高考“明星”考点
——催化剂
四川 卢敬萱
(作者单位:四川大学华西药学院)
2016年高考“明星”考点
——催化剂

据统计,约有80%~85%的化工生产过程使用催化剂,催化剂的研究和应用是21世纪化学的一个极具魅力和应用前景的重大主题,2016年高考试题对此表现出极大的关注。本文以2016年高考试题为线索,揭示催化剂这一隐性考点命题规律及备考策略。
考点1:理论与实验双重探究催化剂的催化过程
【例1】(北京,27节选)以废旧铅酸电池中的含铅废料(Pb、PbO、PbO2、PbSO4及炭黑等)和H2SO4为原料,制备高纯PbO,实现铅的再生利用。其工作流程如下:
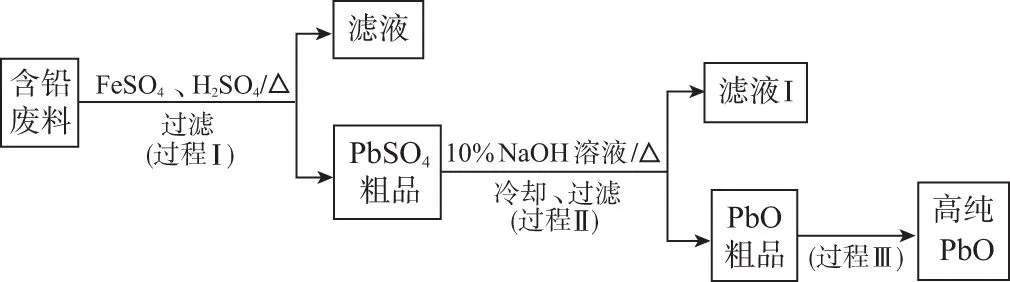
(1)过程Ⅰ中,在Fe2+催化下,Pb和PbO2反应生成PbSO4的化学方程式是___________。
(2)过程Ⅰ中,Fe2+催化过程可表示为:

ⅱ: ……
①写出ⅱ的离子方程式:___________。
②下列实验方案可证实上述催化过程。将实验方案补充完整。
a.向酸化的FeSO4溶液中加入KSCN溶液,溶液几乎无色,再加入少量PbO2,溶液变红。
b.___________。

催化剂的特点是“一变两不变”, “一变”是能改变其他物质的化学反应速率,“改变”包括加快和减慢。“两不变” 是质量和化学性质在化学变化前后不发生改变。


考点2:实验数据助推催化剂的筛选
【例2】(浙江,28节选)催化还原CO2是解决温室效应及能源问题的重要手段之一。研究表明,在Cu/ZnO催化剂存在下,CO2和H2可发生两个平行反应,分别生成CH3OH和CO。反应的热化学方程式如下:
ΔH1=-53.7 kJ·mol-1Ⅰ

某实验室控制CO2和H2初始投料比为1∶2.2,在相同压强下,经过相同反应时间测得如下实验数据:

T(K)催化剂CO2转化率(%)甲醇选择性(%)543Cat.112.342.3543Cat.210.972.7553Cat.115.339.1553Cat.212.071.6
【备注】Cat.1:Cu/ZnO纳米棒;Cat.2:Cu/ZnO纳米片;甲醇选择性:转化的CO2中生成甲醇的百分比
已知:①CO和H2的标准燃烧热分别为-283.0 kJ·mol-1和-285.8 kJ·mol-1

请回答(不考虑温度对ΔH的影响):(1)反应Ⅱ的ΔH2=________kJ·mol-1。
(2)有利于提高CO2转化为CH3OH平衡转化率的措施有___________。
A.使用催化剂Cat.1
B.使用催化剂Cat.2
C.降低反应温度
D.投料比不变,增加反应物的浓度
E.增大CO2和H2的初始投料比
(3)表中实验数据表明,在相同温度下不同的催化剂对CO2转化成CH3OH的选择性有显著的影响,其原因是___________。
(4)在下图中分别画出反应Ⅰ在无催化剂、有Cat.1和有Cat.2三种情况下“反应过程~能量”示意图。


(2)A项,使用催化剂Cat.1,平衡不移动,不能提高转化率,A错;B项,使用催化剂Cat.2,不能提高转化率,B错;C项,降低反应温度,平衡正向移动,可增大转化率,C正确;D项,投料比不变,增加反应物的浓度,相当于增大压强,平衡正向移动,可增大CO2转化率,D正确;E项,增大 CO2和H2的初始投料比,可增大氢气的转化率,二氧化碳的转化率减小,E错;答案选CD。
(3)催化剂的设计与选择,目前主要依靠经验采取筛选的方法,从表中数据分析,首先观察相同温度下,不同的催化剂,二氧化碳的转化率不同。得出结论1:不同的催化剂的催化能力不同。再分析不同温度相同的催化剂,二氧化碳的转化率不同,且温度高的转化率大,由于正反应为放热反应,温度高转化率应该小才符合勒夏特列原理,实验数据违反该原理,得出结论2:表中数据是未达到平衡时的数据。因而在该时刻下对甲醇选择性有影响。
(4)从表中数据分析,在催化剂Cat.2的作用下,甲醇的选择性更大,说明催化剂Cat.2对反应Ⅰ催化效果更好,催化剂能降低反应的活化能,说明使用催化剂Cat.2的反应过程中活化能更低,所画图示为

考点3:真实化工生产情景中分析催化剂对化学反应的影响
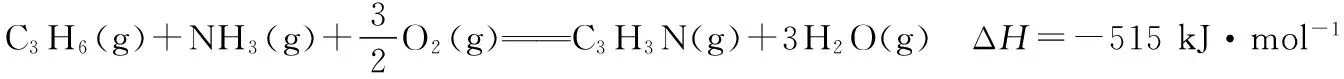

有利于提高丙烯腈平衡产率的反应条件是________;提高丙烯腈反应选择性的关键因素是___________。
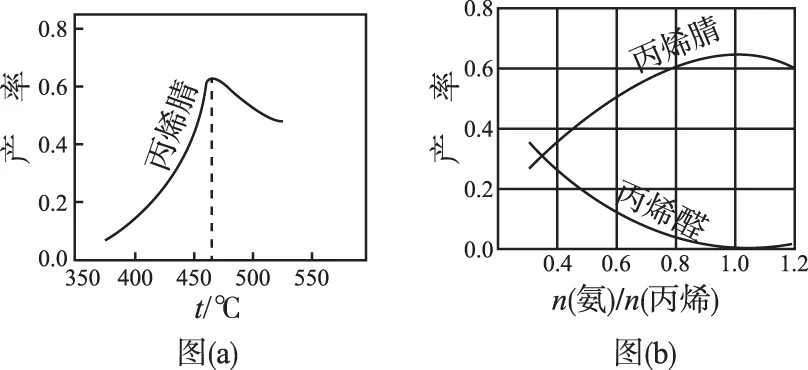
(2)图(a)为丙烯腈产率与反应温度的关系曲线,最高产率对应的温度为460℃。低于460℃时,丙烯腈的产率________(填“是”或“不是”)对应温度下的平衡转化率,判断理由是________;高于460℃时,丙烯腈产率降低的可能原因是________(双选,填标号)。
A.催化剂活性降低________ B.平衡常数变大
C.副反应增多___________D.反应活化能增大
【解析】(1)分析丙烯腈反应特点,气体体积增大的放热反应,根据勒夏特列原理采取降低反应温度和降低压强措施,有利于提高丙烯腈平衡产率。催化剂如果具有较高的选择性,则可以选择性地催化工业生产所需的主反应,而大大减少副反应的发生和副产物的生成。这不仅可以增大原料的利用率,而且可以简化反应后产物的净化、提纯处理等流程,节约成本。提高丙烯腈反应选择性的关键因素是催化剂。
(2)先分析温度对化学平衡的影响关系,该反应为放热反应,平衡产率应随温度升高而降低,事实是低于460℃时,丙烯腈的产率曲线是上升的,由此判断低于460℃时,丙烯腈的产率不是对应温度下的平衡转化率。答案具体表述为:不是,该反应为放热反应,平衡产率应随温度升高而降低。
A选项,催化剂的催化能力一般叫作催化活性。各种催化剂都具有一定的活性最强的温度范围,这个温度范围叫作催化剂的活性温度。若温度过高,活性降低,A正确;B选项,由ΔH=-515 kJ·mol-1可知,升高温度平衡常数变小,B错;C选项,副产物有丙烯醛,催化剂活性降低,副反应增多,导致产率下降,C正确;D选项,Ea(活化能)=E(活化分子的平均能量)-E(普通分子的平均能量)。一般认为温度对反应的活化能无影响,但在温度升高较大时还是会降低反应的活化能的,D错。答案选AC。
考点4:催化剂多重性质对化学反应的影响
【例4】(上海,33节选)乙酸乙酯广泛用于药物、染料、香料等工业,中学化学实验常用如下装置来制备

完成下列填空:
实验时,通常加入过量的乙醇,原因是________。加入数滴浓硫酸即能起催化作用,但实际用量多于此量,原因是____________;浓硫酸用量又不能过多,原因是___________。
【解析】酯化反应是可逆反应,主要利用勒夏特列原理分析问题,加入过量的乙醇增大反应物浓度,使平衡向生成酯的方向移动,提高酯的产率。浓硫酸有三个特性,吸水性、脱水性、强氧化性,实际用量多于此量,原因是浓H2SO4能吸收生成的水,使平衡向生成酯的方向移动,提高酯的产率。浓硫酸用量又不能过多,原因是浓H2SO4具有强氧化性和脱水性,会使有机物碳化,降低酯的产率。
催化剂备考策略
催化原理:改变反应路径,使反应所需的活化能降低。活化能是能量,活化能高反应的难度大,反应速率慢。
三种教材三种图:

理想催化剂的特性:选择性(是指给定条件下反应物之间能够同时发生多个反应情况下,催化剂可以大幅度提高目标产物在最终产物中的比率,酶的选择性极高)。
选择反应温度依据之一:在选择某反应的温度时,首先应考虑催化剂的活性温度,以便最大限度地发挥催化剂的作用。
催化剂中毒:由于某些物质(反应原料中带入的杂质、催化剂自身的某些杂质、反应产物或副产物)的作用而使催化活性衰退或丧失的现象。
催化剂影响速率不影响化学平衡:对于可逆反应,催化剂同等程度地改变正逆反应速率,因而不能改变反应物的转化率,但可缩短反应达到化学平衡的时间。
周期表中催化剂寻找区域:过渡元素区。
中学中常用的催化剂:酶是蛋白质,也是催化剂。二氧化锰、五氧化二矾、铁触媒、铂铑催化剂、Ni、Cu、浓硫酸、稀硫酸。

(作者单位:四川大学华西药学院)

