化学原理题解读
——题变“宗”不变
云南 奠八禄
(作者单位:云南省富源县第一中学)
化学原理题解读
——题变“宗”不变

化学反应原理是高考的核心考点,是考生认知的起点,也是高考能力考查的重要方向,能有效考查考生对化学知识信息的接受、吸收、整合的能力及知识运用迁移的能力。而高考中化学反应原理的题往往知识覆盖面广,难度大,分值高,对考生能力的要求更高。但看每年化学反应原理题,看似所考知识零散无序,难以捉摸,其实这些化学反应原理知识之间都有千丝万缕的内在联系,有规律可循,只要能在复习过程中抓住问题的本质,就能将化学反应原理的内在联系理顺,做到以不变应万变,万变不离其宗的目的。现就原理题进行解读寻“宗”,以期对读者有所帮助。
一、原理题的“宗”
1.原理题的常考考点
(1)通过键能或盖斯定律计算反应热及热化学方程式的书写;
(2)计算化学反应速率、平衡常数K、转化率、产率、各种浓度等;
(3)结合化学平衡移动原理,通过图表考查考生识图识表、进行数据分析判断的能力,吸收、提取、整合有效信息的能力,能解释判断各种平衡点,能解释化学平衡移动的原因,能确定提高转化率的方法和判定温度、压强大小的方法。
2.原理题的“宗”
(1)热化学的“宗”:①键能与反应热的关系;②热化学方程式的书写;③盖斯定律的理解与应用(反应热与反应方程式一样进行加、减、乘、除运算)。
(2)化学平衡的“宗”:①影响化学反应速率与化学平衡的因素;②化学平衡移动原理的理解与应用(如果改变影响平衡的一个条件,化学平衡会向能够减弱这种改变的方向移动);③化学反应速率与化学平衡的图象、图表(看图妙法:一看面,纵坐标与横坐标的意义;二看线,线的走向和变化趋势;三看点,起点、拐点、终点和特殊点);④平衡“三段式法”的计算;⑤各种平衡常数的理解与应用。
(3)电解质溶液的“宗”:①水溶液里的三大平衡(电离平衡、水解平衡、溶解平衡);②水溶液里的三大守恒(电荷守恒、物料守恒、质子守恒)。
(4)电化学的“宗”:① 氧化还原反应原理的应用;②氧化还原反应方程式及电极反应式的书写;③守恒法、关系式法等在计算中的应用。
二、题变“宗”不变
【例1】(2016全国Ⅲ,27节选)煤燃烧排放的烟气含有SO2和NOx,形成酸雨、污染大气,采用NaClO2溶液作为吸收剂可同时对烟气进行脱硫、脱硝,回答下列问题:
(1)在鼓泡反应器中通入含有SO2和NOx的烟气,反应温度为323 K,NaClO2溶液浓度为5×10-3mol·L-1。反应一段时间后溶液中离子浓度的分析结果如下表:
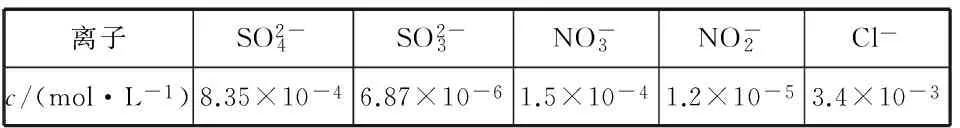
离子SO2-4SO2-3NO-3NO-2Cl-c/(mol·L-1)8.35×10-46.87×10-61.5×10-41.2×10-53.4×10-3
①写出NaClO2溶液脱硝过程中主要反应的离子方程式:________。增加压强,NO的转化率________(填“提高”“不变”或“降低”)。
②随着吸收反应的进行,吸收剂溶液的pH逐渐________(填“提高”“不变”或“降低”)。
③由实验结果可知,脱硫反应速率________(填“大于”或“小于”) 脱硝反应速率。原因是除了SO2和NO在烟气中的初始浓度不同,还可能是________。
(2)如果采用NaClO、Ca (ClO)2替代NaClO2,也能得到较好的烟气脱硫效果。
已知下列反应:
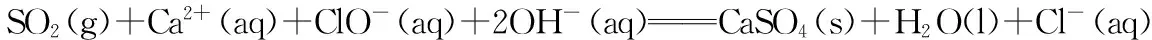
试题分析:本题考查平衡的图表数据、盖斯定律、计算反应热等化学理论知识。

(2)将已知反应依次编号为①②③,据盖斯定律,①+②-③可得目标反应,即ΔH=ΔH1+ΔH2-ΔH3。
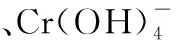
(1)Cr3+与Al3+的化学性质相似,在Cr2(SO4)3溶液中逐滴加入NaOH溶液直至过量,可观察到的现象是___________。
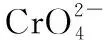
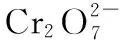
试题分析:本题考查Al(OH)3两性的迁移应用、沉淀溶解平衡的计算及信息条件下氧化还原反应离子方程式的书写。
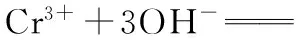
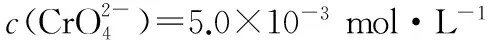
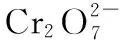
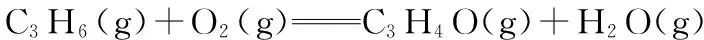
ΔH=-353 kJ·mol-1
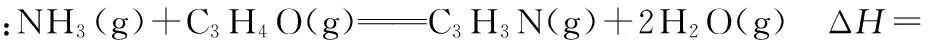
②有利于提高丙烯腈平衡产率的反应条件是___________________________ ;有利于提高丙烯腈反应的速率却不影响丙烯腈平衡产率的因素是________ 。
(2)丙烯腈和丙烯醛的产率与n(氨)/n(丙烯)的关系如表所示。由表可知,最佳n(氨)/n(丙烯)为___________ ,理由是________________ 。进料氨、空气、丙烯的理论体积约为________。
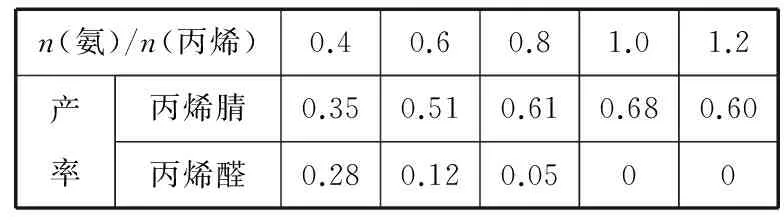
n(氨)/n(丙烯)0.40.60.81.01.2产率丙烯腈0.350.510.610.680.60丙烯醛0.280.120.0500
试题分析:本题考查影响化学反应速率、化学平衡的因素及图表信息的计算。
(1)①根据盖斯定律可得ΔH=-162 kJ·mol-1;②该反应为气体体积增大的放热反应,所以降低温度、降低压强有利于提高丙烯腈的平衡产率;有利于提高丙烯腈反应的速率却不影响丙烯腈平衡产率的因素是催化剂。
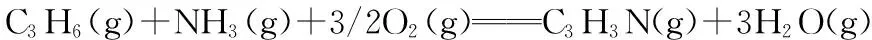
(作者单位:云南省富源县第一中学)

