十二例双组分混合体系检验方案设计
浙江 吴朝辉
(作者单位:湖北省枣阳市第二中学)
(作者单位:浙江省东阳中学)
十二例双组分混合体系检验方案设计

物质检验(鉴别)试题是历年高考的“常客”,要求根据物质或组成物质的离子、基团的特性设计方案,通过分析实验现象,进行判断、推理和分析,并得出最终结果。这类试题综合考查了元素化合物知识,可全面检验我们的思维能力、分析能力。
有些试题会将性质相近、会相互干扰的两种物质组成双组分混合体系,这就需要慎重设计实验方案。
例1:CO2、SO2
方案:将气体试样依次通过品红溶液(如果溶液红色褪去,则试样中含SO2)、KMnO4溶液(除去SO2)、品红溶液(溶液不褪色,则证明SO2已除尽)、澄清石灰水(如果溶液变浑浊,则证试样中含CO2)。
提示:①括号内的内容为现象和结论,下同。②KMnO4可以用FeCl3、碘水等试剂代替。
例2:Fe3+、Fe2+
方案1:取两份试样于两支试管中,分别加KSCN溶液(如果溶液变红色,则试样含Fe3+)、酸性KMnO4溶液(如果紫色褪去,则试样含Fe2+)。
方案2:取两份试样于两支试管中,分别加KSCN溶液(如果溶液变红色,则试样含Fe3+)、铁氰化钾(K3[Fe(CN)6])溶液(如果生成蓝色沉淀,则试样含Fe2+)。

例3:Fe3+、Cu2+
方案:取少量试样于试管中,加过量氨水,如果溶液变成深蓝色,则试样含Cu2+;如果生成红棕色沉淀,则试样含Fe3+。
提示:①检验Fe2+、Cu2+的双组分体系也可用这一方法。②加入过量氨水,发生的反应为

②氯的测定:准确称取样品X,配成溶液后用AgNO3标准溶液滴定,K2CrO4溶液为指示剂,至出现淡红色沉淀不再消失为终点(Ag2CrO4为砖红色)。
回答下列问题:
(3)样品中氨的质量分数表达式为___________。
(4)测定氨前应该对装置进行气密性检验,若气密性不好测定结果将___________ (填“偏高”或“偏低”)。
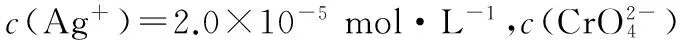

【答案】(3) [10-3(c1V1-c2V2)×17/w] ×100%
(4)偏低
(5)防止硝酸银见光分解 2.8×10-3

(作者单位:湖北省枣阳市第二中学)



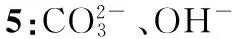


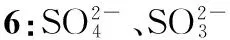
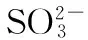

提示:两个方案中的盐酸,均不能用硫酸、硝酸代替。
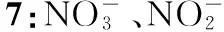
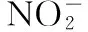
提示:①加入稀硫酸时,反应有


②加入Cu,反应有
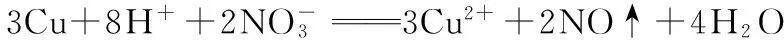
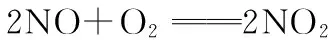
例8:CH3CH2OH、CH3COOH
方案:取少量试样于试管中,依次加少量NaHCO3溶液(如果产生气泡,则试样含CH3COOH)、酸性K2Cr2O7溶液(如果溶液由橙色变绿色,则试样含CH3CH2OH)。
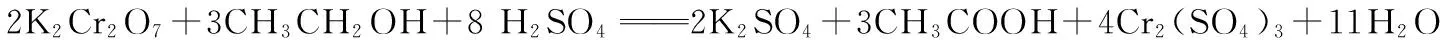
例9:Na2O、Na2O2
方案:准确称取ag试样,加足量水溶解后加入酚酞作指示剂,用bmol/L的标准盐酸滴定至终点,消耗xmL盐酸。如果x=1 000a/31b,则试样只含Na2O;如果x=1 000a/39b,则试样只含Na2O2;如果x介于两者之间,则试样含Na2O、Na2O2。
例10:Na2CO3、NaHCO3
方案:准确称取ag试样,加热至固体质量不再改变,称量剩余固体,质量为bg。如果a=b,则试样只含Na2CO3;如果b=53a/84a,则试样只含NaHCO3;如果b介于两者之间,则试样含Na2CO3、NaHCO3。
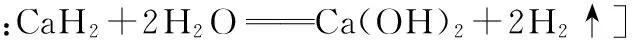
方案:准确称取ag试样,加足量水,收集并测量生成的气体体积,为bL(换算到标准状况)。如果b=0.56a,则试样只含Ca;如果b=1.6a/3,则试样只含CaH2; 如果b介于两者之间,则试样含Ca、CaH2。
例12:Fe、Fe3O4
方案1:取少量试样,加过量CuSO4溶液(如果生成紫红色固体,则试样含Fe),过滤后加过量盐酸(如果溶液,固体溶解后溶液呈蓝色,则试样含Fe3O4)。
方案2:取少量试样,先逐滴加入FeCl3、KSCN混合溶液至过量(如果开始红色褪去,则试样含Fe),过滤后加过量稀盐酸(如果固体溶解,则试样含Fe3O4)。
方案3:称取ag试样,加过量盐酸,再加过量NaOH溶液,充分搅拌后过滤、洗涤、灼烧,得到bg固体。如果b=10a/7,则试样只含Fe;如果b=30a/29,则试样只含Fe3O4;如果b介于两者之间,则试样含Fe、Fe3O4。
提示:①方案1中,加盐酸时的反应有


②方案2中,加HCl时的反应有

加NaOH时的反应有
灼烧时发生的反应为

(作者单位:浙江省东阳中学)

