尿沉渣分析仪检测肾小管管型与手工镜检假阳性率对临床的影响
刘锋
管型的形成必须有蛋白尿, 是指尿液中蛋白质、细胞滤出, 经集合管、肾小管凝固, 逐渐变成圆柱形蛋白聚体,最后被排出, 尿液中出现多量管型, 表示肾实质有病理性变化[1]。尿沉渣为原尿离心后形成的沉渣, 通过尿沉渣检测可有效判断尿道感染等疾病, 尿沉渣分析仪是尿液分析仪器,主要用于临床尿常规分析。IQ200全自动尿沉渣分析仪采用数字化流式形态学技术, 可提供清晰尿液有形成分图像, 样本周转时间短, 结果储存方便, 具有操作便捷, 良好线性范围, 且精准度高, 污染度低, 有较高临床应用价值, 已逐渐被应用于临床各种检测[2,3]。本研究选取本院86例患者, 旨在探讨尿沉渣分析仪检测肾小管管型与手工镜检假阳性率对临床的影响, 现报告如下。
1 资料与方法
1.1 一般资料 选取2014年8月~2016年9月本院患者86例, 使用尿液杯采集患者中段晨尿。其中男49例, 女37例,年龄18~65岁, 平均年龄(48.76±5.43)岁。本研究经本院伦理协会审核批准。
1.2 方法 86例患者标本按照IQ200尿沉渣分析仪操作流程, 进行质控(阳性、阴性), 调节焦距点, 详细根据操作方法检测尿液, 通常检测于120 min内结束。依据管型分析阳性标准(IRIS公司提供), 透明管型为0~2/μl, 未分类管型为0/μl,若管型超出以上范围, 则表现为阳性(其中一项为阳性则表现为阳性)。检查后采用屏幕图像进一步审核, 观察并将结果给予记录。完成后, 经标准化建议, 通过手工显微镜对全部标本进一步确认管型判断, 并记录对比检测结果。将10 ml尿液放置于离心管内, 离心(1500 r/min)5 min, 获取尿液(0.2 ml),通过尿沉渣技术板实施镜检, 并将结果进行记录。
1.3 观察指标 对IQ200尿沉渣分析仪检测情况及图象审核情况进行记录, 并对手工显微镜法进行检测, 进而观察检测管型阳性检出情况及假阳性率。
1.4 统计学方法 采用SPSS21.0统计学软件对数据进行统计分析。计数资料以率(%)表示, 采用χ2检验。P<0.05表示差异具有统计学意义。
2 结果
2.1 IQ200尿沉渣分析仪与手工显微镜检测管型结果对比所有患者均行IQ200尿沉渣分析仪检测, 检测后标本管型均表现为阳性。经图像复核, 管型阳性标本为59例, 阳性率为68.60%;手工显微镜法检测, 确定管型阳性标本65例, 阳性率为75.58%。两种检测方法结果比较, 差异无统计学意义(P>0.05)。见表 1。
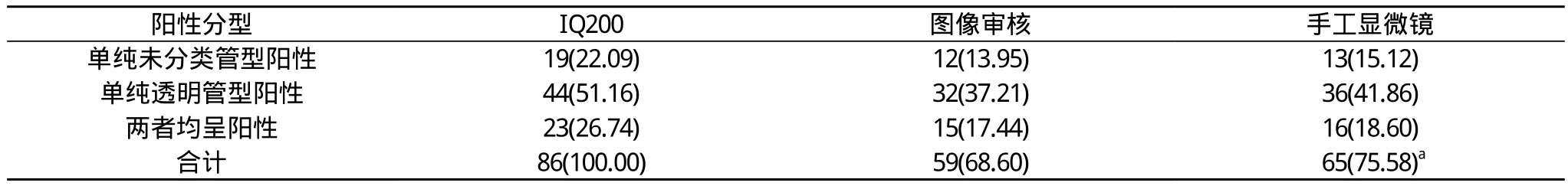
表1 IQ200尿沉渣分析仪与手工显微镜检测管型结果对比[n(%)]
2.2 IQ200尿沉渣分析仪与手工显微镜检测管型结果假阳性率对比 IQ200尿沉渣分析仪对管型未复核假阳性率为31.40%, 经图像审核, 管型假阳性率为9.23%, 两种检测方法对管型假阳性率检查结果比较, 差异有统计学意义(P<0.05)。
3 讨论
尿沉渣检查对泌尿系统疾病诊断尤为重要, 可于早期检查出小儿肾小管-间质肾炎、男性尿道癌、老年人尿路感染、肾性氨基酸尿、肾动脉闭塞及泌尿生殖系滴虫病等[4]。尿沉渣分析仪可自动识别尿沉渣中有形成分个数, 可作为识别尿液有形成分“金标准”, 本研究中IQ200尿液沉渣分析仪结合流式细胞技术及粒子成像分析技术, 其中使用粒子识别系统能分类、量化12种有形成分, 可于荧光屏上显示各种成分形态, 对可疑成分实施人工复核, 进而实现尿液检测自动化、标准化, 具有较高精密度。
IQ200尿沉渣分析仪通过仪器配套鞘液包裹检测样本,利用位相差显微镜、CCD摄像机拍摄数码图像(500帧), 可呈现清晰图像[5-7]。粒子识别系统扫描仪器可通过软件识别能力有效进行定量报告, 主要包括尺度、外形等。另外, 由于IQ200尿沉渣分析仪可判断图像信息, 并且予以修改、整理, 具有较高检测准确性。本研究中, IQ200尿沉渣分析仪对管型未复核假阳性率31.40%, 图像审核后, 管型假阳性率为9.23%, 提示图像审核可预防误诊现象。
尿液有形成分具有复杂性, 多种有形成分互相干扰, 影响检测结果准确性, 实施尿液检测时常因一些干扰因素导致误诊现象出现, 导致管型分类为假阳性, 主要原因有以下几点:尿液中部分相互聚集成分, 促使管型类似物质形成, 影响判断;因为尿液检查时, 存在与管型类似的物质, 导致识别时易将其误判为管型;由于人体尿液中含有微小物质, 对图像造成模糊后影响判断;因为患者尿液存在毛、丝、麻等纤维物质, 易造成误判。因此, 必要时应通过手工显微镜进行复查, 需尽量保证标本新鲜, 放置时间不易过长, 手工混匀, 保证仪器结果可靠性[8-10]。
综上可知, 尿沉渣分析仪检测肾小管管型, 具有较高假阳性检出率, 图像信息复查可降低假阳性率, 可通过手工显微镜法保证检测结果准确性。
[1] 茅蔚, 薛济鸿.尿液分析三种检测方法的应用评价.检验医学与临床, 2015, 12(2):168-171.
[2] 陈小剑, 余玲玲, 舒旷怡, 等.IQ200全自动尿液分析仪流水线复检规则的建立.中华全科医学, 2015, 13(2):268-270.
[3] 于培霞, 高春艳, 张晓慧, 等.IQ200尿沉渣定量分析仪与H-800尿液干化学分析仪联合应用在尿路感染诊断中的价值.中国药物与临床, 2016, 16(1):131-133.
[4] 宗晓龙, 魏殿军.全自动尿沉渣分析仪检测“异型细胞”对尿路上皮癌筛查价值的初步探讨.临床检验杂志, 2016, 34(5):373-377.
[5] 韩淑娥.IQ200全自动尿液分析仪与人工镜检法检测尿中红细胞的比较研究.中国药物与临床, 2016, 16(7):1071-1073.
[6] 张晓峰.IQ200尿沉渣分析仪检测肾小管管型与手工镜检符合率对检测结果的影响.中国继续医学教育, 2016, 8(25):44-45.
[7] 郭晓红.尿镜检管型与尿沉渣分析仪检测的临床分析.中外医疗, 2008, 27(28):160.
[8] 莫巧璇, 钟树奇.全自动尿沉渣分析仪检测管型的影响因素分析.检验医学与临床, 2012, 9(2):183.
[9] 陶立芳, 张国英, 徐桂宁.尿沉渣分析仪和显微镜镜检两种方法检测尿中管型的比较.中国美容医学杂志, 2011, 20(s1):261.
[10] 田芳.全自动尿沉渣分析仪与人工镜检法在管型检测中的效果分析.世界临床医学, 2016, 10(13):79.

